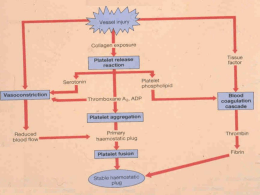
“Indicação e manejo de aférese terapêutica nas síndromes microangiopáticas” Cesar de Almeida Neto [email protected] Doutor em Hematologia pela FMUSP Fundação Pró-Sangue Hemocentro de SP Mulher de 40 anos, afrodescendente, queixa-se de astenia e dor epigástrica há várias semanas. Há 4 dias refere diarreia e vômitos. EF: ndn. Hematócrito=25%. Leucócitos: contagem e diferencial normais. Plaquetas=10.000/mm3. Periférico: células policromatofílicas e fragmentadas. Creatinina=1.1mg/dl, bilirrubina=2,2mg/dl e DHL=722 U/L. Como esta paciente deve ser tratada? definição da anemia microangiopática Caracteriza-se por: anemia hemolítica sem causa aparente microangiopatia (≥2 esquizócitos/100x) trombocitopenia anormalidades neurológicas e/ou renais definições • Púrpura Trombocitopênica Trombótica – mulheres afrodescendentes – adultos – pêntade clássica • anemia hemolítica microangiopática • trombocitopenia, • anormalidades neurológicas • anormalidades renais • febre • Síndrome Hemolítico-Urêmica – clássico: crianças com anemia microangiopática, trombocitopenia e falência renal – após diarreia por Escherichia coli O157:H7 PTT • Rápido reconhecimento • Mortalidade diminui de 90% para 20% após plasmaférese • Eficácia da plasmaférese obriga a utilização de critérios mais abrangentes • Incidência: 4 a 11 casos/milhão de pessoas Peripheral-Blood Smear Showing Abnormalities Characteristic of Thrombotic Thrombocytopenic Purpura. esfregaço sangue periférico PTT George JN. N Engl J Med 2006;354:1927-1935. SHU • 91% das crianças na forma clássica melhoram com cuidados de suporte sem necessidade de plasmaférese • Forma típica (90%) – Toxina da E. coli O157:H7 (epidêmica) – Streptococcus pneumoniae (esporádica) • Forma atípica (10%) – Sistema complemento • Mutação do gene do complemento • Autoanticorpos anti-Fator H • Mutações na proteína do cofator de membrana PTT - etiologia • Idiopática (maioria dos casos) • Secundária: – gravidez ou pós-parto imediato (10%) – doenças autoimune: LES, AR, PTI e Sjögren – infecções ( Escherichia Coli sorotipo O157:H7, Bartonella bacilliformis, HIV) – Neoplasias: adenocarcinoma gástrico e neoplasia de mama – drogas: contraceptivo oral, imunossupressores (ciclosporina, tacrolimus), quimioterápicos (gemcitabina, mitomicina, cisplatina ) e ticlopidina. • Transplante de Medula Óssea • Familiar (Síndrome de Upshaw-Schulman) Fisiopatologia da PTT (atividade ADAMTS-13) Qual é a causa da redução de ADAMTS-13? • Formas agudas e intermitentes idiopáticas – presença de anticorpo dirigido contra a ADAMTS-13 • Forma familiar, crônica recorrente – defeito qualitativo ou quantitativo na síntese de ADAMTS-13 Patogênese da PTT causada pela deficiencia de ADAMTS13 deficiency. Fatores de von Willebrand multiméricos aderem-se às células do endotélio ou tecido conjuntivos expostos nos vasos sanguíneos J. Evan Sadler Hematology 2006;2006:415-420 ©2006 by American Society of Hematology Amostras de diferentes tecidos obtidos na autópsia de uma paciente com PTT coração adrenal George JN. N Engl J Med 2006;354:1927-1935. rim ceco FISIOPATOLOGIA Presença de ULvWf na circulação Agregação plaquetária na circulação Plaquetopenia Suboclusão microcirculação Hemólise Traumática Anemia, DHL, Bilirrubinas, Esquizócitos Plasmaférese nas anemias microangiopáticas plasmaférese na SHU Casos refratários: Eculizumabe plasmaférese na PTT benefícios da troca plasmática com PMF 1. Infusão de grande volume de plasma fresco com provável reposição de ADAMTS-13 2. Remoção de Ac dirigidos com a ADAMTS-13 3. Remoção de ULvWf observação: Na impossibilidade de iniciar PMF e na forma familiar PTT – infusão de plasma fresco (30 ml/kg/dia) Trombocitopenia e anemia hemolítica microangiopática sem causa aparente. PTT diagnosticada Criança com falência renal e pródromo de diarreia? Sim Tratamento de suporte. Sem PMF Não PMF+Corticoide. Investigar causas. Câncer ou sepsis? Sim Parar PMF. Tratar etiologia. Não Continuar PMF. Avaliar DHL e plaquetas. Plaquetas estão aumentando progressivamente? Sim Não Imunossupressores. Aumentar volume de PMF. Plaquetas ≥150.000/mm3X2 dias. Parar gradualmente Plaquetas ≥150.000/mm3X2 dias. Parar PMF. Diminuir progressivamente corticoide. Plaquetas nls após parada? Não Não Sim Sim Reiniciar PMF e intensificar imunossupressão Manter cateter. 1-3 semanas. Remissão (plaquetas nls 30 dias após PMF)? terapia de suporte • Concentrados de hemácias: manter níveis de Hb≥ 8g/dl • Ácido fólico 5 mg /dia • Corticosteroides: prednisona 1-2 mg/kg/dia • Concentrados de plaquetas: somente em casos de sangramento com risco de morte • AAS: contagem de plaquetas ≥ 100.000/mm3 doença refratária Trombocitopenia persistente ou elevação do DHL após 7 dias de tratamento com PMF diárias • Rituximabe – anticorpo anti-CD20 • Vincristina – mecanismo incerto • Ciclosporina • Ciclofosfamida • N-acetilcisteina – inibe agregação de plaquetas ao vWF em ratos complicações das plasmaféreses • 30% dos casos complicações graves • Maior parte relacionadas ao cateter (20%) e a infusão de plasma (10%) • Mais frequente em pacientes com atividade da ADAMTS-13 <10% ( 12 vs. 7 procedimentos) McClain et al. Transfusion 2014:54:3257-9 • Infecção é a causa mais comum de recaída da doença e exacerbação
Baixar