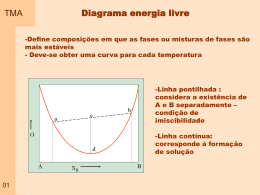
TMA Capacidade calorífica – Volume constante Considerando uma condição em que não é realizado trabalho U q v dU dq v q CT 01 CALORIMETRIA bomba calorimétrica TMA Capacidade calorífica – Volume constante Diagrama da variação da energia interna em função da temperatura a volume constante O coeficiente angular da curva, em cada temperatura é a capacidade calorífica a volume constante U Cv T v 02 TMA Entalpia H U pV U, P, V são funções de estado. Assim H também é; Esta associado ao calor envolvido em um processo realizado a pressão constante 03 TMA Capacidade calorífica – Pressão constante H Cp T p A capacidade calorífica tem sua variação em função da temperatura pode ser considerada como constante para gases ideais Para sistemas não ideais pode ser representada matematicamente Cp C p,m 5 3 R Cv R 2 2 c a bT 2 T Relação entre Cv e Cp 04 Cp Cv nR DSC - Calorímetro diferencial de varredura – Calorimetria diferencial exploratória TMA Expansão adiabática em expansão adiabática q=0 05 TMA Calor específico Temos as duas relações conhecidas: U Cv T v H Cp T p Tentativas de determinar os valores de Cv e Cp 1819 (Dulong e Petit) – definiram que capacidade calorífica molar de todos os elementos sólidos é igual a 3R Cv 3R 24,9 06 TMA Resultados experimentais (1947) Cv(Joules/K) 25 Pb 20 Cu 15 Si 10 5 0 Diamante 0 50 100 150 200 Temperatura (K) 250 300 Einstein – Física quântica – arranjo cristalino de n átomos – considerou que cada átomo apresenta oscilação harmônica independente de sua posição na rede cristalina Temperatura característica de Einstein 07 h E Onde: é a freqüência de vibração atômica TMA Einstein X experimental 25 Cv (Joules/K.mol) 20 Einstein 15 Al D= 385 K 10 5 0 0 0,2 0,4 0,6 0,8 1,0 T/ Se T/ aumenta – Cv tende a 3R Se T tende a zero Cv tende a zero 08 1,2 1,4 1,6 1,8 2,0 Debye TMA Debye – considerou que a freqüência vibracional não era a mesma para todos os átomos. - está entre a distância interatômica e 2x a distância interatômica 25 Cv (Joules/K.mol) 20 Einstein 15 Al D= 385 K 10 5 0 0 09 0,2 0,4 0,6 0,8 1,0 T/ 1,2 1,4 1,6 1,8 2,0 Temperatura de Debye TMA Cv ( Joules/K.mol) 30 25 Substância Pb K Na Sn Cd Au Ag Pt Zn Cu Mo Al Fe C(dia.) 10 D temperatura altas 90 K 99 159 160 160 180 213 225 235 315 379 389 420 1890 baixas 20 15 205 321 379 385 428 2230 O 10 O Ag D=213 O O O O O O O O O O O O O O O O O O O O O O O Al D=389 O O 5 O O O O O O O O O 0 1,0 127 K 129 162 Pb D=90,3 O O 2,0 Log T Oa O O O O O C(diamante) D=1890 3,0 TMA Outras considerações Efeito da temperatura sobre a energia interna e o movimento atômico. Cv 24,93 bT Relação empírica Cp - T Cp a bT cT2 A equação tem validade para intervalos de temperatura definidos Para metais líquidos, em geral Cp = constante 11 Cp – Valores Tabelados TMA Elemento Al (Sólido) Al (líquido) Au (Sólido) Au (líquido) Cu (Sólido) Cu (líquido) Fe () Fe () Fe () Fe () Fe (líquido) C (diamante) C (grafite) O2 (gás) 12 Cp(joules/K.mol) 20,7 +12,4 10-3 T 29,8 23,7 +5,19 10-3 T 29,3 22,6 +6,28 10-3 T 31,4 17,5 +24,8 10-3 T 38 7,7 +19,5 10-3 T 43,9 41,8 9,12 +13,2 10-3 T-6,19 105 T-2 17,2 +4,27 10-3 T-8,79 105 T-2 30,0 +4,18 10-3 T-1,7 105 T-2 Intervalo de T 298 -Tm Tm - 1273 298 -Tm Tm - 1600 298 -Tm Tm - 1600 298 -1033 1033-1181 1181-1674 1674 -Tm Tm- 1873 298 - 1200 298 - 2300 298 - 3000 TMA Cp – Curvas características de materiais 45 Fe() 40 Fe() Fe() Fe() Cp Joule/K.mol 35 30 O2(g) Cu(s) Al(s) 25 Cu(l) Au(l) Al(l) Au(s) C(diamante) 20 C(grafite) 15 10 5 0 400 600 800 1000 1200 Temperatura (K) 13 1400 1600 1800 Exercício TMA 1) 10 litros de gás ideal monoatômico, mantido a 25 ºC e 10 atm é expandido até atingir a pressão final de 1 atm. A capacidade calorífica molar do gás a volume constante (Cv) é 3/2 R e é independente da temperatura. Calcular o trabalho realizado, o calor absorvido e as mudanças de energia interna e entalpia para o gás se o processo ocorre: isotermicamente e reversivelmente adiabaticamente e reversivelmente 14 Termoquímica TMA (ATKINS) – Termoquímica é a investigação do calor produzido ou consumido nas reações químicas. Trabalha com os conceitos de determinação do calor envolvido em processo a pressão ou volume constante e conseqüentemente com U e H correspondendo ao calor de reação. dH q p nCp dT dU qv nCv dT Transformação Física H2O(l) H2O(g) vapH(273) 6,01 kJ / mol Reação química 15 9 C3H 6 (g) O 2 (g) 3CO 2 (g) 3H 2 O 2 r H - 2058kJ/mol TMA Termoquímica Reagentes Produtos Estado padrão – O estado padrão de uma substância, numa certa temperatura, é o da substância pura sob pressão de 1 bar. Variação de entalpia padrão – A variação de entalpia de reação ou processo físico é a diferença entre as entalpias dos produtos nos respectivos estados padrões e a entalpia dos reagentes, também nos respectivos estados padrões. Pode ser referida a qualquer temperatura. Assumiu-se como temperatura de referência 298,15 K. 16 TMA Entalpia de reação Variação de entalpia padrão (a) Entalpia de transformações físicas – variação de entalpia associada a uma mudança de estado físico ( entalpia padrão de transição) H2O(s) H2O(l ) 0 fus H273 6,01 kJ / mol CONCEITO DE FUNÇÃO DE ESTADO H2O(s) H2O(l) fus H H2O(l) H2O(g) vapH H2O(s) H2O(g) 17 sub H fus H vapH TMA 18 Conceito de função de estado TMA Entalpia de reação (b) Entalpia de transformação química – A entalpia padrão de reação é a variação de entalpia associada a transformação de reagente no estado padrão em produtos também no estado padrão Reagente isolado no estado padrão Produtos isolados, puros, nos respectivos estados padrões H 2 ( g ) O2 ( g ) H 2O( g ) 0 r H298 - 241,82kJ/mol Efeito da quantidade de reagentes e produtos 2A B 3C D r H H Pr odutos m H m Re agentes r H 3Hm (C) Hm (D) 2Hm (A) Hm (B) 19 Onde Hm(c)é a entalpia padrão molar da espécie C na temperatura constante TMA Entalpia de reação Reações exotérmicas C O2 CO2 H0298 -393510J Reação endotérmica ZnO C CO Zn 0 H1373 349000J Calor de formação : é a variação de entalpia que acompanha a formação de um mol de um composto, a partir de seus elementos constituintes, na sua forma mais estável ã temperatura de referência ( no caso 298 K ) e sob pressão de 1 atm. 2 Al 1,5O2 Al2O3 20 H0298 1674000J Assume que a reação é completa TMA Entalpia de reação Calor de reação: é a variação da entalpia que acompanha a reação , quando as quantidades de reagentes são totalmente consumidas, de acordo com a equação química balanceada, na temperatura considerada. 3 Fe2O3 CO 2 Fe3O4 CO2 0 H1000 46700J O calor de reação a 1000K é igual a 46700 J. Este é o calor absorvido, sob pressão constante de 1 atm, quando 3 moles de hematita são reduzidos por um mol de monóxido de carbono, para formar dois moles de magnetita e um mol de dióxido de carbono. Supondo-se a reação completa. 21 TMA Entalpia de reação (C) A lei de Hess – é possível combinar as entalpias padrões de várias reações para se ter a entalpia de outra reação A entalpia padrão de uma reação é igual a soma das entalpias padrões de reações parciais em que a reação possa ser dividida. 9 0 C3 H 6 ( g ) O2 ( g ) 3CO2 ( g ) 3H 2 O r H 298 ? 2 0 C3 H6 ( g ) H 2 ( g ) C3 H8 ( g ) r H 298 -124kJ/mol C3 H8 ( g ) 5O2 ( g ) 3CO2 ( g ) 4H2O(l ) 1 H 2O(l ) H 2O( g ) O 2 2 9 C3 H 6 ( g ) O2 ( g ) 3CO2 ( g ) 3H 2 O 2 22 0 r H298 - 2220kJ/mol 0 r H 298 286 kJ/mol 0 r H 298 - 2058kJ/mol TMA Conceito de função de estado (e) Entalpia de reação em função da entalpia de formação 2HN3 (l) 2NO(g) H2O2 (l) 4N2 (g) r H f H(H 2O2 , l) 4 f H( N 2 , g) 2 f H( NH3 , l) 2 f H( NO, g) r H 0 187 ,78 2(0) 2(264 ,0 2(90,25) r H 0 892,3kJ / mol 23 TMA (e) Calor de combustão e poder calorífico Quando um mol de uma substancia é completamente queimado com oxigênio, há liberação de calor; H<0 Exemplo: C O2 CO2 C2 H6O 3O2 2CO2 3H2O 24 H0298 94051cal H0298 Calor de combustao TMA Entalpia e temperatura (f) Entalpia de reação e temperatura – A entalpia de reação em temperatura diferente da temperatura ambiente pode ser estimada a partir da capacidade calorífica e da entalpia de reação na temperatura ambiente. (ou outra temperatura qualquer) T2 H (T2 ) H (T1 ) C p dT T1 25 TMA Exemplo 1 Pb(s) O 2 (g ) PbO (s) 2 H PbO(298) 219000 joule/ mol CPb (s) 23,6 9,75x103 T joule / Kmol de 298K a Tm,Pb CPb (l) 32,4 3,1x103 T joule / Kmol de Tm,Pb a 1200K CPbO (s) 37,9 26,8x103 T joule / Kmol de 298K a Tm,Pb CO(g) 30,0 4,18x103 T -1,7x105 T-2 joule / Kmol de 298K a 3000K Hm,Pb 4810 joule / mol a 600K Tm,Pb 600K Tm,PbO 1159K 26 TMA Exemplo 1 Pb(s) O 2 (g ) PbO (s) 2 40 30 20 Entalpia H (kJ) 10 0 -170 -180 -190 -200 -210 -220 300 27 500 700 900 1100 300 Temperatura (K) 500 700 900 1100
Baixar