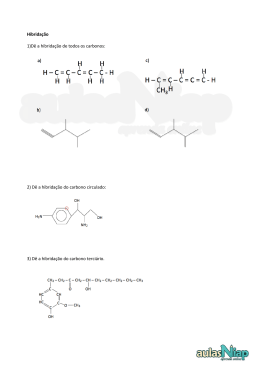
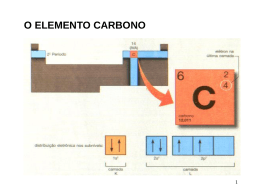
30-09-2007 LIGAÇÃO QUÍMICA NO CARBONO GEOMETRIA MOLECULAR HIBRIDAÇÃO Geometria molecular • O arranjo tri-dimensional dos átomos numa molécula → geometria molecular • A teoria da repulsão dos pares de electrões (ligantes e anti-ligantes) procura explicar o arranjo dos átomos numa molécula. 30-09-2007 2 1 30-09-2007 Teoria da repulsão electrónica • Electrões são cargas negativas, repelem-se mutuamente. • Os electrões ocupam posições espaciais de modo a minimizar o efeito das suas repulsões (de modo a ficar o mais afastados possível uns dos outros). • Num átomo os electrões distribuem-se por espaços chamados orbitais (máximo de 2e numa orbital). 30-09-2007 3 z y ORBITAL s Simetria esférica x ORBITAIS p z y x 30-09-2007 pz orbital px orbital py orbital 4 2 30-09-2007 Ligações covalentes • Resultam da sobreposição das orbitais atómicas dos átomos que participam na ligação. • Os átomos partilham o par de eletrões que forma a ligação. • A ligação covalente pode ser polar ou apolar. • Podem ser do tipo sigma (σ) ou pi (π), conforme a sua simetria. 30-09-2007 5 A molécula de H2 • Caracterizada por uma ligação covalente simples resultante da sobreposição de duas orbitais 1s, uma de cada átomo de hidrogénio. • A ligação tem uma simetria cilíndrica sobre o eixo que une o centro dos dois átomos - ligação σ. • A ligação no H2 (H-H) pode ser resumida em: 1s (H) – 1s(H) Æ ligação σ 30-09-2007 6 3 30-09-2007 A ligação covalente no H2 • A ligação sigma resulta da combinação de duas orbitais s H H H H Simetria cilíndrica da ligação sigma 30-09-2007 7 Cada átomo de H apresenta 1 electrão na orbital 1s. 1s. Este electrão sente a atracç atracção do protão existente no núcleo do átomo de H. Quando dois átomos de H se aproximam, aproximam, o electrão de cada átomo começ começa a sentir a forç força atrativa dos protões de ambos os núcleos. cleos. Na molé atómicas 1s molécula de H2 as duas orbitais ató dão origem a uma orbital molecular que corresponde a uma região com igual probabilidade de encontrar qualquer um dos dois electrões que formam a ligaç ligação covalente. covalente. 30-09-2007 8 4 30-09-2007 GEOMETRIA MOLECULAR • Muitas propriedades (ex:reatividade) das moléculas estão relacionados com sua forma. • A forma depende do ângulo das ligações e do comprimento das ligações. • Utiliza-se o conceito de hibridação dos átomos numa molécula para explicar a forma dessa molécula. 30-09-2007 9 Hibridação de orbitais atómicas • É a combinação de orbitais atómicas de energia próxima e simetria diferente, originando novas orbitais, iguais entre si, mas diferentes das orbitais originais. • As novas orbitais atómicas, denominadas orbitais híbridas, são diferentes em geometria (forma) e na sua energia. • O número de orbitais híbridas obtidas é igual ao das orbitais de partida. 30-09-2007 10 5 30-09-2007 ORBITAIS ANTES DA HIBRIDAÇÃO ORBITAIS APÓS HIBRIDAÇÃO (sp3) z x Orbital s orbital px x hibridação z y orbital pz orbital py 30-09-2007 11 Hibridização sp3 • É a combinação de 3 orbitais p “puras” com uma orbital s “pura”, formando 4 novas orbitais “híbridas” denominadas sp3. • A geometria dos 4 orbitais sp3 é tetraédrica (as 4 orbitais partem do centro do tetraedro e dirigem-se, cada uma, para um dos vértices do tetraedro). • O ângulo entre as orbitais sp3 é de aprox.109° • Acontece no C, que possui 4 electrões de valência distribuídos por 1 orbital s e 3 p (px, py e pz), que o levam a estabelecer no máximo 4 ligações simples (o C é tetravalente). 30-09-2007 12 6 30-09-2007 . . C. . 2s ↑↓ 2px ↑ 2py ↑ 2pz O carbono possui 4 electrões de valência Æ 2s2 2p2 (é tetravalente). O carbono pode formar ligações simples, duplas e triplas. O carbono pode apresentar orbitais híbridas do tipo sp, sp2 e sp3 30-09-2007 13 2p hibridação sp3 2s 30-09-2007 14 7 30-09-2007 30-09-2007 15 Hibridação sp2 • É a combinação de uma orbital s com duas orbitais p (pertencentes ao mesmo átomo), resultando em 3 novas orbitais denominadas híbridas sp2. • As três orbitais híbridas sp2 situam-se no mesmo plano formando ângulos de 120° entre si (geometria triangular plana). • Explica a formação de ligações duplas no C. • Num C do tipo sp2 existirá uma orbital p “pura” que será responsável pela ligação covalente do tipo pi. 30-09-2007 16 8 30-09-2007 HIBRIDAÇÃO sp2 DO CARBONO H Eteno (etileno) H C C H H No etileno, cada carbono é hibrido sp2 . O hidrogénio é 1s. Uma das ligações C-C é sp2 - sp2. A outra é p - p. 2p 2p hibridação sp2 2s 30-09-2007 17 sp2 1 orbital de simetria s e 3 orbitais de simetria p H H C H 30-09-2007 C H 3 orbitais de simetria sp e 1 orbital de simetria p No etileno, a ligação dupla é formada pela combinação de duas orbitais sp2, uma de cada C, formando uma orbital molecular de simetria σ, e pela combinação de duas orbitais p, uma de cada C, formando uma orbital molecular do tipo π. 18 9 30-09-2007 Os ângulos de ligações no C2H4 • Como os átomos centrais são dois carbonos com hibridação sp2 o ângulo entre as ligações sigma será de ≈ 120°. A ligação π é perpendicular ao plano da molécula. • C com uma dupla ligação Æ hibridação sp2 Numa ligação dupla → uma ligação σ e uma ligação π 30-09-2007 19 30-09-2007 20 10 30-09-2007 OUTRAS MOLÉCULAS TRIANGULARES PLANAS hibridação sp2 Ægeometria triangular plana H H C O H H C N H H H H H H H neste exemplo, cada carbono é sp2 30-09-2007 21 Hibridação sp • É a combinação de uma orbital s com 1 orbital p, formando duas novas orbitais denominadas híbridas sp. • As orbitais híbridas sp formam um ângulo de 180° entre si. • A geometria molecular é linear. • Explica a formação de duas ligações duplas no C ou de uma ligação tripla. • Numa ligação tripla formam-se uma ligação sigma e duas pi. 30-09-2007 22 11 30-09-2007 Fórmula estrutural do acetileno H C H C Cada átomo de carbono é um híbrido sp. Os hidrogénios têm orbitais 1s, não hibridas. 2p 2p hibridação 2s sp A ligação tripla é formada por uma σ e duas π . As duas ligações π resultam da combinação de orbitais p não hibridas. 30-09-2007 23 Exemplo de hibridação sp ÆC2H2 • Etino (acetileno) • Em torno dos átomos de C formam-se duas orbitais híbridas sp e duas orbitais p “puras”. • As duas orbitais híbridas do C formam uma orbital molecular de simetria sigma por combinação de uma s (H) e de uma sp (C) e outra também de simetria sigma por combinação de duas sp (C-C). • As duas orbitais p de cada carbono combinam-se para formar duas ligações pi entre os carbonos (resultando numa ligação tripla entre os dois carbonos). • Ligação tripla → uma ligação σ e duas ligações π 30-09-2007 24 12 30-09-2007 A Molécula de C2H2 H C C 30-09-2007 H 25 Momento dipolar • A molécula de HF tem uma ligação polar – devido a diferença de eletronegatividade existente entre o F e o H. • A forma da molécula e a grandeza do dipolo explicam a polaridade total da molécula. δ+H-Fδ− 30-09-2007 26 13 30-09-2007 Momento dipolar e geometria • Moléculas diatómicas homonucleares → não apresentam momento dipolar (O2, F2, Cl2, etc) • Moléculas triatómicas ou maiores ( dependem do efeito resultante de todas ligações polares existentes na molécula). 30-09-2007 27 O momento dipolar depende da geometria da molécula 30-09-2007 28 14 30-09-2007 Mais exemplos polaridade e geometria 30-09-2007 29 15
Baixar