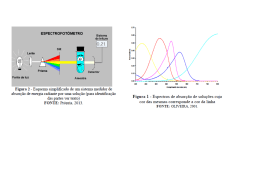
Departamento de Bioquímica Instituto de Química – USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2015 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da lise de leveduras. Para se quantificar a quantidade de proteínas neste extrato, foi utilizado o reagente de Bradford. Junto com suas amostras, duas curvas-padrão foram geradas medindo-se a Absorbância em 595 nm em amostras incubadas com o reagente de Bradford por 8 min. Os dados abaixo são das Absorbâncias subtraídas do Branco. a) Qual a função do Branco? b) Qual dos dois gráficos é mais adequado para se utilizar como uma curva-padrão? Justifique c) Qual a unidade de concentração de proteína que será obtida? d) Qual é a maior e a menor absorbância que a curva-padrão consegue medir com confiança? Qual é a concentração de proteínas nestas absorbâncias? e) Digamos que sua amostra teve uma absorbância de 1.7, a concentração obtida usando a curva-padrão é confiável? Como solucionar este problema? f) As absorbâncias abaixo foram obtidas com uma mesma amostra diluída em concentrações diferentes. Calcule a concentração da amostra sem diluir. Diluição 5x Diluição 50x Diluição 100x Diluição 500x Abs 595 nm 1.8 1.25 0.64 -0.05 2 2. O ácido dinitrosalicílico (DNS) pode ser usado para medir a quantidade de açúcares redutores em amostras, pois a reação deste com o grupo aldeído livre presente no carbono 1 das aldoses, ou com o grupo cetônico presente em frutoses, libera um produto que absorve luz à 540 nm. Alunos de um curso de bioquímica, montaram a seguinte curva padrão usando uma solução de glicose 5 mM (massa molar = 180 g) e obtiveram os seguintes resultados após ferver as amostras por 10 min: Glicose 5 mM Água Reagente DNS Concentração de Abs 540 nm (µl) (µl) (µl) glicose (µg/ µl) 0 500 500 0,010 50 450 500 0,100 100 400 500 0,250 150 350 500 0,380 200 300 500 0,480 250 250 500 0,620 300 200 500 0,680 350 150 500 0,820 400 100 500 0,940 450 50 500 1,100 500 0 500 1,220 O reagente da Glicose Oxidase (TGO) pode ser usado para medir especificamente a quantidade de glicose presente em uma amostra. A glicose oxidase, ao oxidar glicose, reduz um grupo NAD+ para NADH. Essa reação pode ser acoplada à oxidação de um grupo como a o-dianisidina, a qual passa a absorver luz a 420nm ao ser oxidado. Foi montada uma curva padrão com uma solução de glicose 0,5 mM e, após incubar a amostra por 1 h a 37°C para ocorrer a reação foram obtidos os seguintes resultados: Glicose 0,5 mM Água Reagente TGO Concentração de Abs 420 nm (µl) (µl) (µl) glicose (µg/ µl) 0 500 500 0,020 50 450 500 0,120 100 400 500 0,200 150 350 500 0,270 200 300 500 0,390 250 250 500 0,510 300 200 500 0,620 350 150 500 0,660 400 100 500 0,780 450 50 500 0,910 500 0 500 0,980 O reagente Fenol-Sulfúrico (FS) pode ser usado para medir a quantidade de açúcares presentes em uma amostra, pois após a hidrólise pelo ácido sulfúrico e a reação do fenol com os grupos hidroxila é gerado um produto que absorve a 490 nm. Foi montada a curva padrão abaixo com uma solução de glicose 1 mM e após a reação foram obtidos os dados abaixo: 3 Glicose 1 mM (µl) 0 10 20 50 100 150 200 250 300 400 Água (µl) 400 390 380 350 300 250 200 150 100 0 Reagente FS (µl) 400 400 400 400 400 400 400 400 400 400 Concentração de glicose (µg/ µl) Abs 490 nm 0.001 0.050 0.075 0.175 0.450 0.600 0.750 0.990 1.150 1.600 Diferentes variedades de cana-de-açúcar foram testadas para saber qual das variedades possui a maior quantidade de açúcares solúveis, o que é de grande interesse para a indústria açucareira. Pedaços do colmo da cana-de-açúcar foram homogenizados em água e este material foi centrifugado por 10 min a 10.000 g a 4°C. O sobrenadante foi diluído e usado para determinação de açúcares com os métodos do ácido dinitrosalícilico (DNS), glicose oxidase (TGO) e fenol-sulfúrico (FS), utilizando-se os mesmos volumes das respectivas curvas-padrões. Os resultados estão expostos na tabela abaixo: Variedade Massa de Volume Diluição Amostra Abs Abs Abs tecido (g) final (ml) (X) (µl) 540 nm 420 nm 490 nm (DNS) (TGO) (FS) 1 10 10 100 100 0,001 0,003 0,812 2 5 10 20 100 0,005 0,001 1,525 3 7 10 30 100 0,003 0,002 1,210 4 2 10 5 100 -0,002 -0,009 0,994 5 25 10 200 100 -0,010 0,001 0,853 6 12 10 100 100 0,000 0,007 1,112 7 8 10 100 100 0,001 -0,008 1,215 8 10 10 100 100 0,003 -0,001 1,336 9 4 10 15 100 0,002 0,001 1,201 10 1 10 2 100 -0,008 0,002 1,487 a) Qual das técnicas é a melhor para se medir açúcares solúveis em cana-de-açúcar? Como você explicaria esses resultados? b) Calcule a concentração de açúcares solúveis nos diferentes homogeneizados e a massa de açúcar que pode ser obtida por massa de tecido vegetal (g açúcar/ g tecido. Qual das plantas é a melhor para a produção de sacarose? c) Uma indústria farmacêutica está interessada na produção de alfa-glicosidase de levedura para geração de glicose e frutose a partir de açúcar da cana (sacarose). Para tal, obteve várias linhagens de levedura e agora há a necessidade de medir a atividade de alfaglicosidase presente nas células. Quais das técnicas – DNS, TGO ou FS – você usaria para medir a atividade dessa enzima, usando sacarose como substrato? Considere fatores como sensibilidade e tempo de medição. 4 3. A indústria farmacêutica preparou lisados de levedura de diferentes linhagens. Em todas as amostras usou 1 g de células e obtiveram 10 mL de lisado. Esses lisados foram utilizados para ensaios enzimáticos, empregando p-nitrofenil α-glicosídeo (pNPαglc) como substrato. Foram obtidos os resultados a seguir: linhagem A B C D E F diluição lisado diluído (µl) 100x 50x 8x 70x 500x 200x Use a equação da reta protocolos). 100 20 50 200 200 200 Abs420nm = água (µl) pNPαglc (µl) Abs420 nm Abs420 nm (15 min) (30 min) Abs420 nm Abs420 nm (45 min) (60 min) 100 200 0,050 0,100 0,150 0,200 180 200 0,080 0,160 0,240 0,320 150 200 0,250 0,500 0,750 1,000 0 200 0,100 0,200 0,300 0,400 0 200 0,010 0,020 0,030 0,040 0 200 0,075 0,150 0,225 0,300 0,0049 [p-nitrofenolato] + 0,014 (gráfico na apostila de As mesmas amostras foram submetidas à determinação de proteínas com o reagente de Bradford (comassie blue G), obtendo-se os dados a seguir: linhagem A B C D E F diluição 20x 50x 10x 20x 5x 80x lisado diluído (µl) 100 20 50 80 10 100 água (µl) 0 80 50 20 90 0 Reagente Bradford (ml) 1 1 1 1 1 1 Abs595 nm (15 min) 0,265 0,320 0,50 0,105 0,750 0,415 Confeccionou-se também uma curva padrão usando albumina de ovo: Albumina 0,2 g/l (µl) 0 10 20 30 40 50 60 70 80 90 100 água (µl) 100 90 80 70 60 50 40 30 20 10 0 Reagente Bradford (ml) 1 1 1 1 1 1 1 1 1 1 1 Massa de proteína (mg) Abs595 nm (15 min) 0,010 0,080 0,160 0,240 0,320 0,400 0,480 0,560 0,640 0,720 0,800 5 Calcule a concentração de atividade enzimática no lisado de cada uma das linhagens de levedura. Calcule também a atividade obtida por grama de células. Calcule a concentração de proteína em cada um dos lisados e a atividade específica de cada um dos materiais. Se o próprio lisado for utilizado industrialmente como fonte de enzima, qual das linhagens é melhor para produzir essa enzima em larga escala? Se for necessário purificar a enzima, qual das linhagens é a melhor fonte? Justifique as respostas. 4. A enzima COMT (catecol-O-metiltransferase) atua metilando o 4-hidroxi-estradiol, um metabólito carcinogênico derivado da metabolização do estrogênio. Esta reação química é uma importante etapa na detoxificação do 4-hidroxi-estradiol (um catecol), transformando-o em 4-metoxi-estradiol (um guaiacol) como esquematizado na reação abaixo. Guaiacol Sabendo que mulheres que desenvolvem câncer de mama (do subtipo dependente de estrogênio) frequentemente apresentam variantes desta enzima com atividade reduzida, uma industria farmacêutica resolveu desenvolver um medicamento para mulheres contendo esta enzima com o objetivo de ajudar a prevenir o surgimento ou a reincidência do câncer de mama. Para purificar grandes quantidades desta enzima, os investigadores envolvidos no desenvolvimento deste medicamento, obtiveram orgãos bovinos que sabidamente expressam a COMT. O primeiro passo que antecedeu a purificação envolveu o preparo de lisados celulares de cada orgão. Estes lisados foram submetidos aos dois ensaios descritos abaixo. Ensaio de Bradford Tabela 1 – preparo do lisado orgãos fígado Glândulas mamárias (GM) cérebro Rins Quantidade de tecido usada 20 g 12 g 17 g 6g Volume do lisado obtido 25 ml 16 ml 23 ml 9 ml O lisado original de cada órgão foi diluído 100X e usado segundo o protocolo da tabela abaixo (Tabela 2). Após 5 minutos de incubação foi lida a absorbância a 595nm e os resultados foram também registrados na Tabela 2. 6 Tabela 2 – Quantificação da concentração de proteínas L100X (µL) 10 20 30 40 tubos branco fígado GM cérebro rins H2O (µL) 100 90 80 70 60 reagente de Bradford (mL) 1,0 1,0 1,0 1,0 1,0 A595 0,003 0,382 0,686 0,838 0,813 Para este experimento, a curva padrão com albumina forneceu o gráfico abaixo: Absorbância a 595nm Curva Padrão da Albumina 1.4 f(x) = 0.08x + 0.06 R² = 0.98 1.2 1 0.8 0.6 0.4 0.2 0 0 2 4 6 8 10 12 14 16 [Albumina] ug Reação enzimática colorimétrica Para medir a atividade da COMT, foi utilizado um ensaio colorimétrico usando-se os dois substratos da COMT: o doador de grupos metil s-adenosil-L-metionina (SAM) e um substrato artificial contendo um grupo catecol, que passa a apresentar um pico de absorção a 320nm quando metilado. Os lisados originais de cada órgão foram diluídos 20X e usados para monitorar a atividade enzimática segundo o protocolo da tabela abaixo (Tabela 3). Após diferentes tempos de incubação a 37°C, a absorbância a 320 nm das amostras foi medida e colocada na tabela 3. tubo 1 2 3 4 Lisado (ml) 0,2 0,2 0,2 0,2 SAM (ml) 0,1 0,1 0,1 0,1 Substrato Tempo artificial (min) (ml) 0,1 5 0,1 10 0,1 15 0,1 20 Fígado (A320nm) 0,11 0,28 0,4 0,51 Cérebro GM (A320nm) (A320nm) 0,04 0,09 0,15 0,19 0,06 0,12 0,2 0,25 Rins (A320nm) 0,08 0,15 0,21 0,32 7 A curva padrão obtida para relacionar a quantidade de substrato artificial metilado da COMT (produto) com a Absorbância a 320 nm é apresentada no gráfico abaixo: Curva Padrão da atividade da COMT 0.7 Absorbância a 320nm 0.6 f(x) = 0.01x - 0.01 R² = 1 0.5 0.4 0.3 0.2 0.1 0 5 10 15 20 25 30 35 40 45 50 55 micromol de produto Considerando os resultados experimentais acima, calcule para cada lisado: a) a concentração de proteína (mg/mL). b) a concentração da atividade enzimática (U/mL). c) a atividade específica (U/mg de proteína). Com base nos cálculos acima, qual é o melhor órgão a ser utilizado para se obter a maior quantidade da COMT? E o melhor órgão para se obter a COMT mais pura? Justifique. 5. Quatro amostras (1 a 4) foram submetidas à eletroforese em poliacrilamida desnaturante (SDS-PAGE) na presença e na ausência de beta-mercaptoetanol, resultando nos seguinte géis: As distâncias de migração das bandas das proteínas no gel estão colocadas nas tabelas abaixo. 8 Gel em condições redutoras Proteínas Padrão azul de bromofenol banda A banda B banda C banda D banda E banda F banda G banda H Distância (cm) 6,8 0,7 1,6 3,9 5,0 4,4 4,2 4,8 5,3 Gel em condições não-redutoras Proteínas Padrão azul de bromofenol banda I banda J banda K banda L banda M banda N banda O Distância (cm) 6,8 0,7 1,4 1,6 2,9 4,2 4,8 5,3 A curva gerada pelas proteínas padrão pode ser encontrada abaixo: y = -1.3791x + 5.4958 R² = 0.9978 6 logPM 4 2 0 0 0.4 0.8 1.2 migração relativa Responda: a) Qual a função do SDS no SDS-PAGE? b) Qual a razão das diferenças entre o gel com β-mercaptoetanol e sem βmercaptoetanol? c) Qual o peso molecular de cada uma delas? Quais continham mais de uma subunidade e qual o peso molecular de cada cadeia proteica? 5. As figuras a seguir apresentam o perfil de eluição da atividade de alfa-glicosidase em uma cromatografia de troca aniônica em coluna DEAE-celulose. Cada uma das cromatografias 9 foi realizada utilizando um tampão com pH diferente (9,0 – 8,0 – 6,0). Com base nos resultados responda qual a provável faixa de valores do pI (ponto isoelétrico) desta alfa-glicosidase: 6. Você conseguiu purificar uma celulase através da marcha de purificação a seguir. 1º passo: cromatografia de troca aniônica em pH 10. 2º passo: cromatografia de filtração em gel em pH 6,0. Após cada passo os tubos que continham a atividade de celulase foram reunidos. Para este material foi calculada a atividade enzimática total de celulase e também a quantidade de proteína. A tabela abaixo resume estes resultados: Passo Atividade de Atividade de Proteína total Proteína total celulase aplicada celulase recuperada aplicada recuperada (U) (U) (mg) (mg) Troca iônica 500 100 1,0 0,05 Filtração em gel 100 80 0,05 0,02 Após cada cromatografia os tubos que continham atividade de celulase também foram reunidos e analisados por SDS-PAGE em meio redutor: 10 SDS-PAGE de materiais recolhidos ao longo da marcha de purificação. M – meio de cultura; T – material recuperado após cromatografia de troca aniônica; F – material recuperado após cromatografia de filtração em gel; P – padrões de peso molecular. Para a coluna de filtração em gel de 25 ml usada na marcha de purificação foi previamente preparada uma curva de calibração utilizando proteínas de diferentes pesos moleculares. Os dados obtidos estão descritos na tabela abaixo juntamente com o resultado para cromatografia da celulase: Material Proteína padrão de 2.000.000 daltons Proteína padrão de 66.000 daltons Proteína padrão de 45.000 daltons Proteína padrão de 12.400 daltons Proteína padrão de 6.500 daltons Atividade celulásica a) b) c) d) Volume de eluição (ml) 7,53 9,38 10,46 13,70 16,22 9,58 Calcule a recuperação da atividade enzimática após cada um dos passos da purificação da celulase. Calcule a atividade específica da celulase após cada um dos passos da marcha de purificação. Qual dos passos é melhor na purificação desta enzima? Por quê? Calcule a massa molecular da enzima determinada por SDS-PAGE e por filtração em gel. Compare os valores e formule hipóteses para explicar os resultados. 11 7. O tecido embrionário de fígado contém a enzima que catalisa a reação S -> P. O tecido de fígado adulto também apresenta a atividade S -> P. Alguns dados cinéticos obtidos com extratos dos dois tecidos são apresentados abaixo. Que conclusões você pode tirar com relação à identidade das duas enzimas? [S] Velocidade inicial observada (µmoles.mg de proteína-1.min-1) [M] Extrato de Fígado Extrato de Fígado Adulto (E1) Embrionário (E2) 1,67 x 10-5 1,05 5,00 -5 2,50 x 10 1,54 6,66 3,33 x 10-5 1,98 8,00 5,00 x 10-5 2,86 10,00 7,00 x 10-5 3,78 11,67 1,00 x 10-4 5,00 13,33 1,50 x 10-4 6,67 15,00 -4 1,67 x 10 7,15 15,40 2,00 x 10-4 8,00 16,00 -4 3,00 x 10 10,00 17,10 Durante danos consideráveis do fígado, esta enzima é liberada na corrente sanguínea. Após exercícios intensos, uma enzima de músculo, E3, que catalisa a mesma reação, é liberada na corrente sanguínea. E1 e E3 podem ser diferenciadas facilmente porque apresentam diferentes valores de Km (A Km da enzima de músculo é 2 x 10-5 M). Uma determinação com uma amostra de sangue de um paciente apresentou os resultados dados na tabela abaixo: [S] (M) 5,0 x 10-5 7,0 x 10-5 1,0 x 10-4 1,5 x 10-4 2,0 x 10-4 3,0 x 10-4 6,0 x 10-4 V (moles.ml de soro-1.min-1) 43 57 75 100 120 150 200 Sabendo que o paciente chegou inconsciente no hospital, de modo que você não pode fazer a ele nenhuma pergunta, o paciente sofre de uma doença do fígado, ou simplesmente tem se exercitado violentamente? 12
Baixar