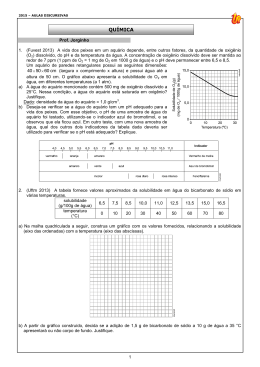
Com base nos dados do gráfico acima, é CORRETO afirmar que: 01) o sulfato de lítio é menos solúvel que o cloreto de amônio. 02) em água a 30°C, é possível dissolver uma massa maior de cloreto de amônio do que de sulfato de lítio. 04) o gráfico sugere que a dissolução do sulfato de lítio constitui um processo exotérmico, ao passo que a dissolução do cloreto de amônio tem caráter endotérmico. 08) a solubilidade do sulfato de lítio seria maior em uma solução contendo Na2SO4 do que em água pura. 16) em água a 0°C, a concentração molar de uma solução saturada de sulfato de lítio é maior que a concentração molar de uma solução saturada de cloreto de amônio. 32) em água a 50°C, é possível dissolver 30 g de sulfato de lítio, mas não é possível dissolver completamente 30 g de cloreto de amônio. Exercício 06 - Módulo 22 Questão 01 Um laboratorista precisa preparar 1,1 kg de solução aquosa saturada de um sal de dissolução exotérmica, utilizando como soluto um dos três sais disponíveis em seu laboratório: X, Y e Z. A temperatura final da solução deverá ser igual a 20 °C. Observe as curvas de solubilidade dos sais, em gramas de soluto por 100 g de água: Soma: ( ) Questão 03 A solubilidade do nitrato de potássio em água, em função da temperatura, é dada na tabela abaixo. 3 Considerando-se soluções de KNO em 100g de água, assinale o que for correto. A massa de soluto necessária, em gramas, para o preparo da solução equivale a: a) 100 b) 110 c) 300 d) 330 o 01) A 20 uma solução com 40 gramas está saturada. o 02) A 0 uma solução com 10 gramas está insaturada. o 04) A 40 uma solução com 120 gramas está supersaturada. o 08) A 100 uma solução com 120 gramas. Questão 02 O gráfico abaixo mostra a variação nas concentrações de soluções saturadas de dois sais em água, Li2SO4 (reta descendente) e NH4Cl (reta ascendente), individualmente, em função da variação na temperatura da solução. A concentração é expressa em termos de percentual massa/massa, ou seja, a massa do sal dissolvido em 100 g da solução. Soma: ( ) Questão 04 O comportamento do gás oxigênio com a variação de Aprovação em tudo que você faz. 1 www.colegiocursointellectus.com.br As solucoes aquosas contidas nos frascos 1, 2, 3 e 4 sao, respectivamente, de a) HCl, NaOH, KCl e sacarose. b) KCl, NaOH, HCl e sacarose. c) HCl, sacarose, NaOH e KCl. d) KCl, sacarose, HCl e NaOH. e) NaOH, HCl, sacarose e KCl. temperatura descrito no gráfico, bem como o comportamento físico geral dos gases, permitem afirmar corretamente que: a) as forças atrativas se sobrepõem às forças de repulsão entre as moléculas do gás oxigênio com o aumento da temperatura. b) as colisões entre as moléculas de um gás aumentam de frequência com o aumento de temperatura, à pressão constante, diminuindo a velocidade média das moléculas e reduzindo sua solubilidade em água. c) a solubilidade de um gás em um líquido depende da energia cinética das moléculas do gás e da pressão exercida sobre o sistema que comporta o soluto gasoso e o solvente líquido. d) dois reservatórios de água mantidos sob as mesmas condições de limpeza e pressão de 1 atm, localizados na Bahia, a 35º C, e no Paraná, a 20º C, terão a mesma concentração de O2(g) dissolvido na água. e) as concentrações de O2(g) dissolvido em amostras de água do mar Báltico e do mar Vermelho independem de suas concentrações salinas, que são 30 g/L e 40 g/L, respectivamente. Questão 07 Tem-se 500g de uma solução aquosa de sacarose (C12H22O11), saturada a 50°C. Qual a massa de cristais que se separam da solução, quando ela é resfriada até 30°C? Dados: Coeficiente de solubilidade (Cs) da sacarose em água: Cs à 30°C = 220g/100g de água Cs à 50°C = 260g/100g de água a) 40,0 g b) 28,8 g c) 84,25 g d) 55,5 g e) 62,5 g Questão 05 Examine o gráfico, que representa a solubilidade (g/L) de um sal iônico em água, em função da temperatura (°C). Questão 08 A 10°C a solubilidade do nitrato de potássio é de 20,0g/100g H‚O. Uma solução contendo 18,0g de nitrato de potássio em 50,0g de água a 25°C é resfriada a 10°C. Quantos gramas do sal permanecem dissolvidos na água? a) 1,00 b) 5,00 c) 9,00 d) 10,0 e) 18,0 Questão 09 Pode-se afirmar que o sal possui a) solubilização exotérmica. b) precipitação endotérmica. c) solubilização endotérmica. d) baixa solubilidade em água. e) solubilidade constante. Foram misturados e agitados 200g de (NH4)2SO4 com 250g de água, resultando um sistema heterogêneo que, por filtração, forneceu 50g de resíduo. Calcule o Cs do sal na temperatura em que a experiência foi realizada. Questão 10 Questão 06 Em um laboratório químico, um estudante encontrou quatro frascos (1, 2, 3 e 4) contendo soluçõess aquosas incolores de sacarose, KCl, HCl e NaOH, não necessariamente nessa ordem. Para identificar essas soluções, fez alguns experimentos simples, cujos resultados são apresentados na tabela a seguir: Industrialmente, a hidrólise de resíduos celulósicos, visando à obtenção de açúcares, é realizada pela ação do ácido sulfúrico, em temperatura e pressão elevadas. Após a hidrólise, a solução apresenta concentração de ácido sulfúrico igual a 49 g/L. Para facilitar a purificação dos açúcares, a solução deve ser neutralizada à temperatura de 50ºC. As seguintes substâncias foram disponibilizadas para a neutralização: óxido de cálcio (cal virgem), solução aquosa de hidróxido de sódio 0,5 mol/L e solução aquosa de hidróxido de amônio 0,5 mol/L. Dado: Soluções aquosas contendo o indicador fenolftaleína são incolores em pH menor do que 8,5 e tem coloração rosa em pH igual a ou maior do que 8,5. É desejável que, após a neutralização, a solução não tenha sofrido um aumento significativo de volume e que não apresente concentração elevada de íons. Baseado Aprovação em tudo que você faz. 2 www.colegiocursointellectus.com.br nas curvas de solubilidade dadas a seguir, indique qual é a substância mais adequada para ser empregada na neutralização, justificando a sua resposta. Escreva a equação da reação correspondente. Considere que a solubilidade dos diferentes sais na solução neutralizada seja a mesma que em água. Aprovação em tudo que você faz. 3 www.colegiocursointellectus.com.br
Baixar