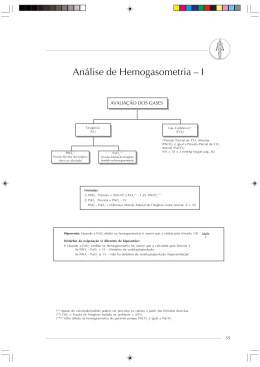
Acidose & Alcalose UTIN – HMIB – Programa de Residência Médica Setembro/2014 Joaquim Bezerra – R3 UTIP HMIB Paula Abdo – R3 UTIP HMIB www.paulomargotto.com.br Referência: DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BÁSICO Autor(es): Paulo R. Margotto/ Geórgia Quintiliano Carvalho da Silva Definições • Ácido: substância doadora de H+; • Base: substância receptora de H+. • Mecanismos de manutenção do pH: – Sistemas tampões – Mecanismo respiratório – Mecanismo renal Equação de Henderson – Hasselbalch pH= pK + log [HCO3-]/[H2CO3] Regulação respiratória do pH • Centro respiratório do Bulbo é sensível a: – PaCO2 – PaCO2 – pH sanguíneo • Receptores químicos do arco aórtico e seio carotídeo • Mecanismos compensatórios temporários Equação de Henderson – Hasselbalch pH= pK + log [HCO3-]/[H2CO3] Regulação respiratória do pH • Centro respiratório do Bulbo é sensível a: – PaCO2 – PaCO2 – pH sanguíneo • Receptores químicos do arco aórtico e seio carotídeo • Mecanismos compensatórios temporários Equação de Henderson – Hasselbalch pH= pK + log [HCO3-]/[H2CO3] Regulação renal do pH • Acidose: – pH urinário 4,5 – Reduz excreção de bicarbonato – Aumento excreção de sais de amônio – Reduz excreção de Na e K Regulação renal do pH • Alcalose: – pH urinário 7,8 – Aumenta excreção de bicarbonato – Reduz excreção de sais de amônio – Aumenta excreção de Na e K ACIDOSE • Aumento da concentração do íon H+ no sangue – Alteração respiratória: excesso de ácido carbônico – Alteração metabólica: excesso de ácidos / redução de bases *Redução na relação HCO³/H²CO³ ACIDOSE RESPIRATÓRIA • Principais causas no RN: – SAM – DMH – Pneumotórax – Derrame pleural ACIDOSE METABÓLICA • Causas no RN: – Hipóxia tecidual, jejum, erro inato do metabolismo – Contratilidade deficiente do miocárdio – Diarréia, obstrução intestinal, acidose tubular renal Alcalose • Termo usado para definir uma concentração de íons H+ no sangue inferior ao normal. • A diminuição da concentração do H+ pode ocorrer em conseqüência de uma alteração respiratória primária (perda de ácido carbônico): ALCALOSE RESPIRATÓRIA; ou de uma alteração metabólica primária (aumento do teor de bases ou a perda de ácidos no organismo): ALCALOSE METABÓLICA. Alcalose • Metabólica: excesso de base ou perda de acido. - PaCO2: aumento da relação HCO3/H2CO3; Aumento do pH • Respiratória: perda de CO2 (e do H2CO3) devido a hiperventilação - Queda da PaCO2, da relação HCO3/H2CO3; Aumento do pH Alcalose Metabólica • No RN, as causas mais comuns são: perda de líquido gástrico pelo vômito (estenose hipertrófica de piloro), condições que expoliam potássio (furosemida) e excesso de NaHCO3. • Correção: tratar a causa básica; dar ao rim condições de excretar o excesso e NaHCO3 (aporte adequado de cloreto, Na+ e K+). Alcalose Respiratória • No RN as principais causas são: encefalite, meningite, febre, doenças pulmonares, localizadas, alterações no SNC, ventilação mecânica. Valores – Gasometria Arterial • • • • • • pH: 7,35 – 7,45 PaCO2: 35-45 mmHg PaO2: manter entre 50 -70 mmHg Bicarbonato: 22-26 mEq/l BE: -2,5 a 2,5 Anion Gap (Na+ + K+) – (Bic + Cl-): 8-16mEq/l Relação pH-K+ sérico/ Cálcio • 0,1 pH ± 0,6mEq/l K (sentido oposto) • 0,1 pH ± 0,46mg% Cai (sentido oposto) GASOMETRIA A LÓGICA DO RACIOCÍNIO (slide) Autor(es): Paulo R. Margotto Gasometria Além das Fórmulas! 1982 Não é necessário muito esforço Para entender a gasometria. É necessário Raciocínio Conhecer sempre a história clínica Nunca interprete a gasometria sem conhecer a história clínica! • Raciocinar com os mecanismos respiratórios e renais ( ter em mente a relação 20/1) • Não tratar a doença como diferenças de base e sim o fator causal • As fórmulas são secas : deve -se apenas melhorar (Nunca queira corrigir completamente) Bicarbonato de sódio-terapia basicamente inútil Autor(es): Judy L. Aschne, Ronald L. Poland. Apresentação: Liana de Medeiros Machado • Apesar de > 50 anos de experiência do uso de NaHCO3, dados não suportam uma rede de benefícios em RN com acidose metabólica • Uma razoável, mas não provada exceção, é de reposição de base em perdas renais ou gastrointestinais • Possíveis efeitos adversos: flutuação nos níveis sanguíneos cerebrais, hemorragia intracraniana, diminuição de oferta de oxigênio aos tecidos, acidose intracelular incontrolável, agravos à injúria miocárdica e deterioração da função cardíaca Manuseio do pH e PaCO2 na UTI Autor(es): Judy Aschner (EUA). Realizado por Paulo R. Margotto • • • • O bicarbonato de sódio (NaHCO3), no início, foi comercialmente produzido no fim dos anos 50. O conceito tradicional é que a acidemia compromete a contratilidade cardíaca, limitando os esforços de reanimação. Os médicos sabem que deve ser corrigida a acidose antes de administrar epinefrina, uma vez que a acidose atenua a contratilidade cardíaca, a pressão arterial e a resposta da freqüência cardíaca às catecolaminas. A idéia de que corrigir a acidose dando NaHCO3 melhora o desfecho clinico, jamais foi demonstrado na literatura que isto seja verdade, havendo dados que possa ser contraproducente. O NaHCO3 corrigiu a acidose metabólica arterial, mas levou a diminuição do pH intramiocárdio (Kette F, et al. Buffer agents do not reverse intramyocardial acidosis during cardiac resuscitation Circulation. 1990 May;81(5):1660-6) e reduziu a probabilidade do sucesso da reanimação. Alem do mais, qualquer solução hipertônica administrada em parada cardíaca tinha um efeito adverso aos esforços de reanimação cardíaca (há uma redução da pressão de perfusão coronariana [PPC], que é a pressão aórtica menos pressão átrio direito). A administração rotineira de bicarbonato de sódio 1mEq/Kg durante a reanimação cardiopulmonar resulta em hipernatremia, hiperosmolalidade e alcalose metabólica. Ambos, a alcalose metabólica e a hiperosmolalidade seguindo a reanimação cardiopulmonar têm sido associadas ao aumento da mortalidade “A experiência é a capacidade de cometer o erro repetidamente com uma segurança cada vez maior”. “Aqueles que não conseguem relembrar o passado estão condenados a repeti-lo”. Dr. Joaquim Bezerra, Dr. Paulo R. Margotto e Dra. Paula Abdo!
Baixar