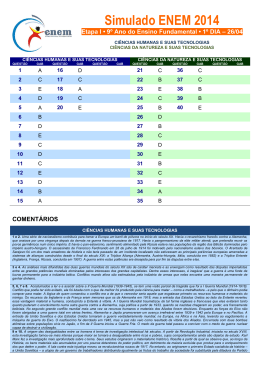
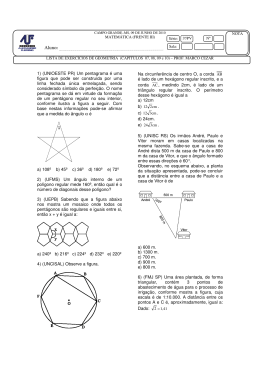
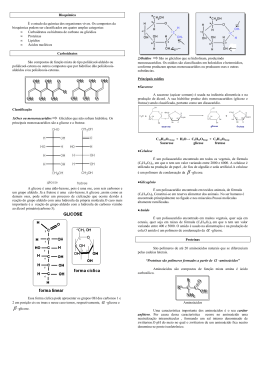
Química Prof. Arilson Aluno(a):______________________________________________________ Em que [α]D Exercícios propostos 20 º C a) Carboidratos b) 01 - (UFG GO) Medidas do teor de glicose no sangue utilizam fitas reagentes nas quais ocorrem a seguinte reação CH2OH H H OH H H + O2 OH O + H2O 2 H oxidase OH H OH H OH OH H O 1C O H OH Glicose H Gab: a) H CH2OH O OH Glicose H Nessas fitas, a água oxigenada formada se decompõe eletroquimicamente, e a intensidade dessa decomposição é medida de modo a determinar o teor de glicose. H b) Para a reação acima, determine o número de oxidação do carbono sp2 e os agentes redutor e oxidante. Escreva a fórmula estrutural plana da glicose com cadeia aberta (acíclica). C OH C H C OH C OH 2 3 4 5 6 a) é o valor do desvio da luz polarizada, a 20ºC. Numere os carbonos na estrutura, a seguir, correspondentemente com os numerados na forma fechada. Explique por que o produto da hidrólise da sacarose recebe o nome de “açúcar invertido”. CH2OH b) Uma solução de sacarose desvia o plano da luz polarizada para a direita, conforme pode ser observado pelo valor de [α ]D 20 º C a esquerda, uma vez que [α]D 20 º C Gab: da glicose = + 52,7º e o da frutose é de – 92,3º, sendo a resultante o valor da soma desses valores, que será igual a – 39,6º. Desse modo, como houve inversão do sinal do desvio sofrido pela luz polarizada, diz-se que o açúcar é “invertido”. a) CH2 OH O H HO = +66,5º . Já a solução resultante da hidrólise (glicose + frutose) desvia o plano da luz polarizada para OH H H OH 03 - (UFAC) A busca do álcool extraído de celulose, chamado de etanol de segunda geração, está mobilizando um número crescente de pesquisadores brasileiros. O alvo é aproveitar o bagaço e a palha da cana-de-açúcar, fontes de celulose, que respondem por dois terços da energia da planta, mas não são convertidos em biocombustíveis. Resíduos, como aparas de madeira, bagaço de cana ou sabugo de milho são formados por celulose e podem transformar-se em biocombustível, quando submetidos a reações de hidrólise, um processo químico de quebra de moléculas. O interesse brasileiro pelo etanol de celulose busca tornar ainda mais competitivo o etanol de cana, ampliando sua produção, sem precisar aumentar, na mesma proporção, a área plantada de cana-de-açúcar. MARQUES, F., O alvo é o bagaço, Revista Pesquisa Fapesp, Edição 163, 2009. (adaptado) O nox = +3 Agente oxidante = oxigênio (O2) Agente redutor = glicose (C6H12O6) b) H O C H C OH HO C H H C OH H C OH H C OH Celulose é um polímero cujos monômeros são: a)moléculas de glicose. d)moléculas de frutose. H 02 - (UFG GO) A sacarose, em meio aquoso ácido, sofre hidrólise produzindo glicose e frutose que co-existem, nessa solução, nas formas aberta e fechada. O produto dessa hidrólise é chamado de “açúcar invertido”. A equação química da reação é mostrada, a seguir: 6 CH2OH 5 O H H OH 4 CH2OH O H H OH H Gab: A 04 - (FEPECS DF) Um processo que pode ser utilizado pelos animais para obter energia sob condições anaeróbicas é a glicólise, que ocorre comumente nos músculos de vertebrados e pode ser representada de modo simplificado pela transformação de glicose em ácido lático de acordo com a equação não balanceada: 1 H OH OH HO H b)lipídeos. c)aminoácidos. e)moléculas de sacarose. OH H OH HO H glicose HO H 20 ºC [α] D = OH CH2OH O O + CH2OH O CH2OH HO H OH H HO HO H H CH2OH sacarose 20 ºC [α] D = +66,5 frutose 20 ºC [α] D www.cursosimbios.com.br OH H +52,7 OH H+ H2O HO H H O O 2 3 OH OH Quando um mol de glicose é degradado em 2 mols de ácido lático, 2 mols de ATP são sintetizados. Na degradação de 4,5 g de glicose, a massa de ácido láctico e o número de mols de ATP produzidos, considerando a transformação completa da glicose em ácido láctico, são respectivamente, iguais a: a)2,25 g e 2 mol; b)2,25 g e 1 mol; c)4,5 g e 1 mol; d)4,5 g e 0,05 mol; e)9,0 g e 0,05 mol. = -92,3 1 a)o etilenoglicol. b)o glicerol. c)a sacarose. e)a frutose. Gab: D 05 - (FUVEST SP) O seguinte fragmento (adaptado) do livro Estação Carandiru, de Drauzio Varella, refere-se à produção clandestina de bebida no presídio: “O líquido é transferido para uma lata grande com um furo na parte superior, no qual é introduzida uma mangueirinha conectada a uma serpentina de cobre. A lata vai para o fogareiro até levantar fervura. O vapor sobe pela mangueira e passa pela serpentina, que Ezequiel esfria constantemente com uma caneca de água fria. Na saída da serpentina, emborcada numa garrafa, gota a gota, pinga a maria-louca (aguardente). Cinco quilos de milho ou arroz e dez de açúcar permitem a obtenção de nove litros da bebida.” Na produção da maria-louca, o amido do milho ou do arroz é transformado em glicose. A sacarose do açúcar é transformada em glicose e frutose, que dão origem a dióxido de carbono e etanol. Dentre as equações químicas, I. (C 6 H10 O 5 ) n + nH 2 O → nC6 H12 O 6 , II. nCH 2 [ CH 2CH 2O ] n + nH2O Gab: D 08 - (UFTM MG) A glicose apresenta a seguinte fórmula estrutural: H H C H C OH H C OH CH2OH Em relação à glicose, são feitas as afirmações: I. é uma substância apolar; II. suas soluções aquosas não apresentam condutividade elétrica; III. suas soluções aquosas são opticamente ativas; IV. é produzida por meio da hidrólise do amido. Está correto o contido apenas em a)I. b)I e II. c)II e III. d)III e IV. e)II, III e IV. III. C12 H 22 O11 + H 2 O → 2 C 6 H12 O 6 , IV. C 6 H12 O 6 + H 2 → C 6 H14 O 6 , Gab: E as que representam as transformações químicas citadas são Dado: C6H12O6 = glicose ou frutose a)I, II e III. b)II, III e IV. c)I, III e V. d)II, III e V. e)III, IV e V. Gab: C 06 - (FUVEST SP) Aldeídos podem reagir com álcoois, conforme representado: OH O H 3C + HOCH2CH 3 H C H3C C OCH 2CH 3 H Este tipo de reação ocorre na formação da glicose cíclica, representada por HO O OH a) b) OH OH Dentre os seguintes compostos, aquele que, ao reagir como indicado, porém de forma intramolecular, conduz à forma cíclica da glicose é b) O OH OH OH H c) OH OH OH O O OH HO H OH OH e) d) OH OH HO OH OH OH HO OH O O OH Gab:C 07 - (UNIFOR CE) O amido, o glicogênio e a celulose têm fórmula molecular (C6H10O5)n. A diferença entre esses compostos está na maneira como os monômeros se ligam e no valor de n. Todos são polímeros naturais, cujo monômero é www.cursosimbios.com.br c) Diabetes. Seria recomendado cereal com baixos (menores) teores de amilopectina em relação à amilose (maiores teores de amilose em relação à amilopectina). O índice glicêmico, de acordo com o texto, está relacionado com o teor de açúcar produzido pela digestão do amido. 10 - (UFABC SP) O principal componente das fibras da polpa de açaí é a celulose, um polímero de glicose que possui função estrutural na célula vegetal, como um componente importante da parede celular.Sobre esse tema, afirma-se que I. a celulose é um polímero natural que resulta da união entre átomos de carbono pertencentes a duas moléculas de glicose. II. para formar fibras lineares de celulose, a polimerização da glicose se faz com eliminação de água. III. a glicose é também o monômero do amido, um polímero que os vegetais utilizam como reserva energética. É correto o que se afirma apenas em OH HO HO OH 09 - (UNICAMP SP) As plantas estocam suas reservas de açúcar como amido nas formas de amilose e amilopectina. A amilose é mais dificilmente transformada nos seus açúcares constituintes; conseqüentemente, alimentos ricos em amilose conduzem a um “índice glicêmico” mais baixo do que aqueles ricos em amilopectina. Por conta disso, pesquisadores têm desenvolvido grãos vegetais em que a relação entre as quantidades dessas duas formas de amido é diferente da que se verifi ca na planta original. O principal interesse dessas pesquisas diz respeito à melhoria da saúde humana pelo uso desses produtos como coadjuvantes no tratamento de certas doenças e no controle de peso corporal. a) De acordo com o texto e com seus conhecimentos sobre ciências, dê o nome de uma doença cujo tratamento poderia utilizar os produtos resultantes dessas pesquisas. b) Se você fosse fabricar um alimento indicado para pessoas que precisassem controlar o peso em valores baixos, que tipo de cereal você usaria preferencialmente: com alto ou baixo teor de amilopectina em relação à amilose? c) Também de acordo com o texto, explique resumidamente o que é o “índice glicêmico”. Gab: OH a) OH HO C H OH V. C 6 H12 O 6 → 2 CH 3 CH 2 OH + 2 CO 2 , O C CH2 , OH d)a glicose. a)I. b)III. c)I e II. d)I e III. e)II e III. Gab: E Proteinas 01 - (UFG GO) Uma das formas de separar proteínas é usar uma coluna de vidro, conforme representado na figura a seguir. 2 H HS O CH2 C C OH NH2 cisteína é um aminoácido alifático; apresenta isomeria óptica; em contato com HCl(aq), (aq), a cisteína é uma base de Brönsted, dando origem a um íon positivo; IV. a união nião entre duas unidades de cisteína dá-se dá por meio de uma ligação peptídica. I. II. III. Considere uma coluna de vidro com partículas carregadas positivamente e três proteínas, denominadas A, B e C, constituídas pelos seguintes aminoácidos ionizados: São corretas as afirmações a)I, II, III e IV. b)I, I, II e III, apenas. d)II e III, apenas. e)II II e IV, apenas. c)I, III e IV, apenas. Gab: A 03 - (FMJ SP) Considere a reação ão orgânica representada na equação: CH 3 CH COOH + CH3 CH NH 2 COOH NH 2 CH 3 CH3 CH CO O NH CH COOH + H 2O NH2 A reação química considerada e a ligação que ocorre na junção de seus reagentes podem ser denominadas, correta e respectivamente, como reação de a) adição e ligação de hidrogênio. b) adição ição e ligação peptídica. c) condensação e ligação de hidrogênio. d) condensação e ligação peptídica. e) desidratação e ligação de hidrogênio. Gab: D a) b) As proteínas deixam a coluna na seguinte ordem: B, C e A. Considerando essas informações, identifique a proteína que tem o maior teor de lisina e a proteína que tem o maior teor de aspartato. Justifique sua resposta. Escreva a fórmula estrutural plana de um fragmento de proteína, cuja sequência de aminoácidos seja Gly-Ala-Leu. Leu. 04 - (UFT TO) As enzimas atuam nos seres vivos como catalisadores das reações bioquímicas e estão presentes ntes em células vivas. Por se tratarem de proteínas, um polipeptídeo, são formadas pela combinação de vinte tipos de moléculas que se unem através de ligações peptídicas. Observe as fórmulas estruturais abaixo de diferentes moléculas, sendo R e R2 representação tação de radicais alquila. Gab: a) A proteína B é a que possui o maior teor de lisina - aminoácido de carga positiva. Assim, escoa mais rapidamente pela coluna, por ser menos atraída pelas partículas positivas as nela contidas. A proteína A é a que possui o maior teor de aspartato, que é um aminoácido carregado negativamente. Por isso, escoa com menor velocidade pela coluna, uma vez que será mais atraído pelas partículas de cargas positvos. O O O R R N(C2H5)2 (II) (I) b) + H3 N O- O + O + + H3 N O- O- O O + H3 N (III) (IV) O OH NO2 NH H2 (V) (V VI) O R2 NO 2 O (VII) O O + 2H2 O N N O H NO2 R2 R H + H3 N - R2 R2 R2 H H NH 2 02 - (FGV SP) Considere as seguintes afirmações sobre a cisteína: OH NH2 O O O R OH H NH 2 O R (VIII) OH N(C2H5)2 (IX)) N(C2H5)2 (X) Assinale a alternativa que representa as duas fórmulas possíveis que ao se combinarem geram um dipeptídeo. www.cursosimbios.com.br 3 a)(III) e (VI) e)(V) e (X) b)(I) e (IX) c)(II) e (VIII) d)(IV) (IV) e (VII) Gab: A 05 - (UFG GO) O gráfico a seguir representa a composição relativa de uma solução de um determinado aminoácido. d) De acordo com o gráfico, esse aminoácido encontra-se se na(s) forma(s) a) zwitteriônica em pH fisiológico. b) aniônica em pH ácido. c) catiônica em pH alcalino. d) zwitteriônica e aniônica em pH 1. e) catiônicas e aniônicas em pH 12. 08 - (UNIFESP SP) O ponto isoelétrico (pI) é o equivalente ao pH de uma solução aquosa de um aminoácido, em que o número de cargas positivas (protonação do grupo amina) de suas moléculas iguala-se iguala ao número de cargas negativas (desprotonação do grupo ácido carboxílico). As diferenças nos valores de pI podem, por meio de técnicas apropriadas, ser se úteis na separação de proteínas. Considere os aminoácidos e intervalos de valores de pI apresentados a seguir. Aminoácidos: alanina: CH 3 – CH(NH 2 ) – COOH aspartato: HOOC – CH 2 – CH(NH 2 ) – COOH Gab: A lisina: NH 2 – CH 2 – CH 2 – CH 2 – CH 2 – CH(NH 2 ) – COOH 06 - (UFSCAR SP) A atual crise mundial de alimentos traz muitas questões para serem discutidas, já que a vida humana depende de de uma alimentação adequada, que garanta a ingestão de diversos nutrientes. Proteínas são compostos orgânicos vitais para o bom funcionamento de nosso organismo, sendo que algumas devem ser ingeridas, pois contêm aminoácidos essenciais que não são sintetizados tizados a partir de outros compostos. Assinale a alternativa que traz apenas exemplos de proteínas. a) b) c) d) e) 1 mol de fenialanina ––– 165 g x ––– 0,33 g x = 2 × 10–3 ou 0,002 mol/L Adrenalina, sacarose e cafeína. Insulina, caseína e glicerina. Vasopressina, nicotina e glicerina. Colágeno, queratina e hemoglobina. Dimetilamina, imunoglobulina e quitina. Gab: D 07 - (UFU MG) Em refrigerantes do tipo light, utiliza-se se fenilalanina como adoçante dietético. A fenilcetonúria – doença cujos sintomas são atraso no desenvolvimento psicomotor, convulsões, hiperatividade, tremor e microcefalia – é caracterizada pelo efeito ou ausência de uma enzima que metaboliza a fenilalanina. Embora seja hereditária, essa doença pode ser detectada logo após o nascimento por meio do “teste do pezinho”. Pessoas com fenilcetonúria devem evitar refrigerantes frigerantes dietéticos à base de fenilalanina, cuja estrutura está disposta abaixo. N H C I: 3,0 – 3,5 II: 5,5 – 6,0 III: 9,0 – 10 Com base nas informações fornecidas, é possível prever que soluções aquosas dos aminoácidos alanina, aspartato e lisina apresentam, respectivamente, pI dentro dos intervalos a)I, II e III. b)I, III e II. c)II, II, I e III. d)II, III e I. e)III, I e II. Gab: C 09 - (UFTM MG) Para determinação da composição das proteínas, a eletroforese é um dos métodos mais aplicados, que consiste na migração de íons submetidos a uma diferença de potencial. Na dissolução de um aminoácido aminoáci em água, há a formação do zwitterion, resultante de uma reação ácido-base ácido intramolecular. Em soluções aquosas, o caráter ácido ou básico da solução determina a forma predominante do aminoácido, representada na equação: H H R C O + H+ C NH 2 H H Intervalos de pI: R + OH- O- C O + H+ O- + OH- C NH +3 O H C CH2 O + H+ R OH C + OH- C NH+3 OH Zwitterion a) b) Dados: Massa Molar: 165 g/mol Com base nessa estrutura, faça o que se pede. a) b) c) d) Identifique duas funções orgânicas presentes na estrutura da fenilalanina. Escreva o nome da fenilalanina segundo a IUPAC. Equacione a reação da fenilalanina com hidróxido de sódio. Calcule a concentração equivalente em mol/L de um refrigerante que contenha 0,33 g/L de fenilalanina. Qual é a forma predominante de um aminoácido quando, submetido à eletroforese, ocorre migração para o pólo positivo? Escreva a reação de formação do dipeptídeo ala-gli ala entre os α aminoácidos glicina (R = H) e alanina [R = CH3]. Gab: a) b) Estará predominantemente na forma negativa. O H 2N CH CH 3 O C H2N OH + CH H C OH Gab: a) b) c) Amina Ácido carboxílico Ácido 2-amino-3-fenilpropanóico www.cursosimbios.com.br 4 O H2N CH C CH3 O N CH H H + H2O C OH H 10 - (UFG GO) A eletroforese é uma técnica utilizada para a separação de substâncias que estejam ionizadas. Consiste na aplicação de uma ma diferença de potencial entre eletrodos, a fim de que as espécies migrem segundo o campo aplicado e de acordo com sua carga e massa molar. Um sistema contendo uma solução com três aminoácidos, representados a seguir, é submetida à eletroforese. O O O HO O OH OH NH 2 NH 2 Glicinna Ácido glutânico O NH HO N NH2 NH2 H Arginina Explique o comportamento do sistema submetido à eletroforese realizada em: a) meio ácido (HCl 0,1 mol/L); b) meio alcalino (NaOH 0,1 mol/L). 11 - (UFTM MG) Para determinação da composição das proteínas, a eletroforese é um dos métodos mais aplicados, que consiste na migração de íons submetidos a uma diferença de potencial. Na dissolução de um aminoácido em água, há a formação do zwitterion, resultante de uma reação ácido ácido-base intramolecular. Em soluções aquosas, o caráter ác ácido ou básico da solução determina a forma predominante do aminoácido, representada na equação: H H O O +H + +H + R C C R C C +OH +OH OONH 2 NH3+ H +H+ R Gab: a) a) O O b) O HO O OH OH Trata-se se de um Zewitterion negativo. H H N+ HO H NH 3+ b) NH 3+ C + C OH H H O O H3C O C C NH 3 OH H O O H O NH 2 Os aminoácidos protonados migrarão conforme a carga total e sua massa molar, sendo ndo que os mais carregados serão atraídos mais fortemente para o pólo negativo; considerando-se os aminoácidos de mesma carga, o de menor massa molar migrará mais rapidamente que o de maior massa. em meio alcalino (0,1 mol/L), os aminoácidos serão desprotonados, despr adquirindo as seguintes configurações: O OH NH3+ Qual é a forma predominante de um aminoácido quando, submetido à eletroforese, ocorre migração para o pólo positivo? Escreva va a reação de formação do dipeptídeo ala-gli ala entre os αaminoácidos glicina (R = H) e alanina [R = CH3]. NH O O C Gab: a) b) NH3+ NH3+ +OH- Zwitterion Em meio ácido (0,1 mol/L), os aminoácidos serão protonados, adquirindo as seguintes configurações: C O - - H O C C NH 2 O N CH H CH3 C OH dipeptídioo ala-gli 12 - (FMJ SP) Nos portadores de uma doença genética denominada fenilcetonúria, o fígado apresenta uma deficiência que não permite a conversão de fenilalanina em tirosina. H H NH 2 NH2 O CH2 NH C COOH HO O CH2 C COOH NH2 NH 2 Tirosina Sobre as substâncias fenilalanina e tirosina, pode-se pode afirmar que a) as duas substâncias tâncias são diferenciadas pela função álcool. b) a função fenol apresenta caráter básico, logo a tirosina reagirá com ácidos. c) as duas substâncias realizam ligações peptídicas na formação de proteínas. d) apenas a fenilalanina apresenta núcleo benzênico. benzên e) as duas substâncias apresentam um carbono quaternário. Fenilalanina - N O NH2 NH 2 H Os aminoácidos desprotonados migrarão conforme a carga total e sua massa molar, sendo que os mais carregados serão se atraídos mais fortemente para o pólo positivo; considerando-se se os aminoácidos de mesma carga, o de menor massa molar migrará mais rapidamente que o de maior massa. www.cursosimbios.com.br 5 Gab: C b) 13 - (UFMA) Quando dissolvido em água, o ácido α , β - diaminopropanóico (um aminoácido) gera: a) um zwittérion neutro e uma solução neutra b) um zwittérion positivo e uma solução ácida c) um zwittérion negativo e uma solução básica d) um zwittérion negativo e uma solução ácida e) um zwittérion positivo e uma solução básica c) Gab: E 14 - (Unioeste PR) A fenilcetonúria é uma desordem metabólica cuja principal conseqüência é o retardamento mental. Esta desordem é proveniente da ausência ou mau funcionamento da enzima fenilalanina hidroxilase, que promove a transformação da fenilalanina em tirosina, como mostrado no esquema abaixo. d) Os ácidos graxos essenciais são aqueles produzidos bioquimicamente pelos seres humanos. Os ácidos graxos insaturados são mais comumente encontrados na gordura animal, enquanto os saturados são mais encontrados em gordura vegetal. São encontrados em materiais elaborados pelos organismos, denominados lipídios, que são biomoléculas insolúveis em água. Gab: D 02 - (UEPG PR) As gorduras trans, que são produzidas durante a hidrogenação de óleos vegetais no processo de obtenção de gorduras hidrogenadas, estão relacionadas com várias patologias. Assim, a Agência Nacional de Vigilância Sanitária (Anvisa) determinou, por meio de uma resolução, a obrigatoriedade, a partir de 1º/8/2006, de os produtos industrializados apresentarem, em seus rótulos, informações a respeito do percentual de gordura trans. Os óleos vegetais, por outro lado, que correspondem aos isômeros cis, são saudáveis quando dentro de uma dieta equilibrada. A respeito deste assunto, analise as estruturas abaixo e assinale o que for correto. CH3 H H2N C H COOH CH2 H2N Fenilalanina hidroxilase C H3C COOH O CH2 HO O2 O HO (I) OH Tirosina Fenilalanina (II) O Considerando as informações acima, assinale a(s) alternativa(s) correta(s). 01. A fenilalanina e a tirosina possuem atividade óptica, pois ambas apresentam carbono quiral. 02. A fenilalanina e a tirosina são isômeros. 04. A massa molar da tirosina é 181 g/mol, considerando as massas atômicas como números inteiros. 08. As enzimas são catalisadores biológicos. 16. A nomenclatura oficial da fenilalanina é ácido 2-amino-1fenilpropanóico. 32. A transformação da fenilalanina em tirosina é uma reação de redução. 64. A fenilalanina e a tirosina são compostos classificados como aminoácidos. Gab: 77 OH (III) OH O CH3 (IV) 01. O composto I representa a gordura trans. 02. Os compostos I, II e III podem transformar-se em IV, numa reação ideal, por adição de 3, 2 ou 1 mol hidrogênio/mol de óleo, respectivamente. 04. Os compostos I e II são saudáveis. 08. Todos os compostos representados são ácidos graxos. Gab: 12 15 - (UECE) As assertivas abaixo se referem às proteínas que têm um papel fundamental em quase todos os processo biológicos. I. Facilitam o transporte e o armazenamento de substâncias, o movimento coordenado e a proteção contra enfermidades II. Apresentam massa molecular relativamente pequena, inferior a 50g; III. Carbono, hidrogênio, oxigênio, nitrogênio e enxofre fazem parte de sua composição IV. O corpo humano contém cerca de 100.000 tipos de proteínas cada uma com uma função específica V. As proteínas do corpo humano são formadas por mais de 40 tipos de aminoácidos distintos São verdadeiras: a)I, II e III b)I, III e IV c)I, IV e V d)II, III e V Gab: B Lipídios 01 - (UECE) As gorduras trans são um tipo especial de ácido graxo, formado a partir de ácidos graxos insaturados. Elas elevam o nível da lipoproteína de baixa densidade no sangue (LDL ou "colesterol ruim"). Nem sempre a indicação do rótulo Zero Trans é verdadeira porque a ANVISA tolera até 0,2 g de gordura trans por porção. Sobre ácidos graxos, assinale o correto. a) CH3 Ácidos graxos ou ácidos gordos são ácidos de cadeia normal que apresentam o grupo carbonila (–COOH) ligado a uma longa cadeia alquílica, saturada ou insaturada. www.cursosimbios.com.br 03 - (UNIRIO RJ) Os lipídios são tipos de biomoléculas que se encontram distribuídos em todos os tecidos, principalmente, nas membranas celulares e nas células de gordura. Embora não apresentem nenhuma característica estrutural comum, os lipídios possuem poucos heteroátomos. Isto faz com que estes sejam pobres em dipolos, daí a razão para serem fracamente solúveis em água. Este fenômeno ocorre devido ao fato de que as moléculas dos lipídios a) apresentam uma polaridade muito alta. b) apresentam uma polaridade semelhante à da água. c) apresentam uma polaridade muito baixa e, em certos casos, igual a zero. d) são moléculas de baixo peso molecular, sendo impossível se dissolver em solventes de baixo peso molecular. e) apresentam momento dipolar negativo, enquanto o momento dipolar da água é igual e zero. Gab:C 04 - (UNICAMP SP) As “margarinas”, muito usadas como substitutos da manteiga, contêm gorduras vegetais hidrogenadas. A diferença fundamental entre uma margarina “light” e outra “normal” está no conteúdo de gordura e de água. Colocou-se em um tubo de ensaio uma certa quantidade de margarina “normal” e, num outro tubo de ensaio, idêntico ao primeiro, colocou-se a mesma quantidade de margarina “light”. Aqueceu-se em banho-maria os dois tubos contendo as margarinas até que aparecessem duas fases, como esquematizado na figura. 6 (Anvisa). Além dessa gordura, outros constituintes devem constar ainda no rótulo dos alimentos, como por exemplo o sódio. O consumo excessivo de gorduras trans pode causar aumento do colesterol, e o de sódio pode resultar no aumento da pressão arterial, que estão associados às doenças do coração, como o infarto. O ácido elaídico, com a estrutura mostrada na figura, é classificado como gordura trans e o seu isômero geométrico é o ácido oléico. 10 CH3 5 (CH2)7 C H a) b) Gab: a) 10 fase lípídica fase aquosa COOH Valor calórico ................ 74 kcal 4% Carboidratos ..................... 0 g Proteínas ........................... 0 g 0% 0% Gorduras totais ................ 8,3g 15% Gorduras saturadas .......... 4,8 g Gordura trans ................... 0,2 g 22% ** Fibra alimentar ................. 0 g 0% Sódio............................... 92 mg (*) Valores Diários com base em uma 4% Gab: a) O OH ácido oléico (gordura insaturada cis) 05 - (UEPG PR) Rancificação é uma reação química responsável pela deterioração de gorduras, percebida pelo aparecimento de gosto ruim (ranço). A equação química abaixo representa o processo, de maneira simplificada: RCH = CHR 1 + O 2 → RCHO + R 1CHO (CH 2)7 dieta de 2.000 kcal (**) VD não disponível a) Apresente a fórmula estrutural do ácido oléico. Qual é a diferença na estrutura química de uma gordura trans e de uma gordura saturada? b) Calcule a quantidade em mol de átomos de sódio (massa molar 23 g/mol) e o número de átomos de sódio na manteiga contida dentro dessa lata. Dado: Constante de Avogadro = 6,0 x 1023 mol–1 5 0 C A tabela refere-se à informação nutricional para uma porção de 10 g que consta no rótulo de uma lata de 200 g de manteiga. Quantidade por porção % VD * 0 Reproduza, na resposta, a figura do tubo correspondente à margarina “light”, identificando as fases lipídica e aquosa. Admitindo que as duas margarinas tenham o mesmo preço e considerando que este preço diz respeito, apenas, ao teor da gordura de cada uma, em qual delas a gordura custa mais e quantas vezes (multiplicação) este preço é maior do que na outra? A fase lipídica é menos densa que a fase aquosa e com isso ela ficará na parte superior do tubo. A margarina "light" é a que apresenta menor fase lipídica. b) Como ambas têm o mesmo preço e o volume de gordura na margarina normal é o dobro da "light", podemos dizer que a gordura da "light" custa duas vezes mais que a da normal. H O OH ácido esteárico (gordura saturada) b) 0,2 mol; 1,2 . 1023 átomos Para reduzir a ocorrência da reação, muitas embalagens são protegidas por folhas de alumínio ou hermeticamente fechadas sob nitrogênio. Nos rótulos de diversos produtos alimentícios embalados desta forma, encontram-se informações como: Assinale o que for correto. 01. A velocidade da rancificação torna-se menor quando a temperatura diminui. 02. Se o lipídio for submetido previamente à hidrogenação, torna-se mais resistente à rancificação. 04. O prazo de validade do alimento diminui após a abertura da embalagem devido à oxidação do alimento pelo ar. 08. Os produtos da rancificação são álcoois. 16. Os alimentos contendo lipídios poliinsaturados são mais resistentes à rancificação. Gab: 07 06 - (UFTM MG) Os rótulos dos alimentos devem informar a presença de gordura trans para atender à norma da Agência Nacional de Vigilância Sanitária www.cursosimbios.com.br 7
Baixar