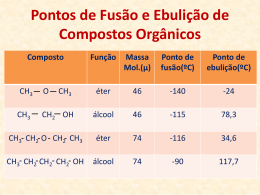
REVISÃO QUÍMICA Profº JURANDIR QUÍMICA 01. Os hidrocarbonetos são extraídos da matéria, principalmente na forma de petróleo e gás natural. A sociedade moderna tornou-se totalmente dependente do consumo desses compostos. Além de ser a principal fonte de energia que move o mundo. As reservas de petróleo e gás natural não são renováveis e que seus preços internacionais causam impacto nas economias de todos os países, no Brasil a PETROBRAS vem investindo na prospecção de petróleo e atingiu, recentemente, a auto-suficiência brasileira, conseguindo atingir a meta de 2 milhões de barris por dia. Sobre o petróleo e seus derivados, coloque verdadeiro ou falso: ( ) O óleo diesel apresenta um ponto de ebulição menor que o óleo lubrificante ( ) Pode-se obter naftaleno, benzeno e antraceno a partir do alcatrão da hulha. ( ) Pode-se obter gasolina a partir de GLP utilizando o craqueamento ( ) O petróleo de base naftênica é de superior qualidade ao de base parafínica. ( ) Método para converter hidrocarbonetos de cadeia aberta em hidrocarbonetos aromáticos é denominado de reforma catalítica FRAÇÃO Nº DE CARBONOS GÁS NATURAL 1a2 G.L.P. 3a4 ÉTER DE PETRÓLEO 5a6 BENZINA 7a8 NAFTA 8a9 GASOLINA 6 a 12 QUEROSENE 10 a 15 ÓLEO DIESEL 15 a 18 ÓLEO LUBRIFICANTE 18 a 20 PARAFINA Acima de 20 ASFALTO Acima de 20 PICHE Acima de 20 DIVISÃO: - Base Parafínica (90% de alcanos). - Base Naftênica (alcanos + 15 a 20% de ciclanos). - Base Aromática (alcanos + 25 a 30% de aromáticos). - Base Asfáltica (Hc de massa molar elevada). Carvão Mineral A destilação seca da hulha à 1 000º C A destilação seca da hulha à 1 000º C fornece: fornece: gásda dahulha: hulha: mistura mistura de 2, CH 4, CO; gás deHH , CH 2 4, CO; águas amoniacais: solução de NH4OH e seus águas amoniacais: Solução de NH OH e 4 sais; seus sais; alcatrão da hulha: líquido oleoso, escuro, alcatrão da hulha: líquido oleoso, escuro, formado principalmente por aromáticos; formado principalmente por aromáticos; carvão coque: principal produto, usado com redutor coque: em metalurgia. carvão principal produto, usado para aquecer fornos siderúrgico. CRACKING DO PETRÓLEO • Significa a “quebra”, por aquecimento (pirólise), na presença de catalisadores, de moléculas de hidrocarbonetos de maior massa molar, com a finalidade de aumentar o rendimento da fração gasolina. REFORMA CATALÍTICA (REFORMING) A reformação catalítica é um processo refinação com duas principais finalidades: conversão de combustível de baixo IO (índice octano) em outra de maior IO; b) produção hidrocarbonetos aromáticos. de a) de de • Método para converter hidrocarbonetos de cadeia aberta em hidrocarbonetos aromáticos. CH3-(CH2)5-CH3 C6H5-CH3 Heptano Metilbenzeno + 4H2 Hidrogênio ISOMERIZAÇÃO • Transformação de compostos de cadeia linear em compostos ramificados. CH3-CH2-CH2-CH3 CH3-CH-CH3 Butano l CH3 Metilpropano ALQUILAÇÃO • É a reação de um alcano ramificado (isoalcano), que possui radical metil no segundo carbono, com um alceno para obter gasolina de maior octanagem. CH3CHCH3+CH2=CCH3CH3C(CH3)2CH2CH(CH3)2 CH3 Metilpropano CH3 Metilpropreno Isoctano 02. Julgue os itens abaixo em verdadeiro ou falso: a) ( ) Viscosidade: Facilidade com que o material escoa. Os líquidos mais viscosos fluem mais lentamente b) ( ) As propriedades físicas podem ser intensivas e extensivas. As intensivas não dependem da quantidade da amostra, já as extensivas dependem da quantidade de material. c) ( ) A Pressão máxima de vapor depende da temperatura e da natureza do líquido. Observa-se experimentalmente que, numa mesma temperatura, cada líquido apresenta sua pressão de vapor, pois esta está relacionada com a volatilidade do líquido. d) ( ) Álcoois apresentam ponto de ebulição menor que um éter de mesma massa molecular. e) ( ) O biodiesel é um combustível obtido a partir da reação do metanol ou etanol, com óleo vegetal. Correspondendo a um éster metílico ou etílico. f) ( ) O poliisopreno é um polímero de condensação, que é uma poliamida, e usado na fabricação de coletes a prova de bala. As propriedades físicas podem ser classificadas de acordo com a quantidade de amostra em duas categorias: 1. Propriedades intensivas: São aquelas que não dependem da massa da amostra; Por exemplo, a temperatura é uma propriedade intensiva, pois imagine que coloquemos água para ferver. Se formos medir a temperatura da água, o valor será o mesmo independentemente se colocarmos o termômetro direto na panela com a água ou se o colocarmos em um copo com um pouco dessa água. A densidade é outra propriedade intensiva. Por exemplo, a densidade de um cubo de gelo e de um iceberg é a mesma (0,92 g/cm3, em temperaturas abaixo de 0ºC ao nível do mar), que é menor que a da água (1,0 g/cm3, sob a temperatura de aproximadamente 4ºC e sob pressão ao nível do mar, que é igual a 1,0 atm). Por isso, tanto um cubo de gelo como um iceberg flutuam sobre a água. 2. Propriedades extensivas: São aquelas que dependem da massa (“extensão”) da amostra. O volume é um exemplo de propriedade extensiva, pois a massa de 1 kg de algodão ocupará um volume muito maior do que a massa de 1 g desse mesmo material. A energia liberada em combustões também é extensiva, pois a energia liberada na queima de um palito de fósforo é bem menor do que a energia liberada na queima de vários galhos numa fogueira. Propriedades intensivas: temperatura (T em K), pressão (p em Pa), ponto de fusão (T em K), ponto de ebulição (T em K). •Propriedades extensivas: massa (m em kg), volume (V em m3), quantidade de substância (n em mol), energia interna (U em J), entalpia (H em J), entropia (S em J/K), energia de Gibbs (G em J). Propriedades coligativas das soluções são propriedades físicas que se somam pela presença de um ou mais solutos e dependem única e exclusivamente do número de partículas (moléculas ou íons) que estão dispersas na solução, não dependendo da natureza do soluto. Isso significa dizer que a quantidade, e não a natureza (como tamanho, estrutura molecular ou massa), das partículas que estão juntas na solução é que irá influenciar na formação das propriedades (ou efeitos) coligativas. •Tonoscopia: diminuição da pressão máxima de vapor. •Ebulioscopia: aumento da temperatura de ebulição. •Crioscopia: abaixamento da temperatura de solidificação. •Osmose: pressão osmótica. 03. A teoria de Bohr introduziu uma série de inovações no modelo atômico. Dentre elas destacam-se: ( I )A energia não é emitida de forma contínua, mas em blocos, denominados quantum. ( II )Os elétrons se movem ao redor do núcleo em número limitado de órbitas bem definidas, que são chamadas órbitas estacionárias. ( III )No núcleo dos átomos, além de prótons, que são positivos, existem partículas sem cargas elétricas, denominadas nêutrons. ( IV ) Ao saltar de uma órbita estacionária, o elétron emite ou absorve um quantum de energia. ( V ) Os elétrons têm, simultaneamente, caráter corpuscular e de onda. Das alternativas, estão corretas apenas: a) I, II, III b) II, III, IV c) I, III, V d) III, IV e) II, IV 04. Em relação a geometria molecular, julgue as afirmações abaixo, colocando verdadeiro ou falso: ( ) A molécula SF4 apresenta geometria em forma de gangorra ( ) A molécula BrF3 apresenta geometria tetraédrica. ( ) A molécula BrF5 apresenta geometria pirâmide quadrada ( ) A molécula I3- apresenta geometria angular. Geometria Molecular SF4 F S F F F BrF3 F Cl F PE=4 PL=1 Gangorra PE=3 PL=2 Forma de T PE=2 PL=3 Linear PE=5 PL=1 Pirâmide quadrada PE=4 PL=2 Plano quadrada F I3 II I BrF5 F F Br F F F XeF4 F Xe F F F 05.A respeito de alguns ácidos comercialmente utilizados na indústria, são feitas as afirmativas a seguir. I - O ácido bromídrico é mais forte que o ácido fluorídrico em solução aquosa. II - O ácido sulfúrico pode ser obtido pela reação do anidrido sulfúrico com água. III - O ácido clorídrico reage com óxido de sódio formando cloreto de sódio e água. IV - O ácido nítrico reage com cobre e mercúrio e não reage com ouro. São corretas as afirmativas: a) I e II apenas. FILA DE REATIVIDADE DOS METAIS b) II e III apenas. (ORDEM DECRESCENTE) Rb K Na Ba Li Sr Ca Mg Al Mn c) I, II e III apenas. Cs Zn Cr Fe Co Ni Sn Pb d) I, II e IV apenas. H Sb Bi Cu Hg Ag Pd Pt Au e) I, II, III e IV. 06. Julgue os itens abaixo, colocando verdadeiro ou falso e fazendo ressalvas e anotações quando possível. a) ( ) O Hidróxido de Amônio (NH4OH) é uma base fraca e solúvel. b) ( ) Calor específico e densidade são consideradas propriedades aperiódicas. c) ( ) Ácido de BRONSTED - LOWRY é qualquer espécie química capaz de ceder pares de elétrons. d) ( ) Base de LEWIS é qualquer espécie química capaz de ceder prótons H+. e) ( ) Todo ácido de BRONSTED - LOWRY é ácido de LEWIS BRONSTED – LOWRY ÁCIDO – CEDE PRÓTONSH+ BASE – RECEBE PRÓTONS H+ LEWIS ÁCIDO – RECEBE PARES DE ELÉTRONS BASE – CEDE PARESD DE ELÉTRONS 07.A que temperatura deve ser aquecido um frasco aberto a fim de que ¼ do gás nele contido, a 27°C seja expulso? a) 400 °C b) 300 °C c) 127 °C d) 100 °C e) 120 °C SITUAÇÃO 1 T1 = 300k n1 = n P1 = P V1 = V SITUAÇÃO 2 T2 = ? n2 = ¾n P2 = P V2 = V P1V1 = n1RT1 P2V2 = n2RT2 1 = n.T1 ¾n .T2 T2 = 300 ÷ ¾ T2 = 400K - 273 = 127°C LETRA: C 08. Considere a equação: N2 (g) + 3 H2 → 2 NH3 (g) Assinale a alternativa que estabelece a relação entre KP e K C: a) KP = KCRT b) KP = KC c) KP = KC/(RT)2 d) KP = KC . (RT)-8 e) KP = KC/(RT)4 RESPOSTA – QUESTÃO 08 N2(g) + 3 H2 KC = ∆n = (c + d) – (a + b) [ NH3]2 [ N2] . 2 NH3(g) Soma dos coeficientes do produto [H2]3 Soma dos coeficientes dos reagentes ∆n = 2 – (1 + 3) = – 2 KP = P(NH3)2 P N2 . 3 ( ) P H2 KP = KC . (RT)∆n KP = KC . (RT)– 2 KP = KC (RT)2 OU 09. Doença cardíaca e hipertensão arterial podem resultar de depósitos de colesterol no interior das paredes das artérias. Esta condição, aterosclerose, é uma forma de arteriosclerose, ou “endurecimento das artérias”. Evidências mostram que o nível de colesterol no sangue, e, portanto a quantidade depositada, está relacionada com a quantidade de gorduras saturadas que você ingere. O colesterol está também presente nos cálculos biliares, depósitos anormais oriundos da bile na vesícula. http://www.infoescola.com/quimica/esteroides/Acessado em 20 de setembro de 2012 Quando a bile é hidrolisada, o esteróide obtido mais abundante é o ácido cólico: O H3C OH OH CH3 CH3 H H HO H H OH O H3C OH OH CH3 CH3 H H HO H H OH Considerando o exposto e a estrutura do ácido cólico, é correto afirmar que a) o ácido cólico, não pode sofrer esterificação. b) o ácido cólico possui onze carbonos assimétricos. c) A bile é um líquido produzido pelo fígado e não se armazena na vesícula biliar. d) as funções orgânicas são respectivamente, álcool; fenol e ácido carboxílico e) apresenta 10 elétrons não-ligantes 10. O citral é uma mistura de isômeros (geranial e neral), obtida a partir do óleo essencial do limão. Devido ao seu odor agradável, é bastante utilizado na preparação de perfumes cítricos. A partir das estruturas apresentadas, podemos dizer: ( ) o geranial é o isômero trans (ou E), e o neral é o isômero cis (ou Z). ( ) o geranial e neral apresentam a mesma fórmula molecular C9H14O. ( ) geranial e neral apresentam uma carbonila como grupo funcional e, por isso, são chamados de cetonas. ( ) geranial e neral são terpenos que apresentam isomeria espacial (óptica). ( ) geranial e neral apresentam uma dupla ligação conjugada a uma carbonila. DADOS 11. Reações de desidratação de álcoois, oxidação de aldeídos e poliadição do cloroeteno dão origem, respectivamente, a: a) alcenos, ácidos carboxílicos e PVC, b) alcanos, fenóis e poliamidas, c) alcinos, aminas e dióis, d) éteres, cetonas e baquelite, e) ácidos carboxílicos, álcoois e proteínas. INTRAMOLECULAR ALCENO DESIDRATAÇÃO DE ÁLCOOIS INTERMOLECULAR OXIDAÇÃO ALDEÍDO ÁC. CARBOXÍLICO ÉTER DADOS 12. Um alceno sofreu ozonólise seguida de hidrólise e produziu 2,3-dimetil – butanal e butanona. Assinale a alternativa que contenha o nome oficial deste alceno. a) 2,3,5 – trimetil – hept-4-eno b) 3,5,6 – trimetil – hept-3-eno c) 3,5 – dimetil – hept-3-eno d) 2,3,– dimetil – hex-3-eno e) 3,5,6 – trimetil – hept-1-eno OZONÓLISE HC = ALDEÍDO H2C = METANAL C = CETONA H 3C CH CH CH3 CH3 CH 3,5,6 - TRIMETIL HEPT – 3 – ENO 2,3 - DIMETIL BUTANAL C CH2 CH3 CH3 CH3 + O CH CH CH3 CH3 C CH2 CH3 BUTANONA O C + H CH3 DADOS 13. O propanal reage com o cloreto de metilmagnésio dando um produto de adição, o qual, por hidrólise, produz o composto orgânico A. O nome do composto A, e sua classificação quanto à posição do grupo funcional na cadeia carbônica é: a) Butan-1-ol (álcool primário) b) 2-metil -butan-2-ol (álcool terciário) c) Butanona ( cetona alifática) d) Butan-2-ol (álcool secundário) e) Propan-2-ol (álcool secundário) METANAL + OUTRO ADEÍDO + CETONA + R - MgX R - MgX R - MgX H 2O H 2O H 2O ÁLCOOL PRIMÁRIO ÁLCOOL SECUNDÁRIO ÁLCOOL TERCIÁRIO O CH3 CH2 OMgCl CH3 CH2 CH + C CH3 MgCl H CH3 + H OH OH CH3 CH2 CH CH3 + Mg(OH)Cl BUTAN – 2 – OL DADOS 14. Considere as afirmativas a seguir: I - a reação de oxidação de um álcool secundário‚ produz uma cetona. II - A desidratação intermolecular que ocorre entre 2 moléculas de etanol a 140°C em presença de H2SO4 gera but-2-eno III - Não ocorre oxidação do CH3-C(CH3)OH-CH3 em presença de ácido sulfúrico. Assinale a(s) afirmativa(s) INCORRETA(S) a) apenas I. b) apenas I e II. c) apenas II. d) apenas I e III. e) apenas III. I. [O] ÁLCOL 1º ALDEÍDO [O] ÁLCOL 2º II. CH3 CH2 OH CH3 CH2 OH NÃO OCORRE CH3 CH2 O CH3 III. CH3 C OH CH3 ÁC. CARBOXÍLICO CETONA [O] ÁLCOL 3º [O] [O] NÃO OCORRE CH2 CH3 + H 2O EU VOU PASSAR!!! Não esqueçam: “Tudo posso Naquele que me fortalece” Que Deus ilumine VOCÊS rumo a sua aprovação. REVISÕES PARA VESTIBULARES Prof. Jurandir
Baixar