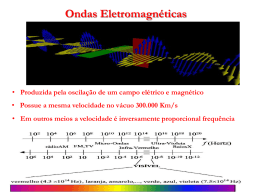
Teste atômico Experimento cadastrado por Leandro Fantini em 06/06/2011 Classificação ••••• (baseado em 6 avaliações) Total de exibições: 5260 (até 31/07/2012) Palavras-chave: química, física, rede difração, espectro, luz, bohr, átomo, chama, teste Onde encontrar o material? em laboratórios e lojas especializadas Quanto custa o material? acima de 25 reais Tempo de apresentação até 10 minutos Dificuldade intermediário Segurança requer cuidados especiais Introdução Faça um teste simples e didático que pode ser usado na abordagem de vários assuntos em química e física. Este teste pode evidenciar a presença de vários tipos de átomos. chama verde no espectro Materiais necessários Metanol Vidros de relógios Sais de vários metais- Use preferencialmente os cloretos Pipeta Rede de difração Passo 1 Mãos à obra Coloque um pouco do sal que contém o metal dentro do vidro de relógio. Para cada sal, use um vidro diferente. Pingue com a pipeta algumas gotas de metanol sobre os sais e em seguida acenda-os usando o palito de churrasco e o algodão como uma espécie de tocha. Cuidados necessários: Use luva e óculos. Não cheire o metanol, sua ingestão ou contato com mucosas pode causar © 2012 pontociência / www.pontociencia.org.br 1 Teste atômico intoxicação e cegueira. Mantenha longe de qualquer fonte de calor. Produto altamente inflamável. Não use quantidades maiores que as indicadas aqui. Chamas de elementos diferentes Passo 2 O que acontece Este experimento é conhecido como “teste de chama”. Esta prática é muito usada em análises químicas por ser um método rápido e barato para detecção de alguns metais. Este teste baseia-se em uma das mais importantes propriedades dos elétrons, enunciada pela primeira vez por Niels Bohr. Ele disse que a energia dos elétrons é "quantizada", isto é, um elétron ocupa sempre níveis energéticos bem definidos dentro de cada átomo e não valores quaisquer de energia. Porém quando fornecemos a energia necessária para um elétron, ele pode “saltar” para um nível de maior energia. Quando o elétron é promovido a um nível de maior energia dizemos que ele se encontra no estado excitado. Porém, neste estado ele se torna menos estável e retorna quase imediatamente ao seu estado de menor energia ou estado fundamental, liberando aquela energia em forma de luz visível. Optamos por usar na maioria dos casos os cloretos de vários metais, como pode ser visto no vídeo, pois eles possuem uma solubilidade maior no metanol. Usamos os cloretos de lítio, cobre (II), sódio, potássio e estrôncio, além de ácido bórico. O uso do metanol também é indicado porque esse produz uma chama quase invisível aos nossos olhos, o que minimiza a interferência com a cor da luz emitida pelo metal. Usamos também uma rede de difração. Mas o que é uma rede de difração? A cada milímetro de sua superfície existem centenas de fendas paralelas e microspócicas. A luz que incide sobre a rede de difração sobfre desvios que dependem do seu comprimento de onda. Por esta razão quando as cores viajam juntas a rede promove a separação delas permitindo ainda que se identifiquem os comprimentos de ondas que contém um dado espéctro Clique para assistir ao vídeo http://www.youtube.com/watch?v=9dqFfE1RebA © 2012 pontociência / www.pontociencia.org.br Powered by TCPDF (www.tcpdf.org) 2
Baixar