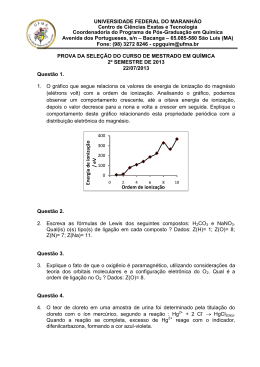
Aula 2 Nesta aula, iremos formalizar o conceito de plasma, rever nosso entendimento sobre temperatura de um gás e finalmente, conhecer alguns processos de ionização. 1.3 Condições para Produção de Íons num Gás em Equilíbrio Térmico Da Física Estatística é possível determinar o grau de ionização de um gás em equilíbrio térmico a uma temperatura ( T ), sem considerar os detalhes do processo de ionização. A equação de Saha relaciona as densidades de átomos ionizados (íons) e átomos neutros com a energia de ionização aplicada ao gás de átomos, de acordo com a equação 1.2.1 U 3/ 2 − i ni T 15 = 2,11× 10 e KT nn ni 1.2.1 ,onde ni e n n são as densidades de íons e átomos neutros, respectivamente em part/cm3, T é a temperatura do gás em Kelvin, K é a constante de Boltzmann e finalmente U i é energia de ionização em eV. Observação: U i denota a energia necessária para remover do átomo o(s) elétron(s) da camada de valência. A tabela abaixo relaciona os elementos químicos com seus respectivos valores de U i . Elemento Químico Energia de Ionização (eV) Hélio Argônio Hidrogênio Nitrogênio Mercúrio Sódio 24,59 15,76 13,60 14,53 10,44 5,14 Elementos Químicos e seus respectivos valores de Energia de Ionização. Como um exemplo, a fração de ionização ( α ) da atmosfera terrestre (78% de Nitrogênio, 21% de Oxigênio e 1% de outros gases) na CNTP é nn = 3 × 1019 part.cm −3 T = 300 K U i = 14,53eV ni ni α = ≅ mas ni + n n n n ⇒ ni = 10−122 nn ∴α = 10 −122 Conclusão do exemplo: Sendo a densidade da atmosfera muito alta, o livre caminho médio ( l ) de um elétron é extremamente curto, como conseqüência não realiza colisões energéticas com os átomos, sendo capturado pelo mesmo, com isso o grau de ionização é muitíssimo baixo. Mas se a densidade do gás ao contrário for baixa, altas frações de ionização podem ser atingidas. Para um gás de átomos qualquer, é possível determinar, a relação entre o grau de ionização ( α ) e a temperatura do gás ( T ), para diferentes valores da densidade total do gás ( nt ), conforme mostra figura abaixo Grau de Ionização para diferentes valores da densidade total. 1.4 Processos de Ionização Os Plasmas são gerados através de vários processos de ionização. A maioria destes processos é colisional. Dependendo da natureza da colisão: elástica ou inelástica, pode ou não ocorrer a ionização do átomo ou molécula neutra. Colisões elásticas: Ocorre apenas transfrencia de momentum entre o alvo e o projétil, portanto não ocorre ionização dos átomos ou moléculas neutras. Colisões inelásticas: Ocorre troca de energia entre o alvo e o projétil, portanto pode resultar em exitação ou até mesmo ionização dos átomos ou moléculas neutras. Entre as exitações por colisões inelásticas, temos: Exitação por Transição de Níveis Eletrônicos: A + B → A + B * , * indica apenas exitação Exitação por Transição de Níveis Vibracionais: A + BC (v ) → A + BC (v , ) , onde v e v , indicam freqüência de vibração Entre as ionizações por colisões inelásticas, temos: Ionização por Impacto Eletrônico: Ionização por colisões inelásticas entre elétrons e átomos) ou moléculas neutras, como um exemplo e − + A → A + + 2e − Tal ionização está, intimamente relacionada com a secção de choque ( σ ) do alvo e a energia do projétil incidente. A figura abaixo mostra como exemplo, a secção de choque do Argônio em função da energia projétil incidente Curva Secção de Choque versus Energia para vários alvos. Ionização por Impacto Iônico: Ionização por colisões inelásticas entre íons e átomos ou moléculas neutras, observe o exemplo 2 A + + e − A + A→ + A+ A + Observação: Alguns processos correlatos aos fenômenos de exitação e ionização são: Relaxação: Ocorre quando elétrons ligados nos átomos exitados, retornam ao seu nível de energia original emitindo radiação (fótons). Dissociação Molecular: Quebra de moléculas por algum processo colisional de ionização, observe o exemplo AB + e − → A* + B + + 2e − , * indica apenas exitação A reação inversa corresponde associativa, observe o exemplo à ionização A* + B + + 2e − → AB + e − Recombinação ou Captura Eletrônica: Processo inverso ao da ionização, pois o íon captura o elétron perdido na ionização, observe o exemplo A+ + e − → A A eficiência na captura dos elétrons pelos íons está, intimamente relacionada com a secção de choque ( σ ) do íon. Alguns processos de recombinação podem resultar em emissão de fótons , isto é, uma recombinação radiativa, observe o exemplo A + + e − → A + hv ,onde hv é a energia do fóton emitido pelo íon Outros Tipos de Ionização: Fotoionização: Ionização obtida pela interação entre fótons e os átomos de um gás, como um exemplo A + hv → A+ + e − , onde hv é a energia do fóton incidente A figura abaixo mostra o processo de fotoionização Ilustração da Fotoionização. A eficiência na fotoionização está, intimamente relacionada com a secção de choque ( σ ) do átomo e também ao comprimento de onda ( λ ) da luz incidente. A figura abaixo mostra como exemplo, a secção de choque do Argônio em função da energia do fóton incidente Curva Secção de Choque versus Energia ou Comprimento de onda para o Ar. Ionização por Ruptura Elétrica: Ionização induzida por um campo elétrico aplicado que, inicialmente polariza as cargas do átomo ou molécula e depois ioniza (dependendo do módulo do campo elétrico). A figura abaixo, mostra uma o processo de ionização por ruptura eletrônica Experimento para Ruptura Eletrônica. As curvas experimentais abaixo (curva de Paschen), mostram a iminência da ruptura eletrônica (ionização) para algumas moléculas e também para elementos puros. Curva de Paschen para algumas Moléculas. Curva de Paschen para alguns Elementos Puros.
Baixar