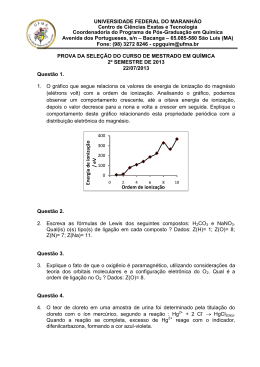
ENFERMEIRA SCHEILA CRISTINA DE MERCEDES COELHO • Ionização, como o próprio nome diz, é o ato de transforma átomos de carga neutra em seus respectivos íons. A energia necessária para transformar um átomo em íon varia de elemento para elemento. Essa transformação se dá devido ao elétron receber energia o suficiente para se libertar da nuvem eletrônica pertencente ao átomo. • Quando um elétron é retirado, passa-se a possuir mais prótons no núcleo do que elétrons na eletrosfera. Isso torna o íon mais “rígido” que seu átomo original. A eletrosfera é atraída mais fortemente pelo núcleo, tornando mais difícil ainda, ou seja, aumentando a energia para a retirada de outro elétron. Caso seja retirado um segundo elétron, a força relativa do núcleo se torna maior e o terceiro elétron requer uma energia maior ainda. • Como tantas outras características, a Energia de Ionização é uma propriedade periódica, significa que ela oscila entre os períodos e grupos da tabela periódica. Ela pode ser medida em eV (elétron Volts) ou KJ/mol (Kilojoule/ mol). • Uma das maneiras de provocar essa ionização é a ionização térmica. Também conhecida como ionização de superfície, já que acontece na superfície de um metal aquecido gradualmente. Nessa superfície se encontra o material purificado que se deseja ionizar. • O aquecimento do metal, gera energia suficiente para a retirada dos elétrons. A probabilidade de o processo acontecer, depende da temperatura do filamento, do material do filamento e, obviamente, da energia de ionização do material. Essa técnica é utilizada em equipamentos de espectrometria de massas. São utilizados geralmente por serem simples e baratos. Sua desvantagem é de que o metal não pode atingir temperaturas altas o suficiente para ionizar algumas espécies. • Quando se trabalha com uma solução ácida ou básica, a ionização está diretamente ligada à força da espécie química. Um ácido forte, como HCl, tem um alto potencial de ionização. Isso significa que ele ira se dissociar completamente e existirá em solução como íons Cl- e H+. O mesmo acontece com uma base. O NaOH, se ioniza muito na água, existindo como os íons Na+ e OH-. A extensão com que essa ionização acontece é medida pela constante K. • Nesse caso, acontece o mesmo de quando queremos transformar átomos neutros em íons. O primeiro H+ é de ionização mais fácil do que o segundo, um bom exemplo desse é o ácido fosfórico, H3PO4. A ionização do 1° H+ é muito mais fácil do que a do 3°. • http://www.infoescola.com/quimica/acidos-fortes/
Baixar