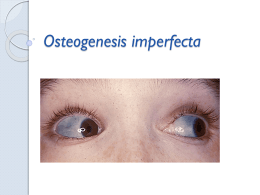
Fundação Oswaldo Cruz Instituto Fernandes Figueira Pós Graduação em Saúde da Criança e da Mulher Aplicação clínica da evidência científica: o caso da Osteogênese Imperfeita e o tratamento medicamentoso com bifosfonatos. Maria Angelica de Faria Domingues de Lima Rio de Janeiro Março/2010 Fundação Oswaldo Cruz Instituto Fernandes Figueira Pós Graduação em Saúde da Criança e da Mulher Aplicação clínica da evidência científica: o caso da Osteogênese Imperfeita e o tratamento medicamentoso com bifosfonatos. Maria Angelica de Faria Domingues de Lima Dissertação apresentada à Pós-Graduação em Saúde da Criança e da Mulher, como parte dos requisitos para obtenção do título de Mestre. Orientadora: Profa. Dra. Dafne Dain Gandelman Horovitz Rio de Janeiro Março/2010 AGRADECIMENTOS Aos pacientes do CROI-RJ e seus familiares, permanente fonte de entusiasmo para o estudo da osteogênese imperfeita. À Maria de Fátima Benicaza dos Santos e ao José Carlos dos Santos da ABOI-RJ, sempre dispostos a ajudar e responder as dúvidas. Aos meus mestres em genética clínica Dra. Dafne Dain Gandelman Horovitz, Dr. Fernando Regla Vargas e Dr. Juan Clinton Llerena Júnior. Aos amigos Aline Teixeira da Costa, Ana Cristina Bohrer Gilbert, Anna Claudia Evangelista dos Santos, Carmem Lia Martins Moreira, Leila Cabral de Almeida Cardoso, Marcelo Pacheco Vieira, Maria Auxiliadora Monteiro Villar e Maria Helena Cabral de Almeida Cardoso que trouxeram um colorido especial ao meu caminho; em especial à Carmem Lia e Maria Helena, sempre capazes de responder às perguntas que eu sequer havia formulado e que constantemente iluminam minha estrada; à vocês minha eterna gratidão. Aos professores da Pós-Graduação em Saúde da Criança e da Mulher, à turma de 2008 do Mestrado Acadêmico, aos membros da Secretaria Acadêmica e da Biblioteca em Saúde da Criança e da Mulher – IFF. Ao Conselho Nacional de Desenvolvimento Científico e Tecnológico, pelo apoio através da bolsa de mestrado. E, por fim, aos meus pais. LISTA DE FIGURAS E QUADROS Figura 1 – Representação esquemática da síntese do colágeno 18 Figura 2 – Imagens de biópsia de osso normal e do osso na osteogênese imperfeita Figura 3 – Distribuição das referências por ano de publicação 21 Figura 4 – Distribuição das referências quanto à intervenção 44 Figura 5 – Distribuição dos autores dos estudos quanto à afiliação por especialidade Figura 6 – Distribuição dos estudos quanto à origem 45 Quadro 1 – síntese das bases eletrônicas utilizadas e dos mecanismos de busca Quadro 2 – referências encontradas nos livros de resumos de reuniões e congressos 41 44 46 42 RESUMO A osteogênese imperfeita é uma condição caracterizada por grande fragilidade óssea e fraturas recorrentes que levam a deformidades, secundária a mutações nos genes codificadores do colágeno tipo I ou de proteínas que participam de seu processamento. O tratamento atual da osteogênese imperfeita fundamenta-se na abordagem multidisciplinar (clínico-cirúrgica e reabilitação), que inclui o uso de medicamentos do grupo dos bifosfonatos. No Brasil, o tratamento da osteogênese imperfeita é uma política pública de saúde, tendo sido disponibilizado à população em 2001, após publicação de estudos internacionais mostrando resultados favoráveis com o uso de pamidronato dissódico em indivíduos com a doença. Todavia, ainda existem divergências sobre os efeitos destas medicações na osteogênese imperfeita. Na tentativa de esclarecer estas questões, realizou-se uma revisão crítica da literatura científica, embasada pelos princípios da epidemiologia clínica. Após a busca por estudos com bifosfonatos em indivíduos com osteogênese imperfeita e a seleção criteriosa dos mesmos, prosseguiu-se à síntese dos dados reportados tomando como desfechos de interesse a densidade mineral óssea, marcadores de metabolismo ósseo e ocorrência de fraturas. Dentre 258 referências encontradas, foram selecionadas 39 que apontaram que o uso de pamidronato dissódico na osteogênese imperfeita associa-se ao aumento da densidade mineral óssea em coluna lombar, a redução do turnover ósseo, traduzindo-se clinicamente na redução do número de fraturas. As informações disponíveis sobre zolendronato ainda são escassas e os dados sobre alendronato dissódico são, por vezes, conflitantes no que diz respeito aos benefícios associados às manifestações clínicas (fraturas). As evidências obtidas com os estudos primários permitiram a elaboração de recomendações a serem aplicadas na prática clínica. Ademais, discutem-se temas relacionados ao programa brasileiro de tratamento da osteogênese imperfeita que caminha na direção da solidificação de uma política pública de saúde voltada para uma doença rara. ABSTRACT Osteogenesis imperfecta is characterized by bone fragility, recurrent fractures and consequent deformities. It is associated to mutations in the type I collagen genes or in proteins that process such collagen. Current treatment approach includes bisphosphonate administration, surgical procedures and rehabilitation. In Brazil, Osteogenesis imperfecta treatment is a public health policy that has been made available to the population in 2001, after the publication of several international studies regarding the use of bisphosphonates in Osteogenesis imperfecta. However, the data is still discrepant on its effects on this disease. As an attempt to clarify such matters a critical review of the scientific literature was executed. After a search and selection of primary studies, we proceeded to summarize the reported data considering as main outcomes bone mineral density, bone metabolism markers and fractures. Among 258 studies, 39 were selected, which pointed to increase of bone mineral density, reduction of bone turnover and reduction of fractures in osteogenesis imperfecta patients treated with pamidronate. Available information regarding zolendronic acid is still scant. Data on alendronate concerning its benefits on clinical manifestations (fractures) is conflicting. Evidences obtained by primary studies were used to formulate several recommendations to be used in clinical practice. Finally, issues regarding the Brazilian Osteogenesis imperfecta treatment program, which moves towards the consolidation of a public health policy concerning a rare disease, are discussed. SUMÁRIO 1. INTRODUÇÃO 9 2. JUSTIFICATIVA 12 3.OBJETIVOS 14 3.1. Objetivo geral 14 3.2. Objetivos específicos 14 4. Quadro teórico 15 4.1. O osso normal 15 4.2. O colágeno e seus aspectos genéticos e proteicos 16 4.3. O osso na osteogênese imperfeita 20 4.4. Osteogênese imperfeita: manifestações clínicas e classificação 21 4.5. Marcadores bioquímicos do metabolismo ósseo 24 4.5.1. Marcadores de formação óssea 26 4.5.2. Marcadores de reabsorção óssea 26 4.6. Densitometria óssea 28 4.7. Tratamento medicamentoso da osteogênese imperfeita 31 5. MATERIAL E MÉTODOS 33 5.1. Fase 1 – Fontes e estratégias de busca 34 5.2. Fase 2 – Seleção dos estudos 37 5.3. Fase 3 – Avaliação da qualidade dos estudos primários 39 5.4. Fase 4 – Coleta de dados 40 5.5. Fase 5 – Análise dos dados 40 6. RESULTADOS 40 6.1. Busca pelos estudos primários 40 6.2. Seleção dos estudos primários 47 6.3. Avaliação de qualidade 48 6.4. Síntese dos dados no que tange a densidade mineral óssea 51 6.4.1. Pamidronato dissódico, estudos clínicos do tipo antes e depois 52 6.4.2. Alendronato dissódico, estudos clínicos tipo antes e depois 53 6.4.3. Alendronato dissódico, estudos com grupo controle 55 6.4.4. Pamidronato dissódico, estudos com grupo controle 55 6.4.5. Pamidronato dissódico x alendronato dissódico 57 6.4.6. Zolendronato 57 6.4.7. Outros estudos 58 6.5. Síntese dos dados de acordo com o metabolismo ósseo 59 6.5.1. Pamidronato dissódico, estudos clínicos tipo antes e depois 59 6.5.2. Alendronato dissódico, estudos clínicos tipo antes e depois 60 6.5.3. Alendronato dissódico, estudos com grupo controle 61 6.5.4. Pamidronato dissódico x alendronato dissódico 62 6.5.5. Outros estudos 62 6.6. Síntese dos dados em relação a ocorrência de fraturas 63 6.6.1. Pamidronato dissódico, estudos clínicos tipo ante e depois 63 6.6.2. Alendronato dissódico, estudos clínicos tipo antes e depois 64 6.6.3. Alendronato dissódico, estudos com grupo controle 65 6.6.4. Outros estudos 65 7. DISCUSSÃO 66 8. CONCLUSÕES 75 REFERÊNCIAS BIBLIOGRÁFICAS 83 APÊNDICE 1 – CLASSIFICAÇÃO CLÍNICA DA OSTEOGÊNESE IMPERFEITA 92 APÊNDICE 2 – FICHA DE SELEÇÃO DOS ESTUDOS PRIMÁRIOS 95 APÊNDICE 3 – FICHA DE CAPTAÇÃO DE DADOS 96 APÊNDICE 4 – ESTUDOS INCLUÍDOS NA REVISÃO 98 APÊNDICE 5 – ESTUDOS PRIMÁRIOS EXCLUÍDOS DA REVISÃO 102 ANEXO 1 – ESCALA DE AVALIAÇÃO DE QUALIDADE DOS ESTUDOS CLÍNICOS 121 9 1. INTRODUÇÃO A osteogênese imperfeita é uma condição potencialmente incapacitante, caracterizada por grande fragilidade óssea, fraturas recorrentes, com deformidades secundárias. Sua freqüência é estimada em 1/5000-10000 indivíduos (Engelbert et al., 2004). A dificuldade em reunir todos os aspectos históricos relacionados a osteogênese imperfeita é grande, visto que a doença foi descrita com diversos nomes ao longo dos séculos, tais como doença de Vrolik, síndrome de Ekman, escleróticas azuladas e ossos quebradiços, entre outros (Weil, 1981; Baljet, 2002). Foi Willem Vrolik que, no século XIX, cunhou o termo osteogenesis imperfecta após o estudo de um espécime da coleção de teratologia de seu pai – um neomorto que apresentava inúmeras fraturas. Ao contrário do que seus contemporâneos acreditavam, Vrolik observou que algumas displasias esqueléticas eram congênitas, além de sugerir que a osteogênese imperfeita fosse um defeito primário de ossificação (Baljet, 2002). Até 1979, a classificação mais empregada era a que dividia os pacientes em dois grupos: “congênita” e “tarda”. Naquele ano, Sillence e colaboradores (1979) propuseram uma classificação em quatro tipos (I – IV), baseados na avaliação clínica de 145 indivíduos com osteogênese imperfeita. A descrição desta série também permitiu a demonstração da grande incapacidade que está associada à condição, visto que a maioria dos pacientes apresentava alguma deformidade com prejuízo da mobilidade (Sillence et al., 1979). Posteriormente, Engelbert e colaboradores observaram que mesmo os pacientes com a forma mais branda da doença (pacientes com osteogênese imperfeita tipo I, de acordo com a classificação de Sillence) apresentavam atraso no ganho dos marcos motores e prejuízo da mobilidade quando comparados com crianças 10 normais. Além disso, nos pacientes com as formas mais graves (tipos III e IV) a limitação funcional e a dependência tornavam-se crescentes com o avanço da idade (Engelbert et al., 1999, Engelbert et al., 2000; Engelbert et al., 2004). O tratamento atual da osteogênese imperfeita fundamenta-se na abordagem multidisciplinar (clínico-cirúrgica e reabilitação) com vistas ao aumento da mobilidade e da funcionalidade do indivíduo (Rauch e Glorieux, 2004). No Brasil, após os resultados iniciais dos estudos com pamidronato dissódico (uma das medicações do grupo dos bifosfonatos), indivíduos com osteogênese imperfeita e seus familiares passaram a exigir que tal terapia fosse disponibilizada no âmbito do Sistema Único de Saúde. Assim, o Ministério da Saúde aprovou este tratamento através da Portaria 2305/2001, designando ao Instituto Fernandes Figueira o papel de Centro de Referência da Osteogênese Imperfeita (CROI) e coordenador do Programa de Tratamento da Osteogênese Imperfeita. O Instituto Fernandes Figueira, unidade materno-infantil da Fundação Oswaldo Cruz, é um hospital de nível terciário, sendo o departamento de Genética Médica o responsável pela coordenação do Programa de Tratamento da Osteogênese Imperfeita no Instituto. Desde 2001 mais de 150 pacientes com osteogênese imperfeita de diferentes idades foram cadastrados no CROIRJ. Com a crescente experiência adquirida ao longo dos anos no CROI-RJ surgiram muitas questões, tais como qual o melhor esquema terapêutico deve ser empregado para modificar os desfechos negativos associados a esta condição? Por quanto tempo a medicação deverá ser utilizada? Os benefícios 11 dos bifosfonatos estendem-se a todos os pacientes? Estas indagações tampouco são adequadamente respondidas pela literatura especializada e mesmo os especialistas mundiais não conseguem responde-las (Rauch e Glorieux, 2005). Desta forma, a pergunta que norteou esta pesquisa foi: será que os resultados do tratamento da osteogênese imperfeita com bifosfonatos, reportados na literatura científica, permitem definir condutas na prática clínica quanto ao melhor esquema terapêutico a ser empregado em cada paciente? Para tentar responder essa questão, sempre tendo em mente a realidade brasileira, processou-se uma revisão crítica da literatura científica. Este trabalho se inicia com um breve quadro teórico que enfatiza alguns aspectos fisiopatológicos da doença, tão importantes para compreensão da clínica e da aplicação das diferentes terapias; e os exames complementares utilizados no seu acompanhamento. Posteriormente, apresentamos a construção da pesquisa, que embasada pela epidemiologia clínica foi adaptada às necessidades deste estudo. Os resultados estão divididos em características gerais dos estudos primários; algumas considerações sobre a qualidade dos estudos e a síntese dos dados no que tange à densidade mineral óssea, os marcadores bioquímicos e a tradução clínica imediata do tratamento – as fraturas. Por fim, são feitas considerações sobre a literatura científica e sugestões de como aplicar esta revisão na prática. 12 2. JUSTIFICATIVA A osteogênese imperfeita é uma doença rara. Doenças raras são definidas como aquelas que afetam um número limitado de indivíduos na população, ou cuja prevalência é menor que 1:20001. Em geral, são doenças crônicas, incuráveis e que estão associadas à deficiência e expectativa de vida reduzida. De modo geral, 80% têm origem genética identificada e 50% manifestam-se inicialmente na infância. Embora o número global seja impressionante, isoladamente elas afetam um grupo restrito de indivíduos, visto que existem entre 5000 a 7000 doenças raras. Neste sentido, políticas públicas de saúde direcionadas as doenças raras são de difícil implementação. Por outro lado, são extremamente necessárias, considerando o grande fardo associado a este grupo de doenças (Eurordis, 2005). No Brasil, as políticas públicas de saúde associadas às doenças raras incluem o programa de tratamento da doença de Gaucher (Portaria SAS n° 449/2002), o programa de tratamento da osteogênese imperfeita (Portaria GM/MS n° 2305/2001), o programa de tratamento da fibrose cística (Portaria SAS nº 263/2001) e algumas doenças incluídas no Programa Nacional de Triagem Neonatal (Portaria GM/MS n°822/2001), tais como a fenilcetonúria e a fibrose cística. O Instituto Fernandes Figueira é o coordenador de todos os CROIs do país, podendo ser considerado um “centro de referência”2 para todos os outros “centros de referência”. Neste sentido, tem papel crucial nesta rede, não 1 Definição utilizada na Europa e na Austrália. Nos Estados Unidos da América é definida como “Centro de referência”: “local adequado para referir pacientes, por sua experiência e disponibilidade de serviços” (Rare Disease Task Force, 2006:8). No entanto, o perfil de um centro de referência é variável, indo desde um espaço focado no diagnóstico e tratamento de doenças raras até a pesquisa clínica com vistas à produção de diretrizes clínicas e fornecimento de pareceres por especialistas (Rare Disease Task Force, 2006). 2 13 somente no que se refere à sua organização, mas especialmente como ponto de apoio para a adequada implantação de uma política pública de saúde em todo o país. De acordo com o Ministério da Saúde é esperado que o tratamento com pamidronato dissódico aumente a massa óssea, reduza a dor crônica, a incapacidade física e a atividade da doença. No entanto, a experiência do tratamento com bifosfonatos é relativamente recente, de modo que os resultados, a médio e longo prazo, somente nas últimas duas últimas décadas, começam a ser investigados, existindo ainda muitas contradições na literatura científica. Durante o período que acompanhei o trabalho do CROI-RJ, como médica residente de genética médica, tive a oportunidade de lidar com muitos pacientes com osteogênese imperfeita e pude perceber a dificuldade de aplicar na prática clínica as inconsistências observadas na literatura científica. Após estabelecer o diagnóstico de uma doença o médico se depara com questões sobre seu prognóstico e tratamento: qual é o curso clínico esperado nesta doença? Há algo a fazer para modificá-lo? O que esperar de uma determinada intervenção? Qual intervenção modificaria os desfechos negativos associados a esta condição? (Sackett et al., 1992). No caso da osteogênese imperfeita isto não é diferente e o paciente, ou mais freqüentemente sua família (uma vez que no IFF se lida com um público constituído majoritariamente por crianças), demanda respostas para as questões supracitadas. Embora a experiência clínica seja importante, a literatura científica é a melhor aliada do clínico para responder a estas dúvidas (Sackett et al., 1992). 14 Por fim, sublinha-se o caráter estratégico desta pesquisa que tem como meta contribuir para o tratamento de pacientes com osteogênese imperfeita no âmbito do IFF, caminhando na direção de implantar o instituído pela Portaria 2305/2001 do Ministério da Saúde. Acresça-se a importância deste tipo de estudo no que diz respeito à saúde coletiva, uma vez que sua finalidade principal é de fornecer subsídios à implantação das redes CROI, dentro de uma política pública, decretada pelo Estado brasileiro. 3. OBJETIVOS 3.1. Objetivo geral Avaliar os resultados do tratamento com bifosfonatos em indivíduos com osteogênese imperfeita reportados pela literatura científica. 3.2. Objetivos específicos Comparar os resultados obtidos com o uso de diversos bifosfonatos em pacientes com osteogênese imperfeita, reportados pela literatura científica, sendo de especial interesse o pamidronato dissódico, o alendronato dissódico e o zolendronato. Comparar os resultados obtidos com o uso destas medicações nos diferentes tipos de osteogênese imperfeita, de acordo com a classificação de Sillence, reportados pela literatura científica. Averiguar, na literatura científica, quais os esquemas terapêuticos de uma mesma medicação que têm sido empregados e se há alguma diferença entre eles. 15 4. QUADRO TEÓRICO 4.1 – O osso normal O osso tem importante papel biológico não só na sustentação e proteção do organismo como também na manutenção de sua homeostase mineral. É um dos poucos tecidos conjuntivos que se mineralizam, sendo composto por uma fase orgânica e uma fase inorgânica. A primeira inclui células e proteínas da matriz óssea e na segunda temos alguns minerais e, em especial, hidroxiapatita de cálcio, o componente responsável pela rigidez do osso (Rosenberg, 2000). Para o adequado desempenho de seu papel mecânico algumas propriedades são imprescindíveis. Ossos têm que ser (1) rígidos para resistirem a deformações e funcionarem como propulsores contra a gravidade; (2) flexíveis para absorverem energia sobre eles colocada; (3) fortes para resistirem aos impactos; (4) leves para não prejudicarem a mobilidade dos indivíduos. Essas propriedades são alcançadas pelo material que o compõe e pela forma como este material é disposto no espaço. A forma e a composição material de um osso serão determinadas por sua função (Seeman, 2008). Uma das principais proteínas do osso – o colágeno – é o grande responsável pela elasticidade deste tecido. No entanto, necessita de minerais que impeçam sua ruptura (Seeman, 2008; Viguet-Carrin et al., 2006). Ao aplicarmos carga (energia) sobre um osso, será o colágeno, juntamente com outras proteínas da matriz óssea, que irá dissipar esta energia, de forma que a parte rígida do osso não quebre (Seeman, 2008). Este sistema precisa se adaptar constantemente às mudanças de carga a ele impostas. 16 Durante a vida, a acomodação às cargas se dá pelo processo de modelação e remodelação. Por meio dele, o osso atingirá a força e a leveza indispensáveis através do depósito de material em local onde isto se faz necessário e pela remoção de material em excesso. A unidade metabólica básica, responsável por este processo, é constituída pelos osteoclastos (que removem material) e osteoblastos (que depositam material) e sua atividade máxima se dá durante o período de crescimento linear do esqueleto (Seeman, 2008). Nesta fase a atividade celular favorece a formação óssea e quando o pico de massa óssea é atingido há um equilíbrio entre as forças formadoras e destruidoras. Estudos sugerem que fatores genéticos são os principais determinantes da modelação e remodelação (Davies et al., 2005). 4.2 – O colágeno e seus aspectos genéticos e proteicos Os diferentes tipos de colágeno formam uma família multigênica, cujos produtos apresentam semelhanças tais como: todos são moléculas com três cadeias; o domínio da tripla hélice é marcado por repetições de sequências de aminoácidos – GLY-X-Y, onde GLY é o aminoácido glicina, presente em intervalos de três aminoácidos; são ricos em hidroxiprolina e hidroxilisina e, têm importante papel estrutural nos tecidos (Byers, 2001). O colágeno tipo I é sem dúvida a mais abundante de todas as proteínas desta família, estando presente em praticamente todos os tecidos do organismo e sempre adaptando sua forma à função que exercerá em um determinado tecido. No osso, na pele e nos tendões fornece força tensional; já nos vasos sanguíneos sua estrutura permite a formação de tubos ocos. É classificado como colágeno fibrilar. São também tidos como colágeno fibrilar os 17 tipos II, III, V e XI. A codificação das proteínas dos colágenos fibrilares é responsabilidade de 10 genes diferentes. No caso do colágeno tipo I, estes se localizam em 17q21.31-22.05 (COL1A1) e 7q22.1 (COL1A2) e estão associados à produção de cadeias 1(I) e 2(I) respectivamente (Byers, 2001). O procolágeno tipo I é um heterotrímero formado por duas cadeias proα1 e uma cadeia proα2. Cada cadeia preproα é sintetizada com uma sequência sinalizante de aproximadamente 20 resíduos que facilita sua passagem pela membrana retículo endoplasmático rugoso. Tal sequência é clivada durante a passagem desta cadeia pelo retículo endoplasmático rugoso. A cadeia preproα1(I) contem uma extensão de 86 resíduos, rica em cistina cuja função é desconhecida. Tanto a cadeia preproα1(I) quanto a cadeia preproα2(I) contem um domínio com 36 resíduos (12 trincas GLY-X-Y) que formam a tripla hélice na molécula de pró-colageno intacta. Esta tripla hélice estabiliza o terminal N da molécula. Há também um domínio telopeptídeo, sem a forma de tripla hélice, que contem o sítio de clivagem proteolítica da extensão do propetideo na ponta N e resíduos de lisina envolvidos na formação de ligações interfibrilares. O maior domínio da tripla hélice tem 1014 resíduos de comprimento e é caracterizado pela repetição de glicina em cada três posições, por este ser o menor aminoácido capaz de ocupar o espaço no interior da tripla hélice (Byers, 2001; Viguet-Carrin et al., 2006). Todo colágeno fibrilar é sintetizado na forma de compostos solúveis chamados procolágeno. A biosíntese do procolágeno é um processo complexo em que diversas enzimas e chaperonas participam na dobragem e trimerização (Viguet-Carrin et al., 2006). Após a secreção do prócolágeno na matriz extracelular, este passará por um processo proteolítico que o converterá em 18 colágeno que então formará fibrilas e irá se ligar a proteínas diversas da matriz (Figura 1) (Byers, 2001). Figura 1: esquema de representa a formação das fibras de colágeno, desde a síntese das cadeias até a formação das ligações interfibrilares (adaptado de Viguet-Carrin et al., 2006). 19 Diversas mutações em genes das cadeias codificantes de colágeno já foram descritas em indivíduos com osteogênese imperfeita. Embora não exista uma clara correlação genótipo-fenótipo, de modo geral, as mutações associadas à diminuição da quantidade de colágeno tipo I estão associadas ao fenótipo de osteogênese imperfeita tipo 1. Por outro lado, mutações associadas à alteração da qualidade do colágeno sintetizado estão associadas aos fenótipos de osteogênese imperfeita tipos 2, 3 e 4 (Cole, 1997; Lund et al., 1999). Aproximadamente 75-80% das alterações no colágeno estão relacionadas a mutações de ponto que substituem o aminoácido glicina. Contudo, em alguns indivíduos com o diagnóstico clínico de osteogênese imperfeita nenhuma mutação nestes genes é identificada. Recentemente foram descritas mutações em genes relacionados ao processamento do colágeno, em indivíduos com fenótipo de osteogênese imperfeita. Entre estas estão mutações na proteína associada à cartilagem (CTRAP) e na proteína prolil 3-hidroxilase 1 (LEPRE1). A proteína associada à cartilagem e a prolil 2-hidroxilase juntamente com a ciclofina B formam um complexo intracelular com o colágeno que facilita a formação da hélice e a sua estabilização. A prolil 3-hidroxilase é considerada uma chaperona do colágeno. (Barnes et al., 2006; Cabral et al., 2007). 20 4.3 – O osso na osteogênese imperfeita A osteogênese imperfeita é uma doença dos osteoblastos, que produzem matriz óssea anormal (Glorieux, 2001). Independente da mutação do colágeno observada, a quantidade de osso produzida será sempre menor, levando à observação de número reduzido de trabéculas ósseas, trabéculas mais finas e pouca massa óssea (Chavassieux et al., 2007). Os três mecanismos pelos quais a massa óssea aumenta em um indivíduo estão prejudicados na osteogênese imperfeita. Primeiro, existe um defeito de modelação do tamanho e forma do osso que pode ser observado pela baixa espessura cortical mantida durante o crescimento de indivíduos com osteogênese imperfeita. Segundo, a produção de trabéculas secundárias pela ossificação endocondral está prejudicada, e terceiro o espessamento das trabéculas pelo processo de remodelação não é adequado. O processo de remodelação no osso com osteogênese imperfeita favorece a atividade osteoclástica. Além disso, a taxa de deposição mineral é mais baixa que em indivíduos normais indicando que os osteoblastos produzem menor quantidade de matriz por período (Rauch et al., 2000). As conseqüências destas alterações podem ser observadas na figura 2. 21 Figura 2: biópsia de osso em indivíduo normal (A), na osteogênese imperfeita tipos I (B), III (C) e IV (D). Pode ser observada a diminuição da quantidade de trabéculas (estrelas), trabéculas mais finas e diminuição da espessura cortical (seta larga) em todos os tipos de osteogênese imperfeita quando comparados ao controle (Rauch et al., 2000). 4.4 – Osteogênese imperfeita: manifestações clínicas e classificação As manifestações clínicas incluem osteopenia, fraturas recorrentes com deformidades secundárias, surdez precoce, escleras azuladas, dentinogênese imperfeita e frouxidão ligamentar. Em 1979, o grupo liderado por Sillence propôs uma classificação em quatro tipos (I-IV) (Sillence et al., 1979). Posteriormente, mais quatro tipos (V-VIII) foram descritos (Glorieux et al., 2000; Glorieux et al., 2002; Ward et al., 2002; Cabral et al., 2007) e embora esta divisão em oito tipos clínicos (Apêndice 1) seja amplamente utilizada, ainda existem inconsistências quanto às características e ao prognóstico de cada tipo (Plotkin, 2006). 22 O tipo I é caracterizado por poucas fraturas ao longo da vida, surdez precoce, escleras azuladas, poucas deformidades e em geral é descrito como a forma mais branda da doença (Sillence et al.,1979). Nestes indivíduos em geral são encontradas mutações que geram alterações quantitativas no colágeno tipo I (Lund et al.,1999). O tipo II é tido como a forma mais grave, letal no período neonatal ou no primeiro ano de vida. As fraturas são observadas já no período intra-útero e classicamente observa-se o fêmur em sanfona na radiografia de ossos longos. Ossos wormianos em geral estão presentes (Sillence et al.,1979). O tipo III é a forma mais grave que sobrevive ao período neonatal. São observadas inúmeras fraturas com trauma mínimo durante a vida, que acarretam notáveis deformidades. A baixa estatura, escleras acinzentadas, ossos wormianos, face triangular e macrocrania são outras características desta forma (Sillence et al., 1979). Em geral, o tipo III está associado a mutações associadas a alterações qualitativas do colágeno tipo I (Lund et al., 1999). Indivíduos classificados como tipo IV apresentam número variado de fraturas ao longo da vida. É marcante nestes indivíduos o arqueamento de fêmures, mesmo sem a ocorrência de fraturas neste sítio. A surdez e escleras azuladas não são observadas nestes pacientes (Sillence et al.,1979). Este grupo é bastante heterogêneo e são encontradas mutações em genes de colágeno tipo I em alguns pacientes. Tais mutações podem representar alterações qualitativas ou quantitativas na proteína (Lund et al.,1999). 23 O tipo V, descrito mais recentemente, é marcado pela formação de calos hiperplásicos em locais de fraturas ou de cirurgias ósseas. Além disso, observa-se calcificação da membrana interóssea no antebraço, o que leva à restrição do movimento de pronação/supinação. Escleras azuis e dentinogênese imperfeita não são encontradas neste grupo. Histologicamente são observadas menor quantidade de osso cortical e trabecular, em relação à indivíduos classificados como tipo IV e as lamelas, quando observadas à luz polarizada, encontram-se desorganizadas e muitas vezes com aspecto tipo rede. Nenhuma mutação nos genes codificadores de cadeias de colágeno foi identificada nestes indivíduos (Glorieux et al., 2000). Os tipos VI e VII foram identificados em pacientes inicialmente classificados como do tipo IV. No entanto, apresentavam características que os separavam do restante. A osteogênese imperfeita tipo VI é marcada pela ausência de ossos wormianos, fragilidade vascular, escleras azuladas e dentinogênese imperfeita. A distinção dos dois tipos (IV e VI) baseia-se em características histológicas. Pacientes do tipo VI apresentam padrão de lamelação do osso como escama de peixe quando observado à luz polarizada. Além disso, a espessura trabecular está diminuída, assim como a largura cortical e o volume de osso mineralizado. É tida como uma forma rara e moderada a grave de osteogênese imperfeita e, assim como no tipo V nenhuma anormalidade nos genes do colágeno foi identificada até o momento (Glorieux et al., 2002). Já o tipo VII foi descrito em famílias originárias de uma comunidade localizada na província de Quebec. Como no tipo VI, a dentinogênese imperfeita não foi observada nestes indivíduos. As deformidades precoces de 24 membros inferiores (coxa vara) são marcantes e surgem mesmo antes da ocorrência de fraturas nestes locais. Além disso, observa-se rizomelia, como resultado do crescimento anormalmente lento de fêmures e úmeros. A avaliação histológica lembra ossos com osteogênese do tipo I e nota-se diminuição de osso cortical e osso trabecular (Ward et al., 2002). A alteração molecular em pacientes com tipo VII foi mapeada em 3p22-24.1, sendo este um locus não relacionado à genes do colágeno (Labuda et al., 2002). Recentemente foi sugerida a classificação do tipo VIII. Cabral e colaboradores (2007) descreveram cinco casos, em sua maioria de origem africana, que apresentavam uma forma grave a letal de osteogênese imperfeita. Todos tinham face arredondada, escleras claras, tórax curto e em barril, associado a múltiplas fraturas, evidentes ao nascimento. As radiografias realizadas no período pré-natal evidenciavam ossos submineralizados e os exames realizados posteriormente, em alguns casos, mostravam metáfises bulbosas e aparente desorganização da matriz. O escore Z da densidade mineral em coluna lombar era mais baixo que em todos os outros tipos de osteogênese imperfeita. Este fenótipo está associado a mutações nulas no LEPRE1 (Cabral et al., 2007). 4.5 – Marcadores bioquímicos do metabolismo ósseo O turnover ósseo é o processo de reabsorção, formação e remineralização de um osso que ocorre na unidade óssea multicelular. Além de proporcionar o crescimento do esqueleto, tal processo é responsável por adaptar o tecido ósseo às cargas a ele impostas. Em algumas doenças, como na osteogênese imperfeita, este processo encontra-se bastante alterado com o 25 favorecimento do turnover, em especial entre pacientes com tipos III e IV (Braga et al., 2004). A monitorização do turnover ósseo é importante ferramenta para o acompanhamento da resposta ao tratamento com bifosfonatos na osteogênese imperfeita, visto que este grupo de medicações promove a diminuição do turnover, com consequente depósito de osso, favorecendo, assim o aumento da espessura da camada cortical do osso, de suas trabéculas e, teoricamente, a diminuição do risco de fraturas entre pacientes com osteogênese imperfeita (Cremers et al., 2008). Os marcadores de turnover incluem metabolitos da degradação do colágeno, enzimas secretadas por osteoclastos e osteoblastos, entre outros. O início do processo de turnover, em geral, se dá pelos osteoclastos que reabsorvem osso em um determinado local, secretando ali proteases ácidas e neutras que degradam as fibrilas de colágeno. São produtos da degradação do colágeno a hidroxiprolina, piridinolina, deoxipiridinolina e telopeptídeos. Além destes são marcadores de reabsorção óssea a fosfatase ácida tartareresistente, galactosil-hidroxilisina e sialoproteína óssea (Cremers et al., 2008). Após esta fase, os osteoblastos iniciam a formação de osso novo e neste processo secretam metabólitos que são os marcadores de formação óssea. Entre eles podemos citar propeptídeos dos terminais N e C do colágeno tipo I, osteocalcina e fosfatase alcalina óssea. Abaixo temos uma descrição sumária de cada um destes metabolitos. 26 4.5.1. Marcadores de formação óssea: Fosfatase alcalina: faz parte de um grande grupo de proteínas ligadas à superfície extracelular. Tem diferentes isoformas e algumas se expressam exclusivamente em certos tecidos, incluindo a fosfatase alcalina óssea (Calvo et al., 1996). Osteocalcina: é uma proteína sintetizada por osteoblastos maduros, odontoblastos e condrócitos hipertróficos. É depositada primariamente na matriz extracelular do osso, mas uma pequena quantidade entra na corrente sanguinea. É um marcador sensível e específico da atividade do osteoblasto e seu nível sérico reflete a taxa de formação de osso (Calvo et al., 1996). Peptídeos de procolágeno tipo I: o polipeptídeo de colágeno recétraduzido (cadeia pré-próα) inclui sequências de sinal nos terminais amina e carboxila. Durante a síntese do colágeno o propeptideo C guia a seleção e associação de cadeias proα individuais e impede a formação prematura da fibrila intracelular. Endoproteinases extracelulares específicas clivam a molécula de procolágeno permitindo a formação das fibrilas (Calvo et al., 1996). 4.5.2. Marcadores de reabsorção óssea: Hidroxiprolina: presente em todos os tipos de colágeno e em todos os tecidos, este aminoácido é liberado sempre que ocorre a quebra de uma fibra de colágeno, jamais sendo reintegrado a uma molécula de colágeno recém-sintetizada. Embora seja muito utilizado não é um marcador específico do osso e não permite distinguir entre formação e 27 degradação óssea, visto que é liberado em ambos os processos (Calvo et al., 1996). Piridinolina e deoxipiridinolina: são estruturas trivalentes que ligam as fibras de colágeno, estabilizando-as. A piridinolina está presente em todos os tipos de tecido, exceto a pele e a deoxipiridinolina é um marcador ósseo mais específico. Apresentam diversas vantagens em relação à hidroxiprolina: sua única fonte é o colágeno maduro; são excretados sem metabolização prévia por outras vias; não são absorvidos na dieta, diminuindo assim fatores de confusão na dosagem (Calvo et al., 1996). Telopeptídeos: são marcadores de degradação do colágeno. O terminal carboxila é liberado do colágeno intacto pela catepsina K, dando origem ao C-telopeptídeo e o outro marcador é liberado do terminal amina (Ntelopeptídeo do colágeno). Ambos são úteis no monitoramento do tratamento com bifosfonatos (Calvo et al., 1996). Fosfatase ácida tartare-resistente: faz parte do grupo de fosfatases ácidas que são hidrolases não específicas (Calvo et al., 1996). Durante o processo de reabsorção, osteoclastos secretam algumas enzimas no espaço entre a sua membrana rugosa e a superfície do osso, sendo uma delas a fosfatase ácida tartare-resistente. Reflete a taxa de reabsorção óssea. Sialoproteína óssea: é uma glicoproteína fosforilada sintetizada por osteoblastos que in vitro parece estimular a formação de cristais de hidroxiapatita (Calvo et al., 1996). 28 Catepsina K: tem a habilidade de clivar as regiões do telopeptídeo e da hélice do colágeno tipo I. Degrada muitas proteínas da matriz óssea, incluindo colágeno tipo I, osteocalcina e osteopontina (Calvo et al., 1996). 4.6 – Densitometria óssea A densidade de um osso é definida pela relação entre sua massa (quantidade de material) e o seu volume (tamanho do osso), sendo diretamente proporcional a massa e inversamente proporcional ao volume. A importância de conhecer a densidade dos diferentes ossos está relacionada ao risco aumentado para a ocorrência de fraturas quando a densidade do osso está diminuída. Embora inicialmente o foco tenha sido mulheres na pós-menopausa e a prevenção de fraturas nesta faixa etária, logo as técnicas utilizadas para estudo da densidade óssea foram aplicadas em outros grupos, incluindo crianças e adolescentes com diversas doenças que cursam com osteopenia ou osteoporose (Fewtrel, 2003). No final dos anos 1980, o principal método de estudo da densidade óssea foi desenvolvido. A absortimetria de raio-x com duas energias ou simplesmente densitometria óssea é o exame mais empregado na investigação da densidade do osso. A densitometria determina a quantidade de mineral (conteúdo mineral ósseo) em uma determinada região (área) usando a absorção de raio-x de duas energias diferentes e as medidas podem ser feitas no corpo todo ou em determinadas regiões, sendo as mais utilizadas colo femural e coluna lombar. O local de escolha para avaliação da densidade irá depender de qual condição está sendo investigada (Fewtrell, 2003). 29 De modo geral, os aparelhos empregam duas tecnologias diferentes (fan beam e pencil beam) para estudo da densidade. Nas que utilizam o método fan beam, o tempo de escaneamento é menor, pois o ângulo dos raios é maior, abarcando uma área mais extensa. Neste método, as principais desvantagens estão relacionadas à radiação, uma vez que a exposição é maior do que com o outro método e à magnificação, por causa da distância entre a fonte de raio-x e o osso. A magnificação é um problema deste método que se acentua em crianças ou adultos pequenos, pois os aparelhos são projetados para realizarem suas medidas considerando valores pré-determinados de distância entre o indivíduo e o aparelho, os quais se baseiam no tamanho de um adulto (Fewtrell, 2003). O outro método utilizado nos densitômetros é o pencil beam. Neste, o ângulo formado pelos raios é menor. Consequentemente, o tempo de aquisição da informação durante o exame é maior (Fewtrell, 2003). A tecnologia de cada aparelho não é a única diferença observada entre os fabricantes. Os aparelhos da GE Lunar são calibrados para medirem sais minerais, enquanto que os da Hologic para identificar cristais de hidroxiapatita. Ainda, a identificação das extremidades dos ossos é realizada por algoritmos que variam com o aparelho. No entanto, em geral, eles são estimados para adultos tornando-se um problema em indivíduos pequenos (crianças) e em ossos de baixa densidade (Fewtrell, 2003). A densidade mineral óssea, que é o valor de interesse, resulta do quociente entre conteúdo mineral ósseo e área medida. Logo, percebe-se que esta é uma medida bidimensional sendo diretamente afetada pelo tamanho do sujeito, tendendo a subestimar a densidade em indivíduos pequenos e 30 superestimar nos grandes. Cabe lembrar que o crescimento não é um processo uniforme em todas as direções, o que dificulta a comparação dos resultados de forma longitudinal (Binkovitz et al., 2007). Os problemas gerados pelo tamanho do objeto de investigação são importantes e diversas abordagens têm sido utilizadas para sua solução. Uma delas é o uso de densidade óssea volumétrica, onde o conteúdo mineral ósseo é ajustado para o volume e não para a área, podendo ser empregada na avaliação de quadril e coluna. Outra abordagem permite avaliar se estamos diante de ossos curtos, estreitos ou finos através do cálculo de altura para idade, área óssea para altura e conteúdo mineral ósseo para área óssea. Independente da abordagem utilizada, é crucial ter em mente que os valores do conteúdo mineral ósseo e da densidade mineral óssea devem ser interpretados de acordo com o tamanho da criança e o estágio puberal (Fewtrell, 2003). Em adultos, a medida da densidade mineral óssea é comparada à densidade mineral óssea de adultos jovens, em geral aos 20 anos, por este ser o momento do pico de massa óssea. Isto permite gerar valores conhecidos como escore T que são desvios-padrão em relação à medida da densidade mineral óssea aos 20 anos. Estes valores permitem estimar o risco da ocorrência de fraturas em adultos e são utilizados para definir conceitos como osteopenia e osteoporose (WHO, 2003). Em crianças e adolescentes esta medida não é adequada e os valores obtidos nestas faixas etárias são comparados a valores obtidos em crianças ou adolescentes, na mesma faixa etária, que não apresentem problemas ósseos. Isto gera um valor conhecido como escore Z, o qual é um valor mais adequado para o acompanhamento de crianças e adolescentes no que tange à densidade mineral óssea. No entanto, 31 não permitem estimar como será o pico de massa óssea, nem fazer inferências sobre o risco de fraturas (Binkovitz et al., 2007). 4.7 – Tratamento medicamentoso da osteogênese imperfeita O tratamento da osteogênese imperfeita baseia-se na cirurgia ortopédica para correção de deformidades, na reabilitação fisioterápica para melhora da funcionalidade e no uso de bifosfonatos para aumento de massa óssea (Engelbert et al., 1998; Rauch e Glorieux, 2004). Os bifosfonatos são moléculas estruturalmente semelhantes ao pirofosfato inorgânico, um composto natural que inibe a calcificação dos tecidos conjuntivos e regula a mineralização óssea. Além da alta afinidade pelo tecido ósseo, a possibilidade de serem absorvidos quando administrados por via oral permitiu o desenvolvimento deste composto como medicação. Atuam inibindo a reabsorção óssea ao interferirem com a função dos osteoclastos. Os diversos compostos deste grupo apresentam diferenças em sua estrutura que estão diretamente relacionados à afinidade por certos tecidos e à sua potência como agente anti-reabsorção. Na primeira geração dos bifosfonatos são listados o clodronato e o etidronato. A segunda geração, que contem um átomo de nitrogênio na cadeia alkali, é constituída pelo pamidronato e alendronato. A introdução de outro átomo de nitrogênio tornou os compostos da terceira geração (olpandronato e ibandronato) ainda mais potentes no que tange a inibição da reabsorção óssea. Os mais recentes, tais como o zolendronato e risendronato possuem um átomo de nitrogênio em um anel heterocíclico, aumentando quase 10000 vezes sua potência (Russel e Rogers, 1999). 32 Desde a descrição inicial de seu uso num paciente com osteogênese imperfeita (Devogelaer et al., 1987), várias medicações do grupo já foram utilizadas em diversos indivíduos com a condição. As primeiras séries que reuniram um número maior de pacientes foram publicadas em 1998. Glorieux e colaboradores (1998) relataram diminuição da dor óssea, melhora da capacidade de deambulação, diminuição da quantidade de fraturas, aumento da densidade mineral óssea e diminuição da reabsorção óssea (redução da excreção de N-telopeptídeo e redução da concentração plasmática de fosfatase alcalina) em crianças, com a forma grave de osteogênese imperfeita, tratadas com pamidronato dissódico, de forma cíclica. Posteriormente, outros grupos relataram resultados benéficos semelhantes (Falk et al., 2003; Aström e Söderhäll, 1998; Aström e Söderhäll, 2002; Barbosa, 2006; Rauch et al., 2002). Atualmente, novas terapias vêm sendo estudadas, tais como o transplante de células tronco, o transplante de medula óssea e a terapia gênica, e embora os resultados iniciais pareçam promissores ainda há muito a esclarecer até que elas possam ser empregadas rotineiramente (MillingtonWard et al., 2005). 33 5. MATERIAL E MÉTODOS A partir dos anos 1960, com o surgimento da pesquisa clínica, emerge um novo modelo de ensino e prática médica. Neste novo modelo, o médico é estimulado a embasar suas decisões clínicas em resultados de estudos sistemáticos, apoiado no conhecimento adquirido pela experiência clínica e pelo estudo da fisiopatologia das doenças. Este novo paradigma contrapõe-se ao padrão anterior, que enfatizava a importância de uma autoridade científica, fornecendo ao médico ferramentas para avaliar a credibilidade da opinião dos especialistas. Este novo modelo recebeu o nome de Medicina Baseada em Evidência e vem ganhando força com o crescente surgimento de estudos clínicos sistemáticos e meta-análise3 (Evidence-based Medicine Workgroup, 1992). No presente estudo, para respondermos às questões sobre qual o melhor tratamento clínico para a osteogênese imperfeita e qual a magnitude desta terapia entre pacientes, com esta condição, foi realizada uma revisão crítica da literatura científica, embasada pelos princípios da epidemiologia clínica4. O estudo dividiu-se em cinco etapas: Fase 1 – Busca pelos estudos primários. Fase 2 – Seleção dos estudos primários para inclusão. 3 Revisão sistemática e meta-análise: são tipos de estudos que visam responder questões clínicas específicas, que utiliza como fonte a literatura científica. Empregam uma abordagem pré-determinada para identificação de estudos primários, para a avaliação de qualidade destes e a síntese dos resultados. Na meta-análise os resultados são combinados com técnicas de estatística, de forma a fornecer informações mais precisas sobre a magnitude do efeito (Fletcher e Fletcher, 2006). 4 Epidemiologia clínica – termo cunhado por John Paul em 1938, deriva de duas ciências – a epidemiologia e a medicina clínica. Emprega métodos utilizados em estudos epidemiológicos para responder as questões clínicas e embasar a tomada de decisão no cuidado com o paciente (Sackett, 2002; Fletcher e Fletcher, 2006). Fletcher e Fletcher (2006) definem como “a ciência que faz predições sobre pacientes individuais utilizando a contagem de eventos clínicos em grupos de pacientes semelhantes e valendo-se de métodos científicos sólidos para garantir que as predições sejam corretas” (p. 21) 34 Fase 3 – Avaliação de qualidade dos estudos incluídos. Fase 4 – Extração dos dados. Fase 5 – Análise dos resultados. 5. 1. Fase 1 - Fontes e estratégias de busca Considerando que o tratamento com bifosfonatos na osteogênese imperfeita é relativamente recente e que os principais estudos iniciais (Glorieux et al., 1998; Aström e Söderhäll, 1998) datam de 1998, a busca eletrônica limitou-se ao período 1998-2008 nas seguintes bases de dados: Medline – Organizada pela Biblioteca Nacional de Medicina dos Estados Unidos. Lilacs – Literatura Latino-Americana e do Caribe em Ciências da Saúde, organizado pela BIREME. CENTRAL – Cochrane Central Register of Controlled Trials; DARE - Database of Abstracts of Reviews of Effects, organizado pelo Centre for Review and Dissemination da Universidade de York – Reino Unido. Clinical trials.gov – Organizado pelo National Institutes of Health – Estados Unidos que inclui o registro de estudos clínicos financiados pela agência. Research Findings Register – Organizado pelo National Health Service – Reino Unido que inclui registro de estudos clínicos. CAPES - Banco de teses e dissertações da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior. 35 OpenSIGLE – System for information on grey literature in Europe que inclui o registro de documentos científicos não publicados em periódicos. OCLC – Online Computer Library Center – Cooperativa de bibliotecas ao redor do mundo. As bases de dados supracitadas foram selecionadas por abrangerem grande número de periódicos de diferentes países ou por incluírem registros de estudos clínicos em andamento ou já finalizados, financiados por instituições governamentais. A opção pela inclusão de bases de dados que reúnem o registro de estudos clínicos nos Estados Unidos e no Reino Unido foi uma tentativa de adicionar estudos não publicados e não indexados nas bases de dados habituais (Medline e Lilacs), evitando assim o viés de publicação. Na tentativa de identificar o maior número possível de estudos para inclusão na revisão, optou-se por uma estratégia de busca mais sensível, em detrimento da especificidade. Para o Pubmed foram utilizados os filtros de busca já existentes nesta base de dados, desenvolvidos por Haynes e colaboradores (2005) especificamente para terapia5. Para as demais bases de dados foram utilizadas combinações diferentes dos termos “osteogenesis imperfecta”, “bisphosphonate”, “alendronate”, “pamidronate” e “zolendronate”. 5 Neste estudo Haynes e colaboradores (2005) propuseram um mecanismo de busca que combina os termos “clinical trial” e “random” de forma a identificar todos os possíveis estudos clínicos randomizados sobre um determinado tema. A sensibilidade desta abordagem é de 99,3% e a especificidade de 70,4%. 36 A outra estratégia de busca concentrou esforços na identificação de estudos da “literatura cinza”6. Para tanto, foram recuperados resumos de trabalhos publicados em congressos e reuniões relacionadas ao tema. Neste processo, consideramos que as especialidades médicas de relação mais próxima ao tema “tratamento clínico com bifosfonatos em indivíduos com osteogênese imperfeita” são a genética médica, a endocrinologia e especialidade relacionadas ao osso (incluindo ortopedia e metabolismo ósseo). Em relação à genética, nos Estados Unidos da América são duas as principais sociedades – American Society of Human Genetics e o American College of Medical Genetics. Na Europa, as diferentes sociedades locais reúnem-se na European Society of Human Genetics. Em relação à endocrinologia temos nos Estados Unidos da América a American Association of Clinical Endocrinology e na Europa a European Society of Endocrinology. Os livros de resumos da European Society for Calcified Tissue também foram pesquisados. Além das conferências organizadas por sociedades de especialistas, a cada três anos uma reunião internacional sobre osteogênese imperfeita é realizada com o apoio de centros de referência em osteogênese imperfeita mundiais e da Osteogenesis Imperfecta Foundation, uma fundação norte-americana de pacientes com osteogênese imperfeita e seus familiares. O contato através de correio eletrônico permitiu a inclusão dos livros de resumo das duas últimas reuniões por eles organizadas. Neste material foi realizada uma pré-seleção de resumos cujo tema era “osteogenesis imperfecta”. 6 Literatura cinza (em inglês grey literature) – literatura não publicada formalmente que inclui relatórios técnicos, resumos de congressos, reuniões científicas, entre outros (Dikersin et al., 1994). 37 5.2. Fase 2 – Seleção dos estudos (Apêndice 2) Todos os estudos identificados na busca inicial tiveram seus resumos avaliados e quando estes não estavam disponíveis estudou-se o artigo na íntegra. Os critérios de seleção incluíram: 1. Tipo de estudo: ensaios clínicos controlados e não controlados. 2. População do estudo: pacientes com osteogênese imperfeita (diagnóstico clínico ou molecular). 3. Intervenções de interesse: pamidronato dissódico, alendronato dissódico ou zolendronato dissódico. 4. Desfechos clínicos: a. densidade mineral óssea; b. marcadores bioquímicos do turnover ósseo (osteocalcina, fosfatase alcalina, fosfatase alacalina óssea, C-telopeptídeo, Ntelopeptídeo); c. número de fraturas; 5. Idiomas: inglês, francês, espanhol e português. Foram incluídos estudos que preencherem todos os critérios 1, 2, 3, 5 e pelo menos um dos subitens do critério 4. Não foram analisados estudos de caso, nem aqueles cuja população envolveu pacientes com outras doenças que causam osteopenia ou cujo grupo controle fosse constituído por controles históricos. Apoiado no fato de que séries de controles históricos, em geral, têm evolução clínica pior que os grupos controle criados de forma contemporânea ao grupo de intervenção (Diehl e Perry, 1986), optou-se pela exclusão destes estudos. 38 Os ensaios clínicos controlados e randomizados são considerados o “padrão-ouro” de evidência sobre o efeito de uma intervenção (Sackett et al., 1992). A qualidade deste tipo de estudo reside na tentativa de eliminar o viés. No entanto possui limitações, sendo a principal a elaboração de amostras de pacientes que são selecionadas de forma a preencherem os estritos critérios de inclusão e exclusão associados a este tipo de estudo. Se por um lado esta característica aumenta a validade interna do estudo, por outro impede a generalização de seus resultados para uma população heterogênea (Fletcher e Fletcher, 2006). Uma maneira de superar este problema é conduzir ensaios clínicos grandes, o que certamente, no caso da osteogênese imperfeita, não é possível visto que se trata de uma condição rara. Por este motivo optamos pela seleção de estudos clínicos não controlados (do tipo antes e depois). De acordo com Fletcher e Fletcher (2006), este tipo de estudo está sujeito a erros quando o curso clínico da doença não é previsível; não há como medir o efeito Hawthorne7; variabilidade da resposta do paciente em aferições subseqüentes (exemplo: variação biológica da freqüência cardíaca) e melhora da doença, apesar do tratamento. Cabe, contudo, algumas considerações sobre estas hipóteses: a osteogênese imperfeita é uma condição progressiva que evolui com inúmeras fraturas e incapacidade, sendo o prognóstico intimamente associado aos subtipos clínicos. O efeito Hawthorne pode influenciar a resposta à dor (subjetividade deste desfecho) e, em estudos que evoquem a memória de pacientes ou familiares, o número de fraturas ocorridas antes e após o tratamento. A dor não será avaliada como desfecho e o modo como o número 7 Efeito Hawthorne – o desejo do paciente em agradar o médico ou obter bons resultados pode superestimar o real efeito da intervenção (Fletcher e Fletcher, 2006). 39 de fraturas foi registrado em cada estudo foi avaliado. Por último, devemos considerar as variações na densidade mineral óssea, pois além do efeito da intervenção, o próprio crescimento do indivíduo (quando se trata de crianças e adolescentes) também influencia as medidas subseqüentes da densidade mineral óssea. 5.3. Fase 3 – Avaliação de qualidade dos estudos primários (Anexo 1) Jadad e colaboradores (1996) definem qualidade como “a probabilidade do desenho de um estudo de gerar resultados sem viés e de se aproximar da verdade terapêutica” (p. 2). No entanto, esta definição limita-se à validade interna de um estudo, ignorando outras questões que devem ser levadas em conta na análise da qualidade deste. A validade externa, magnitude do efeito, intervalos de confiança e perdas são alguns exemplos de fatores que também devem ser considerados quando da leitura crítica de um estudo clínico (Glasziou et al., 2004). Neste sentido, além da aplicação da escala criada por Jadad e colaboradores (1996) (Anexo 1) foram consideradas outras questões, tais como os critérios de inclusão, exclusão e tratamento empregado e o uso de critérios de gravidade clínica e maturação esquelética para a análise estatística. 40 5.4. - Fase 4 - Coleta de dados (Apêndice 3) Foram extraídos dados relacionados ao desenho do estudo, população estudada (dados clínicos, idade), intervenção (tipo de medicação, via de administração, dose empregada, tempo de duração), perdas e desfechos clínicos previamente descritos. 5.5. - Fase 5 – Análise dos dados A síntese dos dados foi realizada de forma descritiva, baseando-se nos resultados individuais de cada medicação e na comparação entre as medicações. 6. RESULTADOS 6.1. Busca pelos estudos primários Na busca dos estudos primários foram acessadas as bases de dados eletrônicas listadas no quadro 1. As palavras utilizadas na busca eletrônica nas diferentes bases também estão listadas no quadro 1. Em algumas bases, realizou-se mais de uma tentativa, uma vez que eram bases consideradas importantes ou porque a tentativa inicial resultou em nenhuma referência. Quando o resumo não estava disponível buscou-se o artigo completo. 41 Base de dados Mecanismo de pesquisa Medline (via pubmed) (limites = humanos, período 1998-2008, idioma portugês, inglês, espanhol, frânces) Osteogenesis imperfecta[MeSH] AND bisphosphonate Osteogenesis imperfecta [MeSH] AND alendronate Osteogenesis imperfecta [MeSH] AND pamidronate Osteogenesis imperfect [MeSH] AND zolendronic acid Osteogenesis imperfecta [MeSH] AND diphosphonate [MeSH] Osteogenesis imperfecta AND bisphosphonate (clinical queries)* LILACS Osteogenesis imperfecta (DeCS) AND diphosphonate (DeCS) Banco de teses da CAPES Osteogenesis imperfecta, bifosfonato (assunto) Biblioteca digital de teses e dissertações Osteogenesis imperfecta, bifosfonato Osteogenesis imperfecta Brasil teses Osteogenesis imperfecta (assunto) Cyberthesis Osteogenesis imperfecta Dissonline.de Osteogenesis imperfecta (assunto) Networked digital library of thesis and dissertations Osteogenesis imperfecta, biphosphonate Osteogenesis imperfecta Portal domínio public Osteogenesis imperfecta (título) Théses en ligne Osteogenesis imperfecta (palavra-chave OU resumo) The Universal Index of doctoral Dissertations in progress Osteogenesis imperfecta (texto) The European Library Osteogenesis imperfecta Cochrane Osteogenesis imperfecta AND biphosphonate Scielo Osteogenesis imperfecta AND bifosfonato Osteogenesis imperfecta OpenSIGLE Osteogenesis imperfecta AND diphosphonate Osteogenesis imperfecta AND alendronate Osteogenesis imperfecta AND pamidronate Osteogenesis imperfecta AND zolendronic acid Osteogenesis imperfecta SCOPUS (TITLE-ABS-KEY (Osteogenesis imperfecta)AND (TITLE-ABSKEY(diphosphonate)) (TITLE-ABS-KEY (Osteogenesis imperfecta)AND (TITLE-ABSKEY(biphosphonate)) ISI Web of Knowledge Osteogenesis imperfecta AND bisphosphonate (title) Osteogenesis imperfecta AND diphosphonate (title) EBSCO (SU(Osteogenesis imperfecta)AND SU(bisphosphonate)) (SU(Osteogenesis imperfecta)AND SU(diphosphonate)) (SU(Osteogenesis imperfecta)AND diphosphonate Número de referências 153 19 100 3 145 162 2 1 0 2 0 1 0 0 12 1 0 0 1 21 0 13 0 0 0 0 6 9 113 0 6 0 0 24 Quadro 1: síntese das bases eletrônicas utilizadas, dos mecanismos de busca empregados em cada base e o número de retornos. MeSH / DeCS= descritor de assunto. SU = assunto. TITLE-ABS-KEY=título, resumo, palavra-chave. *filtro criado por Haynes e colaboradores (2005) que utiliza o seguinte 42 mecanismo de busca [(osteogenesis imperfecta AND bisphosphonate) AND (clinical [TITLE/Abstract] AND Trial [TITLE/Abstract]) OR clinical trials [MeSH terms] OR clinical Trial [Publication Type] OR random*[TITLE/Abstract] OR random allocation [MeSH Terms] OR therapeutic use [MeSH Subheading]). O quadro 2 fornece informações sobre a origem dos livros de resumos, o ano de publicação e a quantidade de referências pertinentes ao tema do estudo. Reunião/Ano American Association of Clinical Endocrinologists th 2006 – 15 annual meeting and clinical congress th 2007 – 16 annual meeting and clinical congress th 2008 – 17 annual meeting and clinical congress European Society of Endocrinology 2001 - Society for Endocrinology Annual Meeting 2002 - Society for Endocrinology Annual Meeting 2003 - Society for Endocrinology Annual Meeting 2004 - Society for Endocrinology Annual Meeting 2005 - Society for Endocrinology Annual Meeting 2006 - Society for Endocrinology Annual Meeting 2006 – European Congress of Endocrinology 2007 - Society for Endocrinology BES 2007 – European Congress of Endocrinology 2008 – Society for Endocrinology BES 2008 – European Congress of Endocrinology American Society of Human Genetics th 1999 – 49 Annual Meeting th 2000 – 50 Annual Meeting st 2001 – 51 Annual Meeting nd 2002 – 52 Annual Meeting rd 2003 – 53 Annual Meeting th 2004 – 54 Annual Meeting th 2005 – 55 Annual Meeting th 2006 – 56 Annual Meeting th 2007 – 57 Annual Meeting 2008 – 58 - Annual Meeting American College of Medical Genetics 2006 2007 2008 European Society of Human Genetics 2001 - European Human Genetics Conference 2002 - European Human Genetics Conference 2003 - European Human Genetics Conference 2004 - European Human Genetics Conference 2005 - European Human Genetics Conference 2006 – European Human Genetics Conference 2007 - European Human Genetics Conference 2008 - European Human Genetics Conference International Conference on Osteogenesis Imperfecta th 2005 – 9 International Meeting on Osteogenesis Imperfecta th 2008 – 10 International Meeting on Osteogenesis Imperfecta European Calcified Tissue Society st 2001 – 1 Joint Meeting IBMS/ESCT th 2002 – 29 European Symposium on Calcified Tissue th 2003 – 30 European Symposium on Calcified Tissue Número de referências 0 0 0 0/134 0/131 0/106 0/104 0/121 0/159 0/1000 0/342 0/746 0/440 0/878 0 1 0 4 1 0 0 0/2390 0/2814 0/2615 0 2 0 0 1 0 0 0 1 0 1 10 13 3 3 3 43 st 2004 – 31 European Symposium on Calcified Tissue nd 2005 – 32 European Symposium on Calcified Tissue rd 2006 – 33 European Symposium on Calcified Tissue th 2007 – 34 European Symposium on Calcified Tissue th 2008 - 35 European Symposium on Calcified Tissue 0 3 1 1 2 Quadro 2: referências encontradas em livros de resumo das principais conferências internacionais relacionadas ao tema deste estudo. Os valores na coluna da direita representam o número de resumos relacionados ao tema e o número total de resumos publicados (quando disponível). Muitas bases eletrônicas indexam os mesmos periódicos e referências redundantes foram recuperadas. O fato de termos utilizado mais de um mecanismo de busca, em algumas bases, também contribuiu para a redundância. No total foram recuperadas 258 referências e nas figuras 3 a 6 suas características gerais estão resumidas. 44 Figura 3: distribuição das referências por ano de publicação. Figura 4: Distribuição das referências quanto à intervenção descrita. 45 Figura 5: distribuição dos autores dos estudos quanto à afiliação por especialidade na área da saúde. *Inclui a subespecialidade pediátrica. ¥Centro de osso refere-se a serviços especializados em doenças do metabolismo ósseo. §Inclui outras especialidades tais como: anestesiologia, ciência animal, cirurgia pediátrica, engenharia biomédica, epidemiologia, farmacologia e toxicologia, hematologia, medicina desportiva, medicina fetal, medicina interna, medicina nuclear, nefrologia, nefrologia pediátrica, neurologia pediátrica, neurobiologia, otorrinolaringologia, patologia clínica, patologia geral, penumologia pediátrica, tecido conjuntivo. 46 Figura 6: distribuição dos estudos quanto à origem. 47 6.2. Seleção dos estudos primários Após a revisão dos resumos, foram selecionados 49 estudos. Depois de uma breve avaliação, percebeu-se que alguns estudos haviam sido conduzidos pelos mesmos autores com população semelhante, desta forma optou-se pela exclusão dos estudos repetidos, dando preferência a manutenção dos que forneciam mais informações. Os apêndices 4 e 5 trazem a lista com referências dos estudos incluídos e dos excluídos, respectivamente. Assim, a amostra aqui apresentada totaliza 39 estudos. Destes, 20 eram estudos clínicos tipo antes-edepois utilizando pamidronato; cinco tinham desenho semelhante com alendronato como intervenção. A comparação entre alendronato e placebo ocorreu em dois estudos; em um o alendronato foi comparado ao pamidronato e em um o pamidronato foi comparado ao zolendronato. Um relatou dados do uso de pamidronato, alendronato e risedronato, sem, no entanto estabelecer comparações entre os grupos. Diferentes doses de pamidronato ou o uso de pamidronato em diferentes tipos de osteogênese imperfeita foram comparados em sete estudos. Ainda, um estudo tratava do uso de zolendronato em indivíduos que já haviam usado esta droga ou que haviam usado pamidronato (estudo de extensão de ensaio clínico controlado) e um era uma revisão sistemática. Os estudos reuniram número de pacientes que variou entre 10 e 165. Foram tratados pacientes com osteogênese imperfeita tipos I, III, IV, V e VI. A maioria (36/39) utilizou como desfechos densidade mineral óssea em coluna lombar (valor bruto ou escore Z). A avaliação da ocorrência de fraturas foi discutida em 25 estudos e em 27 foram utilizados marcadores de metabolismo ósseo. 48 No que se refere à fonte, 30 estudos (77%) vieram de revistas indexadas por diferentes bases de dados e em outros nove a fonte foi a literatura cinza. Quanto ao financiamento, em 18 publicações (46%) esta informação não estava disponível. Dentre as demais, 76% (16/21) foram financiadas. A fonte de financiamento foram fundos de agências governamentais em quatro publicações, organizações de pacientes e familiares ligados a doenças específicas em uma, fundos de hospitais universitários em outra, hospitais ligados a sociedades sem fins lucrativos em oito, indústria farmacêutica em quatro e em duas publicações não foi possível identificar a origem do financiamento. Alguns estudos tiveram financiamento de diversas origens. 6.3. Avaliação de qualidade Após a aplicação da escala de Jadad e colaboradores (1996) a maioria dos estudos obteve nota zero (25/39); nove obtiverem nota um; um, nota dois; um, nota três; um, nota quatro e um, nota cinco. Em um estudo a escala não foi aplicada por tratar-se de uma revisão sistemática. Considerando que a maioria dos estudos selecionados não envolvia grupos controle e a escala é dirigida para avaliação da validade interna de um estudo este resultado já era esperado. O estudo cuja pontuação na escala de Jadad foi cinco (Chevrel et al., 2006) limitou-se ao tratamento da osteogênese imperfeita leve em adultos. A maioria dos pacientes era do tipo I e não foram definidos critérios para início do tratamento. Desta forma a capacidade de generalização destes resultados está limitada pela faixa etária e pela gravidade do quadro. 49 Já o estudo que pontuou quatro na escala de Jadad (Senthilnathan et al., 2008) abordou o tratamento com pamidronato dissódico, comparando doses diferentes da medicação. Foram incluídas crianças com menos de dois anos. Os critérios de início do tratamento foram bem definidos (fratura de compressão vertebral ou fratura com conseqüente deformidade de ossos longos). Embora a faixa etária esteja restringida, foram tratadas crianças, permitindo que estes dados sejam extrapolados para indivíduos com idades semelhantes – crianças, uma vez que são esqueletos ainda em crescimento. Além disso, os critérios de tratamento foram bem definidos. O estudo de DiMeglio e Peacock (2006), o único a pontuar três na escala comparou o tratamento venoso com pamidronato e oral com alendronato. O fato de ter usado medicações cujas vias de administração eram diferentes impossibilitou que o estudo fosse conduzido de maneira cega. Embora, tenham sido incluídos pacientes com os tipos I, III e IV de osteogênese imperfeita, em uma faixa etária que variou entre três e 13 anos, não foram definidos critérios de início de tratamento; o que não impede a extrapolação dos dados para outros grupos. O tipo de osteogênese imperfeita não foi descrito em 12 estudos (Aström et al., 2008; Cabral de Menezes Filho et al., 2007; Glorieux et al., 2008a; Glorieux et al., 2008b; Göksen et al., 2006; Letocha et al., 2003; Marini et al., 2008; Rauch, 2008a; Rauch et al., 2003a; Vallo et al., 2006; Zacharin e Bateman, 2002; Zacharin e Kanumakala, 2004), o que dificulta a extrapolação dos resultados para outros pacientes (validade externa), uma vez que não é possível determinar se foram tratados indivíduos com quadro grave ou leve. No entanto os autores Glorieux e colaboradores (2008b) e Rauch e colaboradores 50 (2003a) definiram os critérios para tratamento utilizados em suas pesquisas (OI tipo III ou IV, com deformidades de ossos longos ou mais de três fraturas ao ano). No que tange a idade, três autores (Marini et al., 2008; Glorieux et al., 2008a; Rauch, 2008a) não informaram a faixa etária dos pacientes tratados, o que novamente impossibilita a extrapolação dos dados para outros grupos de pacientes. De forma geral todos descrevem dados do tratamento em crianças, adolescentes e adultos como um grupo único de indivíduos, sendo que os autores: Glorieux e colaboradores (1998); DiMeglio e Peacock (2006) e, por fim, Sillence e colaboradores (2005) analisaram os dados sob a perspectiva do desenvolvimento puberal. Embora a inclusão de pacientes em todas as faixas etárias seja ideal, uma vez que a osteogênese imperfeita é uma doença crônica, deve-se levar em consideração que a resposta ao tratamento em indivíduos que estão em crescimento costuma ser diferente daquela dos que já completaram o desenvolvimento do esqueleto. Portanto, deve-se ter cautela ao extrapolar dados gerais para as diferentes faixas etárias. A maioria dos autores apresentou como critérios de inclusão o diagnóstico clínico de osteogênese imperfeita, sem fazer menção aos critérios utilizados para inicio de terapia com bifosfonatos. Já nos estudos que definiram tais critérios foram empregados os seguintes: deformidades em ossos longos; ou pelo menos duas a três fraturas/ano nos últimos dois anos; ou fraturas de repetição; ou colapso vertebral (Zeitlin et al., 2006; Senthilnathan et al., 2008; Land et al., 2007; Vyskocil et al., 2005; Poyrazoglu et al., 2008; Rauch et al., 2003b; Forin et al., 2005; Löwing et al., 2007; Rauch et al., 2003a; Cho et al., 2005; Arikoski et al., 2004). Arikoski e colaboradores (2004) e Forin e 51 colaboradores (2005) ainda aplicam como critério para início de tratamento a presença de dor óssea crônica. Em resumo, podemos observar que embora alguns estudos possam ser considerados de boa qualidade no que se refere à validade interna (Chevrel et al., 2006; DiMeglio Peacock, 2006; Senthilnathan et al., 2008) eles também apresentam limitações quanto à extrapolação dos resultados para outros grupos. Para a leitura crítica destas pesquisas, saber os critérios de início de tratamento ou quais pacientes foram tratados (quadro clínico grave x leve) e a faixa etária são de extrema importância. Portanto, os estudos indicados a seguir de: Vallo e colaboradores (2006); Cabral de Meneses Filho e colaboradores (2007); Göksen e colaboradores (2006); Zacharin e Bateman (2002); Zacharin e Kanumakala (2004); Letocha e colaboradores (2003); Marini e colaboradores (2008); Glorieux e colaboradores (2008a); Aström e colaboradores (2008); Rauch (2008a); Glorieux e colaboradores (2008b) e, finalmente, Rauch e colaboradores (2003a) devem ser lidos com prudência. A síntese dos estudos foi realizada de acordo com os desfechos de interesse e as medicações empregadas. No subitem 6.4 estão reunidas informações sobre densidade mineral óssea de coluna lombar; no 6.5 os marcadores de metabolismo ósseo e no 6.6 os dados sobre fraturas. 6.4. Síntese dos resultados no que tange à densidade mineral óssea Antes da síntese dos dados referentes à densidade mineral óssea, cabe ressaltar que alguns autores não informam qual o equipamento de densitometria utilizado, sendo que o restante utiliza equipamentos Lunar ou Hologic com diferentes softwares. Todos, exceto dois (Akcay et al., 2008; 52 Aström e Söderhäll, 2002) utilizaram o mesmo equipamento ao longo dos respectivos estudos. 6.4.1 – Pamidronato dissódico, estudos clínicos do tipo antes e depois Dos 39 estudos, 17 apresentam resultados de densidade mineral óssea em indivíduos com osteogênese imperfeita tratados com pamidronato dissódico, onde cada indivíduo serviu como controle para si mesmo. Nestes estudos, o tempo de tratamento com pamidronato foi heterogêneo, variando de nove meses a seis anos. A dose empregada na maioria das vezes foi de 9mg/kg/ano, variando entre 3mg/kg/ano a 12 mg/kg/ano. A maioria dos autores segue o esquema proposto por Glorieux e colaboradores (1998). Göksen e colaboradores (2006), assim como Rauch (2008a), relatam terem observado aumento da densidade mineral óssea na coluna vertebral sem, no entanto, fornecerem dados mais apurados. O grupo liderado por Göksen é o que utilizou a menor dose (3-4mg/kg/ano) e embora, o estudo tenha incluído 16 indivíduos acompanhados de meio até quatro anos, não há relato de quantos completaram os anos de tratamento. Já Rauch (2008a) não fornece dados sobre a dose de pamidronato utilizada neste estudo. Aström e Söderhäll (2002), como também Andiran e colaboradores (2008) juntamente com Löwing e colaboradores (2007) e Vallo e colaboradores (2006), notaram diferenças estatisticamente significativas antes e após o tratamento, mas não descreveram a magnitude do incremento. Por sua vez, Arikoski e colaboradores (2004), Barbosa (2006), Choi e colaboradores (2007), Glorieux e colaboradores (1998) e também Zacharin e Kanumakala (2004) observaram aumento que variou, em média, 26,2% a 63,5%, todos 53 estatisticamente significativos. Forin e colaboradores (2005) apresentaram estes dados na forma de mediana com valor de 55,4%. Lin e colaboradores (2008), tal como Zacharin e Bateman (2002) afirmam que houve incremento na densidade mineral óssea em taxas de 52,4% em quatro anos e 124,7% em dois anos, respectivamente. No entanto estes autores não informam se esta diferença se deu ao acaso. No que tange o escore Z da densidade mineral óssea em coluna vertebral, Alharbi e colaboradores (2008), Andiran e colaboradores (2008), Bajpai e colaboradores (2007), Barbosa (2006), Choi e colaboradores (2007), Forin e colaboradores (2005), Glorieux e colaboradores (1998), Lin e colaboradores (2008), Poyrazoglu e colaboradores (2008), Zacharin e Bateman (2002) e, dois anos depois, o próprio Zacharin com Kanumakala (2004) relatam que a maioria dos pacientes apresentou melhora neste escore, sendo esta diferença considerada resultado do tratamento com bifosfonato. Glorieux e colaboradores (1998) apresentaram dados referentes à analise de subgrupos (meninos x meninas e pré-puberal x pós-puberal) observando que não houve diferenças entre os grupos. Zacharin e Bateman (2002) afirmam que a idade de início do tratamento não influencia a boa resposta à medicação, sendo esta possível em todas as faixas etárias. 6.4.2 – Alendronato dissódico, estudos clínicos tipo antes e depois O tratamento com alendronato dissódico foi estudado por cinco grupos distintos. Os autores reportam tempos de tratamento com alendronato que variaram entre 10 meses e cinco anos. A dose utilizada variou entre 5-10 mg/dia ou o equivalente semanal (35-70 mg). Os estudos utilizaram diferentes 54 critérios para determinação da dose. Vyscocyl e colaboradores (2005) empregaram 5mg/dia para os menores de 10 anos e 10 mg/dia para os maiores de 10 anos. Cho e colaboradores (2005) assim como Seikaly e colaboradores (2005) definiram as doses baseados no peso de cada indivíduo, sendo o ponto de corte 35 e 30 quilos, respectivamente. Maassalu e colaboradores (2003) afirmam que todos os pacientes tratados (n=15) apresentaram melhora, no entanto não fornece outros dados. Akcay e colaboradores (2008) e Cho com seus colaboradores (2005) apresentam somente dados sobre o escore Z e assim como Vyskocil e colaboradores (2005) observaram diferenças estatisticamente significativas antes e após o tratamento. O valor da densidade mineral óssea em coluna vertebral foi apresentado também por esses últimos autores, no artigo acima referido, como por Shah e Johari (2007). Ambos os estudos reportam melhoras secundárias ao tratamento. No entanto, os valores do escore Z no grupo de pacientes relatado por Shah e Johari (2007) não se alteraram. Além disso, o grupo tratado por eles apresenta inconsistências quanto aos dados reportados no que se refere ao número de pacientes. Neste estudo, embora sejam relatados dados referentes a 11 indivíduos, alguns valores de densidade mineral óssea de coluna lombar e escore Z da densidade mineral óssea não estavam disponíveis. Entretanto, em nenhum dos dois trabalhos foi apresentada informação sobre a dimensão do incremento da densidade mineral óssea. 55 6.4.3. Alendronato disódico, estudos com grupo controle Dois estudos apresentam dados referentes ao uso de alendronato, sendo usados grupos controle em seus desenhos. Ambos utilizaram dose semelhante, de 10mg/dia para indivíduos que pesavam mais de 30kg e de 5mg/dia para os que pesavam menos de 30kg Chevrel e colaboradores (2006) descreveram o uso do alendronato em adultos com osteogênese imperfeita, sendo a maioria da amostra classificada como tipo I (62/64 pacientes). Os autores reportam que, no grupo tratado, observou-se aumento da densidade mineral óssea 9,4% maior que no grupo que usou placebo após três anos de acompanhamento e que esta diferença não ocorreu ao acaso. No entanto, não forneceram dados sobre escore T após o tratamento. Já o estudo de Seikaly e colaboradores (2005) incluiu crianças com idades entre três e 15 anos. Tratava-se de um estudo randomizado, com utilização de placebo onde os grupos foram tratados ou não por 12 meses, com posterior inversão da intervenção pelos 12 meses restantes. Os autores relatam que não houve interação secundária à ordem de tratamento e apresentam dados referentes somente ao escore Z. No grupo tratado com alendronato foi observada melhora no escore Z quando comparado ao grupo não tratado. 6.4.4 – Pamidronato dissódico, estudos com grupo controle Alguns grupos investigaram o efeito do uso do pamidronato dissódico, utilizando desenhos de estudo que incluíam um grupo controle. Foram comparados o uso de pamidronato e nenhuma medicação em dois estudos: um 56 comparou a resposta à droga em diferentes tipos de osteogênese imperfeita e outros três compararam o uso de diferentes doses de pamidronato. Letocha e colaboradores (2003), tal como Rauch e colaboradores (2003b), usaram como grupo controle indivíduos com osteogênese imperfeita sem tratamento. O primeiro utilizou a dose de 120 mg/m²/ano, acompanhando os pacientes durante dois anos e, o segundo utilizou 9mg/kg/ano, com tempo de seguimento de quatro anos. Letocha e colaboradores (2003) não apresentam os dados brutos, no entanto, afirmam que o escore Z aumentou de forma significativa entre os tratados. Rauch e colaboradores (2003b) observaram aumento dos valores de densidade mineral óssea de coluna lombar, que não ocorreram ao acaso e o escore Z aumentou em média 2,6 desvios-padrão nos quatro anos. Marini com seus colaboradores (2008) e Senthilnathan e colaboradores (2008) compararam doses diferentes de pamidronato (6mg/kg/ano e 12 mg/kg/ano), ambos com tempo de seguimento de um ano. Os primeiros referem que foram observados benefícios no grupo que utilizou a dose maior e os segundos relatam não ter havido diferenças significativas entre os grupos, no entanto, quando comparados os dados ao final do estudo com os dados inicias, o grupo tratado com a dose maior apresentou uma diferença significativa, enquanto que para o grupo com a dose menor parece não ter havido diferença. Land e colaboradores (2007), assim como Zeitlin e colaboradores (2006), apresentam o uso do pamidronato em diferentes tipos de osteogênese imperfeita. A dose utilizada foi de 9mg/kg/ano e os indivíduos foram acompanhados durante três anos. A comparação se deu entre indivíduos com 57 osteogênese imperfeita tipo V e o controle era constituído por tipos I, III e IV. Os resultados sugerem que indivíduos do tipo V também se beneficiam do uso do pamidronato dissódico. Sillence e colaboradores (2005) optaram pela comparação entre indivíduos pré e pós puberais, utilizando a dose de 30 mg/m² mensal, durante dois anos. Embora não tenham apresentado os dados brutos, os autores afirmam que melhor resposta ao tratamento foi observada no grupo prépuberal. 6.4.5. Pamidronato dissódico x alendronato dissódico DiMeglio e Peacock (2006) compararam o uso de pamidronato (9mg/kg/ano) e alendronato (1mg/kg/dia) durante 24 meses. Foram tratadas 18 crianças, a maioria com osteogênese imperfeita tipo I (12/18) e as idades variaram entre três e 13,7 anos. Os autores mostram que em ambos os grupos a resposta ao tratamento foi positiva e sugerem que não houve diferença de resposta ao tratamento entre os grupos. 6.4.6. Zolendronato Dois estudos liderados por Glorieux (2008a; 2008b) abordaram o uso de zolendronato em indivíduos com osteogênese imperfeita. Em ambos o tempo de tratamento foi de um ano e se tratam de estudos relacionados, uma vez que um é extensão do outro. No primeiro foi utilizada dose de 0,025 mg/kg de zolendronato para menores de três anos e 0,05 mg/kg para os maiores de três anos, a cada três meses. A dose de pamidronato empregada no estudo que comparou ambas as medicações foi de 9mg/kg/ano. Ainda que não sejam 58 fornecidos os dados brutos, os autores mostram que o uso do zolendronato promoveu aumentos mais significativos na densidade mineral óssea – aumento de 42,7% no grupo com zolendronato e 34,7% no grupo com pamidronato, sendo esta diferença não atribuída ao acaso. No segundo estudo os pacientes que usaram pamidronato foram transferidos para o zolendronato e acompanhados por mais um ano e a dose de zolendronato foi adaptada para 0,05 mg/kg a cada seis ou 12 meses. Embora em ambos os grupos a resposta tenha sido boa, os pacientes que inicialmente utilizaram zolendronato se beneficiaram mais. 6.4.7. Outros estudos Shapiro e colaboradores (2005) reportam dados de indivíduos tratados com pamidronato, alendronato, residronato e não tratados. No entanto, não são feitas comparações entre os grupos e os autores afirmam terem observado diferenças estatisticamente significativas somente nos indivíduos com osteogênese imperfeita tipo I tratados com alendronato. Philipi e colaboradores (2008), em revisão sistemática, incluíram oito estudos que utilizaram pamidronato, alendronato, olpandronato e neridronato. Pelas diferenças de população incluída nos estudos primários, pelos vários modos de reportar os dados e pelo uso de drogas diversas não foi possível sintetizar os dados. Todavia os autores concluem que os estudos fornecem evidências a favor dos bifosfonatos, mesmo que as populações estudadas tenham sido pequenas, permanecendo questões quanto à tradução clínica dos marcadores utilizados, ou seja, se a melhora da densidade mineral óssea e a desaceleração do metabolismo mineral ósseo, de fato, representam diminuição 59 do número de fraturas, da dor e das deformidades tão incapacitantes na osteogênese imperfeita. 6.5. Síntese dos dados de acordo com o metabolismo ósseo. 6.5.1. Pamidronato dissódico, estudos clínicos do tipo antes e depois Vallo e colaboradores (2006), Cabral de Meneses Filho e colaboradores (2007) e também Göksen e colaboradores (2006) apresentam somente dados referentes à fosfatase alcalina. Todos mostram que há redução na média de fosfatase alcalina com o tratamento. Contudo, a diferença observada por Göksen e colaboradores (2006) não foi estatisticamente significativa. Aström e colaboradores (2008), Rauch (2008a), Poyrazoglu e colaboradores (2008), tal como Forin e colaboradores (2005), observaram redução dos marcadores do metabolismo ósseo, todavia não forneceram mais detalhes. Choi e colaboradores (2007) também não apresentaram os dados e afirmam não terem ocorrido diferenças, em sua amostra, no que se refere ao metabolismo ósseo. Para Andiran e colaboradores (2008) as diferenças foram significativas somente na dosagem de fosfatase alcalina e fosfatase alcalina óssea, sendo que a média dos valores de osteocalcina e propeptideo do colágeno tipo I não se modificaram. Zacharin e Bateman (2002) e posteriormente o mesmo Zacharin com Kanumakala (2004) apresentaram dados referentes à fosfatase alcalina, à piridinolina e à deoxipiridinolina demonstrando decréscimo significativo da reabsorção óssea induzido pelo pamidronato. Alharbi e colaboradores (2008) também trabalharam com deoxipiridinolina e observaram decréscimo deste 60 marcador, no entanto, relatam que os valores de osteocalcina não se alteraram com o tratamento. Arikoski e colaboradores (2004) notaram queda de quase 60% nos valores do N-telopeptídeo do colágeno durante seu estudo. Além disso, também registraram redução da fosfatase alcalina (21,3%), diferenças atribuídas ao tratamento. Já Glorieux e colaboradores (1998) apresentam as modificações ocorridas por ano de tratamento e relatam que a fosfatase alcalina sofreu queda média de 13% por cada ano de tratamento e o Ntelopeptídeo do colágeno de 26% em cada ano de tratamento. Todas as alterações diretamente relacionadas ao uso do pamidronato. Aström e Söderhäll (2002) utilizaram como marcadores do metabolismo ósseo a fosfatase alcalina, osteocalcina e propeptídeo C do colágeno tipo 1, sendo que o pamidronato contribuiu para a redução destes marcadores. Rauch e colaboradores (2003a) reportam queda de N-telopeptídeo de colágeno de valores 132% acima da faixa de referência para 49% acima do valor normal para sexo e idade. A fosfatase alacalina também diminuiu, durante o período do estudo, e a fosfatase ácida tartare-resistente variou ao longo do tempo. Contudo, não forneceram dados estatísticos. 6.5.2. Alendronato dissódico, estudos clínicos tipo antes e depois Vyskocil e colaboradores (2005), Akcay e colaboradores (2008), Cho e colaboradores (2005) e também Shah e Johari (2007) reportaram dados sobre o comportamento do metabolismo ósseo com o uso de alendronato. A única alteração significativa observada por Cho e colaboradores (2005) referiu-se ao N-telopeptídeo do colágeno que caiu 47% após o tratamento. Já, Shah e Johari 61 (2007) descrevem apenas dados referente à fosfatase alcalina e não observaram diferenças significativas. Vyskocil e colaboradores (2005) analisaram osteocalcina, deoxipiridinolina e propeptideo C do colágeno tipo 1 e observaram que houve redução destes marcadores com o tratamento. Akcay e colaboradores (2008), por sua vez, não notaram diferenças no que se refere às taxas de osteocalcina e fosfatase alcalina, tendo sido observado somente mudanças significativas com a deoxipiridinolina. 6.5.3. Alendronato disódico, estudos com grupo controle Seikaly e colaboradores (2005) relatam que as modificações ocorridas com osteocalcina, fosfatase alcalina e N-telopeptídeo do colágeno tipo 1 não foram diferentes entre os grupos, ainda que este último tenha reduzido 56% após o tratamento. Chevrel e colaboradores (2006) observaram que o C-telopeptídeo do colágeno tipo 1 caiu, em média, 59,6%; o N-propeptideo do colágeno tipo 1 caiu 52,4% e a osteocalcina caiu 38% no grupo tratado com alendronato, enquanto que no grupo placebo houve aumentos destes marcadores na magnitude de 52,6%; 14,5%; e 21,9% respectivamente. As diferenças entre os grupos puderam ser atribuídas ao alendronato. 62 6.5.4. Pamidronato dissódico x alendronato dissódico DiMeglio e Peacock (2006) afirmam que ambas as medicações foram eficazes na redução dos marcadores do metabolismo ósseo, com a exceção da fosfatase alcalina óssea que pareceu não se modificar. Os outros marcadores utilizados foram N-telopeptídeo do colágeno e fosfatase alcalina. 6.5.5 – Outros estudos Shapiro e colaboradores (2005) fornecem escassos dados a respeito do metabolismo ósseo afirmando apenas que os bifosfonatos (alendronato, pamidronato e risendronato) foram capazes de reduzir os valores de Ntelopeptídeo pela metade em pacientes com osteogênese imperfeita tipos I e IV. Zeitlin e colaboradores (2006), que estudaram os efeitos do pamidronato em indivíduos com osteogênese imperfeita tipo V, ressaltaram que a medicação foi capaz de reduzir o metabolismo ósseo também nestes pacientes. A redução do N-telopeptideo do colágeno foi marcante no terceiro dia após a infusão. Todavia, estes valores caíram de forma constante ao longo do tempo. Glorieux e colaboradores (2008a), na comparação entre pamidronato e zolendronato, afirmaram que só a redução dos marcadores do metabolismo ósseo foi mais significativa no grupo tratado com zolendronato. 63 6.6. Síntese dos dados em relação a ocorrência de fraturas 6.6.1 – Pamidronato dissódico, estudos clínicos do tipo antes e depois Quatorze estudos, que utilizaram pamidronato dissódico como intervenção, apresentaram dados sobre fraturas. Vallo e colaboradores (2006), Andiran e colaboradores (2008), Zacharin e Kanumakala (2004), assim como Poyrazoglu e colaboradores (2008), não informam como os dados sobre fraturas foram coletados. Forin e colaboradores (2005), também Zeitlin e colaboradores (2006), basearam-se em registros de prontuários médicos. Göksen e colaboradores (2006) e Barbosa (2006) relatam que, no período antes do início do tratamento, os dados foram baseados na memória dos pacientes ou seus familiares e após o início do tratamento em radiografias. O estudo de Glorieux e colaboradores (1998), o de Choi e colaboradores (2007) e o de Bajpai e colaboradores (2007) contabilizaram fraturas observadas nas radiografias disponíveis. Arikoski e colaboradores (2004) utilizaram somente a memória dos pacientes ou de seus familiares para a contagem de fraturas. Lin e colaboradores (2008), como Alharbi e colaboradores (2008), utilizaram além da memória dos pacientes e seus familiares dados registrados em prontuário médico e radiografias, respectivamente. Vallo e colaboradores (2006), Forin e colaboradores (2005) e Barbosa (2006) apresentam os dados na forma de medianas, onde se observa a redução do número de fraturas durante o período do tratamento. A análise estatística não foi realizada pelo primeiro autor, enquanto que os dois últimos mostram ter havido diferença atribuída ao tratamento. Choi e colaboradores (2007), Andiran e colaboradores (2008), Bajpai e colaboradores (2007), Lin e colaboradores (2008), Alharbi e colaboradores 64 (2008) e, finalmente, Poyrazolgu e colaboradores (2008) relatam que a taxa anual de fraturas diminuiu com o tratamento de forma significativa. A taxa de fraturas variou entre 2,13 a 3,5 por ano antes do tratamento e após o uso de pamidronato caiu para 0,6 a 1,5 por ano nestes estudos. Glorieux e colaboradores (1998), tal qual Zacharin e Bateman (2002), relatam que o número médio de fraturas por ano antes do tratamento reduziuse com a medicação, porém nenhuma análise estatística sobre este dado é apresentada. Göksen e colaboradores (2006) relatam apenas que houve diminuição e Arikoski e colaboradores (2004) só informam o número de fraturas durante o período de tratamento, sem realizar comparações. 6.6.2 – Alendronato dissódico, estudos clínicos tipo antes e depois Shah e Johari (2007) tal como Maasalu e colaboradores (2003) utilizaram dados do prontuário médico para registro das fraturas. O estudo de Vyskocil e colaboradores (2005) foi o único a utilizar radiografias no registro das fraturas e o de Cho e colaboradores (2005) não informa como este dado foi coletado. Todos relatam que o número de fraturas diminuiu com o tratamento, embora Maasalu e colaboradores (2003) não forneçam os dados brutos. Os outros relatam que a taxa de fraturas passou de 0,875 a 3,77 por ano para 0,1 a 1,1 por ano. Estes valores foram considerados estatisticamente significativos por todos os autores aqui referendados. 65 6.6.3. Alendronato disódico, estudos com grupo controle Chevrel e colaboradores (2006) relatam que empregaram radiografias para avaliação das fraturas e que a diferença na taxa de fraturas entre os grupos, um que usou alendronato e o outro que usou placebo, não foi significativa. Seikaly e colaboradores (2005) também utilizam radiografias para avaliação das fraturas ocorridas antes e após o tratamento. Estes autores afirmam que após três meses de uso do alendronato novas fraturas não ocorreram no grupo tratado e que as diferenças observadas podem ser atribuídas ao tratamento. 6.6.4. Outros estudos Glorieux e colaboradores (2008b) apresentam dados a respeito do uso de zolendronato e reportam que o número de fraturas diminui com o tratamento, no entanto os números não são informados. Marini e colaboradores (2008) assim como Senthilnathan e colaboradores (2008) comparam diferentes doses de pamidronato (6mg/kg/ano x 12 mg/kg/ano). Os primeiros relatam não ter observado diferenças na taxa de fraturas entre os dois grupos e, os segundos informam que todos os pacientes do estudo tiveram redução na ocorrência de fraturas vertebrais, com exceção de um deles. Porém, nenhum dos autores fornece maiores informações. 66 7. DISCUSSÃO Na fase inicial de busca dos estudos primários a maior dificuldade encontrada foi a identificação de bases diferentes das comumente utilizadas em pesquisas de literatura científica, tais como o Pubmed, Lilacs e Scopus. Para a realização de uma ampla revisão, a inclusão de estudos não publicados e pouco distribuídos, a chamada literatura cinza, é ponto considerado importante por muitos autores (Higgins e Green, 2006; McAuley et al., 2000). Nesta pesquisa, foram utilizados estudos provenientes da literatura cinza e, para a identificação destas nove referências adicionais foi necessário pesquisar outras 11 bases de dados, além da busca por resumos de congressos em 45 livros de resumos de sete associações de diferentes especialidades. O esforço empregado em tal tarefa foi grande. Contudo, caso a literatura cinza tivesse sido ignorada, estudos com zolendronato não teriam sido incluídos nesta revisão, assim como um dos estudos com população brasileira. O fato de a osteogênese imperfeita ser uma doença cujo manejo necessita uma equipe multidisciplinar pode ser claramente notado pela afiliação por especialidade dos autores dos diversos estudos. Embora a maioria dos estudos sobre intervenção seja conduzida por geneticistas, pediatras, endocrinologistas e ortopedistas, diversos especialistas participam deste manejo e demonstram interesse na pesquisa sobre a doença. Também foi possível observar que o empenho é maior na investigação dos efeitos do pamidronato dissódico e que após 1998, ano da publicação dos principais estudos de referência para tratamento da osteogênese imperfeita com pamidronato dissódico no mundo (Aström e Söderhäll, 1998; Glorieux et al., 67 1998), o interesse na análise dos efeitos desta medicação vem crescendo a cada ano. E, em parte, com base no estudo de Glorieux e colaboradores (1998), foram definidas indicações e doses para tratamento de indivíduos com osteogênese imperfeita no Brasil. A portaria número 2305/GM, de 2001, instituiu, no âmbito do Sistema Único de Saúde, o tratamento da osteogênese imperfeita com pamidronato dissódico, utilizando dose anual semelhante à apresentada no referido estudo. Ao longo dos anos, diversos Centros de Referência em Osteogênese Imperfeita foram criados e atualmente existem 14 CROIs em funcionamento em todo o país (Santos, 2009). Somente no CROI do Instituto Fernandes Figueira são acompanhados mais de 160 pacientes (Santos, 2009), o que é um número considerável, visto que o maior centro de tratamento da osteogênese imperfeita no mundo congregava pouco mais de 300 pacientes em 2008 (Rauch, 2008b). Considerando que o tratamento da osteogênese imperfeita seja uma política de saúde pública e que existam centros voltados para o acompanhamento e tratamento da condição no país, com número expressivo de pacientes monitorados, chama-nos atenção o pequeno número de estudos nacionais identificados – foram somente 10 estudos brasileiros e o número de pesquisas sobre tratamento com bifosfonatos foi ainda menor, sendo contabilizadas apenas três (Barbosa, 2006; Barbosa et al., 2007; Cabral de Meneses Filho, 2007). Embora, não seja do escopo deste estudo esta é uma questão que merece atenção. 68 A pesquisa médica, sobretudo a pesquisa clínica, não pode ser separada da prática médica. Zago afirma que “a pesquisa tem por objetivo criar novos conhecimentos ou reorganizar o conhecimento já existente pela análise crítica” (2004:365) e ainda sugere que os temas de pesquisa devem estar pautados na importância de “adquirir nossa própria experiência: o Brasil precisa obter seus próprios dados, formular políticas próprias e resolver problemas específicos do país” (2004:365). Apesar deste autor se referir à pesquisa clínica de forma ampla – abordando temas que devem ser primordiais para o país como a redução da mortalidade por doenças cardiovasculares, por causas externas e câncer e a mudança do perfil demográfico da população que vem envelhecendo – também chama a atenção para outras causas de mortalidade infantil diferentes das causas neonatais e infecciosas. Neste grupo encontramse os defeitos congênitos e doenças genéticas. Sendo a osteogênese imperfeita uma doença rara, a importância de conhecer os dados epidemiológicos e clínicos aumenta, uma vez que isto permite melhor abordagem da doença no que se refere ao diagnóstico, tratamento e até mesmo suas conseqüências sociais (Eurordis, 2005). Salzano (2002) ainda chama atenção para o fato de diversas doenças genéticas terem padrões de mutações e correlações genótipo/fenótipo no Brasil que diferem do restante do mundo. O programa de tratamento da osteogênese imperfeita no país, iniciou-se no CROI do Rio de Janeiro em 2002 (Barbosa, 2006) e, segundo o Ministério da Saúde: 69 “(...) a administração intravenosa cíclica de pamidronato em crianças portadoras de OI leva aos seguintes resultados: 1. Aumento significativo da massa óssea; 2. Redução da dor crônica; 3. Redução global do nível de incapacidade física, e 4. Redução da atividade da doença controlada bioquimicamente e histomorfometricamente” (Portaria no 2305, 2001, s.p.). De fato, as evidências favorecendo o uso do pamidronato dissódico, neste grupo de indivíduos, parecem sólidas. Esta medicação tem sido usada em todo o mundo há mais de dez anos e os estudos reportam frequentemente resultados favoráveis. Glorieux e colaboradores (1998), Zacharin e Bateman (2002), Forin e colaboradores (2005), Zacharin e Kanumakala (2004), Poyrazoglu e colaboradores (2008) e, também, Alharbi e colaboradores (2008) reportam aumento da densidade mineral óssea, desaceleração do processo de modelação e remodelação óssea e observam que estes resultados foram traduzidos clinicamente em menor número de fraturas. Todavia, cabem ressalvas ao trabalho de Poyrazoglu e colaboradores (2008), uma vez que os dados sobre densidade mineral óssea foram obtidos por aparelhos que empregam tecnologias diferentes. Embora, os autores tenham transformado os valores em escore Z e as medidas obtidas, com o equipamento Lunar, tenham sido convertidas para valores do Hologic, usando equações previamente descritas (Poyrazoglu et al., 2008), o modo de captação de cada um deles é diferente. 70 Andiran e colaboradores (2008) apresentam resultados semelhantes, contudo os dados sobre metabolismo ósseo não foram estatisticamente significativos, o que talvez possa ser explicado pelo pequeno número de indivíduos dos quais se extraiu esta informação. Aliás, este é um problema em boa parte dos estudos, onde o número inicial de indivíduos na amostra não se mantém constante durante todo o estudo. Também é interessante destacar que neste grupo, Forin e colaboradores (2005), assim como Lin e colaboradores (2008) e Poyrazoglu e colaboradores (2008) definem bem os critérios para início do tratamento com pamidronato, sendo este indicado nos casos mais graves – indivíduos com três ou mais fraturas por ano nos últimos dois anos; deformidade de ossos longos e fratura de compressão vertebral, ou por dor crônica. Ademais os outros autores que informaram os critérios utilizados para início do tratamento também se apoiaram nas manifestações clínicas. As exceções a esta regra foram Sillence e colaboradores (2005) e Chevrel e colaboradores (2006) que utilizaram critérios de densitometria óssea para início da terapia. Além disso, dos quatro artigos que citam como critério para início de medicação a dor óssea, nenhum faz referência a como este critério é empregado. Porém, dois deles – o de Aström e Söderhäll (2002) tal qual o de Löwing e colaboradores (2007) reportam como avaliaram este sintoma e os efeitos da medicação sobre ele. Ambos os trabalhos fizeram uso de “diários da dor”, contabilizando o número de dias em um mês que o indivíduo referia dor óssea. De modo geral os especialistas, no tratamento desta condição, concordam que estas indicações são adequadas e o tratamento de indivíduos com quadros mais brandos deva ser evitado (Rauch e Glorieux, 2005). Além 71 disso, pela dificuldade de interpretação da densitometria óssea em crianças e adolescentes este não deveria ser um critério utilizado nesta faixa etária (Binkovitz et al., 2007). Em adultos, a interpretação da densitometria óssea é mais simples e curvas de risco para fraturas permitem definir osteopenia e osteoporose. No entanto, devemos lembrar que o raciocínio empregado na osteoporose primária pode não ser adequado para a osteogênese imperfeita. Na osteoporose primária, um dos fatores determinantes para a diminuição da massa óssea é o aumento da reabsorção, ou seja, aumento da função dos osteoclastos, local de ação dos bifosfonatos (Raisz, 2008). Por outro lado, a osteogênese imperfeita é uma doença do osteoblasto, com redução da produção de osso. Por isso, a indicação do uso de bifosfonatos, baseado nos valores de densitometria óssea definidores somente de osteopenia ou osteoporose, pode não ser apropriada para este grupo. A Portaria no 2305 de 2001 do Ministério da Saúde também recomenda que o tratamento seja iniciado com base em critérios clínicos. No entanto, contempla apenas indivíduos classificados como tipos I, III e IV. Possivelmente, tais indicações precisam ser revistas uma vez que as evidências fornecidas por Zeitlin e colaboradores (2006), como aquelas de Land e colaboradores (2007), sugerem que não só os pacientes com as formas clássicas de osteogênese imperfeita se beneficiam do tratamento. No que se refere à idade, o texto da Portaria é ambíguo. Embora, tome como critério de inclusão idade até 21 anos, foram criados códigos para o pagamento do tratamento em adultos. Em que pese as pesquisas sobre bifosfonatos na osteogênese imperfeita incluírem, em sua maioria, crianças e adolescentes, os adultos necessitam ter esta terapia à disposição, uma vez que fraturas com deformidades secundárias e fraturas de 72 compressão vertebral podem ocorrer ao longo de toda a vida de um indivíduo com osteogênese imperfeita. Outra questão que merece atenção é a dose de pamidronato dissódico utilizada. A maioria dos artigos consultados refere o uso de 9mg/kg a cada ano, em esquemas que pouco ou nada variam. A Portaria n o 2305, do Ministério da Saúde brasileiro, recomenda um esquema terapêutico cuja dose anual é esta. Cabe ressaltar que dois estudos compararam doses de pamidronato (Marini et al., 2008; Senthilnathan et al., 2008). Ambos confrontaram o uso de 6 mg/kg por ano e 12mg/kg por ano e os dados sugerem melhor resposta no grupo que utilizou 12mg/kg/ano. Na prática, e dentro da realidade brasileira, como mostra o estudo de Barbosa (2006), nem sempre é possível manter a dose anual recomendada pelo Ministério da Saúde e pela literatura científica. Todavia, esforços devem ser direcionados para que esta meta seja alcançada entre os pacientes tratados com pamidronato, visto que os benefícios parecem ser maiores com doses de 9mg/kg/ano ou acima. Outras medicações do grupo dos bifosfonatos também têm sido utilizadas em pacientes com osteogênese imperfeita. Recentemente, o zolendronato dissódico foi testado neste grupo com resultados que parecem favoráveis. No entanto, pela escassez de dados em ambos os estudos uma avaliação adequada não é possível. Vale ressaltar que nenhum estudo de grande porte foi oficialmente ainda publicado e, que esta droga não foi aprovada pelo Food and Drug Administration para uso na osteogênese imperfeita (FDA, 2009) até o presente momento. A terceira droga de interesse neste estudo foi o alendronato dissódico. Embora, não tenha sido incluída no programa de tratamento da osteogênese 73 imperfeita do Ministério da Saúde, esta medicação vem sendo utilizada em diversos CROIs brasileiros, por algumas dezenas de pacientes (Santos, 2009). Os estudos com alendronato são bastante heterogêneos no que se refere ao tempo de uso da medicação, tendo variado entre 10 meses e cinco anos. Cinco autores conduziram estudos sem grupos controle com amostras que variaram entre 11 e 30 pacientes. Destes, quatro apresentaram os valores do escore Z e em três estes valores foram significativos. Vale ressaltar que assim como Poyrazoglu e colaboradores (2008), Akcay e colaboradores (2008) também utilizaram aparelhos diferentes para medição de densidade mineral óssea e sem fazer conversão das medidas entre os aparelhos forneceram dados sobre o escore Z. Entre os três estudos restantes (Vyskocyl et al., 2005; Cho et al., 2005; Shah e Johari, 2007) somente em dois os resultados podem ser atribuídos ao tratamento. Cho e colaboradores (2005) e Vyskocyl e colaboradores (2005) utilizaram doses semelhantes de alendronato para o tratamento de formas leves, em sua maioria pacientes classificados como tipo I ou IV. Ambos os artigos relatam diminuição significativa do número de fraturas com o tratamento. Se Vyskocyl e colaboradores (2005) também observaram modificações do metabolismo ósseo, para Cho e colaboradores (2005) estas alterações ocorreram apenas com o N-telopeptídeo do colágeno tipo I. 74 Chevrel e colaboradores (2006) estudaram a resposta ao alendronato em pacientes somente com formas leves de osteogênese imperfeita, com critérios de inclusão semelhantes ao da osteoporose primária, sendo que as alterações densitométricas observadas não se traduziram em melhora clínica, o que pode ser entendido como a diminuição da ocorrência de fraturas. Os estudos que se centram no alendronato dissódico fornecem evidências que sugerem que pacientes, com formas leves de osteogênese imperfeita, se beneficiam com o uso do medicamento. Deve-se, todavia, ressaltar que a maioria dos pacientes estudados nestes trabalhos tem tipo I de osteogênese imperfeita. Cabem ainda algumas considerações adicionais: o alendronato dissódico, assim como o pamidronato dissódico e o zolendronato, não é aprovado para uso na osteogênese imperfeita pela agência americana Food and Drug Administration8. Esta decisão foi fundamentada em um estudo randomizado, duplo cego, que incluiu 139 pacientes e comparou o uso do alendronato a um placebo. No entanto, não estão disponíveis informações sobre a gravidade das manifestações clínicas dos envolvidos no estudo. Embora exista o relato de melhora da densidade mineral óssea, a não aprovação do uso do alendronato em crianças parece ter sido baseada na ausência de resposta clínica (redução do número de fraturas) e na demora da consolidação de fraturas entre os tratados (FDA, 2005). 8 Para a aprovação de uma droga nova ou para a admissão de um novo uso da medicação, a agência americana Food and Drug Administration exige que sejam realizados estudos clínicos controlados e randomizados (Angell, 2005). 75 Ainda, é interessante observar que paralelamente a esta recusa do FDA foi publicado um estudo que investigou a farmacocinética do alendronato em crianças com osteogênese imperfeita. Os autores observaram que a média de biodisponibilidade do alendronato é menor que 1% em crianças e que a faixa de variação entre indivíduos é muito ampla, o que pode ter impacto na resposta terapêutica individual (Ward et al., 2005). No caso do pamidronato dissódico estudos clínicos randomizados e controlados nunca foram realizados. Apesar da ausência de reconhecimento dos benefícios destas medicações na osteogênese imperfeita e da não permissão do uso em crianças, por agências reguladoras ao redor do mundo9, essas drogas têm sido amplamente utilizadas por indivíduos com osteogênese imperfeita, em todas as faixas etárias. 8. CONCLUSÕES A osteogênese imperfeita é uma doença que necessita abordagem multidisciplinar (clínico-cirurgica e reabilitação fisioterápica) para seu adequado tratamento. Neste estudo abordamos somente as questões relacionadas à terapia medicamentosa. As evidências aqui apresentadas sugerem que o uso dos bifosfonatos, na osteogênese imperfeita, está associado a uma boa resposta clínica. O pamidronato dissódico associa-se à melhora da densidade mineral óssea, diminuição do turnover ósseo e também à tradução clínica destes achados laboratorias – diminuição do número de fraturas. De longe, a experiência mundial com esta medicação é a mais rica, o que permite que 9 No Brasil, a Agência Nacional de Vigilância Sanitária regulamenta apenas o uso de bifosfonatos em adultos, sem mencionar dentre as indicações para uso da medicação a osteogênese imperfeita (Novartis, 2007). 76 sejam feitas recomendações a respeito do seu uso (as recomendações podem ser encontradas a partir da página 79). No que tange ao alendronato, os estudos realizados até o momento apresentam muitas divergências, o que dificulta a elaboração de sugestões para seu uso. Em teoria, o alendronato tem maior poder de inibição dos osteoclastos do que o pamidronato, pois em sua molécula existe um grupamento de carbono adicional (Fleisch, 1998). No entanto, a biodisponibilidade do alendronato é baixa por este ser um composto administrado por via oral, e boa parte da dose administrada passa pelo trato gastrointestinal sem ser absorvida, já que o alendronato forma complexos insolúveis com cátions multivalentes (Ward et al, 2005). No Brasil, esta droga tem sido utilizada por diversos CROIs, uma vez que a administração por via oral torna-se um atrativo. Todavia, deve-se ter cautela com o seu uso, pois os estudos com alendronato parecem ter sido realizados em pacientes com formas mais leves da doença (tipo I) e nem sempre os resultados laboratoriais foram traduzidos em benefícios clínicos. Os estudos primários apresentam diversas limitações que vão desde o tamanho das amostras – lembrando que a osteogênese imperfeita é uma doença rara, assim sendo a seleção de grande número de pacientes em um único centro de tratamento é bastante difícil – às inconsistências relacionadas aos desfechos, visto que nem todos reportam os mesmo desfechos e, mais ainda, não utilizam técnicas semelhantes para medi-los. Além disso, em muitos estudos, as características basais da amostra, no que se refere à gravidade da doença, são abordadas como unívocas. Há de se considerar que indivíduos que apresentam quadros mais brandos, o que no nível molecular poderia 77 corresponder a mutações que diminuem a quantidade de colágeno produzida, certamente, respondem de modo diferente à medicação do que aqueles cuja molécula de colágeno tem sua estrutura alterada. Talvez estes grupos precisem ser estudados de forma separada para que as recomendações sobre o tratamento se tornem mais específicas. As restrições dos estudos primários tornaram-se também obstáculos para esta pesquisa, no que tange à síntese apurada dos dados e à elaboração de recomendações claras para todas as drogas. Ademais, o tratamento da osteogênese imperfeita não pode ser focado no uso de medicação, sendo de extrema importância o emprego de outras modalidades terapêuticas como a reabilitação fisioterápica e a cirurgia. Portanto, o agrupamento de indivíduos com osteogênese imperfeita, em centros de referência, deverá permitir não só uma melhor reunião de dados epidemiológicos, clínicos e de reposta à terapia, como também facilitará a integração dos diferentes profissionais de saúde especializados nesta condição. Deste modo, ressalva-se a necessidade do incentivo e da consolidação dos CROIs ao longo do território brasileiro. A Portaria 2305/2001 está prestes a completar 10 anos de existência. Neste período, novos CROIs foram criados e o tratamento desta condição foi sendo adaptado à realidade de cada local, seja pela conquista de experiência clínica com o atendimento sistemático à esta população ou por contratempos encontrados ao longo da trajetória. De fato, a maioria dos CROIs brasileiros ainda enfrenta dificuldades para implementar integralmente as recomendações do Ministério da Saúde, particularmente no que se refere à regularidade de atendimento ortopédico e realização de exames complementares (Santos, 2009). Este parece um momento propício, tanto para rever as inconsistências 78 existentes no programa brasileiro de tratamento da osteogênese imperfeita, quanto para a transposição das falhas que ainda existem no sistema. Assim, estaremos caminhando não só em direção da consolidação dos CROIs no país, mas também na implementação de bases a futuras pesquisas capazes de ampliar o conhecimento clínico sobre a doença em seus diversos tipos. Pamidronato dissódico – recomendações para seu uso: O uso de pamidronato dissódico na osteogênese imperfeita tem se mostrado benéfico não só no que se refere ao aumento da densidade mineral óssea e melhora dos marcadores bioquímicos do metabolismo ósseo, mas também na tradução clínica destes achados laboratoriais com a redução do número de fraturas e redução de dor óssea. O uso desta medicação parece ser benéfico em todos os tipos de osteogênese imperfeita. Convenciona-se que critérios clínicos de gravidade para início do tratamento são mais apropriados. Tais critérios incluem deformidade em ossos longos; fratura de compressão vertebral e duas a três ou mais fraturas por ano, nos últimos dois anos. Na prática isto se traduzirá no tratamento de todos os indivíduos com osteogênese imperfeita tipo III, e na maioria dos pacientes com tipo IV. Dor óssea crônica e incapacitante pode ser considerada como critério para início de tratamento e, na realidade, estará presente na maioria dos casos onde os critérios supracitados forem empregados. Para recomendação criteriosa da medicação é preciso ter em mente não só suas indicações, como também os efeitos colaterais imediatos e de 79 longo prazo. Deve-se lembrar que o pamidronato dissódico, assim como todas as medicações do grupo dos bifosfonatos, permanece no esqueleto durante anos, de onde são constantemente liberadas. Existe relato de hipocalcemia assintomática no período neonatal e pé torto congênito, em filhos de mulheres tratadas com pamidronato algum tempo antes da gestação (Munns et al., 2004a), servindo de alerta para o fato de que tal medicação pode ter repercussão fetal. Doses cumulativas anuais de 9mg/kg ou acima parecem estar associadas a melhor resposta clínica. Esforços devem ser direcionados para que tal dose seja mantida em todos os pacientes, apesar das dificuldades encontradas pelos CROIs brasileiros. o O esquema para fornecimento desta dose pode ser feito de diversas formas, sendo as mais empregadas aquelas que utilizam 0,5mg/kg/dia em três dias consecutivos, com intervalos de dois meses (oito semanas) entre as aplicações para crianças menores de dois anos e, 1 mg/kg/dia em três dias consecutivos, com intervalos de quatro meses (16 semanas) entre as aplicações para crianças maiores de dois anos. Ainda existe a possibilidade de fracionamento da dose entre dois e três anos de idade, quando seria utilizada a dose de 0,75 mg/kg/dia em três dias consecutivos, com intervalo de 12 semanas entre as aplicações. O acompanhamento da resposta terapêutica deve ser norteado não só pela densitometria óssea, mas também por marcadores de metabolismo ósseo, ocorrência de fraturas e dor crônica. 80 o Sempre que possível as densitometrias devem ser realizadas no mesmo aparelho, ao longo do tempo, para o mesmo indivíduo. Valores de densitometria obtidos em aparelhos que empregam tecnologias diferentes nem sempre podem ser convertidos para comparação. o O uso de valores de referência para densitometria, obtidos a partir de indivíduos brasileiros saudáveis, é o modo mais adequado de comparação, sobretudo no que tange o cálculo dos escores Z e T. o Marcadores bioquímicos do metabolismo ósseo são imprescindíveis ao acompanhamento da resposta terapêutica. Podem servir de base para regular a dose da medicação – aumentando a dose nos pacientes que não respondem a 9mg/kg/ano, e também para o acompanhamento após a interrupção do tratamento. o Fraturas devem ser documentadas, sempre que possível através de radiografias. o O estudo radiográfico de deformidades de ossos longos, sob a perspectiva da biomecânica, é de extrema importância, uma vez que ajuda a compreender pontos de maior fragilidade óssea quando cargas são impostas ao osso. Isso auxilia na indicação de cirurgia ortopédica para correção das deformidades, como também pode orientar de forma mais frutífera o tratamento complementar fisioterápico. o O estudo radiográfico da coluna vertebral é de igual importância, não só para observação de fraturas de compressão vertebral, 81 como também para avaliação de desvios do eixo e acompanhamento do crescimento vertebral com o tratamento com bifosfonato. o Dor óssea crônica e incapacitante deve ser abordada não só com o uso do bifosfonato, mas também com o emprego de analgesia. Diários de dor, tão utilizados em indivíduos com dor crônica por outras causas, podem ser utilizados para monitoramento da terapia. A administração de pamidronato dissódico deve ser feita sempre em ambiente hospitalar por conta dos efeitos colaterais imediatos. o Dentre os efeitos colaterais, os mais comuns são hipocalcemia relacionada à infusão e estado febril agudo. Embora, assintomática na maioria das vezes, a hipocalcemia deve ser monitorada, pois representa, dentre outros, risco para o desenvolvimento de arritmias (Fleisch, 1998). o Outros efeitos colaterais são menos comuns e, em geral, transitórios como a alteração de magnésio e fósforo. No entanto, cabe ressaltar a importância de medir a tensão arterial em crianças e adolescentes, uma vez que este é um procedimento pouco realizado na prática e o uso do pamidronato tem como efeito colateral a hipertensão. Sugere-se que para a realização de cirurgia ortopédica, em indivíduos que usam pamidronato dissódico, o tratamento com tal medicação seja suspenso pelo menos seis meses antes da cirurgia, uma vez que a droga retarda a consolidação da osteotomia (Munns et al., 2004b). 82 O tempo de uso da medicação não foi objeto desse estudo. Existem evidências a favor da utilização prolongada dessas drogas, em especial, nos indivíduos que ainda não completaram o crescimento do esqueleto (Rauch el al., 2006a). Contudo, alguns estudos mostram que após alguns anos de uso do pamidronato, os ganhos ósseos parecem se estabilizar (Rauch et al., 2002; Rauch et al., 2006b), sendo oportuna a discussão sobre como não perder os benefícios auferidos pela terapia medicamentosa. 83 REFERÊNCIAS BIBLIOGRÁFICAS Akcay T, Turan S, Guran T, Bereket A. Alendronate treatment in children with Osteogenesis imperfecta. Indian Pediatr. 2008; 45: 105-109. Alharbi M, Pinto G, Finidori G, Souberbielle JC, Guillou F, Gaubicher S, et al. Pamidronate treatment of children with moderate-to-severe osteogenesis imperfecta: a note of caution. Horm Res. 2008; 71: 38-44. Andiran N, Aliksifoglu A, Gonc N, Ozon A, Kandemir N, Yordam N. Cyclic pamidronate therapy in children with osteogenesis imperfecta: results of treatment and follow-up after discontinuation. J Pediatr Endocrinol Metab. 2008; 21:63-72. Angell M. The creation of a new drug. In: The truth about the drug companies. Nova Iorque: Random House; 2005. p. 21-36. Aronson J. Rare diseases, orphan drugs, and orphan diseases. BMJ. 2005; 333:127. Arikoski P, Silverwood B, Tillmann V, Bishop NJ. Intravenous pamidronate treatment in children with moderate to severe Osteogenesis imperfecta: assessment of indices of dual-energy x-ray absorptiometry and bone metabolic markers during the first year of therapy. Bone. 2004; 34:539-546. Aström E, Söderhäll S. Beneficial effect of bisphosphonate during five years of treatment of severe osteogenesis imperfecta. Acta Pædiatri 1998; 87: 64-68. Aström E, Söderhäll S. Beneficial effect of long-term intravenous bisphosphonate treatment of osteogenesis imperfecta. Arch Dis Child 2002; 86: 356-364. Aström E, Magnusson P, Eksborg S, Söderhäll S. Biochemical markers of bone turnover in children and adolescents with osteogenesis imperfecta. Anais 10 th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Bajpai A, Kabra M, Gupta N, Sharda S, Ghosh M. Intravenous pamidronate therapy in Osteogenesis imperfecta: response to treatment and factors influencing outcome. J Pediatr Orthop. 2007; 27: 225-227. Baljet B. Aspects of the history of Osteogenesis Imperfecta (Vrolik’s Syndrome). Ann Anat 2002; 184:1-7. Barbosa CO. Programa de Tratamento de Portadores de Osteogênese Imperfeita com bifosfonatos no IFF/Fiocruz – CROI/RJ. [Dissertação de Mestrado]. Rio de Janeiro: Pós Graduação em Saúde da Criança e da Mulher, IFF/Fiocruz,2006. 84 Barbosa CO, Santos AC, Villar, MA, Silva AT, Lima MAFD, Magalhães T, et al. Osteogenesis imperfecta treatment with bisphosphonates in Rio de Janeiro – Brazil. Anais da reunião anual do American College of Medical Genetics; 2007 Nashville, Estados Unidos da América. Nashville: American College of Medical Genetics; 2007. Barnes AM, Chang W, Morello R, Cabral WA, Weis M, Eyre DR, et al. Deficiency of Cartilage-Associated Protein in recessive lethal Osteogenesis imperfecta. N Eng J Med. 2006; 355: 2757-2764. Binkovitz LA, Henwood MJ, Sparke P. Pediatric dual-energy X-ray absorptiometry: technique, interpretation, and clinical application. Sem Nucl Med. 2007; 37: 303-313. Braga V, Gatti D, Rossini M, Colapietro F, Battaglia E, Viapiana O, Adami S. Bone Turnover markers in patients with osteogenesis imperfecta. Bone, 2004; 34: 1013-1016. Byers PH. Disorders of collagen biosynthesis and structure. In: Scriver CR, Beaudet AL, Sly WS, Valle D, editors. The Metabolic and Molecular Basis of Inherited Disease. The McGraw-Hill Companies; 2001. v. 4, p.5241-5285. Cabral de Menezes Filho H, Rodrigues JM, Radonsky V, Della Manna T, Kuperman H, Steinmetz L, et al. Decrease of serum alcaline phosphatase after three cycles of pamidronate dissodium in children with severe osteogenesis imperfecta. Horm Res. 2007; 68 (Suppl 5): 207-208. Cabral WA, Chang W, Barnes AM, Weis M, Scott MA, Leikin S et al. Prolyl 3hydroxylase 1 deficiency causes a recessive metabolic bone disorder resembling lethal/severe Osteogenesis imperfecta. Nat Gen. 2007; 39: 359-365. Calvo MS, Eyre DR, Gundberg CM. Molecular basis and clinical application of biological markers of bone turnover. Endoc Rev, 1996, 17: 333-368. Chavassieux P, Seeman E, Delmas PD. Insights into material and structural basis of bone fragility from diseases associated with fractures: how determinants of the biomechanical properties of bone are compromised by disease. Endoc Rev. 2007; 28: 151-164. Chevrel G, Schott Am, Fontanges E, Charrin JE, Lina-Granade G, Dubeof F, et al. Effects of oral alendronate on BMD in adult patients with Osteogenesis imperfecta: a 3-year randomized placebo-controlled trial. J Bone Miner Res. 2006; 21: 300-306. Cho TJ, Choi IH, Chung CY, Yoo WJ, Park MS, Park YK. Efficacy of oral alendronate in children with Osteogenesis imperfecta. J Pediatr Orthop. 2005; 25: 607-612. Choi JH, Shin YL, Yoo HW. Short-term efficacy of monthly pamidronate infusion in patients with Osteogenesis imperfecta. J Korean Med Sci. 2007; 22: 209-212. 85 Cole WG. The molecular pathology of Osteogenesis Imperfecta. Clin Orthop Relat Res 1997; 343: 235-248. Cremers S, Garnero P, Seibel MJ. Biochemical markers of bone metabolism. In: Bilezikian JP, Raisz LG, Martin TJ, editors. Principles of Bone Biology. London: Academic Press, 2008. p. 1857-1881. Davies JH, Evans BAJ, Gregory JW. Bone mass acquisition in health children. Arch Dis Child, 2005, 90:373-378. Devogelaer JP, Malghem J, Maldague B, Nagant de Deuxchaisnes C. Radiological manifestations of bisphosphonate treatment with APD in a child suffering from osteogenesis imperfecta. Skel Radiol 1987; 16: 360-363. Dickersin K, Scherer R, Lefebvre C. Systematic reviews: Identifying relevant studies for systematic reviews. BMJ. 1994; 309: 1286-1291. Diehl LF, Perry DJ. A comparison of randomized concurrent control groups with matched historical control groups: are historical controls valid? J Clin Oncol 1986; 4:1114-1120. DiMeglio LA, Peacock M. Two-year clinical trial of oral alendronate versus intravenous pamidronate in children with Osteogenesis imperfecta. J Bone Miner Res. 2006; 21: 132-140. Engelbert RHH, Pruijs HEH, Beemer FA, Heldres PJM. Osteogenesis imperfecta in childhood: treatment strategies. Arch Phys Med Reahabili 1998; 79: 1590-1594. Engelbert RHH, Beemer FA, van der Graaf Y, Helders PJM. Osteogenesis imperfecta in childhood: impairment and disability – A follow-up study. Arch Phys Med Rehabili 1999; 80:896-903. Engelbert RHH, Uiterwaal CSPM, Gulmans VAM, Pruijs HE, Helders PJM. Osteogenesis imperfecta: profiles of motor development as assessed by a postal questionnaire. Eur J Pediatr 2000; 159: 615-620. Engelbert RHH, Uiterwaal CS, Grever WJ, van der Net JJ, Pruijs HE, Helders PJ. Osteogenesis imperfecta in childhood: impairment and disability. A prospective study with 4-year follow-up. Arch Phys Med Rehabili 2004; 85:772778. EURORDIS. Rare diseases: understanding this Public Health Priority 2005. http://www.eurordis.org (acessado em 27/10/2009). Evidence-based Medicine Workgroup. Evidence-Based Medicine. J.A.M.A. 1992; 268: 2420-2425. 86 Falk MJ, Heeger S, Lynch KA, DeCaro KR, Bohach D, Gibson KS, Warman ML. Intravenous bisphosphonate treatment in children with osteogenesis imperfecta. Pediatrics 2003; 111: 573-578. Fewtrell MS. Bone densitometry in children assessed by dual x ray absorptiometry: uses and pitfalls. Arch Dis Child. 2003; 88: 795 – 798. Fleisch H. Bisphosphonate: mechanisms of action. Endo Rev. 1998; 19:80-100. Fletcher RH, Fletcher SW. Epidemiologia Clínica Elementos Essenciais. Porto Alegre: Artmed 2006. Food and Drug Administration. Fosamax 2005. http://www.fda.org (acessado em 25/11/2009). Food and Drug Administration. Reclast 2005. http://www.fda.org (acessado em 25/11/2009). Forin V, Arabi A, Guigonis V, Filipe G, Bensman A, Roux C. Benefits of pamidronate in children with Osteogenesis imperfecta: an open prospective study. Joint Bone Spine. 2005; 72: 313-318. Glasziou P, Vandenbroucke J, Chalmers I. Assessing the quality of research. BMJ. 2004; 328: 39-41. Glorieux FH, Bishop NJ, Plotkin H, Chabot G, Lanoue G, Travers R. Cyclic administration of pamidronate in children with severe osteogenesis imperfecta. N Engl J Med 1998; 339: 947-952. Glorieux FH, Rauch F, Plotkin H, Ward L, Travers R, Roughley P et al. Type V osteogenesis imperfecta: a new form of brittle bone disease. J Bone Miner Res 2000; 15:1650-1658. Glorieux FH. A disease of the osteoblast. Lancet. 2001; Supp 45: 358. Glorieux FH, Ward LM, Rauch F, Lalic L, Roughley PJ, Travers R. Osteogenesis imperfecta type VI: a form of brittle bone disease with a mineralisation defect. J Bone Miner Res 2002; 17:30-38. Glorieux FH, Bishop N, Bober M, Brain CE, Devogelaer J, Fekete G, et al. Intravenous zolendronic acid (ZOL) compared to IV pamidronate (PAM) in children with severe Osteogenesis imperfecta (OI). Anais 35 th European Symposium on Calcified Tissue; 2008 mai 24-28; Barcelona, Espanha. Barcelona: European Calcified Tissue Society; 2008a. Glorieux FH, Tan M, Mesenbrink P, Bucci-Rechtweg C. Long-term safety and efficacy of i.v. zolendronic acid (ZOL) in children with severe Osteogenesis imperfecta (OI): 1-yr, open-label extension study. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008b. 87 Göksen D, Coker M, Darcan S, Köse T, Kara S. Low-dose intravenous pamidronate treatment in Osteogenesis imperfecta. Turk J Pediatr. 2006; 48: 124-129. Haynes RB, McKibbon KA, Wilczynski NL, Walter SD, Were SR. Optimal search strategies for retrieving scientifically strong studies of treatment from Medline: analytical survey. BMJ 2005; 330: 1174-1184. Higgins JPT, Green S [editors]. Cochrane Handbook for Systematic Reviews of Intervention 4.2.6. In: The Cochrane Library, Issue 4, 2006, Chichester, UK: John Wiley and Sons, Ltd. Jadad AR, Moore A, Carrol D, Jenkinson C, Reynolds JM, Gavaghan DJ et al. Assessing the quality of reports of randomized clinical trials: is blinding necessary? Control Clin Trials. 1996; 17:1-12. Labuda M, Morissette J, Ward LM, Rauch F, Lalic L, Roughley PJ et al. Osteogenesis imperfecta type VII maps to the short arm of chromosome 3. Bone. 2002; 31: 19-25. Land C, Rauch F, Travers R, Glorieux FH. Osteogenesis imperfecta type VI in children and adolescence: effects of cyclical intravenous pamidronate treatment. Bone. 2007; 40: 638-644. Letocha AD, Cintas HL, Paul SM, Gerber NL, Marini JC. Controlled Trial of pamidronate in children with types III and IV OI: lack of effect on motor function and pain. Anais 53rd Annual Meeting American Society of Human Genetics; 2003, nov 4-8; Los Angeles, Estados Unidos da América. Los Angeles: American Society of Human Genetics; 2003. Lin HY, Lin SP, Chuang CK, Chen MR, Chang CY. Intravenous pamidronate therapy in Taiwanese patients with Osteogenesis imperfecta. Pediatr Neonatol. 2008; 49: 161-165. Löwing K, Aström E, Oscarsson KA, Söderhäll S, Elizasson AC. Effect of intravenous pamidronate therapy on everyday activities in children with Osteogenesis imperfecta. Acta Paediatr. 2007; 96:1180-1183. Lund AM, Molgaard C, Müller J, Skovby F. Bone mineral content and collagen defects in Osteogenesis imperfecta. Acta Paediatr. 1999; 88: 1083-1088. Maasalu K, Haviko T, Märtson A. Treatment of children with Osteogenesis imperfecta in Estonia. Acta Paediatr. 2003; 92: 452-455. Marini JC, Obafemi AA, Abukhaled MK, Cintas HL, Troendle JF, Letocha AD, et al. Randomized dose comparison of pamidronate in children with types III and IV Osteogenesis imperfecta: 3 vs 6 month cycles. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. 88 McAuley L, Pham B, Tugwell P, Moher D. Does the inclusion of grey literature influence the estimates of intervention effectiveness reported in meta-analyses? Lancet. 2000; 356:1228-1231. Millington-Ward S, McMahon HP, Farrar GJ. Emerging therapeutic approaches for osteogenesis imperfecta. Trends Mol Med 2005; 11(6): 299-305. Munns CFJ, Rauch F, Ward L, Glorieux FH. Maternal and fetal outcome after long-term pamidronate treatment before conception: a report of two cases. J Bone Miner Res. 2004a; 19:1742-1745. Munns CFJ, Rauch F, Zeitlin L, Fassier F, Glorieux FH. Delayed osteotomy but not fracture healing in pediatric Osteogenesis imperfecta in patients receiving pamidronate. J Bone Miner Res. 2004b; 19:1779-1786. Novartis. Uso do pamidronato dissódico e do alendronato dissódico na osteogênese imperfeita [comunicação pessoal]; 2007. Phillipi CA, Remmington T, Steiner RD. Bisphosphonate therapy for osteogenesis imperfect (Cochrane Review). In: The Cochrane Library, Issue 4, 2008. Oxford: Update Software. Portaria nº 263. Aprova o Protocolo Clínico e Diretrizes Terapêuticas – Fibrose Cística. Diário Oficial da União 2001; 18 jul. Portaria n° 449. Aprova o protocolo clínico e diretrizes terapêuticas – doença de Gaucher. Diário Oficial da União 2002; 9 jul. Portaria no 2305/2001. Aprova o Protocolo de Indicação de Tratamento Clínico da osteogenesis imperfecta com pamidronato dissódico no âmbito do Sistema Único de Saúde – SUS. Brasília: Gabinete do Ministro 2001; 19 dez. Portaria n° 822. Institui no âmbito do Sistema Único de Saúde o Programa Nacional de Triagem Neonatal/PNTN. Brasília: Gabinete do Ministro 2001; 06 jun. Plotkin H. Two questions about Osteogenesis Imperfecta. J Pediatr Orthop 2006; 26 (1): 148-149. Poyrazoglu S, Gunoz H, Darendeliler F, Bas F, Tutunculer F, Eryilmaz SK et al. Successful results of pamidronate treatment in children with osteogenesis imperfecta with emphasis on the interpretation of bone mineral density. J Pediatr Orthop. 2008; 28: 483-487. Rare Disease Task Force. Centres of Reference for rare disease in Europe: State-of-the-art in 2006 and Recommendations of the Rare Disease Task Force. Report; 2006. 89 Raisz LG, Bilezikian JP, Martin TJ. Pathophysiology of osteoporosis. In: Principles of Bone Biology. London: Academic Press; 2008. p. 1635-1647. Rauch F, Travers R, Parfitt AM, Glorieux FH. Static and dynamic bone hystomorphometry in children with Osteogenesis imperfecta. Bone. 2000; 26:581-589. Rauch R, Travers R, Plotkin H, Glorieux FH. The effects of intravenous pamidronate on the bone tissue of children and adolescents with osteogenesis imperfecta. J Clin Invest 2002; 110: 1293-1299. Rauch F, Plotkin H, Travers R, Zeitlin L, Glorieux FH. Osteogenesis imperfecta types I, III and IV: effect of pamidronate therapy on bone and mineral metabolism. J Clin Endocrinol Metab. 2003a; 88: 984-985. Rauch F, Plotkin H, Zeitlin L, Glorieux FH. Bone mass, size, and density in children and adolescents with Osteogenesis imperfecta: effect of intravenous pamidronate therapy. J Bone Miner Res. 2003b; 18: 610-614. Rauch F, Glorieux FH. Osteogenesis imperfecta. Lancet 2004; 363:1377-1385. Rauch F, Glorieux FH. Bisphosphonate treatment in osteogenesis imperfecta: Which drug, for whom, for how long? Annals of Medicine 2005; 37: 295-302. Rauch F, Munns C, Land C, Glorieux FH. Pamidronate in children and adolescents with osteogenesis imperfecta: effect of treatment discontinuation. J Clin Endocrinol Metab 2006a; 91: 1268-1274. Rauch F, Travers R, Glorieux FH. Pamidronate in children with osteogenesis imperfecta: histomorphometric effect of long-term therapy. J Clin Endocrinol Metab 2006b; 91: 511-516. Rauch F. Predictors of the response to pamidronate therapy. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008a. Rauch F. Declaração pessoal ao autor; Montreal; 2008b. Russel RGG, Rogers MJ. Bisphosphonates: From the laboratory to the clinic and back again. Bone 1999; 25 (1): 97-106. Rosenberg A. Ossos, articulações e tumores de partes moles in: Robins Patologia estrutural e funcional. Rio de Janeiro: Guanabara Koogan. 2000. p. 1087-1114. Sackett DL, Haynes RB, Guyatt GH, Tugwell P. Clinical Epidemiology: a basic science for clinical medicine. Boston/Toronto/London: Little, Brown and Company; 1992. 90 Sackett DL. Clinical epidemiology: what, who and whither. J Clinic Epidem 2002; 55: 1161-1166. Salzano FM. Saúde pública no primeiro e terceiro mundos: desafios e perspectivas. Cienc Saud Col. 2002; 7: 7-16. Santos FB. I Encontro Nacional dos Centros de Referência em Osteogênese Imperfecta [Comunicação pessoal]; 2009. Seeman, E. Modeling and remodeling. In: Bilezikian JP, Raisz LG, Martin TJ, editors. Principles of Bone Biology. London: Academic Press, 2008. p. 2-27. Seikaly MG, Kopanati S, Salhab N, Waber P, Patterson D, Browne R, Herring JA. Impact of alendronate on quality of life in children with Osteogenesis imperfecta. J Pediatr Orthop. 2005; 25: 786-791. Senthilnathan S, Walker E, Bishop NJ. Two doses of pamidronate in infants with Osteogenesis imperfecta. Arch Dis Child. 2008; 93: 398-400. Shah I, Johari A. Oral bisphosphonate treatment for Osteogenesis imperfecta – an Indian perspective. Ann Trop Paediatr. 2007; 27: 39-43. Shapiro JR, Hickman C, Brintzenhofeszoc K, Sponseller PD. Results of bisphosphonate treatment in adult Osteogenesis imperfecta. Anais 9 th International Meeting on Osteogenesis Imperfecta; 2005, jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Sillence DO, Senn A, Danks DM. Genetic heterogeneity in osteogenesis imperfecta. J Med Genet 1979; 16, 101-116. Sillence D, Munns C, Briody J, Ault J. Cyclic intravenous pamidronate in Osteogenesis imperfecta type I. Anais 9th International Meeting on Osteogenesis Imperfecta; 2005, jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Vallo A, Rodriguez-Leyva F, Rodriguez Soriano J. Osteogenesis imperfecta: anthropometric, skeletal and mineral metabolic effects of long-term intravenous pamidronate therapy. Acta Paediatr. 2006; 95: 332-339. Viguet-Carrin S, Garnero P, Delmas PD. The role of collagen in bone strength. Osteoporos Int. 2006; 17:319-336. Vyskocil V, Pikner R, Kutílek S. Effet therapeutique de l’alendronate chez les enfants atteints d’ostéogenèses imparfaite. Rev Rhum 2005; 72: 835-843. Ward LM, Rauch F, Travers R, Chabot G, Azouz EM, Lalic L, et al. Osteogenesis imperfecta type VII: an autossomal recessive form of brittle bone disease. Bone 2002; 31: 12-18. 91 Ward LM, Denker AE, Porras A, Shugarts S, Kline W, Travers R, et al. Singledose pharmacokinetics and tolerability of alendronate 35- and 70- milligram tablets in children and adolescents with Osteogenesis imperfecta type I. J Clin Endocrinol Metab. 2005; 90: 4051-4056. Weil UH. Osteogenesis imperfecta: historical background. Clin Orthop Relat Res 1981; 159: 6-10. World Health Organization. Prevention and management of osteoporosis. Geneva; 2003. (WHO – Technical Report Series, 921). Zacharin M, Bateman J. Pamidronate treatment of Osteogenesis imperfecta – lack of correlation between clinical severity, age at onset of treatment, predicted collagen mutation and treatment response. J Pediatr Endocrinol Metab. 2002; 15: 163-174. Zacharin M, Kanumakala S. Pamidronate treatment of less severe forms of Osteogenesis imperfecta in children. J Pediatr Endocrinol Metab. 2004; 17: 1511-1517. Zago MA. A pesquisa clínica no Brasil. Cienc Sau Col. 2004; 9: 363-374. Zeitlin L, Rauch F, Travers R, Munns C, Glorieux FH. The effect of cyclical intravenous pamidronate in children and adolescents with Osteogenesis imperfecta type V. Bone 2006; 38: 13-20. 92 APÊNDICE 1 – CLASSIFICAÇÃO CLÍNICA DA OSTEOGÊNESE IMPERFEITA Tabela 1: resumo das principais manifestações clínicas da osteogênese imperfeita de acordo com a classificação de Sillence. Tipo I Tipo II Tipo III Tipo IV Fragilidade S (++) S (++++) S (+++/++++) S (++/+++) óssea Escleras S S N* N azuladas Fraturas IU/Ao Pré-escolar IU Variável (início) nascimento Deformidade S (+/++) S (++++) S (+++/++++) S (+/+++) em membros Surdez S ? N N Coluna Deformidade Platispondilia Deformidade Deformidade vertebral em 1/5 Ossos N S S S/N wormianos Estatura Baixa Baixa Muito baixa Baixa Dentinogênese N S S S/N imperfeita Letal no primeiro ano Macrocrania, Fragilidade Outros de vida face vascular (neonatal, em triangular geral) Legenda: S = presente; N = ausente; (+) = muito leve; (++) = leve; (+++) = moderado; (++++) = grave; IU = Intra-útero. *em alguns pacientes pode ser acinzentada (Sillence et al, 1979). 93 Tipos descritos posteriormente Tipo V (Glorieux et al, 2000) Fragilidade óssea moderada a grave Tendência à formação de calo após trauma/procedimento cirúrgico Peso e estatura normais ao nascimento Baixa estatura Frouxidão ligamentar Sem dentinogênese imperfeita, escleras claras Limitação do movimento de pronação/supinação do antebraço Tipo VI (Glorieux et al, 2002) Peso e estatura normais ao nascimento Baixa estatura Fraturas frequentes Sem dentinogênese imperfeita Escleras claras Frouxidão ligamentar (50%) Sem ossos wormianos Fraturas de compressão vertebral Defeito de mineralização Tipo VII (Ward et al, 2002) Múltiplas fraturas Deformidade – coxa vara Sem dentinogênese imperfeita, surdez ou frouxidão ligamentar Rizomelia Esclera pouco azulada Bioquímica normal Diminuição do número de trabéculas e osso cortical Tipo VIII (Cabral et al, 2007) Forma grave a letal Múltiplas fraturas ao nascimento 94 Maioria dos casos de origem africana Escleras claras Face arredondada Tórax curto e em barril Metáfises bulbosas e desorganização da matriz óssea 95 APÊNDICE 2 – FICHA DE SELEÇÃO DOS ESTUDOS PRIMÁRIOS Título do estudo: Periódico: Ano: Volume: Páginas: Sim Tipos de estudo Ensaio clínico controlado ou não? Se controlado, grupo controle é constituído por controle histórico? População: somente pacientes com OI? Intervenção Alendronato dissódico? Pamidronato dissódico? Zolendronato dissódico? Desfechos clínicos Densidade mineral óssea Marcadores de turnover ósseo Número de fraturas Idioma: inglês, francês, português ou espanhol? Conclusão Recomenda a inclusão do estudo? Não 96 APÊNDICE 3 – FICHA DE CAPTAÇÃO DE DADOS DOS ESTUDOS PRIMÁRIOS Revisor: Título do estudo: Autores: Periódico: Ano: País de origem: Volume: Páginas: Financiamento: Método Controlado? ( ) Não controlado? ( ) Processo de alocação: Local do estudo: Cegamento na análise? População Tamanho da amostra Idade Critérios de inclusão Critérios de exclusão Tamanho dos grupos Tipo de OI N° Tipo I N° Tipo III N° Tipo IV Sexo Medicação Tratamento: Intervenção Dose Controle: Intervenção Dose Tempo de follow-up: Efeitos colaterais Perdas Desfechos Tratamento N° Total Antes Depois DMO lombar (T) DMO lombar (Z-score) Fosfatase alcalina Fosfatase alcalina óssea NTx CTx Osteocalcina Funcionalidade Antes Controle Depois Estatística 97 Desfechos Tratamento Tipo I Antes Depois DMO lombar (T) DMO lombar (Z-score) Fosfatase alcalina Fosfatase alcalina óssea NTx CTx Osteocalcina Funcionalidade Desfechos Tratamento Tipo III Antes Depois DMO lombar (T) DMO lombar (Z-score) Fosfatase alcalina Fosfatase alcalina óssea NTx CTx Osteocalcina Funcionalidade Desfechos Tratamento Tipo IV Antes Depois DMO lombar (T) DMO lombar (Z-score) Fosfatase alcalina Fosfatase alcalina óssea NTx CTx Osteocalcina Funcionalidade Controle Depois Estatística Antes Controle Depois Estatística Antes Controle Depois Estatística Antes 98 APÊNDICE 4 – ESTUDOS INCLUÍDOS NA REVISÃO Akcay T, Turan S, Guran T, Bereket A. Alendronate treatment in children with Osteogenesis imperfecta. Indian Pediatr. 2008; 45: 105-109. Alharbi M, Pinto G, Finidori G, Souberbielle JC, Guillou F, Gaubicher S, et al. Pamidronate treatment of children with moderate-to-severe osteogenesis imperfecta: a note of caution. Horm Res. 2008; 71: 38-44. Andiran N, Aliksifoglu A, Gonc N, Ozon A, Kandemir N, Yordam N. Cyclic pamidronate therapy in children with osteogenesis imperfecta: results of treatment and follow-up after discontinuation. J Pediatr Endocrinol Metab. 2008; 21:63-72. Arikoski P, Silverwood B, Tillmann V, Bishop NJ. Intravenous pamidronate treatment in children with moderate to severe Osteogenesis imperfecta: assessment of indices of dual-energy x-ray absorptiometry and bone metabolic markers during the first year of therapy. Bone. 2004; 34:539-546. Aström E, Söderhäll S. Beneficial effect of long term intravenous pamidronate treatment of Osteogenesis imperfecta. Arch Dis Child. 2002; 86: 356-364. Aström E, Magnusson P, Eksborg S, Söderhäll S. Biochemical markers of bone turnover in children and adolescents with osteogenesis imperfecta. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Bajpai A, Kabra M, Gupta N, Sharda S, Ghosh M. Intravenous pamidronate therapy in Osteogenesis imperfecta: response to treatment and factors influencing outcome. J Pediatr Orthop. 2007; 27: 225-227. Barbosa CO. Estudo do impacto (efetividade) do tratamento da osteogenesis imperfecta com pamidronato dissódico no centro de referência CROI/IFF/FIOCRUZ [Dissertação de Mestrado]. Rio de Janeiro: PósGraduação em Saúde da Criança e da Mulher, Instituto Fernandes Figueira, Fundação Oswaldo Cruz; 2006. Cabral de Menezes Filho H, Rodrigues JM, Radonsky V, Della Manna T, Kuperman H, Steinmetz L, et al. Decrease of serum alcaline phosphatase after three cycles of pamidronate dissodium in children with severe osteogenesis imperfecta. Horm Res. 2007; 68 (Suppl 5): 207-208. Chevrel G, Schott Am, Fontanges E, Charrin JE, Lina-Granade G, Dubeof F, et al. Effects of oral alendronate on BMD in adult patients with Osteogenesis imperfecta: a 3-year randomized placebo-controlled trial. J Bone Miner Res. 2006; 21: 300-306. 99 Cho TJ, Choi IH, Chung CY, Yoo WJ, Park MS, Park YK. Efficacy of oral alendronate in children with Osteogenesis imperfecta. J Pediatr Orthop. 2005; 25: 607-612. Choi JH, Shin YL, Yoo HW. Short-term efficacy of monthly pamidronate infusion in patients with Osteogenesis imperfecta. J Korean Med Sci. 2007; 22: 209-212. DiMeglio LA, Peacock M. Two-year clinical trial of oral alendronate versus intravenous pamidronate in children with Osteogenesis imperfecta. J Bone Miner Res. 2006; 21: 132-140. Forin V, Arabi A, Guigonis V, Filipe G, Bensman A, Roux C. Benefits of pamidronate in children with Osteogenesis imperfecta: an open prospective study. Joint Bone Spine. 2005; 72: 313-318. Glorieux FH, Bishop NJ, Plotkin H, Chabot G, Lanoue G, Travers R. Cyclic administration of pamidronate in children with severe Osteogenesis imperfecta. N Engl J Med. 1998; 339: 947-952. Glorieux FH, Bishop N, Bober M, Brain CE, Devogelaer J, Fekete G, et al. Intravenous zolendronic acid (ZOL) compared to IV pamidronate (PAM) in children with severe Osteogenesis imperfecta (OI). Anais 35 th European Symposium on Calcified Tissue; 2008 mai 24-28; Barcelona, Espanha. Barcelona: European Calcified Tissue Society; 2008. Glorieux FH, Tan M, Mesenbrink P, Bucci-Rechtweg C. Long-term safety and efficacy of i.v. zolendronic acid (ZOL) in children with severe Osteogenesis imperfecta (OI): 1-yr, open-label extension study. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Göksen D, Coker M, Darcan S, Köse T, Kara S. Low-dose intravenous pamidronate treatment in Osteogenesis imperfecta. Turk J Pediatr. 2006; 48: 124-129. Land C, Rauch F, Travers R, Glorieux FH. Osteogenesis imperfecta type VI in children and adolescence: effects of cyclical intravenous pamidronate treatment. Bone. 2007; 40: 638-644. Letocha AD, Cintas HL, Paul SM, Gerber NL, Marini JC. Controlled Trial of pamidronate in children with types III and IV OI: lack of effect on motor function and pain. Anais 53rd Annual Meeting American Society of Human Genetics; 2003, nov 4-8; Los Angeles, Estados Unidos da América. Los Angeles: American Society of Human Genetics; 2003. Lin HY, Lin SP, Chuang CK, Chen MR, Chang CY. Intravenous pamidronate therapy in Taiwanese patients with Osteogenesis imperfecta. Pediatr Neonatol. 2008; 49: 161-165. Löwing K, Aström E, Oscarsson KA, Söderhäll S, Elizasson AC. Effect of intravenous pamidronate therapy on everyday activities in children with Osteogenesis imperfecta. Acta Paediatr. 2007; 96:1180-1183. 100 Maasalu K, Haviko T, Märtson A. Treatment of children with Osteogenesis imperfecta in Estonia. Acta Paediatr. 2003; 92: 452-455. Marini JC, Obafemi AA, Abukhaled MK, Cintas HL, Troendle JF, Letocha AD, et al. Randomized dose comparison of pamidronate in children with types III and IV Osteogenesis imperfecta: 3 vs 6 month cycles. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Phillipi CA, Remmington T, Steiner RD. Bisphosphonate therapy for Osteogenesis imperfecta. Cochrane Database Sys Rev. 2008; 8:CD005088. Poyrazoglu S, Gunoz H, Darendeliler F, Bas F, Tutunculer F, Eryilmaz SK et al. Successful results of pamidronate treatment in children with osteogenesis imperfecta with emphasis on the interpretation of bone mineral density. J Pediatr Orthop. 2008; 28: 483-487. Rauch F, Plotkin H, Zeitlin L, Glorieux FH. Bone mass, size, and density in children and adolescents with Osteogenesis imperfecta: effect of intravenous pamidronate therapy. J Bone Miner Res. 2003; 18: 610-614. Rauch F, Plotkin H, Travers R, Zeitlin L, Glorieux FH. Osteogenesis imperfecta types I, III and IV: effect of pamidronate therapy on bone and mineral metabolism. J Clin Endocrinol Metab. 2003; 88: 984-985. Rauch F. Predictors of the response to pamidronate therapy. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Seikaly MG, Kopanati S, Salhab N, Waber P, Patterson D, Browne R, Herring JA. Impact of alendronate on quality of life in children with Osteogenesis imperfecta. J Pediatr Orthop. 2005; 25: 786-791. Senthilnathan S, Walker E, Bishop NJ. Two doses of pamidronate in infants with Osteogenesis imperfecta. Arch Dis Child. 2008; 93: 398-400. Shah I, Johari A. Oral bisphosphonate treatment for Osteogenesis imperfecta – an Indian perspective. Ann Trop Paediatr. 2007; 27: 39-43. Shapiro JR, Hickman C, Brintzenhofeszoc K, Sponseller PD. Results of bisphosphonate treatment in adult Osteogenesis imperfecta. Anais 9th International Meeting on Osteogenesis Imperfecta; 2005, jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Sillence D, Munns C, Briody J, Ault J. Cyclic intravenous pamidronate in Osteogenesis imperfecta type I. Anais 9th International Meeting on Osteogenesis Imperfecta; 2005, jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. 101 Vallo A, Rodriguez-Leyva F, Rodriguez Soriano J. Osteogenesis imperfecta: anthropometric, skeletal and mineral metabolic effects of long-term intravenous pamidronate therapy. Acta Paediatr. 2006; 95: 332-339. Vyskocil V, Pikner R, Kutilek S. Effect of alendronate therapy in children with osteogenesis imperfecta. Joint Bone Spine. 2005; 72: 416-423. Zacharin M, Kanumakala S. Pamidronate treatment of less severe forms of Osteogenesis imperfecta in children. J Pediatr Endocrinol Metab. 2004; 17: 1511-1517. Zacharin M, Bateman J. Pamidronate treatment of Osteogenesis imperfecta – lack of correlation between clinical severity, age at onset of treatment, predicted collagen mutation and treatment response. J Pediatr Endocrinol Metab. 2002; 15: 163-174. Zeitlin L, Rauch F, Travers R, Munns C, Glorieux FH. The effect of cyclical intravenous pamidronate in children and adolescents with Osteogenesis imperfecta type V. Bone. 2006; 38: 13-20. 102 APÊNDICE 5 – ESTUDOS PRIMÁRIOS EXCLUÍDOS DA REVISÃO Adami S, Gatti D, Colapietro F, Fracassi E, Braga V, Rossini M, Tatò L. Intravenous neridronate in adults with osteogenesis imperfecta. J Bone Miner Res. 2003; 18:126-30. Intervenção neridronato. Adiyaman P, Ocal G, Berberoglu M, Evliyaoglu O, Aycan Z, Cetinkaya E. The clinical and radiological assessment of cyclic intravenous pamidronate administration in children with Osteogenesis imperfecta. Turk J Pediatr. 2004; 46: 322-328. Allgrove J. Use of bisphosphonates in children and adolescents. J Pediatr Endocrinol Metab. 2002;15 Suppl 3:921-8. Artigo de revisão Allgrove J. Metabolic bone disease. Ped Chil Heal. 2007; 17: 253-259. Artigo de revisão. Amarasena S, Lekamwasam S, Jayawardena P. Cyclical intravenous pamidronate therapy in children with osteogenesis imperfecta. Ceylon Med J. 2005; 50:137-8. Não disponível. Andiran N, Alikasifoglu A, Alanay Y, Yordam N. Cyclic pamidronate treatment in Bruck syndrome: proposal of a new modality of treatment. Pediatr Int. 2008 Dec;50(6):836-8. Antoniazzi F, Adami S, Lauriola S, Donadi L, Gaudino R, Rocchi A, et al. Early bisphosphonate therapy in infants with severe osteogenesis imperfecta. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Intervenção neridronato. Antoniazzi F, Monti E, Franceschi R, Zanon D, Venturi G, Gatti D, et al. Study on the effect of growth hormone in combination with bisphosphonate treatment on boné metabolism in osteogenesis imperfecta. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008 out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Intervenção neridronato e hormônio de crescimento. Antoniazzi, F., Morandi, A., Donadi, L., Brugnara, M., Monti, E., Franceschi, R., Zamboni, G. Bisphosphonate treatment in childhood. General aspects and indications in secondary scheletric pathologies (first part) [II trattamento con bisfosfonati in età evolutiva. Aspetti generali e indicazioni nelle patologie secondarie dello scheletro (prima parte). Rev Ital Med Adol. 2007; 5:10-17. Artigo de revisão. Antoniazzi F, Mottes M, Fraschini P, Brunelli PC, Tatò L. Osteogenesis imperfecta: practical treatment guidelines. Paediatr Drugs. 2000 NovDec;2(6):465-88. Artigo de revisão. 103 Antoniazzi F, Zamboni G, Lauriola S, Donadi L, Adami S, Tatò L. Early bisphosphonate treatment in infants with severe osteogenesis imperfecta. J Pediatr. 2006 Aug;149(2):174-9. Grupo controle histórico. Ashford RU, Dey A, Kayan K, McCloskey EV, Kanis JA. Oral clodronate as treatment of osteogenesis imperfecta. Arch Dis Child. 2003 Oct;88(10):945. Intervenção clodronato. Aström E, Jorulf H, Söderhäll S. Intravenous pamidronate treatment of infants with severe osteogenesis imperfecta. Arch Dis Child. 2007;92(4):332-8. Grupo histórico controle. Åström E. Management of osteogenesis imperfecta. Ped Chil Heal. 2008; 18: 97-98. Revisão. Aström E, Söderhall S. Beneficial effect of bisphosphonate during five years of treatment of severe Osteogenesis imperfecta. Acta Paediatr. 1998; 87: 64-68. Estudo de casos. Aström E, Söderhäll S. Intravenous pamidronate treatment to infants with severe formo f osteogenesis imperfecta. Anais 9th International Meeting on Osteogenesis Imperfecta; 2005, jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Poucas informações disponíveis. Atanasova I, Borisova AM, Lozanov B, Sestrimska N, Kumanov P, Ivanova R, et al.Co-existence of osteogenesis imperfecta and klinefelter syndrome. Anais 29th European Symposium on Calcified Tissue; 2002 mai 25-29; Zagreb, Croácia. Zagreb: European Calcified Tissue Society; 2002. Estudo de caso. Bachrach LK, Ward LM. Clinical review 1: Bisphosphonate use in childhood osteoporosis. J Clin Endocrinol Metab. 2009;94(2):400-9. Artigo de revisão. Banerjee I, Shortland GJ, Evans WD, Gregory JW. Osteogenesis imperfecta and intravenous pamidronate. Arch Dis Child. 2002; 87: 562-563. Poucas informações. Barbosa CO, Santos AC, Villar, MA, Silva AT, Lima MAFD, Magalhães T, et al. Osteogenesis imperfecta treatment with bisphosphonates in Rio de Janeiro – Brazil. Anais da reunião anual do American College of Medical Genetics; 2007 Nashville, Estados Unidos da América. Nashville: American College of Medical Genetics; 2007. Semelhante a outro estudo inculido, com informações mais completas. Barros ER. Considerações sobre etiologia e tratamento da fragilidade óssea na infância: identificação de uma nova mutação no gene LPR5. [Tese de Doutorado]. São Paulo: Pós-Graduação em Endocrinologia Clínica, Universidade Federal de São Paulo; 2008. Outra doença. 104 Batch JA, Couper JJ, Rodda C, Cowell CT, Zacharin M. Use of bisphosphonate therapy for osteoporosis in childhood and adolescence. J Paediatr Child Health. 2003;39(2):88-92. Artigo de revisão. Benhamou CL. Effects of osteoporosis medications on bone quality. Joint Bone Spine. 2007;74(1):39-47. Artigo de revisão. Bin-Abbas BS, Al-Ashwal AA, Al-Zayed ZS, Sakati NA. Radiological features of bisphosphonate therapy in children with osteogenesis imperfecta. Saudi Med J. 2004;25(11):1772-3. Não disponível. Bishop NJ. Osteogenesis imperfecta calls for caution. Nat Med. 1999;5(5):4667. Bishop N. Bisphosphonates in OI. Anais da 10th International Meeting on Osteogenesis Imperfecta; 2008 out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Apresentação oral, revisão geral. Boot AM, de Coo RF, Pals G, de Muinck Keizer-Schrama SM. Muscle weakness as presenting symptom of osteogenesis imperfecta. Eur J Pediatr. 2006;165(6):392-4. Relato de caso. Burnei G, Vlad C, Georgescu I, Gavriliu TS, Dan D. Osteogenesis imperfecta: diagnosis and treatment. J Am Acad Orthop Surg. 2008;16(6):356-66. Artigo de revisão. Boutaud B, Laville JM. Elastic sliding central medullary nailing with osteogenesis imperfecta. Fourteen cases at eight years follow-up. Rev Chir Orthop Reparatrice Appar Mot. 2004;90(4):304-11. Intervenção cirúrgica. Camacho NP, Carroll P, Raggio CL. Fourier transform infrared imaging spectroscopy (FT-IRIS) of mineralization in bisphosphonate-treated oim/oim mice. Calcif Tis Intern. 2003; 72: 604-609. Estudo com animais. Carter S, Mendoza-Londono R, Sutton VR, Bacino CA, Ellis K, Shypailo R et al. Bisphosphonate treatment for osteopenia associated with genetic disease in children. Anais da 52a reunião annual da American Society of Human Genetics; 2002 out 15-19; Baltimore, Estados Unidos da América. Baltimore: American Society of Human Genetics; 2002. Outras doenças. Carvajal CC. Vía intraósea en pediatria. Rev Cubana Pediatr;75(3): 0. Desfecho não era de interesse. Cascella AU, Musella T, Orio T, Palomba F, Bifulco S, Nappi G, Lombardi C, Colac G, Tauchmanova AL. Effects of neridronate treatment in elderly woman with osteoporosis. J Clin Endocrinol Invest. 2005; 28: 202-208. Intervenção neridronato, outra doença. 105 Chan B, Zacharin M. Maternal and infant outcome after pamidronate treatment of polyostotic fibrous dysplasia and osteogenesis imperfecta before conception: a report of four cases. J Clin Endocrinol Metab. 2006;91(6):2017-20. Estudo de casos. Cheung MS, Glorieux FH. Osteogenesis Imperfecta: update on presentation and management. Rev Endocr Metab Disord. 2008;9(2):153-60. Artigo de revisão. Cheung MS, Glorieux FH, Rauch F. Natural history of hyperplastic callus formation in osteogenesis imperfecta type V. J Bone Miner Res. 2007;22(8):1181-6. Chevrel G, Cimaz R. Osteogenesis imperfecta: new treatment options. Curr Rheumatol Rep. 2006;8(6):474-9. Artigo de revisão. Chevrel G. Effects os oral alendronate on bone mineral density in adult patients with Osteogenesis imperfecta. A three-year randomized placebo-controlled trial. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Semelhante a outro estudo incluido, com informações mais completas. Chevrel G, Meunier PJ. Osteogenesis imperfecta: lifelong management is imperative and feasible. Joint Bone Spine. 2001;68(2):125-9. Artigo de revisão. Chien YH, Chu SY, Hsu CC, Hwu WL. Pamidronate treatment of severe osteogenesis imperfecta in a newborn infant. J Inherit Metab Dis. 2002;25(7):593-5. Estudo de caso. Chigladze, T.T., Zhvaniia, M.A., Bekua, M.V. Influence of bisphosphonate treatment on the radiological features of osteogenesis imperfecta in children. Georg Med News. 2006; 131: 62-65. Desfecho não era de interesse Chung G, Keen RW. Prevalence of vitamin D deficienty in patients with Osteogenesis imperfecta. Anais 30th European Symposium on Calcified Tissue; 2003 mai 8-12; Roma, Itália. Roma: European Calcified Tissue Society, 2003. Desfecho não era de interesse. Colapietro F. Adami S, Prizzi R, Gatti D, Braga V, Gerardi D, Righetti D, Rossini M. Intravenous neridronate in adults with osteogenesis imperfecta. Anais 30th European Symposium on Calcified Tissue; 2003 mai 8-12; Roma, Itália. Roma: European Calcified Tissue Society, 2003. Intervenção neridronato. Cole WG. Olpadronate reduced fractures in children with osteogenesis imperfecta. J Bone Joint Surg. 2004; 86A:2575. Comentário D'Eufemia P, Finocchiaro R, Celli M, Zambrano A, Tetti M, Villani C, Persiani P, Mari E, Zicari A. High levels of serum prostaglandin E2 in children with 106 osteogenesis imperfecta are reduced by neridronate treatment. Pediatr Res. 2008;63(2):203-6. Desfechos não são de interesse. D'Eufemia P, Finocchiaro R, Zambrano A, Tetti M, Ferrucci V, Celli M. Reduction of plasma taurine level in children affected by osteogenesis imperfect during bisphosphonate therapy. Biomed Pharmacother. 2007;61(4):235-40. Desfechos não são de interesse. Damiani D, Menezes Filho HC. Metaphyseal sclerosis associated with bisphosphonate therapy. J Pediatr Endocrinol Metab. 2007;20(11):1167. Davies JH, Gregory JW. Radiographic long bone appearance in a child administered cyclical pamidronate. Arch Dis Child. 2003;88(10):854. Delos, D., Yang, X., Ricciardi, B.F., Myers, E.R., Bostrom, M.P.G., Camacho, N.P. The effects of RANKL inhibition on fracture healing and bone strength in a mouse model of osteogenesis imperfecta. J Orthopaed Res. 2008; 26: 153-164. Estudo com animais. Devogelaer JP, Coppin C. Osteogenesis imperfecta: Current treatment options and future prospects. Treat Endocrinol. 2006; 5: 229-242. Artigo de revisão. Devogelaer JP, Coppin C, Depresseux G. Radiographs, boné densitometry and biological parameters of boné remodeling in the treatment of Osteogenesis imperfecta. Anais da 10th International Meeting on Osteogenesis Imperfecta; 2008 out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Apresentação oral da experiência do grupo. Devogelaer JP, Lecouvet F, Depresseux G. Bone in bone after treatment with intravenous infusions of disodium pamidronate in a child suffering from Osteogenesis imperfecta. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Estudo de caso. Desfecho não era de interesse. Devogelaer JP. New uses of bisphosphonates: osteogenesis imperfecta. Curr Opin Pharmacol. 2002;2(6):748-53. Artigo de revisão. Devogelaer JP. Treatment of bone diseases with bisphosphonates, excluding osteoporosis. Curr Opin Rheumatol. 2000;12(4):331-5. Artigo de revisão. Di Iorgi N, Maghnie M. Motor function improvement after intravenous pamidronate in osteoporosis pseudoglioma syndrome. J Pediatr. 2006;149(5):734. Desfecho não era do interesse. DiMeglio LA, Ford L, McClintock C, Peacock M. A comparison of oral and intravenous bisphosphonate therapy for children with Osteogenesis imperfecta. J Pediatr Endocrinol Metab. 2005; 18: 43-53. Semelhante a outro estudo incluido, com informações mais completas. 107 DiMeglio LA, Ford L, McClintock C, Peacock M. Intravenous pamidronate treatment of children under 36 months of age with Osteogenesis imperfecta. Bone. 2004; 35: 1038-1045. Estudo de casos. DiMeglio LA, Ford L, McClintock C, Peacock M. Children with mild OI have a greater response to bisphosphonate therapy than those with severe OI. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Estudo de casos. Djokanovic N, Klieger-Grossmann C, Koren G. Does treatment with bisphosphonates endanger the human pregnancy? J Obstet Gynaecol Can. 2008;30(12):1146-8. Revisão sobre efeitos colaterais de bisfosfonatos na gestação. Dong YL, Cho TJ, In HC, Chin YC, Won JY, Ji HK, et al. Clinical and radiological manifestations of Osteogenesis imperfecta type V. J Korean Med Sci. 2006; 21: 709-714. Estudo de casos. Drake MT, Clarke BL, Khosla S. Bisphosphonates: mechanism of action and role in clinical practice. Mayo Clin Proc. 2008;83(9):1032-45. Artigo de revisão. Duncan EL, Bradbury LA, Barlow s, Geoghenan F, Blumsohn A, Schofield P, et al. The ROSI study (risedronate in adults with Osteogenesis imperfecta type 1). Anais 32nd European Symposium on Calcified Tissue; 2005, jun 25-29; Genebra, Suíça. Genebra: European Calcified Tissue Society; 2005. Intervenção risedronato. el-Sobky MA, Hanna AA, Basha NE, Tarraf YN, Said MH. Surgery versus surgery plus pamidronate in the management of osteogenesis imperfecta patients: a comparative study. J Pediatr Orthop B. 2006;15(3):222-8. Intervenção cirúrgica. Elias ER, Tsai CH, Zemel S. Pamidronate use in infants with Osteogenesis imperfecta (OI). Anais da 52a reunião annual da American Society of Human Genetics; 2002 out 15-19; Baltimore, Estados Unidos da América. Baltimore: American Society of Human Genetics; 2002. Estudo de casos. Escala, M. C; Santiso, A; Montangero, V. E. Osteogénesis y dentinogénesis imperfecta. Rev. Ateneo Argent. Odontol;44(1):33-37, ene.-abr. 2005. ilus. Artigo de revisão. Evans KD, Lau ST, Oberbauer AM, Martin RB. Alendronate affects long bone length and growth plate morphology in the oim mouse model for Osteogenesis Imperfecta. Bone. 2003; 32: 268-274. Estudo com animais. Evans KD, Martin RB, Lau ST, Oberbauer AM. The effect of alendronate on long bone growth and growth plate in the oim mouse model for Osteogenesis imperfecta. Anais 1st Joint Meeting IBMS/ESCT; 2001 jun 5-10; Barcelona, 108 Espanha. Barcelona: European Calcified Tissue Society; 2001. Estudo com animais. Falk MJ, Heeger S, Lynch KA, DeCaro KR, Bohach D, Gibson KS, Warman ML. Intravenous bisphosphonate therapy in children with Osteogenesis imperfecta. Pediatrics. 2003; 111: 573-578. Fleisch H. Introduction to bisphosphonates. History and functional mechanisms. Orthopade. 2007. 36: 103-104. Artigo de revisão. Gandrud LM, Cheung JC, Daniels MW, Bachrach LK. Low-dose intravenous pamidronate reduces fractures in childhood osteoporosis. J Ped Endocrinol Metab. 2003; 16: 887-892. Outra doença. Fleming F, Woodhead HJ, Briody JN, Hall J, Cowell CT, Ault J, Kozlowski K, Sillence DO. Cyclic bisphosphonate therapy in osteogenesis imperfecta type V. J Paediatr Child Health. 2005;41(3):147-51. Estudo de caso. Forin V. Osteogenesis imperfecta. Presse Med. 2007;36(12 Pt 2):1787-93. Artigo de revisão. Forin V. Osteogenesis imperfecta and bisphosphonates. Arch Pediatr. 2005; 12: 688-690. Experiência do grupo, semelhante a outro estudo incluido. Fujiwara I, Ogawa E, Igarashi Y, Ohba M, Asanuma A. Intravenous pamidronate treatment in osteogenesis imperfecta. Eur J Pediatr. 1998;157(3):261-2. García IH, Martín MF, Pérez SL, García AG, Echenique JR. Osteogénesis imperfecta: mosaicismo germinal o evidencia de heterogeneidad genética. Presentación de una familia y revisión bibliográfica. Rev Cubana Pediatr;79(3): 0. Estudo de casos. Gatti D, Antoniazzi F, Prizzi R, Braga V, Rossini M, Tatò L, Viapiana O, Adami S. Intravenous neridronate in children with osteogenesis imperfecta: a randomized controlled study. J Bone Miner Res. 2005;20(5):758-63. Intervenção neridronato. Gatti D, Viapiana O, Lippolis I, Braga V, Prizzi R, Rossini M, Adami S. Intravenous bisphosphonate therapy increases radial width in adults with osteogenesis imperfecta. J Bone Miner Res. 2005;20(8):1323-6. Desfecho não era de interesse. Giraud F, Meunier PJ. Effect of cyclical intravenous pamidronate therapy in children with Osteogenesis imperfecta. Open-label study in seven patients. Joint Bone Spine. 2002; 69: 486-490. Estudo de casos. Glorieux FH. Experience with bisphosphonates in osteogenesis imperfecta. Pediatrics. 2007;119 Suppl 2:S163-5. Artigo de revisão. 109 Glorieux FH. Osteogenesis imperfecta. Best Pract Res Clin Rheumatol. 2008;22(1):85-100. Artigo de revisão. Glorieux FH. Treatment of osteogenesis imperfecta: who, why, what? Horm Res. 2007;68 Suppl 5:8-11. Artigo de revisão. Glorieux FH. The use of bisphosphonates in children with osteogenesis imperfecta. J Pediatr Endocrinol Metab. 2001;14 Suppl 6:1491-5. Artigo de revisão. Glorieux FH. Bisphosphonate therapy for severe osteogenesis imperfecta. J Pediatr Endocrinol Metab. 2000;13 Suppl 2:989-92. Artigo de revisão. Glorieux FH, Rauch F, Shapiro JR. Bisphosphonates in children with bone diseases. N Engl J Med. 2003;349(21):2068-71 Carta resposta. Glorieux FH. Bisphosphonate therapy in OI: update on efficacy and safety. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Atualização em bisfosfonatos na osteogênese imperfeita. Gonzalez E, Pavia C, Ros J, Villarnga M, Valls C, Escolá J. Efficacy of low dose Schedule pamidronate infusion in children with osteogenesis imperfecta. J Pediatr Endocrinol Metab. 2001; 14: 529-533. Goss AN. Bisphosphonates and orthodontics. Aust Orthod J. 2008;24(1):56-7. Artigo de revisão. Graul AI. Filling the gaps: osteogenesis imperfecta. Drug News Perspect. 2005;18(6):400-1. Artigo de revisão. Grigorie D, Barbu C, Neascu E, Dumitrache M, Grigorie M, Dumitrache C. One year study of alendronate effects on vertebral mineral density and bone turnover in women with mild type I Osteogenesis imperfecta. Anais 1 st Joint Meeting IBMS/ESCT; 2001 jun 5-10; Barcelona, Espanha. Barcelona: European Calcified Tissue Society; 2001. Estudo de casos. Grissom LE, Harcke HT. Radiographic features of bisphosphonate therapy in pediatric patients. Pediatr Radiol. 2003;33(4):226-9. Desfecho não era de interesse. Grissom LE, Kecskemethy HH, Bachrach SJ, McKay C, Harcke HT. Bone densitometry in pediatric patients treated with pamidronate. Pediatr Radiol. 2005;35(5):511-7. Guillot M, Eckart P, Desrosieres H, Amiour M, al-Jazayri Z. Osteogenesis imperfecta: a new, early therapeutic approach with biphosphonates. A case report. Arch Pediatr. 2001;8(2):172-5. Estudo de caso. 110 Hartsfield Jr JK, Hohlt WF, Roberts WE. Orthodontic Treatment and Orthognathic Surgery for Patients with Osteogenesis Imperfecta. Sem Orthod. 2006; 12: 254-271. Henderson R. Low doses of pamidronate for the treatment of osteopenia in nonambulatory children. Dev Med Child Neurol. 2006;48(9):708. Artigo de revisão. Hill C, Hampshire D, Silverwood B, Bishop NJ. Recent advances in the management of osteogenesis imperfecta. Curr Pediatr. 2003; 13: 151-157. Huber MA. Osteogenesis imperfecta. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2007;103(3):314-20. Artigo de revisão. Huzjak N, Barisic I, Resic A, Kusec V, Anticevic D, Dodig D, et al. Bisphosphonate therapy in patients with Osteogenesis imperfecta. Anais 29 th European Symposium on Calcified Tissue; 2002 mai 25-29; Zagreb, Croácia. Zagreb: European Calcified Tissue Society; 2002. Estudo de casos. Huzjak N, Barisic I, Resic A, Kusec V, Anticevic D, Dodig D. Bisphosphonate therapy for Osteogenesis imperfecta. Anais European Human Genetics Conference; 2002 mai 25-29; Strasbourg, França. Strasbourg: European Society of Human Genetics; 2002. Estudo de casos. Iwamoto J, Takeda T, Sato Y. Efficacy of oral etidronate for skeletal diseases in Japan. Yonsei Med J. 2005;46(3):313-20. Intervenção neridronato. Iwamoto J, Takeda T, Sato Y. Effect of treatment with alendronate in osteogenesis imperfecta type I: a case report. Keio J Med. 2004;53(4):251-5. Estudo de caso. Iwamoto J, Matsu K, Takeda T, Ichimura S, Uzawa M. Effects of treatment with etidronate and alfacalcidol for osteogenesis imperfecta type I: a case report. J Orthop Sci. 2003;8(2):243-7. Estudo de caso. Jakubowska-Pietkiewicz E, Chlebna-Sokol D. New trends in the treatment of Osteogenesis imperfecta type III – own experience. Ortop Traumatol Rehabil. 2008; 10: 593-601. Apresentação da experiência do grupo, estudo de casos. Kamoun-Goldrat A, Ginisty D, Le Merrer M. Effects of bisphosphonates on tooth eruption in children with osteogenesis imperfecta. Eur J Oral Sci. 2008;116(3):195-8. Desfecho não era de interesse. Kamoun-Goldrat AS, Le Merrer MF. Osteogenesis imperfecta and dentinogenesis imperfecta: diagnostic frontiers and importance in dentofacial orthopedics. Orthod Fr. 2007;78(2):89-99. Artigo de revisão. Kodama H, Kubota K, Abe T. Osteogenesis imperfecta: Are fractures and growth hormone treatment linked? J Pediatr. 1998;132(3 Pt 1):559-60. 111 Kok DH, Sakkers RJ, Janse AJ, Pruijs HE, Verbout AJ, Castelein RM, Engelbert RH. Quality of life in children with osteogenesis imperfecta treated with oral bisphosphonates (Olpadronate): a 2-year randomized placebo-controlled trial. Eur J Pediatr. 2007;166(11):1155-61. Intervenção olpandronato. Kone Paut I, Gennari JM, Retornaz K, Jouve JL, Bollini G. Biphosphonates in children: present and future. Arch Pediatr. 2002;9(8):836-42. Artigo de revisão. Land C, Rauch F, Munns CF, Sahebjam S, Glorieux FH. Vertebral morphometry in children and adolescents with osteogenesis imperfecta: effect of intravenous pamidronate treatment. Bone. 2006;39(4):901-6. Desfecho não era de interesse. Land C, Rauch F, Montpetit K, Ruck-Gibis J, Glorieux FH. Effect of intravenous pamidronate therapy on functional abilities and level of ambulation in children with Osteogenesis imperfeca. J Pediatr. 2006; 148: 456-460. Desfecho não era de interesse. Land C, Rauch F, Glorieux FH. Cyclical intravenous pamidronate treatment affects metaphyseal modeling in growing patients with osteogenesis imperfecta. J Bone Miner Res. 2006;21(3):374-9. Desfecho não era de interesse. Langman CB. Improvement of bone in patients with osteogenesis imperfecta treated with pamidronate-lessons from biochemistry. J Clin Endocrinol Metab. 2003;88(3):984-5. Le Blanc K, Götherström C, Ringdén O, Hassan M, McMahon R, Horwitz E, Anneren G, Axelsson O, Nunn J, Ewald U, Nordén-Lindeberg S, Jansson M, Dalton A, Åström E, Westgren M. Fetal mesenchymal stem-cell engraftment in bone after in utero transplantation in a patient with severe osteogenesis imperfecta. Transplantation. 2005; 79: 1607-1614. Lee DY, Cho TJ, Choi IH, Chung CY, Yoo WJ, Kim JH, Park YK. Clinical and radiological manifestations of osteogenesis imperfecta type V. J Korean Med Sci. 2006;21(4):709-14. Estudo de casos. Lee YS, Low SL, Lim LA, Loke KY. Cyclic pamidronate infusion improves bone mineralization and reduces fracture incidence in Osteogenesis imperfecta. Eur J Pediatr. 2001; 160: 641-644. Estudo de casos. Letocha AD, Cintas HL, Troendle JF, Reynolds JC, Cann CE, Chernoff EJ, et al. Controlled trial of pamidronate in children with types III and IV Osteogenesis imperfecta confirms vertebral gains but not short-term functional improvement. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Desfecho não é de interesse. Letocha AD, Cintas HL, Troendle JF, Reynolds JC, Cann CE, Chernoff EJ, Hill SC, Gerber LH, Marini JC. Controlled trial of pamidronate in children with types III and IV osteogenesis imperfecta confirms vertebral gains but not short-term 112 functional improvement. J Bone Miner Res. 2005 Jun;20(6):977-86. Desfecho não era de interesse. Licata AA. Discovery, clinical development, and therapeutic uses of bisphosphonates. Ann Pharmacother. 2005;39(4):668-77. Artigo de revisão. Lima MAFD, Barbosa CO, Santos AC, Villar MA, Silva AT, Magalhães T et al. Pamidronate dissodium treatment beginning in the neonatal period: preliminary results in 5 osteogenesis imperfecta patients. Anais da reunião anual do American College of Medical Genetics; 2007 Nashville, Estados Unidos da América. Nashville: American College of Medical Genetics; 2007. Estudo de casos. Lindsay R. Modeling the benefits of pamidronate in children with osteogenesis imperfecta. J Clin Invest. 2002;110(9):1239-41. Lipton A. New therapeutic agents for the treatment of bone diseases. Expert Opin Biol Ther. 2005;5(6):817-32. Artigo de revisão. Madenci E, Yilmaz K, Yilmaz M, Coksun Y. Alendronate treatment in osteogenesis impefecta. Clin Rheumatol. 2006; 12: 53-56. Estudo de casos. Malmgren B, Aström E, Söderhäll S. No osteonecrosis in jaws of young patients with osteogenesis imperfecta treated with bisphosphonates. J Oral Pathol Med. 2008;37(4):196-200. Desfecho não era de interesse. Marini JC. Do bisphosphonates make children's bones better or brittle? N Engl J Med. 2003;349(5):423-6. Marini JC. Osteogenesis imperfecta--managing brittle bones. N Engl J Med. 1998;339(14):986-7. Marini JC, Obafemi AA, Abukhaled MK, Cintas HL, Troendle JF, Letocha AD, Reynolds JC, Paul S. Randomized dose comparison of pamidronate in children with types III and IV osteogenesis imperfecta: 3 vs 6 month cycles. Anais 35 th European Symposium on Calcified Tissue; 2008 mai 24-28; Barcelona, Espanha. Barcelona: European Calcified Tissue Society; 2008. Semelhante a outro estudo incluido, com informações mais completas. Marini JC, Obafemi AA, Abukhaled MK, Cintas HL, Troendle JF, Letocha AD, et al. Randomized dose comparison of pamidronate in children with types III and IV Osteogenesis imperfecta: 3 vc 6 month cycles. Anais European Human Genetics Conference; 2008 mai 31 – jun 3; Barcelona, Espanha. Barcelona: European Society of Human Genetics; 2008. Semelhante a outro estudo incluído, com informações mais completas. Markello TC, Boston B, Steiner R. Precocious puberty during outpatient therapy in type I Osteogenesis imperfecta. Anais da 52 a reunião annual da American Society of Human Genetics; 2002 out 15-19; Baltimore, Estados Unidos da 113 América. Baltimore: American Society of Human Genetics; 2002. Efeitos colaterais de bisfosfonato, estudo de caso. McCarthy EA, Raggio CL, Hossack MD, Miller EA, Jain S, Boskey AL, Camacho NP. Alendronate treatment for infants with osteogenesis imperfecta: demonstration of efficacy in a mouse model. Pediatr Res. 2002;52(5):660-70. Trabalho com animais. McQuade M, Houghton K. Use of bisphosphonates in a case of Perthes disease. Orthop Nurs. 2005 Nov-Dec;24(6):393-8. Estudo de caso. Migliaccio S, Barbaro G, Formari R, Di Lorenzo G, Falcone S, Marzano S, et al. Adult patients affectd by osteogenesis imperfecta have impairment of diastolic function. Anais 33rd European Symposium on Calcified Tissue; 2006 mai 10-14; Praga, República Tcheca. Praga: European Calcified Tissue Society; 2006. Estudo de caso. Miller ME, Hangartner TN. Successful treatment of severe Osteogenesis imperfecta with oral alendronate. Anais 50a reunião anual da American Society of Human Genetics; 2000 out 3-7; Filadélfia, Estados Unidos da América. Filadélfia: American Society of Human Genetics, 2000. Estudo de caso. Misof BM, Roschger P, Baldini T, Raggio CL, Zraick V, Root L, Boskey AL, Klaushofer K, Fratzl P, Camacho NP. Differential effects of alendronate treatment on bone from growing osteogenesis imperfecta and wild-type mouse. Bone. 2005; 36: 150-158. Estudo com animais. Montpetit K, Plotkin H, Rauch F, Bilodeau N, Cloutier S, Rabzel M, Glorieux FH. Rapid increase in grip force after start of pamidronate therapy in children and adolescents with severe osteogenesis imperfecta. Pediatrics. 2003 May;111(5 Pt 1):e601-3. Desfecho não era de interesse. Moret Y. Enfermedades Genéticas que afectan la cavidad bucal: Revicion de la literature. Acta odontol. venez;42(1): 52-57. Artigo de revisão. Morris CD, Einhorn TA. Bisphosphonates in orthopaedic surgery. J Bone Joint Surg Am. 2005;87(7):1609-18. Artigo de revisão. Munns CF, Rauch F, Travers R, Glorieux FH. Effects of intravenous pamidronate treatment in infants with osteogenesis imperfecta: clinical and histomorphometric outcome. J Bone Miner Res. 2005;20(7):1235-43. Uso de grupo controle histórico. Munns CF, Rauch F, Zeitlin L, Fassier F, Glorieux FH. Delayed osteotomy but not fracture healing in pediatric osteogenesis imperfecta patients receiving pamidronate. J Bone Miner Res. 2004;19(11):1779-86. Desfecho não era de interesse. Munns CF, Rauch F, Ward L, Glorieux FH. Maternal and fetal outcome after long-term pamidronate treatment before conception: a report of two cases. J 114 Bone Miner Res. 2004;19(10):1742-5. Estudo de casos sobre efeitos do pamidronato na gestação. Munns CF, Rauch F, Mier RJ, Glorieux FH. Respiratory distress with pamidronate treatment in infants with severe osteogenesis imperfecta. Bone. 2004;35(1):231-4. Estudo de caso sobre efeitos colaterais do pamidronato. Nguyen T, Zacharin MR. Pamidronate treatment of steroid associated osteonecrosis in young patients treated for acute lymphoblastic leukaemia Twoyear outcomes. J Ped Endocrinol Metab. 2006; 19: 161-167. Outra doença. Onwuneme C, Abdalla K, Cassidy N, Hensey O, Ryan S. Radiological findings in cyclical administration of intravenous pamidronate in children with osteoporosis. Arch Dis Child. 2007;92(12):1087. Orcel P, Beaudreuil J. Bisphosphonates in bone diseases other than osteoporosis. Joint Bone Spine. 2002;69(1):19-27. Artigo de revisão. Pan CH, Ma SC, Wu CT, Chen PQ. All pedicle screw fixation technique in correcting severe kyphoscoliosis in an osteogenesis imperfecta patient: a case report. J Spinal Disord Tech. 2006 Jul;19(5):368-72. Estudo de caso. Papapoulos SE, Cremers SC. Prolonged bisphosphonate release after treatment in children. N Engl J Med. 2007;356(10):1075-6. Parisuthiman D. Bisphosphonate-related osteonecrosis of the jaws: A call for multidisciplinary approaches. J Med Assoc Thail. 2007; 90: 2699-2708. Estudo sobre efeitos colaterais. Pittari G, Costi D, Raballo M, Maulucci L, Baroni MC, Mangoni M. Intravenous neridronate for skeletal damage treatment in patients with multiple myeloma. Acta Biomed. 2006;77(2):81-4. Intervenção neridronato. Pizones J, Plotkin H, Parra-Garcia JI, Alvarez P, Gutierrez P, Bueno A, Fernandez-Arroyo A. Bone healing in children with osteogenesis imperfecta treated with bisphosphonates. J Pediatr Orthop. 2005;25(3):332-5. Plotkin H. Bisphosphonates in children with bone diseases. N Engl J Med. 2003;349(21):2068-71. Plotkin H, Gibis J, Glorieux FH. Pamidronate treatment improves gross motor function and growth in children with Osteogenesis imperfecta. Anais 1 st Joint Meeting IBMS/ESCT; 2001 jun 5-10; Barcelona, Espanha. Barcelona: European Calcified Tissue Society; 2001. Desfechos não eram de interesse. Plotkin H; Glorieux FH; Rauch F; Shapiro JR; Bjarnason NH; Whyte MP; Wenkert D; McAlister WH; Marini JC. Bisphosphonates in children with bone diseases. N Engl J Med. 2003; 349:2068-2071. Artigo de comentário. 115 Plotkin H, Rauch F, Bishop NJ, Montpetit K, Ruck-Gibis J, Travers R, Glorieux FH. Pamidronate treatment of severe Osteogenesis imperfecta in children under 3 years of age. J Clin Endocrinol Metab. 2000; 85: 1846-1850. Estudo de casos. Popovic J, Jacobson JD. Zolendronate treatment in a patient with severe osteogenesis imperfecta. Anais 30th European Symposium on Calcified Tissue; 2003 mai 8-12; Roma, Itália. Roma: European Calcified Tissue Society, 2003. Estudo de caso Preciado LEL. Efectos adversos del tratamiento con pamidronato en niños con osteogenesis imperfecta en el Perú. [Monografia de conclusão de curso]. Lima: Pós Graduação em Pediatria, Universidade Mayor de San Marcos; 2003. Vinson EM. Clinical image: pamidronate "zebra" lines. Arthritis Rheum. 2008; 58: 2871. Estudo de caso. Primorac D, Rowe DW, Mottes M, Barisić I, Anticević D, Mirandola S, Gomez Lira M, Kalajzić I, Kusec V, Glorieux FH. Osteogenesis imperfecta at the beginning of bone and joint decade. Croat Med J. 2001;42(4):393-415. Pruijs HEH, Engelbert RHH, Sakkers RJB. The influence of bisphosphonate on orthopaedic management in Osteogenesis imperfecta. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Apresentação da experiencia do grupo. Klein GL, Bachrach LK, Holm IA. Effects of pharmacologic agents on bone in childhood: An editorial overview. Pediatrics. 2007; 119 (Suppl2): S125-S130. Editorial. Kocova M, Sukarova-Angelovska E. Stefanovska I, Galicka A. Osteogenesis imperfecta in children, effects of therapy with pamidronate. Anais European Human Genetics Conference; 2006 mai 06-09; Amsterdam, Holanda. Amsterdam: European Society of Human Genetics; 2006. Estudo de casos. Kusec V, Huzjak N, Barisic I, Resic A, Baric I, Anticevic D. Bone markers reveal decreased collagen type I synthesis and change in bone turnover during bisphosphonate treatment in Osteogenesis imperfecta. Anais 29 th European Symposium on Calcified Tissue; 2002 mai 25-29; Zagreb, Croácia. Zagreb: European Calcified Tissue Society; 2002. Informação insuficiente sobre medicação. Radfar L, Masood F. Bisphosphonates, osteonecrosis of the jaw, and dental treatment recommendations. J Okla Dent Assoc. 2008;99(7):28-9. Artigo de revisão. Rao, S.H., Evans, K.D., Oberbauer, A.M., Martin, R.B. Bisphosphonate treatment in the oim mouse model alters bone modeling during growth. J Biomechan. 2008; 41: 3371-3376. Estudo com animais. 116 Rauch F, Cornibert S, Cheung M, Glorieux FH. Long-bone changes after pamidronate discontinuation in children and adolescents with osteogenesis imperfecta. Bone. 2007;40(4):821-7. Desfechos não eram de interesse. Rauch F, Glorieux FH. Treatment of children with osteogenesis imperfecta. Curr Osteoporos Rep. 2006;4(4):159-64. Artigo de revisão. Rauch F, Munns C, Land C, Glorieux FH. Pamidronate in children and adolescents with osteogenesis imperfecta: effect of treatment discontinuation. J Clin Endocrinol Metab. 2006;91(4):1268-74. Rauch F, Travers R, Glorieux FH. Pamidronate in children with Osteogenesis imperfecta: histomorphometrc effects of long-term therapy. J Clin Endocrinol Metab. 2006; 91: 511-516. Rauch F, Glorieux FH. Osteogenesis imperfecta, current and future medical treatment. Am J Med Genet C Semin Med Genet. 2005;139C(1):31-7. Artigo de revisão. Rauch F, Glorieux FH. Bisphosphonate treatment in osteogenesis imperfecta: which drug, for whom, for how long? Ann Med. 2005;37(4):295-302. Artigo de revisão. Rauch F, Travers R, Munns C, Glorieux FH. Sclerotic metaphyseal lines in a child treated with pamidronate: histomorphometric analysis. J Bone Miner Res. 2004;19(7):1191-3. Estudo de caso. Rauch F, Glorieux FH. Osteogenesis imperfecta. Lancet. 2004;363(9418):137785. Artigo de revisão. Rauch F, Travers R, Plotkin H, Glorieux FH. The effects of intravenous pamidronate on the bone tissue of children and adolescents with osteogenesis imperfecta. J Clin Invest. 2002;110(9):1293-9. Desfecho não era de interesse. Reid IR. Bisphosphonates: new indications and methods of administration. Curr Opin Rheumatol. 2003;15(4):458-63. Artigo de revisão. Resic A, Barisic I, Kusec V, Anticevic D. Dodig D. Pamidronate treatment of Osteogenesis imperfecta in Croatia. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008, out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Informações insuficientes. Rieger-Wettengl G, Schönau E, Michalk D. Bisphosphonates and their use in disturbances of bone metabolism in pediatrics. Padiatr Praxis. 2003; 64: 129136. Artigo de revisão. Ringe JD, Dorst A, Faber H, Farahmand P. teriparatide in Osteogenesis imperfecta: treatment results of an 18 months prospective observational study. Anais 34th European Symposium on Calcified Tissue; 2007 mai 05-09; 117 Copenhague, Dinamarca. Copenhague: European Calcified Tissue Society; 2007. Intervenção teriparatide. Robinson RE, Nahata MC, Hayes JR, Batisky DL, Bates CM, Mahan JD. Effectiveness of pretreatment in decreasing adverse events associated with pamidronate in children and adolescents. Pharmacotherapy. 2004;24(2):195-7. Desfecho não era de interesse. Robinson RF, Long LD, Mahan JD. Treatment of poor linear growth in a patient with osteogenesis imperfecta type III. Clin Ther. 2004;26(10):1680-3. Desfecho não era de interesse. Roldan EJA, Capiglioni R, Aymond A, Tubert G, Guelman R, Montanegro VE, et al. Dissociation between tíbia stress-strain indexes (resistometry) with boné mineral content (densitomety). Example cases revealed with a PQCT system. Anais 32nd European Symposium on Calcified Tissue; 2005, jun 25-29; Genebra, Suíça. Genebra: European Calcified Tissue Society; 2005. Outras doenças, desfecho não era de interesse. Roldán EJ, Pasqualini T, Plantalech L. Bisphosphonates in children with osteogenesis imperfecta may improve bone mineralization but not bone strength. Report of two patients. J Pediatr Endocrinol Metab. 1999;12(4):555-9. Estudo de casos. Roughley PJ, Rauch F, Glorieux FH, Hofstetter W, Alini M. Osteogenesis imperfecta - Clinical and molecular diversity. Europ Cells Mat. 2003; 5:41-47. Revisão sobre aspectos moleculares. Roughley PJ, Rauch F, Glorieux FH. Osteogenesis imperfecta--clinical and molecular diversity. Eur Cell Mater. 2003;5:41-7; discussion 47. Artigo de revisão. Royer F, Michel; Stott C, Carlos; Lara F, Carolina; Franulic C, Lenka. Compromiso auditivo en osteogénesis imperfecta. Rev. Otorrinolaringol. Cir. Cabeza Cuello;66(3): 243-246. Desfecho não era de interesse. Rugolotto S, Monti E, Carli M, Pietrobelli A, Antoniazzi F, Tato L. Pulmonary function tests in an infant with osteogenesis imperfecta and early biphosphonate treatment. Acta Paediatr. 2007;96(12):1856-7. Estudo de caso. Sakkers R, Kok D, Engelbert R, van Dongen A, Jansen M, Pruijs H, Verbout A, Schweitzer D, Uiterwaal C. Skeletal effects and functional outcome with olpadronate in children with osteogenesis imperfecta: a 2-year randomised placebo-controlled study. Lancet. 2004;363(9419):1427-31. Intervenção olpandronato. Santili C, Akkari M, Waisberg G, Bastos Júnior JOC, Ferreira WM Avaliação clínica, radiográfica e laboratorial de pacientes com osteogênese imperfeita Rev. Assoc. Med. Bras.;51(4): 214-220. Sem intervenção. 118 Schwartz S, Joseph C, Iera D, Vu DD. Bisphosphonates, osteonecrosis, osteogenesis imperfecta and dental extractions: a case series. J Can Dent Assoc. 2008;74(6):537-42. Desfecho não era de interesse. Seebach C, Kurth A, Marzi I. The influence of bisphosphonates on fracture healing. Orthophade; 2007; 36: 136-140. Desfechos diferentes, outra doença. Semler O, Beccard R, Land C, Koerber F, Schoenau E. Bisphosphonate therapy in OI – the Colgne experience. Anais da 10th International Meeting on Osteogenesis Imperfecta; 2008 out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Intervenção neridronato. Semler O, Fricke O, Vezyroglou K, Stark C, Schoenau E. Preliminary results on the mobility after whole body vibration in immobilized children and adolescents. J Musculoskelet Neuronal Interact. 2007;7(1):77-81. Desfecho não era de interesse. Semler O, Kron M, Schoenau E. Height and weight development during bisphosphonate therapy in children with primary osteoporotic disease. Anais 9 th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Outras doenças. Shapiro JR, Hickman C, Sponseller P. Postpartum osteoporosis in type I A Osteogenesis imperfecta: response to bisphosphonates. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Estudo de caso. Shapiro JR, McCArthy EF, Rossiter K, Ernest K, Gelman R,Fedarko N et al. The effect of intravenous pamidronate on bone mineral density, bone hystomorphometry, and parameters of bone turnover in adults with type IA Osteogenesis imperfecta. Calcif Tissue Int. 2003; 72: 103-112. Estudo de casos. Shapiro J. Wu Y, Nunes W, Pfeifer K, Gillen L, Thompson C. Current evaluation of the response of Oi adults treated with bisbhosphonates. Anais 10th International Meeting on Osteogenesis Imperfecta; 2008 out 15-18; Ghent, Estados Unidos da América. Ghent: Osteogenesis Imperfecta Foundation; 2008. Semelhante a outro estudo incluido, com informações mais completas. Shaw NJ, Bishop NJ. Bisphosphonate treatment of bone disease. Arch Dis Child. 2005;90(5):494-9. Artigo de revisão. Silverwood B. Osteogenesis imperfecta: care and management. Paediatr Nurs. 2001;13(3):38-42. Artigo de revisão. Simmons JH, Zeitler PS. Osteopenia in pediatric patients: When and how to intervene. Curr Opin Endocrinol Diab. 2006; 13: 21-25. Artigo de revisão, outras doenças. 119 Smith EJ, Little DG, Briody JN, McEvoy A, Smith NC, Eisman JA, Gardiner EM. Transient disturbance in physeal morphology is associated with long-term effects of nitrogen-containing bisphosphonates in growing rabbits. J Bone Miner Res. 2005;20(10):1731-41. Estudo com animais. Smith R. Severe osteogenesis imperfecta: new therapeutic options? BMJ. 2001;322(7278):63-64. Artigo de revisão. Souza ASR, Cardoso AS, Lima MMS, Guerra GVQL. Diagnóstico pré-natal e parto transpelviano na osteogênese imperfeita: relato de caso. Rev. Bras. Ginecol. Obstet.;28(4): 244-250. Estudo de caso. Speiser PW, Clarson CL, Eugster EA, Kemp SF, Radovick S, Rogol AD, Wilson TA; LWPES Pharmacy and Therapeutic Committee. Bisphosphonate treatment of pediatric bone disease. Pediatr Endocrinol Rev. 2005;3(2):87-96. Artigo de revisão. Srinivasan R. Pamidronate lines. Indian Pediatr. 2005;42(9):959-60. Estudo de caso. Srivastava T, Alon US. Bisphosphonates: from grandparents to grandchildren. Clin Pediatr (Phila). 1999;38(12):687-702. Artigo de revisão. Syamlal S, Shine S, Kunju M. Brainstem and cerebellar hypoplasia associated with osteogenesis imperfecta type-5. J Postgrad Med. 2006;52(2):152-3. Estudo de caso. Tanaka H. Bone quality in osteogenesis imperfecta. Clin Calc. 2005; 15: 985989. Artigo de revisão. Tau C. Treatment of osteogenesis imperfecta with bisphosphonates. Medicina (B Aires). 2007;67(4):389-95. Artigo de revisão. Thompson GA, Burgio DE, Russel DA, Sun LA, Bishop N. Risedronate pharmacokinetics in children with osteogenesis imperfecta. Anais 32 nd European Symposium on Calcified Tissue; 2005, jun 25-29; Genebra, Suíça. Genebra: European Calcified Tissue Society; 2005. Desfecho não era de interesse, intervenção risedronato. Thornton J, Ashcroft DM, Mughal MZ, Elliott RA, O'Neill TW, Symmons D. Systematic review of effectiveness of bisphosphonates in treatment of low bone mineral density and fragility fractures in juvenile idiopathic arthritis. Arch Dis Child. 2006;91(9):753-61. Inclui outras doenças. Unal E, Abaci A, Bober E, Buyukgebiz A. Oral alendronate in osteogenesis imperfecta. Indian Pediatr. 2005;42(11):1158-60. Estudo de caso. Vasikaran SD. Bisphosphonates: an overview with special reference to alendronate. Ann Clin Biochem. 2001;38(Pt 6):608-23. Artigo de revisão. 120 Vega-Briceño L, Contreras I, Sánchez I, Bertrand P. Uso precoz del BiPAP en el tratamiento de la insuficiencia respiratoria en un lactante con osteogénesis imperfecta: Case report. Rev. méd. Chile;132(7): 861-864. Estudo de caso. Waltimo-Sirén J, Kolkka M, Pynnönen S, Kuurila K, Kaitila I, Kovero O. Craniofacial features in osteogenesis imperfecta: a cephalometric study. Am J Med Genet A. 2005;133A(2):142-50. Desfecho não era de interesse. Ward KA, Adams JE, Freemont TJ, Mughal MZ. Can bisphosphonate treatment be stopped in a growing child with skeletal fragility? Osteoporos Int. 2007;18(8):1137-40. Desfecho não era de interesse. Ward LM, Denker AE, Porras A, Shugarts S, Kline W, Travers R, Mao C, Rauch F, Maes A, Larson P, Deutsch P, Glorieux FH. Single-dose pharmacokinetics and tolerability of alendronate 35- and 70-milligram tablets in children and adolescents with osteogenesis imperfecta type I. J Clin Endocrinol Metab. 2005;90(7):4051-6. Desfecho não era de interesse. Weber M, Roschger P, Fratzl-Zelman N, Schöberl T, Rauch F, Glorieux FH, Fratzl P, Klaushofer K. Pamidronate does not adversely affect bone intrinsic material properties in children with osteogenesis imperfecta. Bone. 2006;39(3):616-22. Desfecho não era de interesse. Winzenberg TM, Shaw K, Fryer J, Jones G. Calcium supplementation for improving bone mineral density in children (Cochrane Review). In: The Cochrane Library, Issue 1, 2009. Oxford: Update Software. Intervenção calcio. Whyte MP, Clements KL, Wenkert D. Bisphosphonate treatment for children: assessing for toxicity. Anais 9th International meeting on Osteogenesis Imperfecta; 2005 jun 13-16; Annapolis, Estados Unidos da América. Annapolis: Osteogenesis Imperfecta Foundation; 2005. Atualização em efeitos colaterais. Young SD 3rd, Nelson CL, Steinberg ME. Transient osteoporosis of the hip in association with osteogenesis imperfecta: two cases, one complicated by a femoral neck fracture. Am J Orthop. 2008;37(2):88-91. Estudo de casos cirúrgicos. Yurekli Y, Erdogan S, Cullu E. Unusual bone scan of a child with osteogenesis imperfecta. Clin Nucl Med. 2003;28(2):156. Estudo de caso. Zeitlin L, Rauch F, Plotkin H, Glorieux FH. Height and weight development during four years of therapy with cyclical intravenous pamidronate in children and adolescents with osteogenesis imperfecta types I, III, and IV. Pediatrics. 2003;111(5 Pt 1):1030-6. Desfecho não era de interesse. Zeitlin L, Fassier F, Glorieux FH. Modern approach to children with osteogenesis imperfecta. J Pediatr Orthop B. 2003;12(2):77-87. Artigo de revisão. Zeitlin L, Wientroubl S, Blumberg N. Updates in osteogenesis imperfecta. Harefuah. 2003; 142: 688-693. 121 ANEXO 1 – ESCALA DE AVALIAÇÃO DA QUALIDADE DE ESTUDOS CLÍNICOS10 Questões: 1. O estudo foi descrito como randomizado (inclui palavras “randomly”, “random”, “randomization”)? 2. O estudo foi descrito como duplo-cego? 3. Houve descrição dos indivíduos deixaram ou foram retirados do estudo? Pontuação: Atribui-se 1 ponto para as respostas “sim” a cada uma das perguntas ou nenhum ponto para as respostas “não”. Atibui-se um ponto adicional se: a. Na questão 1 o método de randomização foi descrito e era apropriado (tabela com números randomizados ou gerado por computador etc.) ou b. Na questão 2 o métedo de duplo cegamento foi descrito e era apropriado (placebo idêntico etc.) Deduz-se um ponto se: a. Na questão 1 o método para gerar a sequencia de randomização foi descrito, mas era inapropriado (pacientes alocados alternadamente ou de acordo com data de nascimento etc) ou b. Na questão 2 o método de cegamento foi descrito, mas não foi apropriado (comparação de injeção e comprimidos etc). 10 Adaptado de Jadad et al, 1996.
Baixar