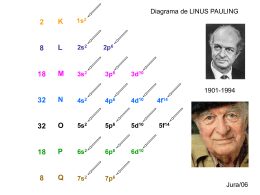
Química Geral Professor Celso Rapaci TOMO II Configuração Eletrônica INTRODUÇÃO Neste capítulo aprenderemos como os elétrons estão distribuídos na eletrosfera do átomo, em diferentes níveis e subníveis de energia. Aprenderemos ainda o conceito de orbital e de spin eletrônico, completando os conhecimentos necessários para o entendimento do Princípio de Pauli, da Regra de Hund e dos Números Quânticos. A forma exposta na figura anterior é de dificil memorização, porém uma forma simples e de fácil aplicação esta exoposta a seguir, é o chamado Diagrama de Linus Pauling. INÍCIO DISTRIBUIÇÃO ELETRÔNICA Ainda no início do século XX o Químico Linus Pauling, determinou experimentalmente que os subníveis de energia ordenam-se da seguinte forma, com relação à quantidade de energia agregada. Diagrama de Linus Pauling Para completar o procedimento segue abaixo o número máximo de elétrons que cada subnível pode abrigar. Subnível No Máximo de Elétrons s 2 p 6 d 10 f 14 O número sobrescrito logo após o subnível de energia indica o número de elétrons que este contém. Por exemplo: Ordem Energética dos Subníveis de Energia 4d5 Æ cinco elétrons no subnível 5d 3p6 Æ seis elétrons no subnível 3p Em se sabendo que OS ELÉTRONS OCUPAM PRIMEIRO OS SUBNÍVEIS DE MENOR ENERGIA, Linus Pauling determinou a ordem de preenchimento dos orbitais. Notemos que ocorrem alguma inversões na ordem intuitiva de preenchimento, observe que os elétrons ocupam primeiero o subnível 4s para só depois ocuparem o subnível 3d. 1 É fundamental que o aluno saiba como usr o Diagrama anterior, e ainda memorize a forma de contruí-lo pois no dia do Vestibular este não será fornecido. Observe os exemplos de Distribuição Eletrônica dos átomos neutros em seu Estado Fundamental*1. FORMA DOS SUBNÍVEIS A forma com que os orbitais se distribuem espacialmente é bastante diferente de um subníve para outro. Observemos abaixo a forma geométrica dos orbitais. Æ 1s2 2s2 2p6 3s1 2 2 6 2 6 2 10 4p5 35Br Æ 1s 2s 2p 3s 3p 4s 3d 11Na *1 – Diz-se que os elétrons estão em seu Estado Fundamental quando a distribuição eletrônica segue exatamente o Diagrama de Linus Pauling, garantindo que cada elétron ocupe a posição de menor energia que lhe é permitida. ORBITAL O orbital eletrônico pode ser encarado como mais uma subdivisão da eletrosfera, ou seja, dizemos que “um subnível de energia divide-se em orbitais”. Completando temos que: EM CADA ORBITAL CABEM, NO MAXIMO, DOIS ELÉTRONS. Observemos a representação gráfica de cada subnível em função dos orbitais que o formam: Subnível Representação (1) - bolinhas s p Forma dos Orbitais Na figura acima temos orbitais atômicos (1s, 2p, 3d, 4f) e orbitais moleculares (σs-s, σp-p e πp-p). De forma bastante simples dizemos que: ORBITAIS MOLECULARES SÃO FORMADOS QUANDO HÁ A FORMAÇÃO DE MOLÉCULAS ATRAVÉS DE UMA LIGAÇÃO QUÍMICA. ou seja, orbitais atômicos pertencem a átomos e orbitais moleculares a moléculas (conjunto de átomos). Não nos aprofundaremos mais por, aguardemos o tópico de Ligações Químicas, por vir. d Mostremos a seguir, em detalhe os orbitais atômicos de interesse imediato. f Subnível Representação (2) - retângulos s Orbital 1s p d Orbital 2p f Notemos que: - o subnível s posui somente um orbital - o subnível p apresenta três orbitais - o subnível d e f apresentam, respectivamente, cinco e sete orbitais. 2 Química Geral CASD Vestibulares No entanto o subnível p apresenta três orbitais, notemos a distribuição espacial desses três orbitais. Orientação Espacial dos Orbitais 2p Modelo do Spin eletrônico Temos de informação notável: - o orbital 1s tem simetria esférica - temos três orbitais 2p, cada um orientado por um eixo coordenado (x, y e z). - apesar de possuirem naturezas distintas, tanto um orbital 1s quanto um 2p contém no máximo 2 elétrons. Entendido o conceito de SPIN, enunciemos o Princípio da Exclusão de Pauli e em seguida a Regra de Hund, que serão nossos guias no procedimento sistemático de determinação de Configuração Eletrônica por Orbitais. Notemos a diferença de se dizer: UM SUBNÍVEL 2p AGREGA ATÉ 6 ELÉTRONS, e UM ORBITAL 2p AGREGA ATÉ 2 ELÉTRONS! PRINCÍPIO DA EXCLUSÃO DE PAULI: dois elétrons só ocupam o mesmo orbital se possuírem spins opostos. REGRA DE HUND: elétrons tendem a ocupar orbitais vazios, ou seja, um subnível só possui dois elétrons em um mesmo orbital no momento em que todos os orbitais ja receberam um elétron. Observe as distribuições abaixo: 2 2 6 1 11Na Æ 1s 2s 2p 3s DISTRIBUIÇÃO ELETRÔNICA ORBITAIS e o conceito de SPIN: EM 3s1 35Br A distribuição dos elétrons em orbitais é tão simples quanto as formas antecessoras, é como andar de bicicleta! Só se aprende tentando, e depois de aprendido NUNCA mais se esquece. Mas antes de subirmos em nossa bike irada! Temos de conhecer o conceito de SPIN. Não é intuitivo que dois elétrons (enfatizemos que ambos possuem carga elétrica negativa) consigam de forma agradável permanecer em um mesmo orbital uma vez que há uma força de repulsão que tenderia a afastá-los. Neste contexto e que surge o SPIN do elétron. Spin é a característica do elétron de se comportar como um ímã, devido a sua rotação ao redor de seu próprio eixo. Temos então somente duas possibilidades, rotação pra um lado com spin positivo e rotação para outro lado com spin negativo! CASD Vestibulares Æ 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5 4p5 Acima temos descrita a Configuração Eletrônica para o “último” Subnível de Energia, dito SUBNÍVEL DE DIFERENCIAÇÃO pois é o mais energético de todo o átomo. Mas por quê? Pense, tente, faça um cursinho diferente! Química Geral 3 Número Quântico de Spin: NÚMEROS QUÂNTICOS: De maneira MUITO informal podemos dizer que os Números Quânticos são o “endereço do elétron”, são um conjunto de quatro números que descrevem a energia do elétron no átomo. Dividem-se em: - Número Quântico Principal - Número Quântico Secundário - Número Quântico Magnético - Número Quântico de Spin Representado pela letra “S”, indica o spin do elétron, ou seja indica se o tal elétron é o primeiro o ocupar o orbital ou é o segundo. O Spin do elétron pode valer + ½ ou – ½. Nenhum outro valor é possível. Exemplos: Forneça o conjunto de números quânticos para o elétron de diferenciação dos seguintes átomos (Adote que o primeiro elétron a ocupar o orbital terá Spin Negativo): 11Na Número Quântico Principal: 0 Representado pela letra “N”, indica o nível de energia em que o elétron está. - N = 1, primeiro nível de energia - N = 2, segundo nível de energia 3s1 35Br Número Quântico Secundário: Representado pela letra “L”, indica o subnível de energia em que o elétron está, e consequentemente a forma do orbital. Subnível L s 0 p 1 d 2 f 3 Note que não basta se lembrar da letra que caracteriza o subnível, devemos lembrar também o Número Quântico Secundário que o caracteriza. Como regra geral temos: 76Os 0 ≤ L ≤ N −1 Representado pela letra “M”, indica o orbital em que o elétron esta dentro do subnível descrito pelo número quântico secundário. Como regra geral temos: −L ≤ M ≤ + L Observe a seguir a caracterização de cada orbital nos subníveis de interesse. 0 4 Æ Æ 1s2 2s2 2p6 3s1 N=3 L=0 M=0 S=–½ 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5 –1 ; 0 ; +1 N=4 L=1 M = +1 S=–½ 4p5 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d6 –2 ; –1 ; 0 ; +1 ; +2 N=5 L=2 M = –2 S =+½ 5d6 Quando não é fornecida convenção para o spin do elétron aconselha-se usar o valor ± ½. Número Quântico Magnético: –3 Æ Princípio da Heisenberg: Incerteza de Modernamente adota-se o conceito MecânicoOndulatório para o elétron, o que nos remete ao Princípio da Incerteza, que pode ser enunciado da seguinte forma: NÃO É POSSÍVEL DETERMINAR COM PRECISÃO A VELOCIDADE E A POSIÇÃO DO ELÉTRON EM UM MESMO INSTANTE DE TEMPO –1 0 +1 –2 –1 0 +1 +2 –2 –1 0 +1 +2 +3 Química Geral CASD Vestibulares 34Se Æ1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p4 (Ordem Energética) a A forma acima, como ja vimos exaustivametne, trata da ordenação dos elétrons de acordo com Energias Crescentes, então trata-se da Ordem Energética. CAMADA DE VALÊNCIA É O NÍVEL DE ENERGIA (CAMADA) MAIS EXTERNO NA ELETROSFERA DO ÁTOMO. A Ordem Geométrica traz os elétrons em ordem crescente de distância do núcleo: 2 2 6 2 6 10 4s2 4p4 (Ordem Geométrica) 34Se Æ1s 2s 2p 3s 3p 3d Camada de Valência e Configuração Eletrônica de Íons: Para nossos átomos-exemplo, o Sódio e o Bromo temos: 2 2 6 1 11Na Æ 1s 2s 2p 3s 1s2 2s2 2p6 3s1 onde identifica-se o 3º Nível de Energia como “Camada de Valência” 35Br EXERCÍCIOS: Æ 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5 Para se determinar a Distribuição eletrônica de Íons, basta retirar-se elétrons (no caso de Cátions) ou adicionar-se (no caso de 6Anions) A PARTIR DA CAMADA DE VALÊNCIA. Observemos o exemplo que segue: Ca2+ Æ (Configuração Eletrônica do átomo neutro) – 2e– Æ 1s2 2s2 2p6 3s2 3p6 4s2 Retirando-se 2 elétrons a partir da camada de valência temos: 2+ Æ 1s2 2s2 2p6 3s2 3p6 20Ca 20Ca ORDEM ENERGÉTICA GEOMÉTRICA E ORDEM É importante percebermos que os elétrons estão ordenados no átomos de acordo com suas ENERGIAS CRESCENTES, e não distância do núcleo crescente. Quando os elétrons estão ordenados de acordo com Energias Crescentes trata-se da Ordem Energética. Enquanto que quando de acordo com Distância do Núcleo crescentes diz-se Ordem Geométrica. No entanto vale lembrar que a ordem de energia é que rege a acomodação dos elétrons na eletrosfera do átomo. Exemplo: CASD Vestibulares 1-) Forneça a configuraçao eletrônica por subníveis dos seguintes átomos neutros no Estado Fundamental. (Lembre-se de não consultar o Diagrama de Linus Pauling, você deve memorizá-lo AGORA!) a-) 5B Æ b-) 12Mg Æ c-) 33As Æ d-) 10Ne Æ e-) 52Te Æ f-) 37Rb Æ g-) 84Po Æ h-) 64Gd Æ i-) 26Fe Æ 2-) Determine o Número Atômicos dos seguintes átomos neutros em seu Estado Fundamental com elétron de diferenciação nos subníveis: a-) 3s2 (11Na) b-) 5p3 (49In) c-) 5d10 (48Cd) d-) 3p5 (17Cl) e-) 4d1 (39Y) 3-) Determine o conjunto de números quânticos do elétron de diferenciação dos seguintes átomos neutros em seu Estado Fundamental. a-) 52Te Æ b-) 67Ho Æ c-) 8O Æ d-) 55Cs Æ e-) 78Pt Æ f-) 31Ga Æ Química Geral 5 4-) (VUNESP) Um átomo tem número de massa 31 e 16 nêutrons. Qual é o número de elétrons de seu nível mais externo? a-) 2 b-) 4 c-) 5 d-) 3 e-) 8 5-) (ESPCEX – 1996) Um átomo de número de massa 86 apresenta oito orbitais em subnível d. Portanto, o seu número de nêutrons é: a-) 42 b-) 44 c-) 45 d-) 47 e-) 64 6-) (IME – 2000 - Modificada) Para um possível elemento X de nº atômico Z = 119, determine: a-) sua configuração eletrônica por níveis e subníveis mais provável; b-) os valores dos números quânticos principal, secundário e magnético do último elétron; d-) sua configuração eletrônica supondo que o número quântico de spin possa assumir os valores 1/2, 0 ou 1/2, mantendo-se inalteradas as regras que governam tanto os valores dos outros números quânticos quanto a ordem de preenchimento dos subníveis. 7-) .(UFPB – 1995) Especifique os números quânticos do último elétron representado por 5d4. 8-) Esquematize os subníveis de maior energia dos átomos cujos elétrons de diferenciação apresentam os seguintes números quânticos: a-) n = 5; L = 0; m = 0; s = - ½ b-) n = 6; L = 0; m = 0; s = + ½ c-) n = 4; L = 2; m = +1; s = - ½ d-) n = 6; L = 1; m = 1; s = + ½ e-) n = 3; L = 2; m = 1; s = - ½ 9-) (UMC-SP) A transformação do átomo neutro Ca0 no cátion Ca2+ dá-se quando esse átomo: a-) adquire 2 prótons. b-) perde 2 prótons. c-) perde 2 elétrons. d-) adquire 2 nêutrons. e-) adquire 2 elétrons 12-) (VUNESP) Dentre as alternativas abaixo, indique a que contém a afirmação correta: a-) Dois átomos que possuem o mesmo número de nêutrons pertencem ao mesmo elemento químico. b-) Dois átomos com mesmo número de elétrons em suas camadas de valência pertencem ao mesmo elemento químico. c-) Dois átomos que possuem o mesmo número de prótons pertencem ao mesmo elemento químico. d-) Dois átomos que possuem o mesmo número de massa são isótopos. e-) Dois átomos com iguais números de massa são alótropos. 13-) (UFPI) Assinale a alternativa que representa um conjunto de números quânticos permitido: a-) n = 3; L = 0; m = 1; s = + ½ b-) n = 3; L = 2; m = 1; s = + ½ c-) n = 3; L = 3; m = 0; s = + ½ d-) n = 3; L = 4; m = 1; s = + ½ e-) n = 4; L = 0; m = 3; s = – ½ 14-) (FESP-SP) Em relação ao íons férrico (Fe3+) no estado fundamental, é correto afirmar que: (Fe (Z = 26). a-) ele apresenta apenas 24 elétrons distribuídos em seus orbitais. b-) ele apresenta cinco elétrons desemparelhados ocupando, cada um, um orbital “d’”. c-) ele apresenta dois elétrons no orbital 4s e três elétrons distribuídos em orbitais “d”. d-) ele apresenta seis elétrons distribuidos segundo a Regra de Hund em orbitais “d”. e-) so elétrons removidos para a formaçãp do íon foram todos retirados do terceiro nível de energia. 15-) (IME - 1999) Alguns elementos apresentam irregularidades na sua distribuição eletrônica já que as configurações d5, d10, f7 e f14 são muito estáveis. Por exemplo, o Cu (Z=29), em vez de apresentar a distribuição 1s2 2s2 2p6 3s2 3p6 4s2 3d9, apresenta 1s2 2s2 2p6 3s2 3p6 4s1 3d10. Determine os 4 números quânticos do elétron mais externo da prata (Z = 47) sabendo que o mesmo tipo de irregularidade ocorre para este elemento. 10-) (UFSE) Dentre os elementos seguintes qual o que apresenta 16 elétrons no terceiro nível energético? a-) 16S b-) 28Ni c-) 30Zn d-) 35Br e-) 40Zr 11-) (CESGRANRIO) Assinale o número atômico do átomo cuja configuração eletrônica no estado fundamental é [18Ar] 3d5 4s2: a-) 17 b-) 32 c-) 23 d-) 24 e-) 25 6 Química Geral CASD Vestibulares 9-) C 10-) A 11-) E 12-) C 13-) B 14-) B GABARITO: 1-) a-) 1s2 2s2 2p1 b-) 1s2 2s2 2p6 3s2 c-) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5 d-) 1s2 2s2 2p6 e-) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p2 f-) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 g-) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p4 h-) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f8 i-) 1s2 2s2 2p6 3s2 3p6 4s2 3d6 2-) a-) 11Na c-)48Cd e-) 39Y 3-) a-) 5p4 Æ 5; 1 ; –1 ; + ½ b-) 4f14 Æ 4 ; 3 ; 0 ; + ½ c-) 2p4 Æ 2 ; 1 ; –1 ; +½ d-) 6s1 Æ 6 ; 0 ; 0 ; – ½ e-) 5d8 Æ 5 ; 2 ; 0 ; + ½ f-) 4p1 Æ 4 ; 1 ; –1 ; – ½ 4-) C b-) 49In d-) 17Cl 15-) A distribuição eletrônica da prata (Z = 47) é 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d9 Entretanto, devido a estabilidade da configuração d10, a distribuição real é: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d10 O elétron mais externo, está no subnível 5s1, logo os números quânticos são: - Número Quântico Principal: n=5 - Número Quântico Secundário l=0 - Número Quântico Magnético m=0 - Número Quântico Spin s = -1/2 (utilizou-se a convenção -½,para elétron isolado no orbital.) 5-) C 6-) a-) 119X – 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f1 5d10 6p6 7s2 5f14 6d10 7p6 8s1 b-) O último elétron está no 8s1 N = 8; L = 0; M = 0; S = ± ½ d-) Com a suposição de que os spins podem valer +½, 0, – ½, então existiriam 3 elétrons por orbital. Com isso: Então, a configuração seria: 1s2 2s3 2p9 3s3 3p9 4s3 3d15 4p9 5s3 4d15 5p9 6s3 4f21 5d14, em um total de 119 elétrons. 7-) 5 ; 2 ; +1 ; – ½ 8-) a-) 5s1 b-) 6s2 c-) 4d4 d-) 6p6 e-) 3d4 CASD Vestibulares Química Geral 7
Download