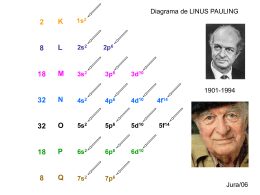
Química Prof. Nilsonmar Estrutura Atômica Prof. Thiago Cristófoli Química Partículas Fundamentais PRÓTON NÊUTRON Carga Relativa +1 0 Massa relativa 1 1 ELÉTRON –1 1/1836 Prof. Thiago Cristófoli Química Nº DE MASSA A=P+N Elemento Químico ÁTOMO P = e- CARGA = ZERO CÁTION ÍON ÂNION Nº ATÔMICO Z=P Nº DE ÁTOMOS Prof. Thiago Cristófoli Exemplo: Química átomo neutro: íon: 40 40 20 20 0 Ca Z = 20 P = 20 E = 20 N = 20 A = 40 Ca 2+ Z = 20 P = 20 E = 18 N = 20 A = 40 Prof. Thiago Cristófoli Isoátomos Química Isótopos São átomos com o mesmo número de prótons e diferentes números de massa. 1 H 1 Prótio 2 D 1 Deutério 3 T 1 Trítio Isóbaros São átomos de elementos químicos diferentes que possuem o mesmo número de massa. 40 Ca 20 40 Ar 19 Prof. Thiago Cristófoli Isoátomos: Química Isótonos São átomos de elementos químicos diferentes que possuem o mesmo número de nêutrons. 19 F 9 20 Ne 10 Isoeletrônicos São átomos ou íons com o mesmo número de elétrons. 3N 7 10 elétrons 2O 8 10 elétrons 1F 9 10 elétrons 0 Ne 10 10 elétrons 1+ Na 11 10 elétrons Prof. Thiago Cristófoli Química Semelhanças entre os átomos ISÓTO ISÓB ISÓTO OS ROS OS ISOEL TRÔNICOS Prof. Thiago Cristófoli Química Diagrama de Linus Pauling K 0 20Ca = 2 20Ca L 8 M 8 N 2 0 =1s2 2s2 2p6 3s2 3p6 4s2 Obs.: o diagrama coloca os subníveis em ordem crescente de energia. Linus Pauling ( 1901-1994) – Prêmio Nobel de Química em 1956 e Nobel da Paz em 1962. Prof. Thiago Cristófoli Química 0 =1s2 2s2 2p6 3s2 3p6 4s22 3d66 Fe 26 + energético último Prof. Thiago Cristófoli Química Cuidado!!! 2+ = 2 2s2 2p6 3s2 3p6 4s2 3d4 Errado!!! Fe 1s 26 2+ = 1s2 2s2 2p6 3s2 3p6 3d6 Fe Certo!!! 26 Prof. Thiago Cristófoli
Baixar