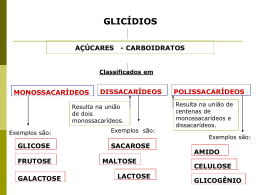
ANÁLISE BROMATOLÓGICAS CARBOIDRATOS Profa. Ionara F. R. Vieira INTRODUÇÃO São macronutrientes cujos maiores representantes pertencem ao reino vegetal, seja na forma de carboidrato complexo (amido e/ou celulose) ou na forma de açúcar (dissacarídeos) como a sacarose, além da glicose e da frutose, os monossacarídeos mais comuns da dieta. A fórmula geral é (CH2O)n INTRODUÇÃO Suas funções principais nos seres vivos são: energética (oxidação de glicose) reserva alimentar (amido e glicogênio) estrutural (celulose e quitina) genética (pentoses fazem parte do DNA e RNA) Fonte primária de energia para o organismo - liberação de energia química para a formação de ATP MONOSSACARÍDEOS Tabela 1. Fontes e papel nutricional dos principais monossacarídeos Monossacarídeos Fonte Função Componente dos ácidos nucléicos e coenzimas ácido ribonucléico (RNA), flavoproteínas D-ribose Formado nos processos metabólicos D-glicose “açúcar” dos corpo: Sucos de frutas, hidrólise do e dos açúcar, cana-de-açúcar, maltose e sangüíneos combustível celular lactose D-frutose Frutas, sucos, mel, hidrólise da sacarose da cana-de-açúcar Transformação para glicose no fígado e no intestino para servir como combustível básico do organismo D-galactose Hidrólise da lactose (açúcar do leite) Mudança para glicose no fígado; combustível celular; sintetizada na glândula mamária para produzir lactose do leite; constituinte dos glicolípides e glicoproteínas fluidos tecidos; Classificação: aldoses e cetoses. Propriedades: açúcares são geralmente sólidos cristalinos, incolores e têm sabor doce. São facilmente solúveis em água, e suas soluções são opticamente ativas. OLIGOSSACARÍDEO São polímeros compostos de resíduos de monossacarídeos unidos por ligações glicosídicas, em número que variam de duas até, aproximadamente, dez unidades. Entre os oligossacarídeos, os mais importantes são os dissacarídeos, e entre eles encontram-se a maltose, a celobiose, a lactose e a sacarose, sendo que apenas os dois últimos são encontrados livres na natureza; a maltose e a celobiose são obtidas por hidrólise do amido e celulose, respectivamente. OLIGOSSACARÍDEO Formação da ligação glicosídica entre um carbono anomérico α e o grupo hidroxila na posição 4, formando uma ligação α-1,4. DISSACARÍDEOS REDUTORES MALTOSE: É formada quando 2 moléculas de glicose unidas por ligação alfa. Elemento básico da estrutura do amido, podendo ser obtida por hidrólise ácida ou enzimática. É hidrolisada pela maltase. DISSACARÍDEOS REDUTORES LACTOSE: Açúcar comum do leite Hidrolisada por -galactosidase - ligação glicosídica em posição É o menos doce dos dissacarídeos, aproximadamente 1/6 da doçura da sacarose DISSACARÍDEOS NÃO REDUTORES SACAROSE: Açúcar de cana ou açúcar de beterraba - fotossíntese Dissacarídeo mais importante O grupo aldeído da glicose e o cetona da frutose estão envolvidos na ligação glicosídica, por isto a sacarose não é redutora. Hidrolisada por -glucosidade e invertase: ligação glicosídica é -Dglucose - -D-frutose INVERSÃO DA SACAROSE: A sacarose é hidrolisada por ácidos diluídos ou enzimas, resultando na reação do “açúcar invertido”. Vantagens: O xarope de açúcar invertido reúne: a elevada solubilidade da frutose à difícil cristalização da glicose, aumentando seu poder edulcorante (cabor doce) e diminuindo os riscos de cristalização (vasto uso na indústria alimentícia). POLISSACARÍDEOS Macromoléculas naturais ocorrendo em quase todos os organismos vivos Condensação de muitas unidades de monossacarídeos, unidas entre si por ligações glicosídicas Funções: Estrutura das paredes celulares de plantas superiores (celulose, hemicelulose, pectina) ou de animais (quitina, mucopolissacarídeos) Reservas metabólicas de plantas (amidos, dextranas) e de animais (glicogênio) Protetoras de plantas, devido à sua capacidade de reter grandes quantidades de água. AMIDO A mais importante reserva de nutrição de todas as plantas Estrutura do amido: amilose e amilopetina Variação de acordo com as espécies vegetais e grau de maturação Influenciam a viscosidade e o poder de formação de gel Amilose: Amido Corresponde de 15 a 20% da molécula de amido Macromolécula constituída de 250 a 300 resíduos de Dglicose, ligadas por pontes glicosídicas α-1,4, que conferem a molécula uma estrutura helicoidal. Amilopectina: Amido Macromolécula, menos hidrossolúvel que a amilose, constituída de aproximadamente 1400 resíduos de α-glicose ligadas por pontes glicosídicas α-1,4, ocorrendo também ligações α-1,6. A amilopectina constitui, aproximadamente, polissacarídeos existentes no grão de amido 80% dos MÉTODOS DE DETERMINAÇÃO MÉTODO POR DIFERENÇA Normalmente para a composição centesimal dos alimentos os carboidratos são analisados por diferença (NIFEXT): Carboidrato total = 100 - (proteína + umidade + cinzas + gordura) Ou Carboidrato = 100 - (proteína + umidade + cinzas + gordura + fibras) Carboidratos complexos = carboidrato total - açúcares – fibras Problema - incorporação de erros das outras determinações PREPARO DA AMOSTRA preparo da amostra: - sólida – moagem - Remoção de lipídeos e clorofila (geralmente removidos por extração com éter de petróleo). - Clarificação: Uso de agentes clarificantes (metais pesados), cuja função é de precipitar as substâncias que irão interferir na análise do açúcar como pigmentos solúveis, aminoácidos e proteínas, lipídeos, compostos fenólicos. Elimina a turbidez (proteína e amido solúvel), que afetam polarimetria e titulação. Agentes clarificantes: solução de acetato de chumbo, ácido fosfotungístico e ácido tricloroacético, ferricianeto de potássio e sulfato de zinco. MÉTODOS QUANTITATIVOS 1. Métodos Cuprimétricos Oxidação de açúcares redutores por soluções alcalinas quente de Cu +2. O açúcar degrada e reduz o Cu+2 (aq) em Cu2O (s). Métodos gravimétricos ou volumetricos. REAÇÃO CUPRIMÉTRICA COM AÇÚCARES 1.1. MÉTODO LANE-EYNON (MÉTODO CUPRIMÉTRICO) Açúcar redutor + reagente de Fehling A (sulfato de cobre) + Reagente de Fehling B ( tartarato duplo de Na+ e K+ / hidróxido de sódio (COR AZUL) Determinação dos açúcares redutores Inversão da sacarose + mesma reação Método Volumétrico Titulação à quente, usando azul de metileno como indicador Formação do precipitado de Cu2O (cor vermelho tijolo) Titulação Determinação dos açúcares totais = Redutores e não redutores 1.2. MÉTODO MUNSON-WALKER (MÉTODO CUPRIMÉTRICO) Açúcar redutor + reagente de Fehling A (sulfato de cobre) + Reagente de Fehling B ( tartarato duplo de Na+ e K+ / hidróxido de sódio em EXCESSO Formação de um precipitado: O açúcar degrada e reduz o Cu+2 formando Cu2O Método gravimétrico O precipitado de Cu2O é filtrado em cadinho de porcelana poroso Secagem e pesagem do precipitado Uso de tabela que relacionam o peso de Cu2O com a quantidade de açúcar 1.3 MÉTODO SOMOGYI (MÉTODO CUPRIMÉTRICO) Açúcar redutor + reagente de Fehling A + Fehling B em EXCESSO O açúcar degrada e reduz o Cu+2 formando Cu2O . O Cu+2 em excesso é oxidado por KI em excesso formando I2 Titula-se o excesso de iodo com Na2S2O4. Para pequenas quantidades de açúcar – microtitulação 2 – MÉTODO DO FERROCIANETO ALCALINO Foi desenvolvido para determinação de açúcares em sangue (1923) e modificado para alimentos (1929). Redução do ferrocianeto por açúcar redutor. Pode titular diretamente usando azul de metileno (indicador) Ou o excesso de iodo é titulado com tiossulfato. 2K3Fe(CN)6 + 2KI 2K4Fe(CN)6 + I2 Fe+3 Fe+2 3- MÉTODOS IODOMÉTRICOS Específico para aldoses, as cetoses não são oxidadas. A amostra dissolvidas é tratada com excesso de I2 e este titulado com solução de tiossulfato. RCHO + I2 + 3NaOH RCOONa + 2NaI + 2H2O 4- MÉTODOS CROMATOGRÁFICOS Açúcares determinados individualmente: separação dos diversos tipos. Podem isolar, fracionar, identificar e determinar quantativamente. a) Cromatografia de papel e camada delgada: Servem para isolar e identificar. De papel: não dá boa resolução e é demorado. Camada delgada – tempo de corrida é menor, melhor resolução. Limitados para identificação quantitativa (vários passos). b) Cromatografia gasosa: Separação, identificação e determinação de açúcares. Carboidratos são pouco voláteis, dificulta o uso da CG. c) Cromatografia de coluna: extensão predeterminada- secionada em zonas. Alta capacidade de separação. 5- MÉTODOS FÍSICOS a)Refratometria refratômetro – mede o índice de refração (quando a radiação eletromagnética passa de um meio para outro ela muda de direção, refrata); utilizada em alimentos onde a composição é predominantemente de água e açúcar (mel, xarope, geléias, sucos); mede o teor de sólidos solúveis (açúcares totais); teor de Grau Brix – tabela de conversão (índice de refração – teor de açúcares). b)Polarimetria Carboidratos são opticamente ativos- quirais; Mede a rotação óptica de solução pura de açúcar. Não é destrutivo, rápido e preciso. 5- MÉTODOS FÍSICOS c)Densimentria Mede a densidade exata de soluções de açúcar e aproximada em alimentos açucarados. Determina concentrações de açúcar em soluções líquidas. d)Espectroscopia de Infravermelho Usado para estudo das estruturas dos carboidratos. É complicado para açúcares simples – são praticamente insolúveis nos solventes orgânicos usados
Baixar