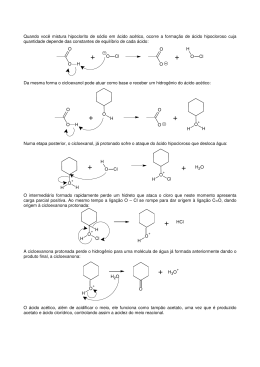
▼ Questão 5 Em um laboratório, há dois frascos com soluções aquosas diferentes: — Ácido acético de concentração 1,0 mol/L; — Ácido clorídrico de concentração 4,2 × 10 –3 mol/L. Fazendo dois testes, em condições iguais para as duas soluções, observou-se que, — ao mergulhar, nas soluções, os eletrodos de um aparelho para medir a condutibilidade elétrica, a intensidade da luz da lâmpada do aparelho era a mesma para as duas soluções; — ao adicionar a mesma quantidade de indicador universal para ácidos e bases a amostras de mesmo volume das duas soluções, a coloração final observada era a mesma. a) Explique por que duas soluções tão diferentes exibem comportamentos tão semelhantes. b) Considerando os valores fornecidos nesta questão, calcule a constante de dissociação iônica do ácido acético. Mostre os cálculos. Resolução a) O ácido acético é um ácido fraco, portanto pouco ionizado, enquanto o ácido clorídrico é forte, possuindo um grau de ionização de aproximadamente 100%. As duas soluções têm comportamento químico semelhante devido ao fato de terem uma concentração iônica semelhante. Isso ocorre porque, apesar de o ácido acético ser fraco, sua solução está mais concentrada do que a de ácido clorídrico. b) Como o HC é um ácido forte (α ≈ 100%), temos: H +(aq) HC(aq) C–(aq) + 4,2 ⋅ 10 –3 0 0 início gasta (≈ 100%) ≈ 4,2 ⋅ 10 –3 forma 4,2 ⋅ 10 –3 forma 4,2 ⋅ 10 –3 reação ≈0 4,2 ⋅ 10 –3 4,2 ⋅ 10 –3 equilíbrio A solução de ácido acético possui mesma condutividade elétrica, ou seja, mesma concentração de íons. Com isso, no equilíbrio do ácido acético, temos: CH3COO –(aq) CH3COOH(aq) Ka = H+(aq) + 1 0 0 início gasta 4,2 ⋅ 10 –3 forma 4,2 ⋅ 10 –3 forma 4,2 ⋅ 10 –3 reação ≈1 4,2 ⋅ 10 –3 4,2 ⋅ 10 –3 equilíbrio [CH3COO – ] ⋅ [H +] [CH3COOH] = (4,2 ⋅ 10 –3 ) ⋅ (4,2 ⋅ 10 –3 ) Ka = 17,6 ⋅ 10 –6 ≈ 1,8 ⋅ 10 –5 (1)
Baixar