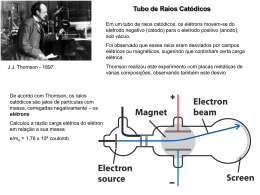
Dalton Dalton • Modelo “Bola de bilhar” • Esfera maciça indestrutível Modelo “Bola de bilhar” • Esfera homogênea • átomos de diferentes elementos podem se unir e formar compostos • nas reações químicas, os átomos não são criados, destruídos ou alterados • átomos iguais massas iguais • Átomos ≠ massas ≠ 2 Dalton 3 4 Thomson Thomson Thomson Thomson Tubo de Raios Catódicos Thomson • Modelo “pudim de passas” • Descobriu o elétron. • Tubos de raios catódicos. Rutherford Rutherford Rutherford • Modelo “Planetário” • Descobriu o núcleo. • Átomo imenso vazio. • Núcleo 10.000 x menor que o átomo. 15 Bohr AUMENTA A ENERGIA Modelo Atômico de Sommerfeld A. J. W. Sommerfeld (1868 — 1951) Descobriu que os níveis energéticos são compostos por SUBNÍVEIS DE ENERGIA (s, p, d, f) e que os elétrons percorrem ÓRBITAS ELÍPTICAS na eletrosfera, ao invés de circulares. Modelo Atômico Atual Louis de Broglie - DUALIDADE DA MATÉRIA: Toda e qualquer massa pode se comportar como onda. Heisenberg - PRINCÍPIO DA INCERTEZA: É impossível determinar ao mesmo tempo a posição e a velocidade do elétron. Se determinarmos sua posição, não saberemos a medida da sua velocidade e vice-versa. Schrödinger – ORBITAIS: Desenvolve o "MODELO QUÂNTICO DO ÁTOMO" ou "MODELO PROBABILÍSTICO", colocando uma equação matemática (EQUAÇÃO DE ONDA) para o cálculo da probabilidade de encontrar um elétron girando em uma região do espaço denominada "ORBITAL ATÔMICO".
Baixar