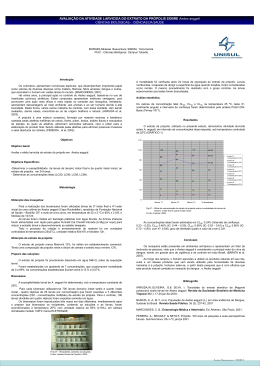
Rossana Vanessa Dantas de ALMEIDA* Ricardo Dias de CASTRO** Maria do Socorro Vieira PEREIRA*** Marçal Queiroz de PAULO**** Josemar Pereira SANTOS**** Wilton Wilney Nascimento PADILHA***** Cárie dentária; Própolis; Streptococcus mutans. Dental caries; Propolis; Streptococcus mutans. *Mestre em Odontologia Preventiva e Infantil - UFPB. Professora Responsável pela Disciplina de Odontopediatria da FACIMP (MA). ** Mestrando em Odontologia Social pela UFRN, Professor Substituto do Curso de Odontologia da UFRN. *** Professora Doutora da Universidade Federal da Paraíba. **** Professores Doutores da Universidade Federal da Paraíba. ***** Professor Doutor em Clínica Integrada pela Universidade de São Paulo. 87 A cárie dentária tem sido descrita como uma doença de etiologia multifatorial que necessita da interação entre fatores do hospedeiro, dieta e placa dental. O processo carioso não se desenvolve na ausência da placa dental ou de carboidratos fermentáveis oriundos da dieta sendo considerada uma doença dieta-bacteriana (BUISCHI, 2000; MALTZ, 2000; ZERO, 1999). Recentemente, o termo placa dental tem sido substituído por biofilme dental, que reflete a característica dinâmica de sua formação e composição. Na prevenção da cárie necessita-se de condutas direcionadas a minimizar o desafio cariogênico e aumentar a resistência da superfície dentária. Isto pode ser alcançado através do controle do biofilme dental mecânica e/ou quimicamente (STOOKEY, 1998). A remoção mecânica do biofilme é um fator importante na prevenção da cárie e igualmente da doença periodontal. Frente a limitações dos métodos mecânicos, recomenda-se lançar mão de agentes químicos visando o controle do biofilme. Dessa forma, os agentes químicos têm sido empregados com a finalidade de reduzir a população de microorganismos, em particular bactérias cariogênicas. Dentre os microrganismos encontrados no biofilme dentário, os S. mutans podem contribuir de forma expressiva no processo carioso (ZERO, 1999). Diversos trabalhos têm avaliado as propriedades antimicrobianas de substâncias indicadas na prevenção e controle do biofilme e da cárie. Algumas delas, como a clorexidina e os fluoretos, são bastante discutidas na literatura científica; outras ainda são pouco exploradas pela ciência odontológica, a exemplo dos extratos vegetais. Dentre os agentes empregados com potencial antimicrobiano, a clorexidina parece ser a substância que vem apresentando as melhores características em função de suas particularidades, (VINHOLIS et al, 1996). Os efeitos benéficos advindos do seu uso são documentados na literatura, onde vários estudos demonstraram o seu potencial antimicrobiano, inibindo o acúmulo de biofilme e o aparecimento da doença periodontal, além do efeito antimicrobiano seletivo, especialmente sobre S. mutans (PETERLINI et al, 1998; ZANELA et al, 1997; ZANELA; BIJELLA; ROSA, 2002). Por outro lado, seus efeitos colaterais não são poucos, podendo causar pigmentação dos dentes, interferência gustativa, descamação da mucosa e resistência de germes quando do uso diário prolongado, além de possuir sabor amargo (BARROS; FIORINI, 2000; CURY et al., 2000). Na Odontologia atual, produtos à base de extratos naturais vêm sendo empregados com propósito 88 terapêutico in vivo (PEREIRA, 2002). Grande parte dos produtos de origem vegetal apresenta em sua composição substâncias com atividade anticariogênica que podem suprimir o crescimento de bactérias presentes na cavidade bucal, além de inibir a síntese de glucano a partir da sacarose pela glicosiltransferase. A própolis é uma substância resinosa elaborada pelas abelhas da espécie Apis mellifera através da coleta de brotos, flores e exsudatos de plantas, nas quais as abelhas acrescentam secreções salivares, cera e pólen para elaboração final do produto (KOO et al., 2002b; MANARA et al., 1999). É encontrada nas colméias, onde é responsável pela impermeabilização, isolamento térmico, vedação e tratamento anti-séptico (SANTOS, 1999). Várias substâncias químicas têm sido isoladas da própolis, sendo os flavonóides considerado o composto biologicamente ativo (KOO et al 2002b). Tem sido relatada atuação antimicrobiana expressiva do extrato de própolis contra bactérias grampositivas e gram-negativas (FERREIRA; VALENTE; BARBOSA, 1996; WOISKY; GIESBRECHT; SALATINO, 1994), e especificamente contra bactérias colonizadoras do biofilme, (GEBARA; ZARDETTO; MAYER, 1996), além do efeito inibitório sobre a síntese de glucano (KOO et al, 2000) somado ao fato de sua capacidade de inibir o desenvolvimento da lesão cariosa em animais (IKENO; IKENO; MIYAZAWA, 1991; KOO et al., 1999). Sua incorporação em produtos de higiene oral tem sido estimulada pelos resultados promissores obtidos tanto na formulação de dentifrícios (BAAKILINI; LARA; PANZERI, 1996; PANZERI et al., 1999) como no emprego em soluções de bochecho, reduzindo os níveis de S. mutans (MORAES et al, 1996 STEINBERG; KAINE; GEDALIA, 1996; ZÁRATE-PEREIRA, 1999), o acúmulo de biofilme (KOO et al., 2002a; MURRAY; WORTHINGTON; BLINKHORN, 1997) e a doença gengival (DUARTE; KFOURI, 1999; MOTA, 2000). O presente estudo objetivou verificar a atuação de uma solução anti-séptica à base de própolis sobre índices clínicos de acúmulo de biofilme e doença gengival, bem como nos níveis salivares de S. mutans em crianças cárie ativa. Este estudo foi aprovado pelo Comitê de Ética em Pesquisa do Centro de Ciências da Saúde da Universidade Federal da Paraíba (47a Reunião Ordinária em 23/11/2003). Foram realizados testes in vitro a fim de se determinar à concentração do bochecho de própolis. A origem da própolis empregada é a região sul do estado de São Paulo e na obtenção do extrato esta foi pulverizada e macerada em meio hidroalcoólico, obtendo-se uma solução de própolis a 60% e determinada à atividade antimicrobiana sobre linhagem de S. mutans ATCC 25175 em meio sólido para determinação da Concentração Inibitória Mínima (CIM). Estabelecida a CIM do extrato de própolis, foi confeccionada a solução de bochecho conforme preconiza Zárate-Pereira (1999, 2003) que emprega uma concentração superior a CIM encontrada devido às condições inerentes da cavidade bucal. Dessa forma, foi empregada a solução de bochecho de própolis numa concentração de 6,25%. Por meio de ensaio clínico cruzado 15 crianças foram submetidas às soluções de própolis e clorexidina. Empregou-se inicialmente a solução própolis diariamente, por quinze dias consecutivos. Após o período de repouso de 21 dias (intervalo), as crianças utilizaram à solução controle (clorexidina) conforme o Quadro 1. Os bochechos foram diários, no mesmo horário, supervisionados e executados durante 60 segundos. Recomendava-se que após a realização dos bochechos as crianças aguardassem um período de 30 minutos para ingestão de alimento ou bebida. Nos finais de semana as soluções para bochecho foram entregues em potes identificados e orientados pelos responsáveis. Foram mensurados as condições doença gengival e acúmulo de biofilme dentário através do índice de sangramento gengival (ISG) e Índice de Higiene Oral Simplificado respectivamente, antes (T0) da aplicação das soluções de bochecho e 24 horas após (T1) o término do último bochecho em ambas as fases. Foram obtidas amostras salivares antes (T0) da aplicação das soluções de bochecho e após (24 horas T1; 7 dias T7; 15 dias T15; 21 dias T21) o término do último bochecho, em ambas as fases para contagem dos níveis de S. mutans. O meio de cultura empregado foi o Ágar Mitis Salivarius Bacitracina (MSB) segundo técnica preconizada por Gold, Jordan e Van Houte (1973). Q uadro 1. Dem onstração esquem ática dos tem pos (T 0, T 1 , T 7 , T 15 e T 21) avaliados no experim ento e ordem de em prego das soluções de bochecho. 1ª Fase Intervalo 2ª Fase Intervalo PRÓ PO LIS CLO REXIDINA Coleta de dados Coleta de dados T0 T 1 T 7 T 15 T 21 T0 T 1 T 7 T 15 T 21 15 dias 21 dias 15 dias 21 dias A Tabela 1 mostra os valores médios dos níveis salivares de S. mutans em UFC/mlx105 observados antes (T0) da aplicação das soluções de bochecho (própolis e clorexidina) e após (24 horas T1; 7 dias T7; 15 dias T15; 21 dias T21) o término do último bochecho. 15 30 21 8 Soluções T0 T1 T7 T 15 T 21 Própolis 9,52 2,63 6,10 2,83 8,79 Clorexidina 8,79 2,17 4,35 4,56 6,26 22 29 10 7 21 10 23 0 Própolis Antes A Figura 1 ilustra através de gráfico boxplot os diferentes níveis salivares de S. mutans obtidos antes e após o emprego das soluções de bochecho de própolis e clorexidina. 21 14 20 Tabela 1. Valores médios de S. mutans (UFC/mlx105) obtidos antes (T0) e 24 horas (T1), 7 dias (T7), 15 dias (T15) e 21 dias (T21) após a realização dos bochechos de própolis a 6,25% e clorexidina a 0,12%. 30 15 24 horas Clorexidina 7 dias 15 dias 21 dias Figura 1. Distribuição dos níveis salivares de S. mutans antes (T0) e 24 horas (T1), 7 dias (T7), 15 dias (T15) e 21 (T21) dias após a realização dos bochechos de própolis a 6,25% e clorexidina a 0,12%. 89 Os valores médios obtidos do Índice de Sangramento Gengival (ISG) e Índice de Higiene Oral Simplificado (IHOS) mensurados antes (antes - T0) e após (24 horas - T1) o término do último bochecho de própolis a 6,25% e clorexidina a 0,12% são apresentados na Tabela 2. Tabela 2. Valores médios do ISG e IHOS obtidos antes (T0) e 24 horas (T1) após a realização dos bochechos de própolis a 6,25% e clorexidina a 0,12%. Soluções T0 - ISG T1 - ISG T0 - IHOS T1 - IHOS Própolis 23,02% 14,61% 2,09 1,89 Clorexidina 17,58% 8,84% 2,36 2,07 Sendo a cárie dentária uma doença de caráter multifatorial, necessitando especialmente da interação entre bactérias e dieta cariogênicas, os S. mutans contribuem de forma significativa no desenvolvimento do processo carioso. Assim, soluções antimicrobianas podem ser empregadas na sua prevenção e controle, minimizando o risco e atividade. Diversos trabalhos investigaram a atividade antimicrobiana da própolis sobre diferentes microrganismos (PANZERI et al., 1999; WOISKY; GIESBRECHT; SALATINO, 1994), observando interferência no seu crescimento conforme a concentração e o contato com o extrato (FERREIRA; VALENTE; BARBOSA, 1996). Comparando a atuação das soluções teste (própolis) e controle (clorexidina) sobre as contagens de S. mutans obtidos nos diferentes momentos (Figura 1) observa-se que 24 horas após o término dos bochechos de própolis ocorreu ação expressiva sobre os níveis salivares, bem como da solução controle, com reduções de 72,3% e 75,3%, respectivamente. A atuação antimicrobiana observada neste estudo, sobre os níveis de S. mutans, coincide com os resultados obtidos por Moraes et al. (1996), Steinberg, Kaine e Gedalia (1996) e Zárate-Pereira (1999), conferindo a própolis eficiência sob a forma de bochechos diários. Conforme análise estatística, a solução de própolis a 6,25% interferiu de forma significativa no crescimento dos microrganismos (p<0,001), sendo observada redução semelhante quando do emprego da solução de clorexidina a 0,12% (p<0,01). Decorridos 21 dias da aplicação das soluções de bochecho, os níveis bacterianos se mostraram próximos aos valores iniciais, não identificando diferenças significativas entre estas contagens (T0 x T21) para ambas as soluções. Zárate-Pereira (1999) verificou que após 7 e 90 15 dias o término dos bochechos os níveis de S. mutans tendiam aos valores inicias. Em todas as contagens realizadas não foram encontradas diferenças estatisticamente significativas na atuação antimicrobiana das soluções de própolis e clorexidina sobre os níveis de S. mutans. O desempenho da solução de própolis sobre a condição gengival mensurada pelo ISG revelou redução significativa no incremento da doença (p<0,05), porém a clorexidina apontou maior potencial inibitório (p<0,01). Na literatura há relatos da atuação da própolis sobre a condição gengival, considerando-a um recurso terapêutico e preventivo no controle da doença periodontal. Mota (2000) verificou uma redução acentuada em relação ao sangramento gengival (27,3%) e à condição gengival (9,8%) com o uso de uma solução de própolis a 10%. Panzeri et al. (1999) verificaram redução significativa na condição gengival aos 15 dias (p<0,05) e 30 dias (p<0,01) após a utilização de um dentifrício contendo própolis a 3%. Contrário a esses resultados, Duarte e Kfouri (1999) não verificaram redução na condição gengival com uso de uma solução de própolis a 0,84%. Através do índice IHOS, o emprego da solução de própolis promoveu uma redução não significativa (p>0,05), diferindo da clorexidina (p<0,05). Este alteração não significativa sobre o acúmulo de biofilme dentário decorrente do uso da própolis concorda com os resultados encontrados por Murray, Worthington e Blinkhorn (1997) onde a clorexidina promoveu uma redução consideravelmente maior comparada à própolis. Duarte e Kfouri (1999) e Mota (2000) igualmente relataram redução não significativa resultante do uso da própolis, observando decréscimo de 13,3% e 5,4% respectivamente sobre o acúmulo de biofilme dentário. Assim, a solução própolis mostrou-se eficiente no controle químico do biofilme dentário, ratificando sua atuação como agente antimicrobiano, tendo desempenho clínico e microbiológico semelhante à solução de bochecho a base de clorexidina. A partir da metodologia empregada e dos resultados obtidos pode-se concluir que a solução de bochecho de própolis a 6,25% reduziu significativamente os níveis de S. mutans, atuou sobre as condições de doença gengival e acúmulo de biofilme, demonstrando comportamento semelhante ao da clorexidina, podendo ser indicado como agente químico terapêutico. BAAKILINI, M. F.; LARA, E. H. G; PANZERI, H. Adición de própolis en formulaciones de dentífricos. Evaluación de sus propriedade y estabilidad. Rev Fola Oral, São Paulo, v. 2, n. 6, p. 130-133, dez.1996. BARROS, L. M.; FIORINE, J. E. Efeito da clorexidina e da água ozonizada sobre os S. viridans da placa bacteriana supragengival. Rev Assoc Paul Cir Dent, São Paulo, v. 54, n. 1, p. 185-190, jan./fev. 2000. BUISCHI, Y. P. Promoção de saúde bucal na clínica odontológica. São Paulo: Artes Médicas, 2000. CURY, J. A.; ROCHA, E. P.; KOO, H.; FRANCISCO, S. B.; CURY, A. A. D. B. Effect of saccharin on antibacterial activity of chlorhexidine gel. Braz Dent J, Ribeirão Preto, v. 11, n. 1, p. 2934, jan./jun. 2000. DUARTE, C. A.; KFOURI, L. S. Ação da própolis sob a forma de bochechos na formação da placa bacteriana e gengivite. RGO, Porto Alegre, v. 47, n. 2, p. 82-84, abr./jun. 1999. FERREIRA, R. C. V.; VALENTE, P. H. M.; BARBOSA, A. D. Atividade antibacteriana da própolis. LECTA USF, Bragança Paulista, v. 14, n. 2, p. 65-93, jul./dez. 1996. GEBARA, E. C. E.; ZARDETTO, C. G. D. C.; MAYER, M. P. A. Estudo in vitro da ação antimicrobiana de substâncias naturais sobre S. mutans e S. sobrinus. Rev Odontol Univ São Paulo, São Paulo, v. 10, n. 4, p. 251-256, out./dez. 1996. MOTA, H. C. N. Avaliação clínica da própolis sobre a placa bacteriana e gengivite. 87f. Dissertação (Mestrado e Odontologia Preventiva). Natal: Faculdade de Odontologia da UFRN; 2000. PANZERI, H.; PEDRAZZI, V.; OGASAWARA, M. S.; ITO, I. Y.; LARA, E. H. G.; GABARRA, F. R. Um dentifrício experimental contendo própolis: avaliações físicas, microbiológicas e clínicas. Rev ABO Nac, São Paulo, v. 7, n. 1, p. 26-30, fev./mar. 1999. PERREIRA, J. V. Estudos com o extrato da Punica granatum Linn. (romã): efeitos antimicrobiano in vitro e avaliação clínica de um dentifrício sobre microrganismos do biofilme dental. 88f. Tese (Doutorado em Estomatologia), João Pessoa: UFPB/ UFBA, 2002. PETERLINI, C.; ELMADJAN NETO, M.; VALLE, P. D.; ROMERO, S. S. Efeitos adversos da clorexidina. Rev Odontol Univ Santo Amaro, São Paulo, v. 3, n. 1, p. 32-34, jan./jun. 1998. SANTOS, V. R. Própolis: antibiótico natural alternativo em Odontologia (revisão de literatura). Rev CROMG, Belo Horizonte, v. 5, n. 3, p. 192-195, set./dez.1999. STEINBERG, D.; KAINE, G.; GEDALIA, I. Antibacterial effect of propolis and honey on oral bacteria. Am J Dentistry, San Antonio, v. 9, n. 6, p. 236-239, Dec.1996. STOOKEY, G. K. Caries prevention. J Dent Educ, Washington, v. 62, n. 10, p. 803-811, 1998. GOLD, O. G.; JORDAN, H. V.; VAN HOUTE, J. A selective medium for Streptococcus mutans. Arch Oral Biol, Oxford, v. 18, n. 11, p. 1357-1364, Nov. 1973. TWETMAN, S.; GRINDEFJORD, M. Mutans streptococci supression by chlorhexidine gel in toddlers. Am J Dentistry, San Antonio, v. 12, n. 2, p. 89-91, Apr.1999. IKENO, K.; IKENO, T.; MIYAZAWA, C. Effects of propolis on dental caries in rats. Caries Res, Basel, v. 25, n. 5, p. 347-351, 1991. VINHOLIS, A. H. C. et al. Mecanismo de ação da clorexidina. Rev Periodontia, São Paulo, v. 5, n. 3, p. 281-283, jan./jun.1996. KOO, H.; ROSALEN, P. L.; CURY, J. A.; PARK, Y. K.; IKEGAKI, M.; SATTLER, A. Effect de Apis mellifera propolis from two brazilian regions on caries development in desalivated rats. Caries Res, Basel, v. 33, n. 5, p. 393-400, Sep./Oct. 1999. WOISKY, R. G.; GIESBRECHT, A. M.; SALATINO, A. Atividade antibacteriana de uma formulação preparada a partir de própolis de Apis mellifera. Rev Farm Bioquím Univ São Paulo, São Paulo, v. 30, n. 1, p. 19-21, jan./jun. 1994. KOO, H.; GOMES, B. P.; ROSALEN, P. L.; AMBROSANO, G. M.; PARK, Y. K.; CURY, J. A. In vitro antimicrobial activity of propolis and Arnica montana against oral pathogens. Arch Oral Biol, Oxford, v. 45, n. 2, p. 141-148, Feb. 2000. ZANELA, N. L. M. et al Influência de bochechos com soluções de digluconato de clorexidina a 0,2%, fluoreto de sódio a 0,05% pH 3,4 e esteviosídeo a 0,1% na inibição da placa dentária “in vivo”, em crianças. Rev Fac Odontol Bauru, Bauru, v. 5, n. 1/2, p. 71-78, jan./jun.1997. KOO, H.; CURY, J. A.; ROSALEN, P. L.; AMBROSANO, G. M.; IKEGAKI, M.; PARK, Y. K. Effect of a mouthrinse containing selected propolis on 3-day dental plaque accumulation and polysaccharide formation. Caries Res, Basel, v. 36, n. 6, p. 445448, Nov./Dec. 2002. KOO, H.; ROSALEN, P. L.; CURY, J. A.; PARK, Y. K.; BOWEN, W. H. Effects of compounds found in propolis on Streptococcus mutans growth and on glucosyltransferase activity. Antimicrob Agents Chemother, Washington, v. 46, n. 5, p. 1302-1309, May. 2002. MALTZ, M. Cárie dental: Fatores relacionados. In: PINTO, V. G. Saúde bucal coletiva. São Paulo: Santos, 2000. p. 319-339. MORAES, E.; OTA, C.; FANTINATO, V.; SHIMIZU, M. T. Influência da própolis na contagem de estreptoccocos do grupo mutans. In: Reunião Anual da SBPqO, 13, 1996. São Paulo: Sociedade Brasileira de Pesquisa Odontológica, 1996. p. 111. ZANELA, N. L. M.; BIJELLA, M. F. T. B; ROSA, O. P. S. The influence of muothrinses with antimicrobial solutions on the inhibition of dental plaque and on the levels of mutans streptococci in children. Pesq Odontol Bras, São Paulo, v. 16, n. 2, p. 101-106, abr./jun. 2002. ZÁRATE-PEREIRA, P. Análise da atividade de bochechos contendo fluoreto de sódio 0,05%; fluoreto de sódio 0,2% e própolis 5% acrescida de fluoreto de sódio 0,05%, sobre níveis salivares de estreptococos do grupo mutans em pacientes cárie-ativos. 74f. Dissertação (Mestrado). São Paulo: Faculdade de Odontologia da USP; 1999. ZÁRATE-PEREIRA, P. Avaliação in situ da ação de própolis de Apis mellifera no desenvolvimento da cárie dentária e na formação do biofilme dental. 116f. Tese de Doutorado. São Paulo: Faculdade de Odontologia da USP; 2003. 91 Pesq Bras Odontoped Clin Integr, João Pessoa, v. 6, n. 1, p. 87-92, jan./abr. 2006 ZERO, D. T. Dental caries process. Dent Clin North Amer, Philadelphia v. 43, n 4, p. 635-663, Oct. 1999. Recebido para publicação: 24/11/05 Enviado para reformulação: 13/12/05 Aceito para publicação: 16/01/06 Correspondência: Rossana Vanessa Dantas de Almeida Faculdade de Imperatriz - FACIMP Av. Prudente de Morais, s/n - Qd. 1 a 6 Resid. Kubitscheck Imperatriz - MA. CEP: 65900-000 E-mail: [email protected] 92
Baixar