R$ 5,00 ano III número 18 janeiro/fevereiro de 2001 BIOTECNOLOGIA/KL3 REPETE FOTOLITO 2 Biotecnologia Ciência & Desenvolvimento BIOTECNOLOGIA/KL3 REPETE FOTOLITO Biotecnologia Ciência & Desenvolvimento 3 Biossegurança no Brasil segue padrões científicos internacionais Entrevista concedida a Lucas Tadeu Ferreira ENTREVISTA A dicotomia entre ciência e sociedade não é privilégio deste século O Brasil ingressou efetivamente na era das pesquisas e desenvolvimento de Organismos Geneticamente Modificados OGMs, conhecidos também como produtos transgênicos, somente no ano de 1995. Neste ano, o Congresso Nacional aprovou e o Presidente da República sancionou a Lei de Biossegurança (n.o 8.974/95), além de ter aprovado o seu Decreto regulamentador (n.o 1.752/95), instituindo, assim, no âmbito do Ministério da Ciência e Tecnologia, a Comissão Técnica Nacional de Biossegurança - CTNBio, único órgão responsável pela regulamentação e liberação de OGMs no nosso País. Está previsto nestes dispositivos legais, entre outros, que as instituições públicas e privadas interessadas em desenvolver projetos de pesquisa de OGMs têm que requerer obrigatoriamente à CTNBio um Certificado de Qualidade em Biossegurança (CQB), implantar uma comissão interna de biossegurança e designar um técnico responsável para cada projeto de pesquisa que envolva a aplicação da tecnologia do DNA recombinante. Elas têm ainda que encaminhar os projetos de OGMs à CTNBio para aprovação, e ficam sujeitas a fiscalizações e às diversas penalidades administrativas, civis e criminais previstas na citada Legislação, em caso de descumprimento. Biossegurança e transgênicos são, portanto, temas bastante relevantes para a sociedade brasileira atualmente, como um todo, ao mesmo tempo difíceis de compreensão, e estão inseridos numa complexa rede de poder e interesses, já que têm implicações éticas, políticas, econômicas, religiosas, legais etc. Para falar um pouco do estado da arte dos transgênicos e da biossegurança, no Brasil, e do funcionamento da CTNBio, órgão do qual participa desde a sua criação e que passou a presidir em agosto de 1999, a pesquisadora da Fundação Instituto Oswaldo Cruz, LEILA MACEDO ODA, concedeu esta entrevista a Lucas Tadeu Ferreira para a revista BIOTECNOLOGIA Ciência & Desenvolvimento. LEILA ODA é pesquisadora da Fiocruz, graduada e mestre em Química, tendo feito Doutorado em Microbiologia pela UFRJ. Em 1995, se especializou em avaliação de riscos de OGMs no International Center for Genetic Engineering and Biotechnology ICGEB, Trieste, Itália. 4 Biotecnologia Ciência & Desenvolvimento BC&D O que motivou a senhora a aceitar a presidência da CTNBio e a partir de quando? Leila Oda - A biossegurança faz parte da minha vida profissional desde 1983, quando pela primeira vez participei de um evento promovido pela Organização Mundial de Saúde (OMS Genebra). Naquela época, a biossegurança começava a se estabelecer como uma nova Ciência que objetivava a minimização de riscos. De lá para cá, sempre tive como objetivo profissional, como cientista microbiologista, entender que o desenvolvimento científico e tecnológico não pode colocar em risco o homem e o meio ambiente. Daí, a biossegurança passou a ter um papel fundamental no desenvolvimento de minhas atividades. Quando o Brasil entendeu a importância da tecnologia do DNA recombinante para o seu desenvolvimento científico e tecnológico, também simultaneamente entendeu a importância de que esta tecnologia teria que ser controlada e avaliada criteriosamente para que não houvesse riscos para o homem e o meio ambiente. A Lei de Biossegurança, na qual eu tive a possibilidade de colaborar na contextualização técnica, vem exatamente permitir este controle. Quando a Lei 8974 foi aprovada pelo Congresso Nacional em 1994, e homologada pelo executivo em janeiro de 1995, eu tive a grata satisfação de ver todo um esforço reconhecido, sendo convidada pelo Ministério da Saúde para representá-lo na CTNBio. Participo da Comissão desde a sua primeira reunião, em junho de 1996, presidida pelo Exmo Vice-Presidente da República, Marco Maciel, autor do anteprojeto de Lei. O desafio de ser Presidente da CTNBio foi uma nova etapa na minha jornada em prol de uma causa na qual acredito que só quando a ciência é desenvolvida de uma forma ética e responsável pode contribuir para a superação dos desafios da humanidade e promover o bem-estar social. Foi por isso que eu aceitei em agosto de 1999 ser Presidente da Comissão, ao ser indicada pelos membros e nomeada pelo Exmo Sr. Ministro da Ciência e Tecnologia. BC&D - Quantos são, qual o perfil e como é feita a escolha dos técnicos que integram a CTNBio? Leila Oda - A CTNBio é composta por 36 membros, sendo 18 titulares e 18 suplentes, tendo representantes de 6 Ministérios (Ciência e Tecnologia, Saúde, Agricultura, Meio Ambiente, Educação, Relações Exteriores), 8 representantes da comunidade científica indicados pelas sociedades científicas, representante de órgãos de defesa do consumidor, de proteção à saúde do trabalhador e do setor empresarial de biotecnologia. Os representantes dos Ministérios são indicados pelos respectivos Ministros das pastas e os membros da comunidade científica devem ser doutores (Ph.D) na temática da biotecnologia e áreas afins. Todos são nomeados pelo Ministro de Estado da Ciência e Tecnologia, a partir de uma lista tríplice. O importante a ressaltar é que todos os membros devem ter um perfil técnico, pois a Comissão avalia tecnicamente cada Organismo Geneticamente Modificado.- OGM. "Infelizmente, devido aos impedimentos judiciais, não podemos ainda hoje dispor desses dados no Brasil, o que é uma lástima, pois certamente iriam contribuir bastante para o aprimoramento das ações de controle e para o desenvolvimento da própria tecnologia" BC&D Por que os Organismos Geneticamente Modificados OGMs (ou transgênicos) têm que ser objeto de análise pela CTNBio? Leila Oda - O Brasil optou por um modelo regulatório da tecnologia do DNA recombinante, que prevê a análise caso a caso de cada Organismo Geneticamente Modificado antes que sejam realizadas pesquisas ou liberações no meio ambiente, de modo a prevenir possíveis riscos. A análise e os procedimentos de manejo de risco são essenciais para permitir o desenvolvimento seguro desta tecnologia no Brasil. Os procedimentos adotados pela CTNBio são os preconizados internacionalmente e seguidos por países que já vêm utilizando esta tecnologia há mais de 5 anos. A CTNBIO elaborou 20 Instruções Normativas de forma a regular todos os procedimentos que devem ser seguidos no Brasil para que as atividades com OGMs possam ser realizadas de forma segura. BC&D Quando os primeiros produtos transgênicos estarão disponíveis no mercado brasileiro? Por que nenhum está sendo legalmente comercializado até hoje? Leila Oda - São várias as etapas que devem ser cumpridas até que um produto possa ser comercializado no Brasil. A primeira etapa exige que a instituição ou empresa tenha um Certificado de Qualidade em Biossegurança, que atesta sua competência, responsabilidade e idoneidade. Depois, a CTNBio deve analisar e aprovar os projetos de pesquisa em contenção e as liberações planejadas no meio ambiente brasileiro de forma controlada para mensurar possíveis riscos (são necessários inúmeros experimentos nas mais diversas condições edafoclimáticas). Só então, após esses resultados, é que o solicitante pode fazer um pedido para a comercialização do OGM. O único OGM que cumpriu todas essas etapas até agora foi a soja tolerante ao herbicida glifosato, que teve parecer favorável da CTNBio para comercialização no Brasil. Entretanto, uma ação judicial colocou sub-judice este parecer e até hoje o Brasil não pode plantar este OGM para fins comerciais. A CTNBio também analisou a segurança alimentar das variedades de milho transgênico atualmente comercializadas no mundo e emitiu parecer favorável para a comercialização desses produtos como ração animal. Embora várias ações jurídicas também tenham sido demandadas, não existe impedimento técnico ou jurídico para a importação de milho transgênico para consumo em ração animal. Apenas esses produtos passaram até então por todo o crivo necessário à comercialização segura no país. BC&D Para a análise e liberação de OGMs a CTNBio mantém parcerias ou acordos com outras instituições ou recorre a consultores nacionais ou internacionais? Leila Oda - Cada caso que é submetido à CTNBio sofre análise de pelo menos Biotecnologia Ciência & Desenvolvimento 5 2 pareceristas de cada área específica, na maioria das vezes são os próprios cientistas da CTNBio que procedem à análise, mas algumas vezes também são solicitados pareceres de especialistas ad hoc nacionais. A CTNBio também mantém contatos com especialistas estrangeiros das Comissões de Biossegurança e órgãos de governo de outros países para permitir o intercâmbio de informações científicas sobre o tema. BC&D O que está faltando para que as liberações de OGMs pela CTNBio estejam sincronizadas com o Poder Judiciário, já que a Comissão libera e a Justiça impede a liberação? Leila Oda - Acredito que o grande problema que levou a este impasse foram os dois vetos da Lei 8974 pelo poder executivo. A Lei, na forma original aprovada pelo Congresso Nacional, delegava à CTNBio a competência exclusiva de emitir o parecer técnico final sobre qualquer matéria relacionada à tecnologia do DNA recombinante. Entretanto, os vetos aos artigos que criavam a CTNBio e atribuía suas competências, deixaram dúvidas quanto ao poder da Comissão, gerando inúmeras ações jurídicas. Acreditamos que agora com a edição da Medida Provisória, que resgata os poderes da CTNBio aprovados originalmente pelo Congresso Nacional, em 1994, este impasse será resolvido. BC&D Como serão monitorados e avaliados no campo e no mercado os OGMs liberados pela CTNBio? Leila Oda - Cada caso deve ser considerado de forma particular. Para o caso da soja tolerante ao glifosato, a CTNBio estabeleceu que as áreas de plantio deveriam ser monitoradas por pelo menos cinco anos, onde a partir de uma modelagem experimental, previamente aprovada pela CTNBio, seria previsto o monitoramento com a participação inclusive de representantes da sociedade civil. Infelizmente, devido aos impedimentos judiciais, não podemos hoje ainda dispor desses dados no Brasil, o que é uma lástima, pois certamente iriam contribuir bastante para o aprimoramento das ações de controle e para o desenvolvimento da própria tecnologia. 6 Biotecnologia Ciência & Desenvolvimento BC&D Os produtos transgênicos poderão representar algum risco para a megabiodiversidade brasileira, já que existe a possibilidade de cruzamentos de plantas transgênicas com culturas silvestres ou primitivas? Leila Oda - O objetivo da CTNBio é exatamente o de analisar cada caso à luz do conhecimento científico, de modo a evitar riscos ao homem e ao meio ambiente. Cada característica específica do OGM, tais como o gene inserido, a característica reprodutiva da espécie, as condições edafoclimáticas onde o OGM será liberado, a possibilidade de transferência do gene, a estabilidade da construção, entre outras inúmeras informações, são exigidas do interessado para que a CTNBio possa emitir o seu parecer conclusivo sobre a segurança daquele OGM. BC&D Em seus pareceres, a CTNBio prevê a necessidade de zoneamento agro-ecológico para o cultivo de transgênicos? Leila Oda - Cada condição experimental é pré-avaliada e estabelecida, incluindo, aí, o distanciamento necessário e o isolamento para aquele OGM e a cultura específica. É claro que existe uma grande diversidade de condutas a serem adotadas em função das características do OGM. Por exemplo, para o caso do arroz modificado geneticamente, a cultura exige cuidados de isolamento e monitoramento muito mais rigorosos do que, por exemplo, para o caso da soja, em função da possibilidade de cruzamento das espécies de arroz e da existência do arroz vermelho, que é considerada uma grande praga na agricultura. É por isto que a CTNBio analisa cada situação específica e dimensiona o risco e as medidas necessárias para o manejo do risco inerente ao OGM e às condições experimentais específicas. BC&D O Brasil já dispõe de uma política de biossegurança e também de protocolos de análise de risco ambiental aceitos pela comunidade científica? Leila Oda - As normas utilizadas pela CTNBio estão dentro dos parâmetros estabelecidos internacionalmente por órgãos como a Organização Mundial de Saúde e a FAO. Além disso, a comunidade científica participa da CTNBio através de seus representantes como representantes da SBPC, Sociedade Brasileira de Genética, Academia Brasileira de Ciências, entre outras. Entretanto, é importante ressaltar que o consenso científico não existe em nenhuma área da ciência. As decisões da CTNBio sobre cada caso são sempre pautadas no que existe de melhor e mais recente do conhecimento científico nacional e internacional, estando sempre atenta aos avanços da ciência. BC&D - Muitas empresas estão desenvolvendo produtos transgênicos visando à produção de fármacos, ou seja, biofábricas de medicamentos. Pedidos já foram protocolados na CTNBio nesse sentido? Leila Oda - O Brasil, mesmo antes da Lei de Biossegurança, já utilizava fármacos e vacinas produzidas pela tecnologia do DNA recombinante, como a vacina contra hepatite B e a insulina. Hoje, temos no país cerca de 130 instituições credenciadas para pesquisa com OGMs, na sua maioria (80%) são instituições públicas que desenvolvem projetos que visam à obtenção de fármacos e vacinas em plantas, tais como vacina para leishmaniose, hepatites virais e doenças diarréicas que constituem grave problema de saúde pública no nosso país. Entretanto, todas essas pesquisas ainda levarão certo tempo até podermos disponibilizar o produto para comercialização. O importante é que o Brasil dispõe da tecnologia e tem mecanismos de controlar possíveis riscos, o que se constitui na missão da CTNBio. BC&D - Que procedimentos técnicocientíficos são recomendados pela CTNBio para evitar ou reduzir os riscos biológicos dos transgênicos à saúde humana? Leila Oda - Entre os aspectos importantes para a saúde humana a CTNBio avalia possíveis problemas relacionados a características alergênicas de proteínas expressas pelo transgene. É fundamental assegurar que nenhum produto que possua proteínas alergênicas não previstas no produto convencional seja liberado para consumo humano. Outro aspecto importante é o da isenção de substâncias tóxicas ou que possam causar algum dano ao organismo, ou ter interações indesejáveis com outros elementos. São exigidos pela CTNBio uma bateria de ensaios tanto in vitro como in vivo que permitam comprovar essas informações. Além disso, é fundamental que as características nutricionais do alimento sejam mantidas. O consumo de um alimento geneticamente modificado não deve introduzir nenhuma variável que venha prejudicar a saúde humana; muito pelo contrário, já estão sendo desenvolvidos alimentos que possuem características nutricionais melhoradas para reduzir doenças cardíacas ou com maior teor vitamínico. BC&D - Os OGMs podem aumentar a toxicidade natural das plantas e modificar as suas características nutricionais? Leila Oda - É claro que podem ser desenvolvidos OGMs que incorporem em sua composição elementos tóxicos ou alergênicos, como foi o caso do feijão com o gene da castanha do Pará. Como todos sabem, a castanha do Pará possui proteínas com características alergênicas e, ao transferir-se um gene da castanha do Pará para o feijão, esta característica foi transferida. Por isso mesmo que este produto não chegou às prateleiras, pois a análise de risco evidenciou este efeito. Este é o papel da CTNBio, analisar cada caso e permitir que apenas produtos seguros sejam liberados para consumo. BC&D Na sua opinião, os Ministérios da Agricultura, Saúde e Meio Ambiente estão suficientemente equipados para fiscalizar e monitorar os produtos transgênicos em todo o País? Leila Oda - O problema da fiscalização é um dilema em todos os países do mundo. Temos ouvido freqüentemente o recall de produtos e problemas como o da vaca louca e a dioxina, entre outros. Isto não tem nada a ver com transgênicos e, no entanto, representam grave problema de saúde pública. É importante fortalecer e descentralizar as ações fiscalizatórias que não são responsabilidade apenas do governo federal. Os estados e municípios devem ter programas sistemáticos de capacitação dos seus fiscais e de monitoramento da qualidade dos produtos e serviços oferecidos para a população, independentemente de serem transgênicos ou não. BC&D - Quais são as vantagens comparativas e potenciais que os transgênicos oferecem para os produtores rurais e consumidores? Leila Oda - Temos muito poucos dados até então sobre vantagens sócio-econômicas do uso comercial de transgênicos no mundo, porque somente agora esses estudos começam a ser concluídos. É claro que mais uma vez quero ressaltar que não podemos generalizar. Alguns produtos poderão ter vantagens e outros não. Mas, certamente, aqueles que não representarem uma vantagem para quem planta não irá sobreviver no mercado. Podemos citar o exemplo da China que vem intensificando o cultivo de transgênicos e observou que, por exemplo, o cultivo do algodão Bt reduz em até 8 vezes o uso de defensivos agrícolas, elevando a produção e con- "Que futuro teriam nossas instituições de pesquisa investindo 5, 10, 15 anos ou mais em pesquisa se elas não teriam como aplicar o que está sendo desenvolvido?" seqüentemente reduzindo os custos. Para sabermos o que acontecerá no Brasil, só quando tivermos nossos próprios dados, mas o indicativo desses mesmos dados da China, nos deixam otimistas, pelo menos quanto ao benefício para a saúde e para o meio ambiente pela redução no uso de agrotóxicos. BC&D - Por quê, na sua avaliação, determinados segmentos representativos da sociedade civil mídia, partidos políticos, ONGs, órgãos de defesa do consumidor etc. são contrários à pesquisa, desenvolvimento e comercialização de produtos transgênicos no Brasil e no exterior? Leila Oda - A dicotomia entre ciência e sociedade não é privilégio deste século. Sempre houve resistência por parte da sociedade à descobertas e tecnologias que ela não via de imediato a sua aplicação ou sentia segurança quanto ao seu uso. Por outro lado, os inúmeros desastres causados pela falta de controle de algumas das descobertas humanas contribuem para este cenário de espanto, medo e resistência. Entretanto, a ciência tem contribuído para solucionar inúmeros problemas de saúde pública e aumentar a expectativa de vida do homem. Na minha opinião, não será negando o desenvolvimento científico que avançaremos. Será, sim, estabelecendo mecanismos de controle legítimos e éticos, onde a sociedade sinta-se parte do processo. A Lei de Biossegurança, aprovada pelo Congresso Nacional representa a forma mais legítima de participação social no desenvolvimento de uma tecnologia no país. BC&D O que está faltando, ou não está sendo conduzido de forma correta, na interlocução da comunidade científica favorável aos transgênicos com a sociedade? Leila Oda - O cientista sempre foi refratário a sair do seu laboratório e interagir com a sociedade. É muito difícil transmitir a informação científica de forma clara para ser assimilada pelo leigo. Nem sempre somos bem sucedidos em comunicar o que queremos, sobretudo quando existem lacunas entre os diferentes aspectos do conhecimento científico. Seria fundamental dispormos de interlocutores que permitissem a passagem da informação de forma clara e precisa, estabelecendo o elo entre o cientista e a sociedade. Acho que, neste caso, o papel de jornalistas científicos especializados e que possuam o dom da comunicação supriria esta lacuna. BC&D A CTNBio é favorável à rotulagem dos produtos geneticamente modificados? Quais as vantagens ou desvantagens que a rotulagem pode proporcionar aos consumidores? Leila Oda - A rotulagem transcende as competências da CTNBio, estando no âmbito do Código de Defesa do Consumidor. A rotulagem de um produto deve transmitir informações corretas sobre as características nutricionais e de composição do produto, permitindo a livre escolha do consumidor. Um alimento para ser disponibilizado para consumo deve antes de mais nada ser Biotecnologia Ciência & Desenvolvimento 7 seguro e apresentar a qualidade exigida, portanto o papel da CTNBio antecede ao da rotulagem, pois se um OGM não for considerado seguro jamais ele poderá ser utilizado para o consumo. A desinformação sobre o real papel da rotulagem tem levado a argumentações de alguns segmentos de que devemos exigir o rótulo, pois não sabemos se o transgênico é seguro ou não. Este argumento mostra o nível de desinformação sobre o real papel da rotulagem e confunde o consumidor, tornando-o refratário, pondo por terra todo o trabalho de avaliação e controle realizado pela Comissão. BC&D E qual a posição oficial da Comissão em relação à necessidade ou não da moratória dos produtos transgênicos? Leila Oda - Eu entendo a proposta de moratória como uma tentativa de paralisar o desenvolvimento científico e tecnológico no Brasil. Estamos vivendo em um mundo globalizado onde o incremento da área mundial plantada com transgênicos cresceu de zero em 1995 para 45 milhões de hectares em 2000. Que vantagens teria o Brasil em não utilizar esta tecnologia para fins comerciais? Que futuro teriam nossas instituições de pesquisa investindo 5, 10, 15 anos ou mais em pesquisa se elas não teriam como aplicar o que está sendo desenvolvido? Isto faria com que os outros países que estão plantando e comercializando há mais de 5 anos parassem? Se existe um incremento nas áreas plantadas com transgênicos, sobretudo em países desenvolvidos, então é porque, certamente, benefícios econômicos, sociais e outros estão sendo obtidos por esses países. Sabemos que, se não tivermos competitividade em um mercado globalizado, o país perecerá, sobretudo por possuir uma economia fortemente de base agrícola. As conseqüências sociais e econômicas disso podem ser imprevisíveis: elevação do preço dos alimentos, diminuição de áreas virgens em busca de um aumento na produção, uso cada vez maior de defensivos agrícolas e conseqüentemente maior dano ambiental e para a saúde, menor investimento em C&T, entre outras. Por outro lado, a lógica da moratória, se é que tem alguma lógica, propõe de forma abstrata um período de 5 anos 8 8 Biotecnologia Ciência & Desenvolvimento Biotecnologia Ciência & Desenvolvimento sem plantio comercial de transgênicos. A minha pergunta é: o que muda em 5 anos se o Brasil estará impedido de ter seus próprios dados a partir da experiência vivida? Porque 5 anos e não 10, 15 ou 20 anos? Eu, como cientista, não posso aceitar uma proposta sem que haja uma argumentação científica para o fato. BC&D Diante de todo esse cenário dos OGMs, na sua opinião, quem perde e quem ganha com a pesquisa e o desenvolvimento dos produtos transgênicos no Brasil e no exterior? "É fundamental assegurar que nenhum produto que possua proteínas alergênicas não previstas no produto convencional seja liberado para consumo humano. Outro aspecto importante é o da isenção de substâncias tóxicas ou que possam causar algum dano ao organismo, ou ter interações indesejáveis com outros elementos. São exigidos pela CTNBio uma bateria de ensaios tanto in vitro como in vivo que permitam comprovar essas informações. Além disso é fundamental que as características nutricionais do alimento sejam mantidas" Leila Oda - A Ciência deve ter, no final da linha, um objetivo social. Eu, enquanto pesquisadora da área da saúde, acredito que a tecnologia do DNA recombinante abre uma perspectiva sem precedentes para darmos resposta a uma gama de problemas de saúde pública. A possibilidade de termos uma planta vacina, um fármaco produzido em plantas modificadas, enriquecermos o valor nutritivo de alimentos ou diminuirmos o uso de agrotóxicos, me parecem bastante meritórios para não investirmos nesta tecnologia. Se pararmos e pagarmos para ver o que acontece em outros países, corremos o risco de perdermos o trem da história e aumentarmos ainda mais a desigual- dade sócio-econômica pela dependência tecnológica. BC&D A transgenia tem impactos na saúde, no meio ambiente, na economia, na religião, nas relações internacionais, na propriedade intelectual e industrial. Quais devem ser os limites éticos das pesquisas com OGMs? Leila Oda - A ética deve estar presente balizando todo desenvolvimento científico. A reflexão ética possibilita que a aplicação de uma descoberta científica traga reais benefícios para a humanidade. Nenhuma tecnologia assustou tanto o homem como esta, pelo simples fato de estar manipulando o que foi sempre considerado a essência da vida a molécula do DNA. A busca incessante do homem por alternativas que permitam a sobrevivência da espécie humana é o que o diferencia das outras espécies. Nunca uma tecnologia foi tão discutida e avaliada. Talvez se outras descobertas tivessem tido este mesmo balizamento crítico social teríamos evitado muitos desastres e aplicações impróprias. Certamente, a ética será o esteio para o desenvolvimento e aplicação desta tecnologia em prol da humanidade. Um Código de Ética de Manipulações Genéticas deverá refletir o pensamento de uma sociedade e o que ela quer para melhorar sua qualidade de vida e minimizar o seu sofrimento. BC&D - O Parlamento Britânico aprovou recentemente o uso e a clonagem de células-tronco obtidas de embriões humanos para o desenvolvimento de pesquisas biotecnológicas com fins terapêuticos. Qual a sua avaliação a respeito desta medida dos britânicos? Leila Oda - Todo cidadão tem direito à vida e a um ambiente saudável. Este é um dos princípios basilares da nossa Carta Magna. A terapia com célulastronco abre a possibilidade de darmos o direito à vida a milhares de cidadãos que necessitam de um transplante de órgãos. Estaríamos sendo éticos com esses cidadãos negando a eles esta possibilidade? Acho que a sociedade brasileira tem que se informar, refletir e participar do debate de forma consciente. PORTAL WWW.BIOTECNOLOGIA.COM.BR (Repete fotolito) Obs.: Saiu na página 9 da edição anterior (nº17) Biotecnologia Ciência & Desenvolvimento 9 Carta ao Leitor BIOTECNOLOGIA Ciência & Desenvolvimento KL3 Publicações Fundador Henrique da Silva Castro Direção Geral e Edição Ana Lúcia de Almeida Diretor de Arte Henrique S. Castro Fº Departamento Comercial, Redação e Edição: SRTV/Sul - Quadra 701 Ed. Palácio do Rádio II Sala 215 - CEP 70340-902 Brasília - DF Tel.: (061) 225-1512 (061) 225-0976 Fax: (061) 224-2830 E-mail [email protected] Home-Page www.biotecnologia.com.br Projeto Gráfico Agência de Comunicação IRIS www.agenciairis.com.br [email protected] Impressão: Gráfica São Francisco Fotolito: Ribelito Assinaturas O pedido de assinatura é realizado através da carta resposta-comercial encartada em cada revista, por telefonema ou fax diretamente à KL3 ou pela Internet através dos nossos endereços eletrônicos. A revista não tem vendedores autorizados. Os artigos assinados são de inteira responsabilidade de seus autores. ISSN 1414-4522 10 Biotecnologia Ciência & Desenvolvimento Uma das leis mais importantes aprovadas nos últimos anos, no Brasil, foi com certeza a lei de Biossegurança que permitiu a criação da Comissão Técnica Nacional de Biossegurança CTNBio, órgão vinculado ao Ministério da Ciência e Tecnologia responsável pela liberação de Organismos Geneticamente Modificados OGMs. Parabenizamos, na oportunidade, o então senador e hoje Vice-Presidente da República, Marco Maciel, pela autoria do projeto desta lei e, principalmente, pela capacidade visionária que teve à época (1995) de buscar amparo legal para que o País pudesse competir em pé de igualdade com a vanguarda científica internacional nas pesquisas com a tecnologia do DNA recombinante. Assim, não poderíamos deixar de dedicar uma edição exclusiva ao tema Biossegurança pela repercussão e importância que a biotecnologia tem, hoje, em quase todos os ramos da ciência moderna como, por exemplo, na saúde, agricultura, direito, meio ambiente, economia, assim como também nas relações internacionais, política, religião, entre muitos outros. Neste mesmo contexto, a entrevistada desta edição foi a Dra. Leila Oda, presidente da CTNBio, que aborda aspectos da biossegurança no Brasil e no mundo. Publicamos ainda, entre muitos outros, um polêmico artigo sobre Bioética da Dra. Maria Celeste que aborda assuntos de clonagem e reprodução, à luz da legislação vigente no nosso País. Lembramos aos leitores que sobre clonagem a edição número 11 já trouxe um artigo do Dr. Sérgio Danilo Penna que, de forma brilhante, aborda também esta mesma questão. Esclarecemos aos nossos leitores que longe está a nossa pretensão de esgotar assunto tão abrangente numa única edição, e que pretendemos voltar sempre a este tema. Dr. Henrique da Silva Castro Conselho Científico Dr. Dr. Dr. Dr. Dr. Dr. Dr. Dr. Dr. Colaboraram nesta edição: Aluízio Borém - Genética e Melhoramento Vegetal Henrique da Silva Castro - Saúde; João de Deus Medeiros - Embriologia Vegetal; Maçao Tadano - Agricultura; Naftale Katz - Saúde; Pedro Juberg - Ciências; Sérgio Costa Oliveira - Imunologia e Vacinas; Vasco Ariston de Carvalho Azevedo - Genética de Microorganismos; William Gerson Matias - Toxicologia Ambiental. Conselho Brasileiro de Fitossanidade - Cobrafi Dr. Ivan Rud de Moraes - Toxicologia; Dr. Luís Carlos Bhering Nasser - Fitopatologia Fundação Dalmo Catauli Giacometti Dr. Eugen Silvano Gander - Engenharia Genética; Dr. José Manuel Cabral de Sousa Dias - Controle Biológico; Dra. Marisa de Goes - Recursos Genéticos Instituto de Pesquisas Energéticas e Nucleares - IPEN Dr. José Roberto Rogero Aluízio Borém Aron Jurkiewicz Edson Watanabe Hermann G. Schatzmayr Ilana Felberg Lêda C. S. Mendonça-Hagler Lucas Tadeu Ferreira Márcio A. F. Belém Maria Celeste Cordeiro Leite Santos Maria José Sampaio Marília R. Nutti Marli B. M. de Albuquerque Sérgio Costa Oliveira Vasco Azevedo Entrevista Leila Oda pág. 04 Biossegurança A Biossegurança nas infecções de origem viral pág. 13 Biodiversidade e Biossegurança pág. 16 Biossegurança no manejo de modelos animais pág. 30 Biossegurança de alimentos derivados da biotecnologia rDNA Biossegurança - Uma visão da História da Ciência pág. 42 Vacinas de DNA e Biossegurança pág. 46 Avaliação dos Riscos de Escape Gênico pág. 54 pág.34 Bio Ética Clones, Gens e Imortalidade pág. 24 BioNotícias pág. 50 Biotecnologia Ciência & Desenvolvimento 11 A biologia molecular aplicada à virologia criou novas áreas de pesquisa e de desenvolvimento tecnológico, com perspectivas sequer imaginadas anteriormente. Essas tecnologias têm permitido, por exemplo, a criação de vírus novos a partir de segmentos de vírus anteriormente conhecidos, o que indica, portanto, uma grande responsabilidade social, ética e moral do cientista e da sociedade sobre a questão da Biossegurança e do risco que ela deve gerenciar em âmbito mundial. Hermann G. Schatzmayr Chefe do Departamento de Virologia Instituto Oswaldo Cruz /FIOCRUZ [email protected] Fotos: Dra. Ortrud Monika Barth 12 Biotecnologia Ciência & Desenvolvimento A introdução de normas e procedimentos de Biossegurança somente ocorreu nas ultimas décadas, motivadas, principalmente, por sucessivos relatos de graves infecções ocorridas em laboratório. Assim, ao longo de nossa carreira de mais de 40 anos de virologia, observamos a evolução e a implantação dessas normas, inexistentes na década de 60, quando se utilizava regularmente a pipetagem, sem maior cuidado com materiais infecciosos, e mesmo o manejo em laboratórios comuns, de animais inoculados com vírus de alta periculosidade, hoje classificados como de risco biológico de nível 4. A legislação brasileira em Biossegurança preocupou-se quase que exclusivamente com os Organismos Geneticamente Modificados (OGMs), deixando de lado os microorganismos não modificados, muitos deles de alto risco para o operador e o meio ambiente. Em nossas instituições como um todo, é notória a grande variação nos níveis de manejo do problema da Biossegurança, e, sem dúvida, é necessário um grande esforço para se alcançar um adequado patamar em todo o país. Algumas instituições, de forma pontual, têm procurado cobrir essa lacuna através do preparo de Manuais e da formação de pessoal para o reconhecimento dos riscos e o manejo de agentes patogênicos em suas áreas, servindo de modelo e apoio para as demais instituições no país. Os vírus constituem um extenso grupo de microorganismos , no qual se incluem agentes patogênicos para o homem, animais e plantas. Suas características principais, além do reduzido tamanho, são a replicação exclusiva no interior de células vivas e a presença de um único ácido nucléico (ribonucléico ou desoxiribonucléico) em sua estrutura. Os vírus não possuem formas de resistência como os esporos de algumas bactérias, sendo, inclusive, bastante susceptíveis à ação de agentes químicos e físicos, porém, a gravidade dos quadros clínicos que muitos deles podem causar torna essencial a aplicação de rígidos padrões de Biossegurança no seu manejo em laboratório e mesmo com os pacientes infectados. Os vírus foram cultivados inicialmente pela inoculação em organismos completos, como plantas e animais, onde começaram a ser isolados e identificados, no início do século passado. Na década de 30, foi introduzido o uso de embriões de galinha, com cerca de 10 a 12 dias de vida, meio bastante favorável ao desenvolvimento de vários vírus e para o preparo, ainda hoje utilizado, de vacinas, como a antiamarílica e as vacinas para influenza. Ao final da mesma década, surgiram as primeiras culturas de células vivas em laboratório, em maior escala, metodologia estendida e aperfeiçoada nas décadas seguintes e que revolucionou a virologia, permitindo a descoberta de centenas de novos vírus e o Fig. 1 Vírus da Hepatite B concentrado de soro humano apresentando os três tipos de partículas: pequenas, esféricas, alongadas e grandes esféricas infecciosas. (aumento = 157.500x) Fig. 2 Vacina de hepatite B, constituída de suspensão purificada de partículas não-infecciosas. (aumento = 180.000x) preparo de novos agentes imunizan- dor e o meio ambiente, incluindo apeos vírus Marburg e Ebola, além de tes. vários vírus que podem afetar animais nas o vírus, o que enfatiza o grau de A biologia molecular aplicada à risco desses agentes. Essa classificação de interesse econômico. virologia criou novas áreas de pesquisa se baseia na patogenicidade do agente Em seu processo de replicação no e de desenvolvimento tecnológico, com para o homem, os vegetais ou animais organismo, os vírus podem lesar irreperspectivas sequer imaginadas anteri- de interesse econômico; risco indivi- versivelmente células do organismo ormente. Essas tecnologias têm permi- dual ou comunitário pelas infecções superior ou entrar em aparente equilítido, por exemplo, a criação de vírus que causam; pelo seu modo de trans- brio com elas, gerando, posteriormennovos a partir de segmentos de vírus missão mais ou menos eficaz e pela te, quadros degenerativos como neoanteriormente conhecidos, o que indi- existência ou não de tratamento ou de plasias, ao longo dos anos, pós-infecca, portanto, uma grande resção, como é o caso das hepaponsabilidade social, ética e tites B e C, e outros vírus moral do cientista e da socioncogênicos, humanos e aniOs vírus não possuem formas de resistência edade sobre a questão da mais. como os esporos de algumas bactérias, sendo, Biossegurança e do risco que Os vírus se disseminam por inclusive, bastante susceptíveis à ação de ela deve gerenciar em âmbivários processos de um hospeagentes químicos e físicos, porém, a gravidade to mundial. deiro a outro, destacando-se o dos quadros clínicos que muitos deles podem Do ponto de vista da Bicontato direto através das vias causar, torna essencial a aplicação de rígidos ossegurança, a inoculação de respiratórias e sexual. Há tampadrões de Biossegurança no seu manejo em animais de experimentação bém a transmissão por artrólaboratório e mesmo com os pacientes com vírus patogênicos conspodes, como mosquitos e carinfectados. titui o mais perigoso método rapatos, por água e alimentos, de cultivo e exige uso de alta como as das hepatites A e E, os tecnologia para um manejo seguro, e vacinas eficientes. No nível 4, se clas- vírus que causam diarréia e os que se sificam os vírus de alto risco de trans- transmitem por contato com sangue e aplicação de estritas regras de Biossemissão nas comunidades e de alta seus derivados, tendo estes últimos gurança no cultivo de vírus, de acordo patogenicidade, sem vacinas ou trata- gerado um complexo problema para o com o nível de risco biológico do mento eficaz disponível, como os vírus controle de infecções iatrogênicas; pelas agente em questão. agentes de febres hemorrágicas gra- hepatites B e C, e pelo vírus HIV. Os vírus se classificam nos níveis 2, 3 e 4 de risco biológico; este último, de ves, algumas encefalites transmitidas Em laboratorio e no manejo de máxima periculosidade para o opera- por carrapatos, o herpes vírus tipo B e pacientes, são especialmente perigoBiotecnologia Ciência & Desenvolvimento 13 Fig. 3 Vacina contra poliomielite apresentando partículas virais inteiras e incompletas. (aumento = 280.000x) sos os vírus passíveis de propagação respiratória, como os hantavírus, e em especial, na ocasião de sua inoculação em animais de experimentação ou na coleta de animais silvestres portadores do vírus. Para a prevenção de infecções por vírus, o conceito básico é a percepção do risco das operações a serem estabelecidas, ou seja, todos os profissionais envolvidos devem ter plena conscientização dos riscos envolvidos na manipulação dos pacientes, dos espécimens clínicos e dos animais ou culturas infectadas. Deve estar claro que não existe o chamado risco zero e que todos os esforços devem ser no sentido de se alcançar um nível mínimo de possibilidades de acidentes e infecções do pessoal envolvido. Nas enfermarias e laboratórios, devem ser observadas as seguintes linhas de cuidados na prevenção de infecções por vírus: - Definir um responsável pelas ope14 Biotecnologia Ciência & Desenvolvimento rações nas áreas de risco, o qual deverá introduzir previamente o treinamento de todo o pessoal envolvido, inclusive o pessoal de apoio e limpeza, os quais têm freqüentemente contato direto com material infeccioso, antes de sua esterilização e descarte. O responsável deve ainda supervisionar a presença e o uso dos Equipamentos de Proteção Individual (EPI) e dos Equipamentos de Proteção Coletiva (EPC). A ele devem ainda ser reportados quaisquer problemas surgidos, em especial acidentes, para que tome as providencias Fig. 4 Rotavírus concentrado de fração de gradiente. (aumento = 150.000x) cabíveis em relação ao acidentado e ao local onde surgiu o problema. - Sinalizar as áreas de trabalho de maneira completa, incluindo o nível de risco biológico (mapas de risco), os locais que contêm substâncias corrosivas, tóxicas, inflamáveis e radioativas, bem como proibir a entrada de estranhos nas áreas de risco e demais aspectos específicos do agente e do laboratório e enfermaria. - Seguir as regras básicas nas quais se incluem a proibição de alimentos, bebidas e fumo em áreas de trabalho, bem como a aplicação de cosméticos e o manejo de lentes de contato. - Os EPIs, como roupas de proteção, devem ser usadas apenas no locais de trabalho; luvas, sapatos fechados e máscaras adequadas ao risco previsto; e protetores faciais, quando existe o risco de haver projeção de fluidos contaminados no rosto. Esses equipamentos são essenciais, devem estar em perfeito estado e devem ser sendo substituídos sempre que necessário. - Os EPCs, como cabines de fluxo laminar, sistemas de ventilação, exaustão e resfriamento; autoclaves e semelhantes, devem ser certificados regularmente segundo as recomendações do fabricante, e garantindo seu perfeito funcionamento. - A vacinação prévia contra agentes patogênicos de todo profissional que trabalha nas áreas de risco, deve ser implementada, como é o caso da influenza, raiva e hepatites A e B, sendo coletadas amostras de sangue após a vacinação, para comprovação sorológica da imunidade alcançada. Os protocolos respectivos devem ser guardados para referência no caso de infecção acidental e planejamento de revacinações , quando recomendado. - As normas operacionais de trabalho nas áreas de risco devem estar escritas, à disposição de todos os que trabalham na área. Essas normas devem ser apresentadas com clareza a todos os novos profissionais que começam o seu trabalho nesses locais, antes que iniciem suas atividades. - Precauções especiais no manejo de instrumentos cirúrgicos, seringas e agulhas. Estas nunca devem ser recapeadas após o uso e sim descartadas, juntamente com as seringas, em caixas de pape- lão de paredes resistentes, antes de serem autoclavadas e posteriormente descartadas. - Os espécimens clínicos coletados de pacientes devem ser recebidos no laboratório em local próprio, sendo as embalagens abertas cuidadosamente por profissional portando EPIs adequados, como máscaras, luvas e roupas de proteção. No caso de quebra de frascos e vazamentos que contaminem extensamente as embalagens, pode ser recomendável a eliminação de todo o conteúdo, com a sua autoclavação antes do descarte final. - Cuidados especiais na rotulagem, manejo e guarda dos espécimens são essenciais. As amostras de materiais contendo vírus, devem ser guardadas em frascos padronizados, colocados em caixas ordenadas, para que possam ser facilmente localizáveis. Os vírus são conservados em temperaturas baixas, sempre abaixo de 40º negativos, quando estocados por longos períodos. - Operações como centrifugação e uso de aparelhagens automáticas de bio-ensaio, devem ser monitoradas cuidadosamente, quanto a formação de aerossóis e vazamentos no seu interior. No trabalho de concentração e purificação de suspensões virais de alto risco, como hepatite B, recomenda-se trabalhar em nível de Biossegurança 3, quando o mesmo vírus é normalmente operado em nível 2. O mesmo ocorre com os hantavírus, que são enquadrados no nível 3, porém para a inoculação de animais e purificação viral se exige o nível 4, pelo alto risco da formação de aerossóis. - Todo material contaminado com vírus, deve ser esterilizado antes de seu descarte final, e a autoclavação é a operação mais segura. As carcassas animais não devem ser imersas previamente em desinfetantes e sim autoclavadas, em embalagens fechadas e à prova de vazamento. As bancadas e outros locais de trabalho, devem ser limpas com hipoclorito a 0,5%, com soluções preparadas diariamente. Materiais plásticos não descartáveis e outros pequenos equipamentos cirúrgicos e vidraria podem ser esterilizados por imersão em hipoclorito a 1%. O formol, em baixas concentrações, como 1%, pode ser igualmente utilizado para a esterilização desses materiais. - Os resíduos líquidos e sólidos hospitalares, passíveis de conter vírus e outros agentes infecciosos devem ser descartados conforme as legislações em vigor, prevendo-se a coleta dos sólidos em sacos plásticos de cor branca para descarte diferenciado no meio ambiente. Assinale-se que o país não dispõe de nenhum laboratório de alta segurança de nível 4 para manejo de vírus desse nível de periculosidade, o que nos torna dependentes de laboratórios Fig. 5 Parapoxvírus isolado de bovino. (aumento = 150.000x) do exterior para o esclarecimento de infecções graves, como febres hemorrágicas, nas quais uma etiologia viral seja suspeitada. Com isso, não temos to de pacientes com infecções graves de etiologia desconhecida. Essas lacunas precisam ser urgentemente cobertas, sob risco de aumentarmos, cada vez mais, nossa dependência tecnológica, bem como mantermos o risco de termos de enfrentar uma virose de alta periculosidade, que surja no país ou nele seja introduzida pelo tráfego aéreo, cada vez mais intenso no mundo, e contaminar o pessoal de saúde e mesmo segmentos populacionais importantes, por falta de local adequado para isolamento precoce dos pacientes. As medidas de controle das infecções virais na população compreendem as vacinações e as campanhas de esclarecimento dos seus meios de transmissão, estas últimas nem sempre eficazes, devido ao seu baixo nível de divulgação entre a população como um todo. O uso de máscaras individuais, no caso de infecções respiratórias, por exemplo, que é prática comum na Ásia, por razões culturais e econômicas, não se conseguiu introduzir em outras regiões. Para concluir, os vírus constituem um amplo grupo de agentes patogênicos para o homem, os vegetais e os animais de interesse econômico e podem se transformar em pandemias de alta gravidade, como é o caso da AIDS e da influenza. O manejo desses agentes em laboratório e do paciente infectado exige normas com estritos padrões e procedimentos de Biossegurança capazes de gerenciar os riscos de contaminação dos profissionais de saúde, das populações e do meio ambiente, e de prevenir os riscos inerentes à manipulação genética de vírus, em âmbito internacional. Referências bibliográficas Fig. 6 Orthopoxvírus isolado de caso humano. (aumento = 150.000x) condições de estudar vírus como o Sabiá e o Rocio, por exemplo, que causaram casos humanos fatais no país. Igualmente, não dispomos de uma enfermaria de alto risco, segundo padrões internacionais, para internamen- 1. Comissão Técnica Nacional de Biossegurança, Instrução Normativa no. 7, 1997. 2. Laboratory Safety, Eds: Fleming D.O. & Richardson J.H., ASM Press, 2ª edição, 1995. 3. OMS, Laboratory Safety Manual, 2ª edição, Genebra, 1993. 4. OMS, Guidelines for the safe transport of infectious substances and diagnostic specimens, Genebra, 1997. 5. Schatzmayr, H.G., Biossegurança em doenças provocadas por vírus, Anais do I Encontro Norte-Nordeste de Biossegurança e produtos transgênicos, Recife, Setembro 27-29, 2000. Biotecnologia Ciência & Desenvolvimento 15 O desenvolvimento científico sobre a dinâmica dos processos naturais e o aperfeiçoamento de estratégias de manejo dos riscos permitirão usufruir os benefícios dos avanços biotecnológicos, de forma sustentável, preservando a biodiversidade, o meio ambiente e a saúde humana. Lêda C. S. Mendonça-Hagler Prof. Titular Univ. Federal do Rio de Janeiro [email protected] Fotos: Prof. A. .N. Hagler 16 Biotecnologia Ciência & Desenvolvimento Avaliação de impactos ambientais da Biotecnologia literatura encontra-se na faixa de 1.7 milhões, enquanto o número estimado de espécies existentes é de 13 A biodiversidade, sinônimo de milhões. Os grupos de organismos diversidade biológica, significa a va- mais ricos em espécies são os microrriedade de organismos vivos presen- ganismos e os insetos, (Wilson, 1999), tes em todos os ecossistemas do (Tabela 1). Os microrganismos posplaneta. A biodiversidade compreen- suem o mais rico repertório de diverde três níveis hierárquicos de organi- sidade genética e metabólica existenzação: os genes, as espécies e as te na natureza. Cerca de 50% do protoplasma da biosfera encontra-se no componente microbiano (bactérias, fungos, algas e protozoários). Os microrganismos registram mais de 3,5 bilhões de anos de história evolutiva e são imprescindíveis para os ciclos Figura 1a: Diversidade microbiana. biogeoquímiBactérias cultiváveis de bromélia cos e cadeias alimentares, mantendo intecomunidades . A diversidade genéti- rações vitais entre si e com os orgaca representa a variação nas seqüên- nismos superiores. A contribuição cias de bases do DNA em populações dos microrganismos é essencial para de organismos da mesma espécie. A a vida no planeta (Groombridge, diversidade de espécies refere-se, 1992). principalmente, à riqueza de espéciA espécie representa o ponto es de um hábitat. A biodiversidade é focal dos mecanismos evolutivos. A vasta, complexa e pouco conhecida. definição de espécie biológica consiO número de espécies descritas na dera os grupos de populações que são capazes, ou potencialmente capazes, de cruzamento fértil, (Mayr, 1969). Esse conceito não se aplica a organismos que possuam reprodução exclusivamente vegetativa, como os procariontes. Para contornar essa limitação, surgiu o conceito filogenético de espécie, que agrupa as populações oriundas de um ancestral comum e que são distintas geneticamente de outras populações. As técnicas moleculares facilitaram a comparação de genomas, o delineamento de espécies e a determinação de relacionamentos filogenéticos entre os organismos (Woese et al. 1990). A avaliação da biodiversidade deve considerar o papel ecológico das espécies na estrutura das comunidades, a estimativa de abundância relativa de cada espécie e o número de espécies representativas nos diferentes grupos taxonômicos da escala evolutiva. A avaliação global da biodiversidade considera, adicionalmente, os conceitos de endemismo, centros de origem e de diversidade das espécies. A biodiversidade, em geral, tende a ser mais elevada em áreas tropicais, decrescendo com o aumento da latitude e da altitude, sendo maior em regiões chuvosas e menor em regiões áridas. As florestas tropicais úmidas, como a Amazônia, representam as regiões mais ricas em biodiversidade. Esses biomas cobrem 7% da superfície do globo e podem abrigar a grande maioria das espécies. Outras áreas de grande diversidade são os recifes de corais e as áreas de clima tipo mediterrâneo. Os ambientes marinhos apresentam menos diversidade de espécies e maior diversidade taxonômica superior, em comparação com os ambientes terrestres. O Brasil encontra-se entre os 12 países detentores de megadiversidade. Estima-se que 20% das espécies do planeta estão no território brasileiro. O país possui o maior número de espécies de plantas e de anfíbios e encontra-se entre os mais ricos em pássaros, répteis e mamíferos (Groombridge, 1992). A Mata Atlântica e o Cerrado estão entre os 25 hot spots de biodiversidade ameaçados de devastação (Wilson, 1999). Figura 1b: Bromélia Neoregelia cruenta de restingas Perda e preservação da Biodiversidade O aparecimento e a extinção das espécies representam fenômenos naturais em tempos geológicos. Entretanto, é incontestável a influência negativa das atividades humanas na conservação dos recursos biológicos. As estimativas de extinção de espécies estão baseadas em conhecimentos sobre a riqueza de espécies nos ecossistemas e a previsão de devastação de áreas nos respectivos hábitats. A redução da diversidade de espécies usadas na alimentação humana tem pouca importância em termos de biodiversidade global. Não obstante, a erosão genética dessas espécies tem grandes implicações econômicas na produção de alimentos e na sustentabilidade da agricultura. As ações antrópicas sobre os ecossistemas naturais constituem a causa principal de perda de diversidade. Essencialmente, qualquer forma de atividade humana, não sustentável, pode resultar em impacto ambiental, afetando a abundância relativa das espécies e, em casos extremos, levando-as à extinção. A manutenção da biodiversidade pode ser feita in situ, com a preservação dos ecossistemas e ex-situ, em coleções de culturas e células, herbários, zôos, bancos de sementes etc. A preservação da biodiversidade pode ser vista como uma maneira de manter a vida no planeta. O homem utiliza a biodiversidade como recurso biológico para alimentação, habita- ção, transporte, geração de energia, remédios, lazer e outros usos. O valor econômico da biodiversidade é de difícil mensuração. O uso mais importante da biodiversidade para o homem é a alimentação. Apesar do grande número de espécies comestíveis, apenas uma pequena percentagem de plantas e animais é usada em escala comercial. A biodiversidade tem gerado produtos industriais de alto valor agregado. A maioria dos fármacos, por exemplo, tem origem vegetal ou microbiana, representando um faturamento anual de dezenas de bilhões de dólares. Outros benefícios da biodiversidade para o homem incluem o papel das florestas na preservação de mananciais de água e na estabilização de solos, dos mangues e recifes de corais, sustentando regiões de pesca e uso de ambientes naturais para o ecoturismo. A perda de biodiversidade pode contribuir para mudanças climáticas que produzem impactos nas atividades humanas e na biosfera. A conservação da biodiversidade possui valores estéticos e éticos relacionados com a preservação do patrimônio genético para as futuras gerações. Biodiversidade e Biossegurança Os recursos genéticos adquiriram grande expressão econômica depois da Engenharia Genética, que permite a inserção de genes provenientes de espécies filogeneticamente não relacionadas, formando organismos em combinações improváveis de ocorBiotecnologia Ciência & Desenvolvimento 17 rência natural. Os organismos genemento de organismos vivos geneticaticamente modificados (OGMs) ofemente modificados, entre os países. recem uma multiplicidade de apliAs negociações posteriores, no âmbicações e benefícios, existindo o to da CBD, resultaram na adoção das potencial para efeitos adversos à recomendações de Biossegurança saúde humana e ao meio ambiente. propostas pela UNEP (1995) e no A utilização de OGMs e derivados é recente Protocolo de Cartagena. precedida de avaliação de risco, A legislação brasileira de Biossecaso a caso, com base na experigurança está representada na Lei nº mentação científica e na familiarida8.974, de 05/01/1995, recentemente de de conhecimentos. A preocupaalterada pela Medida Provisória 2.137, ção com a segurança da nova biode 28/12 2000. Em cumprimento à tecnologia está inserida em acordos legislação, o governo recebe assessointernacionais, como a Agenda 21 e ramento técnico da Comissão Técnia Convenção da Diversidade Biolóca Nacional de Biossegurança (CTNgica (CBD), negociados durante a Conferência das Nações Unidas para o Desenvolvimento e o Meio Ambiente (UNCED, 1992), realizada no Rio de Janeiro. A CBD foi ratificada por 170 países e faz parte do ordenamento jurídico brasileiro. O texto da CBD reconhece o valor da biodiversidade e o direito soberano dos países sobre seus recursos genéticos, ficando res- Figura 2: Pantanal Matogrossense ponsáveis pela sua preservação e uso sustentável. Preconiza o acesso e a distribuiBio) para as atividades de avaliação ção justa e eqüitativa dos benefícios de risco de OGMs e derivados e para oriundos dos recursos, entre os pao estabelecimento da política nacioíses detentores da biodiversidade e nal, na referida área (CTNBio, 2000). os geradores de tecnologias. Menciona o princípio da precaução: quanBiossegurança e do houver risco de redução signifiAvaliação de Risco cativa ou perda da biodiversidade, a falta de completo conhecimento, As questões de Biossegurança ulnão deve ser razão para postergar trapassaram a esfera científica e pasmedidas que evitem ou minimizem saram a ser alvo de um debate emoo risco. As ações na área de Biossecional, polarizado entre grupos que gurança estão mencionadas nos arapóiam a nova biotecnologia e grutigos 8(g) e 19(3) da CBD sobre a pos que são radicalmente contra. A biotecnologia, recomendando a immaior controvérsia está centrada na plantação de instrumentos para resegurança das plantas transgênicas e gulamentar, administrar e controlar dos alimentos derivados. A biotecnoos riscos associados com o uso e a logia tem recebido melhor aceitação liberação de OGMs, com potencial pública para aplicações na indústria de causar impactos ambientais que bioquímica e na saúde. Novos avanpossam afetar a conservação e o uso ços científicos, como a clonagem, os sustentado da diversidade biológitestes genéticos e a terapia gênica ca, incluídos os riscos à saúde hutêm estimulado diversos questionamana e o estabelecimento de um mentos de natureza ética. Apesar da protocolo que contenha os procedipolêmica, o desenvolvimento da bimentos apropriados para o moviotecnologia agrícola tem sido expo18 Biotecnologia Ciência & Desenvolvimento nencial. No ano passado, a área global cultivada com plantas transgênicas foi superior a 44 milhões de hectares. Globalmente, cerca de 40 plantas geneticamente modificadas estão liberadas para plantio e comercialização. Os EUA cultivaram cerca de 70% do total, a Argentina 14%, o Canadá 9%, a China 3% e outros 9 países, 4%. Os cultivos transgênicos de maior expressão foram soja (53%), milho (27%), algodão (9%) e canola (8%). Os genes inseridos conferem às plantas tolerância a herbicidas (69%), resistência a insetos (21%), a combinação de tolerância a herbicida e resistência a insetos (7%) e resistência a vírus (3%), (ISAAA, 2000). Em pequena escala, estão os cultivos de plantas transgênicas que conferem melhor qualidade aos alimentos, e em desenvolvimento, plantas para obtenção de fármacos. No Brasil, cerca de 700 hectares foram cultivados com plantas transgênicas, em experimentos de campo. A soja resistente ao glifosato (soja RR) obteve parecer favorável para comercialização, emitido pela CTNBio, estando o plantio sob julgamento. As liberações planejadas de plantas transgênicas no país, analisadas caso a caso, estão listadas na Tabela 2 (CTNBio, 2000). Os procedimentos de Biossegurança visam a evitar ou minimizar as conseqüências adversas dos OGMs e seus derivados para o homem e o meio ambiente. Os possíveis efeitos deletérios decorrentes da liberação de OGMs durante a experimentação ou a comercialização são avaliados ao mesmo tempo em que se estabelecem medidas de monitoramento para detecção de conseqüências adversas, bem como mitigação de impactos indesejáveis. Os OGMs são organismos vivos com capacidade de reprodução, dispersão e evolução biológica no ambiente, gerando questões de segurança diferentes se comparados com produtos oriundos de tecnologias químicas e físi- cas. A história da introdução de espécies exóticas no ambiente tem trazido benefícios, em alguns casos, e consideráveis danos ecológicos em outros exemplos (abelhas africanas no Brasil, coelhos na Austrália, etc.). Ao adquirir novas características genéticas, um organismo pode ter seu comportamento alterado no ambiente, daí a necessidade da avaliação de riscos. Durante a obtenção de dados para análise de risco, é fundamental a comparação com o organismo parental, não modificado. A avaliação de risco identifica e caracteriza a magnitude e o potencial de fatores adversos previamente identificados, em qualidade e quantidade. A avaliação de risco considera informações sobre o grau de risco do organismo parental, as características dos novos genes inseridos e os processos de inserção , o fenótipo do OGM resultante e as características do ambiente receptor . A obtenção de dados tem início em experimentos de microcosmos e amplia progressivamente a escala Figura 3: Mata Atlântica, região costeira do Rio de Janeiro vios indicam alta probabilidade de segurança e eficácia para o OGM, a comercialização pode ser licenciada. A liberação de um OGM em ambientes diferentes requer repetição dos experimentos de campo. O monitoramento periódico, após liberação em novo ambiente, é essencial, para detectar danos ambientais inesperados. O uso de marcadores moleculares pode auxiliar a detecção do OGM Tabela 1. Número Aproximado de Espécies nos Principais Grupos Taxonômicos e Percentual Descrito Grupo Microrganismos Bactérias Fungos Protozoários Algas Plantas Animais Nematódeos Moluscos Crustáceos Insetos Vertebrados Espécies Descritas Total Estimado Percentual 4.000 72.000 40.000 40.000 270.000 1.000.000 1.500.00 200.000 400.000 320.000 0,4% 4,8% 20% 10% 84% 26.000 70.000 40.000 950.000 45.000 400.000 200.000 150.000 8.000.000 50.000 6% 35% 26% 12% 90% Wilson (1999) e Groombridge (1992) para mesocosmos, casas de vegetação e, posteriormente, para testes de campo. Os modelos matemáticos de simulação podem ser usados para complementar dados experimentais e estimar parâmetros, como dispersão e fluxo gênico. Quando os resultados dos experimentos pré- e dos descendentes no ambiente (Edmonds Institute, 1998). Impactos ambientais de OGMs Os principais impactos associados à liberação de OGMs no ambiente incluem: fluxo gênico, aumento de competitividade (weedness), impactos em organismos não alvo, desenvolvimento de resistência, erosão genética e efeitos nos ecossistemas (Rissler & Melon, 1996; Edmonds Institute, 1998). Os impactos associados à segurança alimentar, tais como alergenicidade e toxicidade, não serão tratados no presente artigo. Fluxo gênico: A possibilidade de fluxo gênico do OGM para espécies sexualmente compatíveis é uma questão fundamental na avaliação de risco ambiental, particularmente nas proximidades dos centros de origem e de diversidade das espécies cultivadas, para evitar a chamada poluição gênica. A formação de híbridos entre plantas transgênicas e seus parentes silvestres é bem documentada (Gliddon, 1994; Dale, 1994; Mikkelsen et al. 1996; Bergelson et al. 1998). A probabilidade de fluxo gênico depende de muitos fatores, entre eles, os processos de reprodução da planta, os mecanismos de dispersão de pólen e de sementes e o ambiente de liberação. Experimentos feitos com Brassica napus (canola), resistente ao glifosato e Brassica campestris, demonstrou diferentes graus de dispersão de pólen e formação de híbridos transgênicos. Resultados referentes à dispersão de pólen encontrados para outras plantas também apresentaram variações (Conner & Dale, 1996; Dale & Scheffler, 1996). Os procedimentos recomendados para manejo de risco, visando a minimizar o fluxo gênico incluem: o isolamento Biotecnologia Ciência & Desenvolvimento 19 disseminar genes com resistência a antibióticos reside no uso indiscriminado desses produtos na medicina e na pecuária. Aumento de competitividade (weedness): A previsão de impactos ambientais de longo prazo é uma tarefa difícil. As modificações genéticas introduzidas nos OGMs podem causar mudanças que aumentem a capacidade de competição do OGM em relação ao organismo parental. Os efeitos ecológicos dependem das possibiFigura 4: Cerrado, Chapada dos Guimarães lidades de estabelecimento, persistência e fluxo gênico do OGM tência a antibióticos. Recentemente, (Mikkelsen et al. 1996; Radosevich espacial ou temporal, em relação a foi demonstrada a transformação da et al. 1996). O desafio para o espécies sexualmente compatíveis, a bactéria Acinetobacter sp. com DNA manejo consiste em identificar moretirada de florescências das plantas, de planta transgênica em condições dificações no genótipo que confio uso de plantas macho estéril, o uso otimizadas de laboratório. A trans- ram características de competitivide bordaduras de plantas incompatíformação de bactérias com DNA de dade em condições naturais. Uma veis com a planta transgênica, os plantas, quando detectável, ocorre abordagem coerente consiste em procedimentos apropriados de desem baixa freqüência (Smalla, 2000). testar a sobrevivência OGM, ou carte do material transgênico e o Os conhecimentos atuais não des- seus híbridos, fora das condições monitoramento pós-colheita, elide cultivo, em comparação com minando plantas voluntárias. A o organismo parental isogênilocalização geográfica da libera- Tabela 2. Liberações Planejadas de co. Hibridações naturais são coção é um dado importante, parti- plantas geneticamente modificadas, no nhecidas entre os cultivos alicularmente quanto à presença de Brasil mentares, incluindo arroz, triespécies capazes de cruzamento go, milho, soja e algodão, e 104 IR, (HT+IR) fértil com o OGM. A identificação Algodão respectivas espécies selvagens 1 HT do risco de escape de pólen é Arroz aparentadas. Os riscos mais pre3 VR parte do problema. A próxima Batata ocupantes estão focalizados nos HT,IR,VR etapa da avaliação de risco consi- Cana de açúcar 24 genes de resistência a herbici2 HT dera as conseqüências da intro- Eucalipto das. O aumento de área cultiva1 HT gressão do transgene, que resulta Feijão da com plantas tolerantes favo2 VR em possível vantagem competiti- Fumo rece o aparecimento de plantas 1 VR va para as espécies nativas. Exis- Mamão daninhas com tolerância múlti1062 HT,IR,(HT+IR) tem, no Brasil, espécies silvestres Milho pla a herbicidas de amplo es107 HT,IR de várias plantas de importância Soja pectro, resultantes de eventos econômica, tais como o algodão, HT: genes de tolerância a herbicidas. de transferência gênica e preso arroz, a batata e a mandioca. são seletiva, que conferem a IR: genes de resistência a insetos A transferência horizontal de VR:genes de resistência a vírus essas plantas vantagem compegenes no ambiente pode ocorrer CTNBio (2000) titiva nos agroecossistemas. Esse em organismos procariontes, atrarisco pode ser reduzido pela vés de processos de conjugação, modificação da construção do transdução e transformação. A freOGM para dificultar a introgressão cartam a possibilidade de eventos qüência de recombinação genética é de genes em espécies sexualmente de transferência de DNA de plantas maior quando os genes se encontram compatíveis (Gressel, 2000). para microrganismos, no trato dinos plasmídeos. Assim sendo, na Impactos em organismos não gestivo de animais. Os genes de construção de microrganismos genealvo: As plantas transgênicas que resistência a antibióticos ocorrem ticamente modificados, os novos geexpressam endotoxinas proveninaturalmente nos microrganismos. nes devem ser inseridos no cromosentes de Bacillus thuringiensis e A disseminação de genes de resissoma, para dificultar a transferência outras bactérias entomopatogênitência a antibióticos oriundos de gênica no ambiente (Aráujo et al. OGMs, representa um risco pouco cas atuam como biopesticidas. As 1993). Genes de origem bacteriana significativo, particularmente na au- chamadas toxinas Bt, codificadas são comumente inseridos nas plantas sência de pressão seletiva. Reco- pelos genes cry, apresentam estransgênicas, como os genes de resisnhecidamente, o real problema de pectro diferente de toxicidade, po20 Biotecnologia Ciência & Desenvolvimento dendo ser usadas para controle de insetos das ordens Lepdóptera, Coleóptera e Díptera. A expressão de toxinas Bt na planta transgênica pode alterar direta ou indiretamente as populações de espécies não alvo (Birch et al. 1997). Os efeitos dessas toxinas nos insetos dependem da susceptibilidade das espécies e da concentração da toxina contida nos tecidos da planta transgênica. Experimentos de laboratório mostraram impactos adversos nas larvas de borboletas monarcas pela ingestão de pólen de milho Bt da planta hospedeira (Losey, 1999). Experimentos recentes efetuados em condição de campo confirmaram o efeito larvicida de pólen de milho Bt (Jesse & Obryck, 2000). Outro impacto possível de planta Bt consiste na redução de inimigos naturais das pragas alvo, com implicações em outros níveis tróficos e na biodiversidade. Algumas plantas transgênicas podem afetar a diversidade microbiana do solo alterando os ciclos do carbono e do nitrogênio e interferindo na fertilidade do solo. A biodegradação de toxinas Bt é reduzida em solos ácidos e com alto teor de argila, onde a toxina fica detectável durante meses (Palm et al. 1996). Estudos em laboratório detectaram a exudação de toxina Bt na raiz da planta transgênica, trazendo questionamentos sobre as interações com a biota de solo. (Saxena et al. 1999). Desenvolvimento de resistência na população alvo: O uso de pesticidas, inclusive os biopesticidas, favorece o desenvolvimento de resistência na população alvo. Associações de toxinas Bt, largamente usadas em formulações convencionais de inseticidas e na agricultura orgânica, dificultam o desenvolvimento de resistência. Entretanto, recentemente, foi detectada em insetos a resistência múltipla à Cry1Ab e outras toxinas Bt. O gene responsável pela resistência encontra-se presente em 10 % da população sensível como heterozigoto. Outro gene que confere resistência a Cr1Ac foi encontrado em 0,1% da população de insetos alvo (Tabashnik, 1994; Hilbeck et al. 1998). O manejo de resistência recomenda a estratégia que combina alta dose de exposição à toxina e plantio de áreas sem a planta transgênica, denominadas refúgios (Gould, 1998). Os refúgios de indivíduos sensíveis permitem o cruzamento destes com indivíduos resistentes, resultando populações vulneráveis à toxina. O sucesso do manejo depende da sincronia de cruzamento entre indivíduos sensíveis e resistentes, nas populações de insetos. Nos EUA, os cultivos de milho e algodão Bt incluem refúgios que variam de 4 a 50% da área plantada. A introdução de genes que conferem resistência a vírus apresenta alguns riscos. A recombinação entre o RNA de vírus e outro RNA viral presente na planta transgênica pode resultar em novo patógeno (Steinbrecher, 1996). Os riscos decorrentes da formação de novos vírus por meio da recombinação ou da transcapsidação precisam ser investigados para aplicação segura da tecnologia. (Paoletti & Pimentel, 1996) Erosão Genética: O número de espécies usadas na alimentação humana é relativamente pequeno, considerando a diversidade de plantas comestíveis. A agricultura convencional concentrou esse número, dando prioridade a poucas espécies e selecionando os cultivares mais produtivos. A expansão da biotecnologia agrícola sinaliza uma tendência ainda maior para a redução de diversidade genética, em escala global. A variabilidade genética de plantas obtidas através do melhoramento tradicional e usadas em diferentes regiões do mundo, pode ser reduzida a poucos cultivares transgênicos, aumentando a vulnerabilidade da agricultura (Tripp, 1996). Efeitos de OGMs nos ecossistemas: Os efeitos ecológicos devem ser avaliados com base em conhecimentos sobre a estrutura, os processos e a persistência dos ecossistemas a serem atingidos em decorrência da liberação de OGMs. Interações diretas do OGM com outros organismos no ambiente (parasitismo, predação, competição, simbiose) devem ser con- sideradas durante a avaliação de risco. Os efeitos indiretos, quando a atividade do OGM pode alterar a densidade de outras espécies ou causar mudanças em fatores abióticos, afetando outras populações, também são relevantes. Grandes cultivos com plantas Bt, por exemplo, podem reduzir significativamente a população de insetos, afetar pássaros, outros predadores e inimigos naturais das pragas (Campbell & Cooke, 1997). O plantio de cultivares transgênicos tolerantes a herbicida pode reduzir o alimento de insetos e pássaros, devido à eliminação de outras plantas sensíveis. Herbicidas de amplo espectro podem reduzir a vegetação nos agroecossistemas e ambientes adjacentes. Os principais riscos ambientais associados aos microrganismos geneticamente modificados, usados para a biorremediação, envolvem suas habilidades competitivas e a possível produção de substâncias tóxicas que possam atingir as cadeias alimentares do homem e de animais (Roughgarden, 1998). Mudanças na estrutura das comunidades podem não provocar grandes alterações nos ecossistemas devido à dinâmica compensatória de espécies funcionalmente similares, que atuam como tampão. Em alguns casos, as alterações na estrutura das comunidades podem ocasionar impactos substanciais nos processos ecológicos. (Wahl et al. 1995). A experiência adquirida com a introdução de espécies exóticas no ambiente pode auxiliar a avaliação de risco de OGMs. Considerações finais O processo de avaliação dos impactos ambientais resultantes da liberação de organismos geneticamente modificados tem limitações. A complexidade dos diferentes ecossistemas dificulta a previsão de efeitos de longo prazo. O melhoramento genético convencional está restrito à variabilidade existente entre espécies sexualmente compatíveis. A engenharia genética remove esses Biotecnologia Ciência & Desenvolvimento 21 limites, oferecendo amplas possibilidades de transferência de fenótipos desejáveis para os diversos organismos. A Biotecnologia Molecular tornou-se um instrumento poderoso, justificando, desde os primórdios, na década de 70, a constante avaliação quanto à Biossegurança. O desenvolvimento científico sobre a dinâmica dos processos naturais e o aperfeiçoamento de estratégias de manejo dos riscos permitirão usufruir os benefícios dos avanços biotecnológicos, de forma sustentável, preservando a biodiversidade, o meio ambiente e a saúde humana. Referências Bibliográficas Araújo, M.A.V.; Mendonça-Hagler, L.C.; Hagler, A.N.; van Elsas, J.D. 1993. Survival of genetically modified Pseudomonas fluorescens introduced into subtropical soil microcosms. FEMS Microbial Ecology.13: 205-216. Arriola, P.E.; Ellstrand, N.C. 1996. Crop to weed gene flow in the genus Sorghum (Poaceae); spontaneous interspecific hybridization between johnsongrass, Sorghum halepense and crop sorghum, S. bicolor. Amer. J. Botany. 83: 1153-1160. Bergelson, J.; Purrington, C.B.; Wichmann, G. 1998. Prosmiscuity in transgenic plants. Nature. 398: 25 Birch, A.N.E.; Geoghegan, I.E.; Majerus, M.E.N.; Hackett, C.; Gatehouse, A.M.R. 1999. Tri-trophic interactions involving pest aphids, predatory 2-spot ladybirds and transgenic potatoes expressing snowdrop lectin for aphid resistance. Mol. Breed. 5:75-83. Campbell, L.H. and Cooke, A.S. 1997. The indirect effects of pesticides on birds. Joint Nature Conservation Committee. CBD, 1994. Convention on Biological Diversity. Text and Annexes. Switzerland. UNEP/CBD/94/1. Conner, A.J. and Dale, P.J. 1996. Reconsideration of pollen dispersal data from field trials of transgenic potatoes. Theoretical Appl. Genetics. 88:770-774. CTNBio, 2000. Comissão Técnica Nacional de Biossegurança. http:/ 22 Biotecnologia Ciência & Desenvolvimento /www.ctnbio.gov.br Dale, P.J. 1994. The impact of hybrids between genetically modified crop plants and their related species: general considerations. Mol. Ecology 3: 31-36. Dale, P.J. and Scheffler, J.A. 1996. Gene dispersal from transgenic crops. In Transgenic Organisms and Biosafety. Schimit, E.R. and Halkeln, T. (Eds.). Springer-Verlag, Berlin. Edmonds Institute. 1998. Manual for assessing ecological and human health effects of genetic engineered organisms. Washington. Gliddon, C. 1994. The impact of hibrids between genetically modified crop plants and their related species: biological models and theoretical perspectives. Mol. Ecology 3:41-44. Gould, F. 1998. Sustainability of transgenic insecticidal cultivars: integrating pest genetics and ecology. Annu. Rev. Entomol. 43:701-726. Gressel, J. 2000. Molecular biology of weed control. Transgenic Res. 9:355-382. Groombridge, B. 1992. Global Diversity. Chapman and Hall, London. Hilbeck, A.; Baumgartner, M.; Fried, P.M. Bigler, F. 1998. Effects of transgenic Bacillus thuringiensis corn-fed prey on mortality and development time of immature Chrysoperla carnea (Neuroptera:Chrysopidae). Environ. Entomol. 27: 480-487. ISAAA. 2000. International Service for the Acquisition of Agri-biotech Applications.http:// www.agbioview.lisbot.com. Jesse, L.C.H. and Obrycki, J.J. 2000. Field deposition of Bt transgenic corn pollen: lethal effects on the monarch butterfly. Oecologia.(on line 19/08/2000). Losey, J.E. 1999. Transgenic pollen harms monarch larvae. Nature 399:314. Mayr, E. 1969. Principles of Sistematic Zoology. MacGraw Hill. N.Y. Mikkelsen, T.R.; Andersen, B.; Jorgensen, R.B. 1996. Risk of crop transgene spread. Nature 380: 31-32. Palm, C.J.; Schaller, D.L.; Donegam, K.K.; Seidler, R.J. 1996. Persis- tence in soil of transgenic plant produced Bacillus thuringiensis var. kurstaki d-endotoxina. Can. J. Microbiol. 42: 1258-1262. Paoletti, M. G.; Pimentel, D. 1996. Genetic engineering in agriculture and the environment: assessing the risks and benefits. BioScience 46: 665-6671. Radosevich, R.S.; Holt, J.S.; Ghersa, C.M. 1996. Weed Ecology: Implications for Weed Management. John Wiley & Sons, N.Y. Rissler, J; Mellom, M. 1996. The Ecological Risks of Engineered Crops. Cambridge, MIT Press. Roughgarden, J. 1998. Primer of Ecological Theory. Prentice Hall. N. Jersey. Saxena, D.; Flores, S.; Stotzky, G. 1999. Inseticidal toxin in root exudates from Bt corn. Nature 402:408. Smalla, K. 2000. Horizontal transfer of antibiotic resistance genes from transgenic plants to bacteria - are there new data to fuel the debate? WHO Seminar. p 13-14. http:// www.who.it/Emissues/GMO/ gmos.htm Steinbrecher, R.A. 1996. From green to gene revolution: the environmental risks of genetically engineered crops. The Ecologist 26, 273-282. Tabashnik, B.E. 1994. Genetics of resistance to Bacillus thuringiensis. Ann. Rev. Entomol. 39.47-79. Tripp,R. 1996. Biodiversity and modern crop varieties: sharpening the debate. Agric. Human Values 13: 48-62. UNEP, 1995. International Technical Guidelines for Safety in Biotechnology. Nairobi, Kenia. United Nations Environment Programme. Wahl. D.H.; Stein, R.A.; DeVries, D.R. 1995. An ecological framework for evaluating the success and effects of stock fishes. Amer. Fish. Soc. Symp. 15:176-189. Wilson, E.O. 1999. The Diversity of Life. Norton Co. N.Y. Woese, C.R.; Kandler, O.; Weelis, M.L. 1990. Towards a natural system for organisms: proposal for the domains Archaea, Bacteria and Eucarya. Proc. Natn. Acad. Sci. USA. 87: 45764579. ANÚNCIO NOVO (Fotolito em anexo) Colocar o anúncio nº 01 (foram enviados 02 anúncios) Biotecnologia Ciência & Desenvolvimento 23 Clones, Gens e Imortalidade Maria Celeste Cordeiro Leite Santos, Professora Associada da Faculdade de Direito da USP, Livre Docente em Direito Penal FDUSP, Doutora em Filosofia do Direito PUC/SP, Membro da Sociedade Internacional de Bioética, Coordenadora da Comissão de Bioética e Biodireito da Ordem dos Advogados do Brasil, Secção São Paulo. Autora do livro O Equilíbrio do Pêndulo A Bioética e a Lei, Editora Ícone. [email protected] O futuro da reprodução humana assistida: Aspectos jurídicos e bioéticos Como a dignidade humana aparece configurada como um direito universal, não se pode esgrimí-la como limite à liberdade científica. A garantia institucional de um núcleo inviolável constitui limite à liberdade científica e tecnológica ( mínimum invulnerável ), que todo estatuto jurídico deve assegurar. 1. Breve resenha histórica A experimentação com seres humanos, sujeitos de inovações, tem sido feita ao longo dos séculos, sem grandes cogitações ou revelações. A necessidade de se criarem mecanismos de controle, porém, tornou-se premente após os abusos cometidos nos campos de concentração, durante a Segunda Guerra Mundial, e resultou no Código de Nuremberg (1947). O aumento do número de situações abusivas levou a Organização Mundial de Saúde a rever esse documento e a promulgar a nova regulamentação conhecida como a Declaração de Helsinque I em 1964, seguida da II, em 1975, da III, em 1983, IV, em 1989, e da V, em 1996. No âmbito da Bioética é importante ressaltar o Relatório Belmont ( The Belmont Report: ethical guidelines for the protection of human subjects, 1978). Desde a década de setenta, os grandes avanços científicos e tecnológicos levaram o Conselho de Organizações Internacionais de Ciências Médicas, juntamente com a Organização Mundial de Saúde, a elaborar as Diretrizes Internacionais para a Pesquisa Biomédica em Seres Humanos, em 1981. Esse documento foi traduzido e editado pelo Ministério da Saúde do Brasil, em 1985 (revisto em 1993). Em 13 de junho de 1988, o Conselho Nacional de Saúde edita a Resolução n.º. 1, que prevê as normas para a pesquisa em Saúde. Hoje vigora no país a Resolução 196/ 96, do Conselho Nacional de Saúde, dispondo expressamente sobre as Diretrizes e normas regulamentadoras de pesquisas envolvendo seres humanos; cumpre as disposições da Constituição Federal do Brasil, de 1988, e da legislação correlata, especialmente as Leis n.º. 8.974, de 5 de janeiro de 1995, sobre o uso de técnicas de engenharia genética e liberação no meio ambiente de organismos geneticamente modificado,s e a Lei n.º. 9.279/96, relativa à propriedade industrial. Vigora ainda a Resolução n.º. 24 Biotecnologia Ciência & Desenvolvimento 1.358/92, do Conselho Federal de Medicina e tramitam, no Congresso Nacional vários Projetos de Lei sobre a matéria, entre eles: o PL 3.638/93, do Deputado Luiz Moreira, o PL 2.855/97, do Deputado Confúcio Moura, e o mais discutido, PL 590/99, do Senador Lúcio Alcântara. Comparativamente, a Resolução nº 1.358/92, do C.F.M. não menciona a clonagem e, entre os projetos citados, apenas o de 97, do Deputado Confúcio Moura, a proíbe, considerando o procedimento como crime. Nesse sentido, também a Lei de Biossegurança Nacional (Lei 8.974/95 e o Decreto 1.752/95) proíbe a clonagem, no art. 8º: É vedado, nas atividades relacionadas a 0GM: ( ... ) II a manipulação genética de células germinais humanas e no art. 13 Constituem crimes: I a manipulação genética de células germinais humanas. A Instrução Normativa CTNBio n.º. 8, de 9 de julho de 1997, em seu artigo 1º, dispõe: art. 1º - Para efeito desta Instrução Normativa, define-se como: ( ... ) IV Clonagem em humanos processo de reprodução assexuada de um ser humano; V - Clonagem Radical processo de clonagem de um ser humano a partir de uma célula, ou conjunto de células, geneticamente manipulada (s) ou não. Art. 2º Ficam vedados nas atividades com humanos: I a manipulação genética de células germinais ou totipotentes; II experimentos de clonagem radical através de qualquer técnica de clonagem. Segue-se a Instrução Normativa CTNBio n.º 9, de 10.10.97 Anexo Normas sobre Intervenção Genética em Seres Humanos, que, em seu Preâmbulo, considera: a) todo experimento ou manipulação genética em humanos como Pesquisa em seres humanos, enquadrando-a na Resolução 196/96, do Conselho Nacional de Saúde, e obedecendo aos princípios de autonomia, não maleficência, beneficência e justiça; b) Somente serão consideradas propostas de intervenção ou de manipulação genética em humanos aquelas que envolvam células somáticas. É proibida qualquer intervenção ou manipulação em células germinativas humanas ( ... ) É importante ressaltarmos ainda a Declaração Universal do Genoma Humano e dos Direitos do Homem, do comitê Internacional de Bioética da UNESCO, de 1997, cujo art. 11, ao se referir às Pesquisas com o Genoma Humano, dispõe: ( ... ) art. 11 não serão permitidas práticas contrárias à dignidade humana, tais como a clonagem reprodutiva em seres humanos ( ... ), a Declaração de Manzanillo, de 1996, revista em 1988, que destaca a importância do Convênio do Conselho da Europa para a Proteção dos Direitos Humanos e a Dignidade do Ser Humano em relação às aplicações da Biologia e da Medicina, que declara em seu considerando n.º 2 b que o genoma humano constitui patrimônio comum da humanidade como uma realidade e não como uma expressão meramente simbólica. 2. Introdução Em junho de 1982, o Secretário de Estado da Saúde e Serviços Sociais da Grã-Bretanha nomeou Mary Warnock, conceituada filósofa da Universidade de Oxford, para presidir um Comitê de Inquérito sobre Fertilização Humana e Embriologia. O Relatório resultante foi dividido em duas partes. A primeira examina os vários procedimentos possíveis para o nascimento de bebês de casais inférteis, considerando o potencial e avançado desenvolvimento da Medicina, ciência e biotecnologia. A segunda parte focaliza os benefícios obtidos pela sociedade com esses procedimentos e considera que precisam ser aplicados procedimentos penais para a salvaguarda de direitos e inclui considerações éticas fundadas na razão. A ênfase da nossa argumentação será ora na primazia dos interesses da criança e valores familiares, ora nos direitos individuais de cada sociedade, advertia Warnock ( Report of the Commitee of Inquirity into Human Fertilisation and Embriology, jul. 1984). Em Moral, não existe um simples e correto ponto de vista. A lei, não obstante, não pode ser apenas a expressão moral. O utilitarismo de certos procedimentos permite-nos calcular os custos e benefícios. Conjugado ao princípio da responsabilidade, o princípio da precaução, conhecido dos juristas e filósofos, aparece como o ponto de equilíbrio na autorização (ou não) de experimentações científicas como a Clonagem Humana. Para Treinch, o mundo da precaução é um mundo onde há uma interrogação, onde os acontecimentos são colocados em questão. No mundo da precaução há uma dupla fonte de incerteza: o perigo, considerado em si mesmo, e a falta de conhecimento científico sobre o perigo. A precaução visa a gerir a espera pela informação. Ela nasce da diferença de tempo entre a necessidade imediata da ação e o momento no qual nossos conhecimentos científicos vão se modificar. Nesse contexto, o Relatório Warnock dedicou o Capítulo 12 a Recomendações sobre os possíveis e futuros desenvolvimentos em experimentação humana (ou manipulação genética da espécie humana). Especificamente sobre a Clonagem procedimento dedicado a produzir seres com um núcleo integrado por genes idênticos aos do organismo, a partir do qual a clonagem foi realizada, com o objetivo de lograr seres geneticamente idênticos. Como tal, a clonagem tem sido vedada por todas as legislações. Para Allbin Eser (Ingenieria genética y reproducion assistida), a divisão artificial de células é eticamente justificável somente quando os valores humanos ficam incólumes. Precisamente o contrário ocorre na produção de clones múltiplos, já que aí podemos formar um número indefinido de indivíduos com um genótipo idêntico, suprimindo assim o caráter individual e único de um sujeito em potencial. A lei alemã de Proteção aos Embriões (art. 7º) ao reconhecer a importância fundamental da inviolabilidade genética, pune a clonagem com sanção penal (Embryonenschutzgesetz ESchgt). Quem cause por meios artificiais a formação e ulterior desenvolvimento de um embrião humano, que possua a mesma informação genética que outro embrião, feto, de pessoa viva ou morta, será punido com reclusão de até 5 anos ou multa. Também a Lei espanhola n.º 35, de 22 de novembro de 1988, considerou, em seu artigo 20, letra h, uma infração muito grave criar clones ou vários seres humanos idênticos. Do mesmo modo, a Lei 42/1988 sobre Doação e Utilização de Embriões e Fetos Humanos, ou de suas Células, Tecidos e Órgãos, dispõe, no artigo 22, que: Serão castigados com a pena de prisão de um a cinco anos e inabilitação especial para emprego ou cargo público, profissão e ofício de seis a dez anos quem fecunde óvulos com qualquer fim distinto da procriação. E o artigo 22.2, especificamente, incrimina:. Com a mesma pena se castigarão a criação de seres humanos idênticos por clonagem e outros procedimentos dirigidos à seleção da raça. Esse instrumento jurídico internacional funda-se na necessidade de proteger a identidade do ser humano, de preservar o caráter aleatório de sua combinação genética natural e seu caráter único, assim como impedir sua instrumentalização. Os genes, as menores unidades de transmissão dos caracteres hereditários, constituem um patrimônio da humanidade. Em 12 de janeiro de 1998, dezenove países europeus firmaram um protocolo na Convenção Européia de Bioética, para proibir a clonagem de seres humanos. ( Art. 1º - toda intervenção que tenha por fim criar um ser humano idêntico a outro vivo ou morto. Jean Michaud comenta que após vários anos de reflexão, a França promulgou várias leis no âmbito da Bioética, com vistas a prevenir os perigos para a integridade da espécie humana (Lei 94.548, de 1º.7.94; Lei 94.653, de 29.7.94, Lei 94.654, de 29.7.94). Condena eugenia e proíbe a patenteabilidade do conhecimento total ou parcial do gen humano, bem como a clonagem. O Direito francês, como o alemão, é uma das poucas legislações que trata especificamente da terapia gênica de célula somática, não aceitando a terapia da linha germinal. Na Itália, o Projeto de 8 de junho de 1992 pronuncia-se a favor da tutela da vida humana desde o seu início, castigando a lesão de embriões ou fetos e a alteração da estrutura genética, bem como a produção de híbridos e a clonagem (art. 5º). O Comitê Nacional de Bioética Italiano aprovou (1990) um documento intitulado Terapia gênica, no qual examina os problemas éticos e jurídicos suscitados pela possibilidade de se aplicar no indivíduo a engenharia genética com a finalidade de corrigir enfermidades hereditárias. O Comitê opõe-se frontalmente à aplicação de Biotecnologia Ciência & Desenvolvimento 25 terapia genética em células germinais. A Convenção do Conselho da Europa, a resolução da Comissão de Direitos Humanos das Nações Unidas, de 8 de março de 1995 (1995/82), as resoluções da Organização Mundial de Saúde, em especial a de 14 de maio de 1997, e a Declaração Universal sobre o Genoma Humano e a dos Direitos do Homem, da UNESCO, de 1997, não permitem práticas contrárias à dignidade humana, ( ... ) tais como a clonagem reprodutiva de seres humanos. Os Estados e as organizações internacionais competentes são convidados a cooperar na identificação de tais práticas e a determinar, no âmbito nacional ou internacional, as medidas apropriadas a serem tomadas para assegurar o respeito pelos princípios expostos nesta Declaração (art. 11). A Inglaterra, em julho de 2000, anunciou que permitirá a clonagem humana para fins de terapia. Íntima é a correlação das disciplinas éticas e legal. Como vimos, o Brasil, a Alemanha, a Austrália, a Dinamarca e a Espanha proíbem expressamente a clonagem humana. Recentemente, a França anunciou, por intermédio do primeiro Ministro Lionel Jospin, que está redigindo uma nova lei que permite a pesquisa no embrião humano para ajudar a corrigir defeitos genéticos de nascença e doenças. Para tanto, seria permitida a retirada de células tronco de embriões de entre 7 e 12 dias, que não forem destinados à reprodução assistida, para serem transferidas para pacientes que sofram de doenças incuráveis como diabete ou o mal de Alzheimer (Reuters e EFE, in: Jornal o Estado de 29.11.2000, p. A14). 3. A arte do possível O impacto da biotecnologia e, em particular, da revolução genética em nossa vida acentuou-se quando, em 1993, os professores Robert Stillmann e Jerry Hall, da Universidade George Wahington, nos Estados Unidos anunciaram a clonagem de embriões humanos (New York Times, 01.11.93). Segundo os cientistas apontados, chegou-se à clonagem como tentativa de ampliar as possibilidades de fertilização in vitro. Não pensaram em levar adiante a evolução de mais do que um embrião monozigótico, de tal modo que os clones não passaram da fase embrionária (duas a oito células de um único embrião). O procedimento usado é conhecido 26 Biotecnologia Ciência & Desenvolvimento como cellmass division ou embryo splitting. Foi usado como o twin (gêmeo) para biópsia, evitando-se danos e procedimentos invasivos. Quantos múltiplos de uma constituição genética particular podem ser criados? 4. Indivíduos, múltiplos e variação genética A clonagem não produz cópias idênticas do mesmo indivíduo. Ela apenas produz cópias idênticas do mesmo genótipo. Gêmeos naturais não são distintos dos artificiais. Há objeções quanto à clonagem pela criação de indivíduos idênticos separados pelo tempo (já que podem ser implantados em diferentes ciclos, talvez anos, como, por exemplo, os filhos de Mr. e Mrs. Wright, cujos twins nasceram com um espaço de dezoito meses, graças a técnicas de procriação humana assistida, na Inglaterra. Podemos chamá-los de gêmeos?) O bebê não pode ser reduzido a seus pais, não a o que é o clone, senão a quem é? Essa visão fundamenta-se na distinção jurídica entre coisa e pessoa (sujeito e objeto). Filhos da Ciência, frutos de um instante do futuro, o tempo virtual. 5. Usando embriões clonados em benefício de outros (siblings) É eticamente dúbio o procedimento que sacrifica um elemento para salvar outro. É diversa a situação em que tiramos uma célula ou duas para biópsia embrionária da que tiramos a célula para criarmos um clone? Antes do estágio de 32 células, temos um número viável de embriões em potencial. Esses embriões podem ser recombinados em um outro embrião viável. 6. Substituição nuclear (transferência nuclear) Em julho de 1996, em Roslin, na Escócia, nasce Dolly, uma amistosa ovelhinha da raça Finn-Dorset. A equipe de Ian Wilmut e Keith Campbell conseguiu uma cópia idêntica de uma ovelha mais velha, a partir de uma célula retirada de sua glândula mamária cultivada in vitro. Outros clones famosos de Roslin, as ovelhas Megan e Morag, nasceram um ano antes dela, em 1995. O procedimento de transferência nuclear inclui: preparação de um ovócito enucleado (citoplasto), isolamento da célula doadora ou do núcleo doado, ativação do citoplasto, fusão celular, cultura do embrião, transferência do embrião para um útero hospedeiro. Outros procedimentos foram usados em Honolulu, pelo grupo de Ryuzo Yanagimachi, para clonar camundongos (Wakayama et alii, 1998). Eles o clonaram a partir de células cumulus que circundam o óvulo no ovário (MAGIC). Através desse método produziram 22 fêmeas de camundongos saudáveis, que, depois, foram cobertas e reproduziram. As aplicações práticas desses procedimentos em animais são: a pesquisa, produzir variedades de laboratórios mais puras; a pecuária e outras áreas de criação domestica pela replicação de animais de elite; a preservação de espécies; a multiplicação de tecidos, em vez da de indivíduos inteiros para serem utilizados na medicina humana; clínicas reprodutivas humanas, etc. 7. Variação sobre o tema: a clonagem de tecidos No final de 1998, o Human Fertilization and Embryology Authority, em um relatório conjunto com o Human Genetics Advisory Commission, autorizou a tecnologia de clonagem para cultivar tecidos humanos que fossem usados para recuperação. As células seriam usadas para criar um embrião e depois as células do jovem embrião seriam cultivadas para fornecer tecido geneticamente idêntico ao do doador. O embrião propriamente dito seria sacrificado (até 14 dias). Os médicos, destarte, poderiam começar a ativar e a desativar genes conforme desejassem. Ao mesmo tempo, os biólogos estão desenvolvendo maneiras de induzir células cultivadas a crescerem dentro e em torno de moldes, de modo que se formem fac-símiles de órgãos humanos. A Roslin Bio Med, a nova companhia de biotecnologia do Instituto Roslin, vem trabalhando nesse campo. 8. Clonagem com transferência genética: a produção de drogas de valor farmacêutico Pharming, a criação extensiva de animais transgênicos é exemplo desse caminho. Sem dúvida, a ciência avança num ritmo estonteante e há ainda uma imensidade de coisas a serem descobertas. Quanto tempo levará para que os seres humanos completos possam ser clonados rotineiramente? Para Ian Wilmut: ( ... ) Consideramos a clonagem de ser humano como uma temível manobra diversionária: supérflua, como procedimento médico e, de maneira geral, repugnante. ( ... ) A clonagem humana está agora no espectro de possibilidades futuras e nós, mais do que quaisquer pessoas, contribuímos para que lá fosse colocada. Gostaríamos que não fosse assim, mas é e continuará sendo enquanto a civilização existir. (The Second Creation, 2000). Richard Seed, formado em física, em 1998, lançou uma campanha para clonar um ser humano. Faltavam-lhe fundos, mas, em meados de 1999, anunciou que clonará sua esposa. Um desejo equivocado de imortalidade contagia muitos. Ainda assim, será que justifica a clonagem de seres humanos? A engenharia de linhagem germinativa acha que há uma grande probabilidade de acontecer no século XXI. 9. Apenas mais uma tecnologia reprodutiva? 10. Direitos humanos, deveres humanos A reprodução não ocorre com facilidade entre os seres humanos. Todavia, a clonagem não é projetada para auxiliar a reprodução sexual normal. Ela é um exercício de replicação. A fertilização é substituída por outro processo: o de transferência nuclear. Crucial é o fato de que a clonagem não produz indivíduos geneticamente singulares. O sacrifício da singularidade nos leva a perguntar se são os indivíduos clonados realmente idênticos ou apenas semelhantes? Os genes não são tão constantes como imaginamos. Eles são sujeitos a mutações. Além disso, eles operam em constante diálogo com o ambiente que os circunda. Gêmeos idênticos podem dividir um mesmo útero, mas não ocupam a mesma parte do útero. Há probabilidade de as diferenças serem ligeiras, mas, a despeito disso, pode haver diferenças físicas e até funcionais. O clone ancestral pai ou mãe e o clone criança estão em pontos diferentes de seu programa genético. Deixando de lado as diferenças de mutação e expressão, eles estão operando permutações diferentes de seus genes, retiradas de pontos diferentes, no programa. Funcionalmente, a qualquer momento dado no tempo, eles serão pessoas muito diferentes. Por outro lado, a influência dos genes é difundida. A criança clonada estaria operando no mesmo programa genético em que seu clone progenitor ainda estivesse, e poderia esperar, no mínimo, que se restabelecesse ou se recriasse a pessoa que fora seu pai ou sua mãe. Em suma, a clonagem pode produzir um conjunto de indivíduos quase indistinguíveis. Contudo, esses podem ser visivelmente diferentes, sendo que os clones genotípicos diferem mais do que os outros que são gêmeos idênticos convencionais. Os recentes conhecimentos sobre o genoma humano e suas aplicações repercutiram em todos os seres, dado que o genoma é uma constante comum a todos. Em relação às intervenções genéticas humanas, abre-se uma nova perspectiva: a dos deveres humanos para com outros membros da espécie humana, derivados da solidariedade e da responsabilidade coletiva. O controle e a prevenção de algumas ações relacionadas com o genoma humano comporta a declaração legal de sua licitude. Uma vez estabelecido este marco é preciso delimitar os bens jurídicos, valores ou interesses, que podem se ver afetados por essas intervenções. Em qualquer caso, não se pode aspirar a soluções definitivas, primeiro porque ainda não são suficientemente conhecidos os resultados a que podem dar lugar as aplicações derivadas desse conhecimento. Em segundo lugar, porque o que na atualidade pode se mostrar como indesejável, pode não ser percebido assim no futuro. As correntes humanistas das últimas décadas deram especial reconhecimento à dignidade humana e ao livre desenvolvimento da personalidade, como valores individuais do ser humano. A maior parte dos bens jurídicos de titularidade individual como a vida, a integridade física e psíquica, a liberdade de decisão ou autodeterminação, a intimidade, podem se ver comprometidos pela clonagem. Perfilam-se outros de caráter coletivo: a inalterabilidade e intangibilidade do patrimônio genético do ser humano, para garantir a própria integridade e diversidade da espécie humana; a identidade e irrepetibilidade característica do ser humano, como garantia de sua individualidade; a dotação genética, de linha genética masculina e feminina e a própria sobrevivên- cia da espécie humana como tal. Além desses, há ainda os bens jurídicos de natureza difusa (interesses difusos), que se referem à sociedade como um todo, de forma que os indivíduos não têm disponibilidade sem afetar a coletividade. O manejo ecológico das espécies tem por base a proteção da diversidade biológica. Diversidade designa a riqueza do conjunto dos seres vivos (biocenose), localizada em determinada área (biotopos). A clonagem põe em questão o equilíbrio ecológico da espécie humana. 11. O direito de clonar e de ser clonado Em face dessas realidades, e pensando para além delas, não estár excluído que se desenvolvam atividades mais ou menos clandestinas, é natural que se reflita sobre o enquadramento jurídico dessas novas técnicas e sobre alguns procedimentos, como a clonagem, em particular. Sendo um problema básico de cidadania, ele requer humildade para que se faça escutar a voz de todos os cidadãos. O artigo 226, §7º, da Constituição Federal Brasileira, consagra o direito fundamental de constituir família. Trata-se do direito fundamental de procriar e de ver a prole juridicamente reconhecida. A questão que nos interessa é, porém, diferente: é a de saber se há um direito à autoprocriação ou replicação própria ou de terceiros, por meio do recurso das novas técnicas biomédicas. É fácil dizer que o preceito não foi elaborado com essa última acepção. Trata-se apenas de uma faceta de um pretenso direito subjetivo ao que é possível tecnologicamente. A questão seria tida como privada e não serão bem aceitas mais do que os vagos limites da licitude, estabelecidos, aliás, com generosidade. A Família e o Estado vivem em permanente tensão dinâmica que, segundo a matéria de que se trata, se resolva mais a favor dos critérios particulares dos indivíduos ou segundo as exigências do interesse público. Não se estranha que, nesse assunto particular, a tensão se torne aguda. Segundo a nossa tradição cultural, a reserva da intimidade da vida familiar não pode excluir o Estado e a lei de uma intervenção extensa, nesta matéria. Na Europa e no nosso país, o Estado não fixou as barreiras longínquas da legalidade, deixando à mera consciência dos Biotecnologia Ciência & Desenvolvimento 27 cientistas o poder de fixar o que é lícito e bom. O direito à identidade pessoal releva entender-se que o conhecimento das raízes genéticas e de sua dotação é tão forte que outros interesses não justificam sua restrição. O Direito Penal limita-se a tutelar a dignidade humana e a defender a liberdade da decisão individual. Em outro artigo do Código Civil, afirma-se que, as ações relativas a filiação, são admitidos, como meio de prova, os exames de sangue e quaisquer outros métodos cientificamente comprovados. Quem são os pais do ser clonado? Na inflação de pretensos direitos, não tem sentido, no caso, interpretar a expressão direito ao filho, contra a sociedade ou a espécie humana. Continuar a espécie continuar-se é a liberdade das liberdades e a recurso da clonagem não cabe no exercício da liberdade constitucional de procriar. 12. Artificial Life Clones e Imortalidade Para Christopher Langton, a vontade de purificação dos genes pertence à vontade de purificação do planeta. Fala-nos de seres artificiais purificados de toda doença possível, em um mundo absolutamente perfeito. Em sua utopia, a higiene aparece como fator dominante de regulação social, permitindo a recriação de Adão, no Paraíso, antes do pecado, através do artefato tecnológico. A clonagem do indivíduo perfeito aparece nessa lógica utópica da saúde perfeita ou de um Chernobyl biológico. Como vimos, a clonagem pode nos tornar imortais. De que forma os gens são imortais? Nossos gens provêm do mais antigo ancestral humanóide e esses gens provêm da mais antiga forma de vida na Terra. Transmitem-se para as próximas gerações pelo conhecido método de reprodução. Essa é uma espécie de imortalidade. Sob certo aspecto é esse o sentido da palavra reprodução. As partes envolvidas pela Clonagem Humana são: a) os indivíduos que desejam a clonagem própria ou de terceiros, outra pessoa viva ou morta, como um filho morto, por exemplo; b) a equipe técnicocientífica, que dispõe dos meios para realizar essa vontade; 28 Biotecnologia Ciência & Desenvolvimento c) o ser humano que resultar clonado: o clone; pode suceder que as duas primeiras partes coincidam. Por outro lado, até que a clonagem se converta em uma técnica viável e efetiva para a reprodução humana, temos que incluir todas as mulheres e embriões humanos que sofreram a experimentação. a) O ponto de vista do clonador ou a extensão do direito à reprodução O ponto de partida da clonagem com fins reprodutivos é a vontade de alguém que quer clonar outro. Existe um direito da pessoa a auto-reprodução, ou à reprodução alheia, pela técnica de clonagem, ou existe, ao contrário, o direito a ser concebido sob determinadas condições? Poderia o Direito criar a situação de órfãos biológicos ? Não pode haver paternidade nem maternidade sem reprodução sexual. A clonagem, como mecanismo de reprodução assexual, faz desaparecer ambas as figuras (pai, mãe). A falta de pais biológicos não é a única conseqüência desse processo. A pessoa clonada está geneticamente predeterminada pela vontade do clonador. Suas características genéticas não serão aleatórias, mas conseqüência de uma eleição julgada útil para o clonador. O criar clones para utilidade do clonador, ou da sociedade, é uma instrumentalização humana intolerável, que abre as portas ao Admirável Mundo Novo, de Huxley. O ser humano tem o direito a que seu patrimônio genético seja único, irrepetível e não predeterminado por ninguém. Isso não mostra que seja justificada a intervenção genética na linha germinal, com finalidade estritamente terapêutica. O problema delicado consiste em determinar quais são as patologias que justificariam esse tipo de intervenção. Na atualidade, o Convênio dos Direitos Humanos e a Biomedicina proíbem qualquer modificação do genoma humano que afete a descendência. b) O ponto de vista do agente da clonagem. Os limites à liberdade de investigação A segunda parte envolvida na clonagem é a equipe científica capaz de levála a termo. Aqui, o conflito se daria entre a liberdade de investigação e a proteção da dignidade humana. Assegura-se que as tecnologias sendo a clonagem mais uma são em si mesmas neutras e que sua valoração depende dos objetivos perseguidos. Todavia, a experimentação nesse campo exige o sacrifício de muitos embriões humanos e a utilização de várias mulheres (instrumentalização e desproteção do embrião). Em todo o caso, o resultado que oferece a técnica em si é a de um ser geneticamente idêntico a outro, desprovido de pais biológicos. Não parece que tal resultado seja neutro, porque afeta um terceiro: o novo ser humano. Por isso, quando orientada a reprodução humana para a clonagem, não se exerce aí um direito, mas uma atividade ilícita. Como a dignidade humana aparece configurada como um direito universal, não se pode esgrimi-la como limite à liberdade científica. A garantia institucional de um núcleo inviolável constitui limite à liberdade científica e tecnológica (mínimum invulnerável), que todo estatuto jurídico deve assegurar. c) O ponto de vista do ser humano clonado: o direito a uma determinada forma de concepção O dilema que se propõe é: Será irrelevante para um ser humano ser geneticamente idêntico a outro, por decisão de um terceiro e não possuir pais biológicos? Ou, em outros termos, a unicidade da dotação genética, mais a paternidade e a maternidade biológicas são essenciais ao ser humano? Devem ser tutelados juridicamente? Desde logo, se a resposta é afirmativa, a tutela deve-se centrar precisamente no momento da concepção. O filho a ser concebido tem direito a ser fruto de uma reprodução sexual, que é a única que outorga uma filiação biológica e não atenta contra o princípio da igualdade na concepção. O novo ser humano não pode ser fabricado com um propósito ou fim. O modelo clonado resulta de um processo de reprodução, uma propriedade, em que um fornece a matéria e o outro elabora. Ele nada mais é que um programa preconfigurado pelas expectativas daqueles que elegeram sua dotação genética. As vítimas dessa situação sofrem um autêntico aprisionamento genético, que é uma das formas mais invasivas de atentar contra a liberdade. A liberdade é irredutível a qualquer manipulação. Não pretendemos justificar uma sanção irreversível dos tratamentos terapêuticos na linha germinal, assunto a que já nos referimos. Uma coisa é realizar uma terapia gênica para evitar o desenvolvimento posterior de uma enfermidade, e outra é projetar e criar um ser humano, com um determinado código genético. Supostamente, quando falamos de terapia gênica não incluímos a eliminação de embriões pré-implantatórios. Isso não é terapia, porque não cura, mas é sim acabarmos com uma vida humana incipiente. A reprodução sexuada produz indivíduos geneticamente diferentes. A clonagem, em conseqüência, constitui um procedimento dirigido a produzir seres com um núcleo integrado por genes idênticos aos do organismo a partir do qual a clonagem foi realizada. Tem como objetivo lograr seres geneticamente idênticos. A clonagem humana, como método de auto-reprodução ou de reprodução de terceiros (um filho morto), é contrária à natureza da pessoa humana, sendo vedada pela maioria das legislações vigentes. A Convenção de Oviedo (12.01.98) celebrada em Paris, elaborou um Protocolo de Clonagem. Esse protocolo foi firmado por dezenove Estados. Um dos pontos a ressaltar é que: ( ... ) Proíbe-se qualquer intervenção que tenha por objetivo criar um ser humano geneticamente idêntico a outro, seja vivo ou morto. Para os efeitos deste artigo, a expressão ser humano geneticamente idêntico a outro ser humano significa compartilhar com o outro a mesma carga nuclear genética. Conclusões Contra a clonagem humana não se pronunciaram apenas autoridades religiosas, teólogos, políticos e filósofos da categoria de Hans Jonas, mas também relevantes homens da Ciência. Para citar um só exemplo: o legendário James Watson, que, em 1953, junto com Francis Crick, descobriu a dupla hélice do DNA, e é um dos responsáveis pelo Projeto Genoma Humano, nunca olhou com bons olhos esse assunto. Já em 1971, escreveu um artigo: Moving towards the clonal man: is this what we want ?, advertindo sobre a possibilidade de que, em um prazo de 20 ou 50 anos, fosse viável a reprodução clônica da espécie humana. A Lei sobre Técnicas de Reprodução Assistida, de1988, da Espanha, tem relação com o caso concreto que estamos examinando, no artigo 20.B.2, letras K e L: ( ... ) criar seres humanos idênticos, por clonagem e outros procedimentos dirigidos à seleção da raça; e a criação de seres humanos por clonagem ou qualquer das variantes, ou qualquer procedimento capaz de originar vários seres humanos idênticos constituem delitos. Também o Código Penal Espanhol, de 1995, no seu artigo 162:2, prevê: Com a mesma pena se castigarão a criação de seres humanos idênticos por clonagem e outros procedimentos dirigidos à seleção de raça. a) O bem jurídico protegido é de caráter coletivo: a identidade e a irrepetibilidade do ser humano e a intangibilidade do patrimônio genético. Não devemos esquecer a importância da diversidade biológica, como garante, a longo prazo, a sobrevivência das espécies, no caso, a humana. b) Há também uma projeção individual, enquanto tal lesão comporta, ao mesmo tempo, um atentado à dignidade das pessoas afetadas, no caso em que cheguem a nascer. O primeiro tipo não compreende as práticas de clonagem em si mesmas, que se realizem sobre um óvulo mediante sua enucleação e a introdução de um novo núcleo de uma célula somática, o que poderia dar lugar ao tipo de manipulação genética. Clones: filhos sem pais, nem humanos, nem animais, nem sequer divinos! À vista do exposto, podemos concluir que o direito dos pais a se reproduzirem tem um conteúdo de direitodever. Direito que consiste em ninguém poder impedir ou obrigar um casal a procriar, mas que não inclui satisfazer a ânsia de reprodução a qualquer preço. Tem também uma dimensão de dever, que inclui, em primeiro lugar, o princípio da filiação, que assegura a existência de um pai e uma mãe biológicos e de um código genético original. A liberdade de investigação tem como limite o respeito aos direitos, o que veda a clonagem humana. Além disso, não se sabe a idade da pessoa clonada (se a cronológica ou a da pessoa da qual se extraiu a informação genética), nem a evolução vital dessas pessoas, se serão estéreis (ou não). A possibilidade da eugenia, a redução da diversidade genética humana, o desequilíbrio ecológico das espécies, a criação de bancos de órgãos de seres humanos clonados são fatores que não podem ser descartados. Por outro lado, Higuera Guimera atenta para casos difíceis de ser avaliados, nos quais a clonagem não só seria legítima, mas também lícita, na Espanha. Concretamente, trata-se do recurso à técnica de divisão gemelar para garantir o êxito da fecundação in vitro, quando a mulher tem problemas de ovulação, e para praticar sem riscos o diagnóstico pré-implantatório do embrião. Finalmente, a clonagem não é uma intervenção curativa, sequer alternativa. Cria uma situação assimétrica entre o homem e a mulher. A mulher pode se auto-reproduzir, o que será impossível para o homem, podendo mesmo se chegar à extinção total da figura masculina. A clonagem produz alterações, ou até mesmo cancela, as relações parentais e familiares conhecidas. A consciência de ser a cópia genética de outro indivíduo humano poderá sufocar a autenticidade, a peculiaridade do próprio ser. A clonagem humana deve ser posta, por tais motivos, em um plano qualitativamente diverso do da clonagem animal. Referências Bibliográficas WAKAYAMA Teru, Perry AC, et alii Full Term development of mice from enucleated oocytes injected with cumulus cell nuclei, in : Nature. 394: 369-374, 1998. WILMUT,Ian et CAMPBELL, Keit. The Second Creation. Trad. Ana Deiró, Rio de Janeiro, Objetiva, 2000. SANTOS, Maria Celeste Cordeiro Leite. Imaculada Concepção. Nascendo in vitro e morrendo in machina. Aspectos históricos e bioética da procriação humana assistida no Direito Penal Comparado. São Paulo, Ed. Acadêmica, 1993. ________ O Equilíbrio do Pêndulo. A Bioética e a Lei. Implicações Médico Legais. São Paulo, Ícone Editora, 1998. MINTIER,Brigitte Feuillet LEmbryon Humain Approche Multidisciplinaire. Paris, Economica, 1996. HEYMANN DOAT Genetique & Droits de LHommo. Paris, Univ. Paris Sud, 1998. Biotecnologia Ciência & Desenvolvimento 29 As inúmeras modificações que estão sendo feitas em alguns dos milhares de genes de camundongos já oferecem uma lista de centenas de animais knockouts ou transgênicos, à disposição de cientistas de todo o mundo. Aron Jurkiewicz Diretor Geral do Centro de Desenvolvimento de Modelos Experimentais em Medicina e Biologia (CEDEME) e Professor Titular de Farmacologia da EPM/UNIFESP FOTO CEDIDA PELO AUTOR A maioria dos genes humanos parece ter uma versão equivalente em outros animais, o que torna possível obter novos e melhores conhecimentos sobre a fisiologia, farmacologia e enfermidades humanas usando, por exemplo, camundongos modificados geneticamente. Estima-se que, somente no ano passado, foram criados e utilizados 25 milhões de camundongos em todo o mundo, destinados a pesquisas em biomedicina, prevendo-se um aumento de 10% a 20% por ano, na primeira década do novo milênio (Malakoff, 2000). Parte desses camundongos pertence ao grupo dos animais geneticamente modificados (AnGMs ). As inúmeras modificações que estão sendo feitas em alguns dos milhares de genes de Figura 1 Caixa de passagem (pass-through) de aço inoxidável, aberta, em um laboratório de criação. Notar: 1- As duas portas internas abertas mostram o interior da caixa de passagem. 2- Gaiolas de camundongos no interior, para dar uma idéia do espaço disponível; 3A parte interna das duas portas do lado oposto, fechadas, ao fundo. Essas portas externas estão travadas, enquanto as portas internas estão abertas. Fechando-se as portas internas, acende-se uma luz UV interna, por algum tempo, sendo que as portas interna e externa ficarão travadas durante esse período. 4- Painel de controle, em que a lâmpada piloto vermelha está acesa, indicando que alguma porta está aberta. Há um outro painel e uma lâmpada na parede oposta, que não sâo mostrados. 5- Visor de vidro isolante térmico e acústico, que permite a observação do laboratório a partir do corredor externo 30 Biotecnologia Ciência & Desenvolvimento camundongos já oferecem uma lista de centenas de animais knockouts (ou seja, com gens deletados) ou transgênicos, à disposição de cientistas de todo o mundo. Há dois anos atrás, o catálogo de um dos produtores comerciais, os Laboratórios Jackson (1998), nos Estados Unidos, listava modelos de animais com deficiência ou com superexpressão de receptores de drogas (como adrenalina, angiotensina e insulina), de enzimas (como as produtoras de óxido nítrico), de substâncias endógenas (como interferon), entre inúmeros outros modelos. Sob o ponto de vista econômico, o uso de AnGMs tem sido alvo de importantes análises, críticas e especulações. Apenas para exemplificar sua importância econômica, sabe-se que a manutenção de duas a três mil gaiolas de camundongos transgênicos custa anualmente de US$ 800.000,00 a US$ 1.000.000,00 (Vogel, 2000). Outros aspectos, como os relativos a direitos de patentes, têm gerado muitas discussões (Marshall, 2000) que, entretanto, fogem do objetivo do presente artigo. Pretendemos, neste artigo, discorrer sobre a biosseguranca em relação a AnGMs, quanto à produção, manutenção e utilização desses animais em laboratório. Por que biossegurança para AnGMs ? Embora possamos antever inúmeros benefícios em conseqüência do desenvolvimento e das pesquisas com animais geneticamente modificados, existem, pelo menos, três tipos de risco que devem ser evitados. Basicamente, podemos enumerar: 1) contaminação acidental do pesquisador ou do tratador; 2) liberação acidental de um AnGM potencialmente danoso; 3) contaminação de animais não-GM ou de outros An-GMs. Portanto, a biossegurança trata fundamentalmente de medidas que visam a controlar e evitar esses riscos. Níveis de biossegurança Os riscos podem variar de acordo com as características do AnGM, já que, obviamente, esses animais diferem entre si segundo o risco que poderiam oferecer. Dessa forma, os AnGMs são classificados em 4 níveis de biossegurança (tabela 1). Em resumo, os AnGMs são de nivel de biossegurança cada vez mais elevado, conforme o eventual risco de transmissibilidade de doenças (devido, por exemplo, à incorporação de uma parte do genoma de um vírus que tenha sido utilizado na fabricação do AnGM ), de produção de substâncias tóxicas; de sua susceptibilidade a infecções que não ocorrem na espécie equivalente não geneticamente modificada; ou da sua maior aptidão de sobrevivência em relação aos equivalentes não geneticamente modificados. Segundo a instrução normativa n. 12 da CTNBio, considerando os respectivos níveis de biossegurança, os AnGMs são classificados em 2 grandes grupos de risco: o grupo I (compreendendo AnGMs do nivel de biossegurança 1) e grupo de risco II (compreendendo AnGMs dos níveis de biossegurança 2, 3 e 4). Obviamente, as medidas de biossegurança variam de acordo com o grupo de risco e o respectivo nível de biossegurança. Critérios e normas de biossegurança para AnGMs como evitar e controlar os riscos Os mecanismos ou procedimentos disponíveis para controlar e evitar riscos foram por nós divididos arbitrariamente em, pelo menos, sete grupos distintos, a saber: 1) Estabelecimento de um sistema de controle e de credenciamento institucional, em nível governamental; 2) Existência de edificações especiais e adequadas; 3) Uso de equipamentos e outros materiais apropriados; Tabela 1 - Classificação dos animais geneticamente modificados (AnGMs) quanto ao nível de biossegurança Nível 1 Aqueles que, após manipulação genética, não tiverem alteradas as características de transmissibilidade de doenças. Podem conter genoma, mesmo que completo, de vírus que não leva a doenças infecciosas transmissíveis Nível 2 Aqueles que, passam a expressar substâncias sabidamente tóxicas, para as quais existam formas de prevenção ou tratamento. Aqueles que tiverem mais de 75% do genoma de vírus (da classe de risco 2) capaz de levar a doenças infecciosas transmissíveis; e aqueles que passam a ser susceptíveis a infecções que não ocorrem na espécie equivalente. Nível 3 Aqueles que tiverem mais de 75% do genoma de vírus (da classe de risco 3) capazes de levar a doenças infecciosas transmissíveis. Aqueles que passam a ser mais aptos à sobrevivência que os equivalentes não geneticamente modificados. Nível 4 Aqueles que tiverem mais de 75% do genoma de vírus (da classe de risco 4) capazes de levar a doenças infecciosas transmissíveis. Aqueles que passam a expressar substâncias sabidamente tóxicas, para as quais não existam formas de prevenção ou tratamento. 4) Participação de pessoal treinado; 5) Uso de sistemas de controle e vigilância institucionais; 6) Outros mecanismos como controle sanitário, genético, nutricional e ambiental; 7) Outras atividades: fabricação de AnGMs, pesquisa , banco de embriões, etc. Controle institucional e governamental Esse setor está bem estruturado em nosso país e permite o trabalho com AnGMs sob um controle eficiente e sem grandes exigências burocráticas. Em 5 de janeiro de 1995, o Brasil regulamentou a competência da Comissão Técnica de Biossegurança (CTNBio), através da Lei 8.974, que foi recentemente alterada pela Medida Provisória 2.137, de 28 de dezembro de 2000. Compete à CTNBio, entre outras atribuições, o estabelecimento de normas técnicas de biossegurança para atividades que envolvam Organismos Geneticamente Modificados (OGMs). A manipulação de AnGMs só pode ser realizada por instituições que possuam Certificados de Qualidade em Biossegurança (CQBs) e que tenham constituído Comissões Internas de Biossegurança (CIBios), segundo a Instrução Normativa n. 1 da CTNBio. Essas instituições devem apresentar relatórios anuais de suas atividades com OGMs e podem ser vistoriadas pela CTNBio. Pelas instruções normativas 12, 13 e 15 da CTNBio foram estabelecidos critérios para trabalhos em contenção com AnGMs (cujos detalhes veremos, em parte, abaixo), para importação de AnGMs e para trabalho com animais não-AnGMs, onde AnGMs são manipulados. Normas para trabalho em contenção com AnGMs Essas normas envolvem critérios operacionais, descrição de edificações e laboratórios, equipamentos e outros materiais apropriados, cuidados com o pessoal que manipula os animais e sistemas de vigilância e controles locais. Os critérios mínimos necessários, mas não suficientes, são simples. Basicamente, os animais devem estar alojados em área física separada, de fácil limpeza e munida de barreiras contra insetos e outros animais. O acesso só deve ser permitido a pessoal credenciado (tabela 2). A partir desses critérios mínimos, os biotérios e salas de experimentação são divididos em quatro níveis de biossegurança, de NB-A1 a NB-A4, que estão apresentados nas tabelas de 3 a 6. Para animais de nível NB-A1, a única exigência adicional é que o descarte de animais e outros materiais e a criação sejam feitos com Biotecnologia Ciência & Desenvolvimento 31 Tabela 2 - Características mínimas necessárias, mas não suficientes, para que Biotérios e Salas de Experimentação possam ser usados para trabalhos com AnGMs (Instrução normativa nº. 12, de 27/5/98) Elemento Porta principal Acesso ao biotério Construção Animais Barreiras físicas para insetos e outros animais Condição Sempre trancada Restrito a pessoas credenciadas Deverá: a) facilitar a limpeza e a desinfecção b) Evitar acúmulo de poeira Alojados em áreas fisicamente separadas, se de diferentes espécies e não envolvidos em um mesmo experimento. Presentes em todas as áreas que permitam ventilação Tabela 3 - Características do Biotério e Sala de experimentação NB-A1 (Adequados para trabalhos com AnGMs de Nível de Biossegurança 1) Elemento Características mínimas descritas na tabela 2 Descarte de material proveniente de OGMs Manipulação Condição Presentes Feito de forma que evite seu uso como alimento de outros animais, salvo em condições especiais. Feita de forma que evite a liberação acidental do animal no meio ambiente. Tabela 4 - Características do Biotério e Sala de experimentação NB-A2 (Adequados para trabalhos com AnGMs de Nível de Biossegurança 1 e 2) Elemento Condições exigidas para NB-A1 Normas de acesso para pessoas autorizadas, qualificadas e cientes dos riscos inerentes aos experimentos. Vacinação de pessoal contra agentes infecciosos usados nos experimentos Presença de ante-sala Condição Presentes Elaboradas pela CIBio, Quando apropriado. Obrigatória, entre área de circulação e área de alojamento dos animais Material contaminado Acondicionados apropriadamente para desinfecção, que poderá ser feita fora do biotério Agulhas, seringas, ou instrumentos que Devem ser acondicionados em recipientes resistentes, até o possam ferir a pele. momento da descontaminação Obrigatório Uso de máscara, gorro, luva e protetores para os pés, todos descontaminados. maior rigor, para evitar a liberação no meio ambiente (tabela 3). Para NB-A2, além das características anteriores, aumentam-se as exigências quanto ao pessoal (vestimenta especial e eventual vacinação), edificação (ante-sala) e descarte (tabela 4). Embora não exigível, é recomendável o uso de câmara de passagem de dupla porta (pass32 Biotecnologia Ciência & Desenvolvimento throughs). Essa câmara permite a saída de gaiolas e outros materiais usados (Figura 1). Para NB-A3, as exigências são ainda maiores (tabela 5), destacando-se, basicamente, a obrigatoriedade de autoclave de dupla porta para a entrada de material e alimentos, pressão de ar diferenciada nas salas e corredores, com detectores, microiso- ladores para os animais, incinerador e alarmes. Finalmente, para NB-A4 as exigências são ainda maiores (tabela 6). Outros controles: sanitário, genético, nutricional, ambiental Embora esses controles, bem como as outras atividades referidas abaixo, não se relacionem diretamente com biossegurança de AnGMs, é fundamental que os biotérios tenham um sistema de controle sanitário (para detectar a presença de ecto e de endoparasitas, e de infecções por microorganismos e vírus); genético (para detectar eventuais mutações ); nutricional (para garantir a qualidade dos alimentos e do animal); e ambiental (para controlar eventuais alterações de temperatura, umidade e presença anormal de gases e vapores). Outras atividades: fabricação de AnGMs, pesquisa, banco de embriões Entendemos que um biotério moderno deva estar envolvido com pesquisa científica em todos os níveis, incluindo aquela relacionada com a fabricação de animais transgênicos. Outro setor de maior importância deve ser o da criopreservação, que deve manter um banco de embriões congelados, que podem servir de salvaguarda em caso de acidentes que levem à extinção de uma ou mais colônias. Referências Bibliográficas CTNBio MCT, Resolução n. 03, de 30/10/1996 - aprova o estatuto nacional da Comissão técnica Nacional de Biosegurança - CTNBio, Cadernos de Biossegurança 1 (CTNBio) - Legislação, p. 61, 2000. CTNBio MCT, Instrução Normativa n. 01, de 6/9/1996 - Dispõe sobre o requerimento e a emissão do certificado de qualidade em biossegurança CQB e a instalação e o funcionamento das comissões internas de biossegurança - CIBio, Cadernos de Biossegurança 1 (CTNBio) - Legislação, p. 75, 2000. CTNBio MCT, Instrução Normativa n. 12, de 27/5/1998 - Normas para trabalho em contenção com animais geneticamente modificados, Cadernos de Biossegurança 1 (CTNBio) - Legis- Tabela 5 - Características do Biotério e Sala de experimentação NB-A3 (Adequados para trabalhos com AnGMs de Nível de Biossegurança 1, 2 ou 3) Elemento Condições exigidas para NB-A2 Quatro áreas distintas: (1) ante-sala, (2) sala de materiais, (3) sala de a-nimais, (4) sala de experimentação. Fluxo de ar Pressão de ar Detector de alterações de pressão de ar Alojamento dos animais em microisoladores. Animais Material biológico capaz de propagar o agente infeccioso Líquido efluente do biotério (pias, ralos, etc) Pia e chuveiro acionáveis sem o uso das mãos. Ralos Autoclave de dupla porta Incinerador de animais Descontaminação de superfícies Procedimentos de emergência (incluindo o uso de alarmes) em caso de acidentes. Coleta de amostras de soros dos usuários no início dos experimentos. Condição Presentes Presentes No sentido de 1 para 4, com filtros esterilizantes na entrada e na saída de ar. No final, o ar deve ser jogado no meio externo. Sala dos animais e de experimentação com pressão negativa em relação à sala anterior. Presentes Obrigatório Jamais poderão deixar as salas apropriadas Não poderá deixar o biotério sem descontaminação. Deverá ser descontaminado antes de esgo-tamento sanitário, em caixas de contenção. Presentes na ante-sala e na sala de materiais. Ausentes na sala de animais ou de experimentação. Ausentes na sala de animais ou de experimentação. Presente Presente. Diariamente Presentes Obrigatório Tabela 6 - Características do Biotério e Sala de experimentação NB-A4 (Adequados para trabalhos com AnGMs de Nível de Biossegurança 1, 2, 3 ou 4) Elemento Condições exigidas para NB-A3 Construção Usuário Condição Presentes Prédio isolado, patrulhado 24 horas por dia. Acesso por cartão magnético ou digital. Registro obrigatório do nome do usuário e do tempo de cada permanência. Toda informação será arquivada por tempo 5 vezes maior que o maior período de incubação das doenças a que estão expostos. Duas áreas adicionais: 1) sala de troca de vestimenta, Presentes, com incineração obrigatória dos animais antes com chuveiro central, armários e pia; 2) sala de do descarte. necropsia com incinerador. Comunicação entre salas Dupla porta, abertura sem mãos. Filtração e exaustão de ar Dupla barreira de filtragem, para caso de mal funcionamento de uma delas. Sistema de contenção de 100% do ar circulante, em Presente relação aos usuários Sistema automático de alarme com travamento de Presente portas em caso de vasamentos de ar lação, p. 195, 2000. CTNBio MCT, Instrução Normativa n. 13, de 29/5/1998 - Normas para importação de animais geneticamente modificados (AnGMs) para uso em trabalho em regime de contenção, Cadernos de Biossegurança 1 (CTNBio) Legislação, p. 207, 2000. CTNBio MCT, Instrução Normativa n. 15, de 8/7/1998 - Normas para trabalho em contenção com animais não geneticamente modificados, onde organismos geneticamente modificados são manipulados, Cadernos de Biossegurança 1 (CTNBio) - Legislação, 212, 2000. MALAKOFF, D. , The rise of the mouse, biomedicines model mammal, Science 288, 217-388, 2000 MARSHALL, E., A deluge of patents creates legal hassles for research, Science 288, 217-388, 2000 THE JACKSON LABORATORY, Induced mutant resource, Bar Harbour, ME, 1998. VOGEL, G., The mouse facility as a recruiting tool, Science 288, 217-388, 2000. Biotecnologia Ciência & Desenvolvimento 33 A tecnologia de modificação genética oferece a oportunidade de reduzir ou eliminar alergênicos protéicos que ocorrem naturalmente em alimentos específicos. Pesquisadores têm trabalhado para retirar alergênicos naturalmente presentes em trigo, leite e até mesmo amendoim. Assim, a biotecnologia tem trabalhado para reduzir problemas com alergias alimentares e não para agravá-los. Biotecnologia rDNA Márcio A. F. Belém Ph.D., M.Sc., P.Eng. Consultor e Diretor-Presidente da Belém Biotech. [email protected] Edson Watanabe Ilana Felberg Pesquisadores da Embrapa Agroindústria de Alimentos Maria José Sampaio Pesquisadora da Embrapa Sede Marília R. Nutti Chefe Geral da Embrapa Agroindústria de Alimentos 34 Biotecnologia Ciência & Desenvolvimento Biotecnologia é a aplicação de organismos e de sistemas biológicos na produção de bens e serviços (OTA, 1984). Tradicionalmente, a aplicação da biotecnologia na indústria de alimentos se restringia à produção de pães, queijos, álcool, vinagre e iogurte. Mais recentemente, aumentou o interesse pelo uso dessa tecnologia na extração e produção de ingredientes não nutritivos, biologicamente ativos. Na última década, foram feitos enormes progressos especificamente nas técnicas de produção de alimentos e de bioingredientes por fermentação, por processos enzimáticos e por engenharia genética a partir de sistemas biológicos derivados do DNA recombinante (rDNA) (Belem, 1999). O desenvolvimento de tecnologias baseadas na aplicação de organismos e de sistemas biológicos derivados do rDNA para a produção de bens e serviços - a biotecnologia rDNA 5 iniciou-se em 1944, quando foi estabelecido o mecanismo de transferência genética que envolve o reconhecimento e a integração de um DNA isolado de um organismo por outro organismo (IFT Expert Report on Biotechnology and Foods, 2000). Mas, somente na última década, é que foi observado o impacto dessa tecnologia na mesa do consumidor, com o aparecimento dos alimentos derivados de organismos geneticamente modificados (OGM), como o tomate geneticamente modificado para reduzir a velocidade de amadurecimento do fruto e a soja geneticamente modificada, tolerante ao glifosato, que foram aprovados para comercialização em 1994, pelo US-FDA. Vantagens da biotecnologia rDNA A biotecnologia rDNA permite transferir com eficiência o material genético de um organismo para outro. Por exemplo, ao invés do cruzamento de plantas por várias gerações, ou do uso da ação de agentes mutantes para se obter uma característica desejada em uma planta melhoramentos genéticos tradicionais - que permitem a introdução de modificações imprevistas e indesejáveis, a biotecnologia rDNA permite que se identifique e se insira um ou mais genes responsáveis por uma característica específica em uma planta com muito maior precisão e velocidade. Esses genes transferidos, ou transgenes, podem ser oriundos de espécies não relacionadas, ser funcionais e transferíveis para quaisquer or- ganismos vivos, se desejável (IFT Expert Report, 2000). A evolução histórica da biotecnologia rDNA para a produção de alimentos Na realidade, a biotecnologia rDNA é o mais recente passo na seqüência de intervenções realizadas pela humanidade para o melhoramento genético de microorganismos, plantas e animais para produção de alimentos, iniciada há 10.000 anos atrás (IFT Expert Report, 2000). As plantas e os animais que alimentam a humanidade são o resultado de dezenas de séculos de melhoramento e aperfeiçoamento genéticos. Nas plantas, essa intervenção humana sobre a natureza permitiu, entre muitos outros benefícios, a seleção de variedades de sementes com maior rendimento e, por exemplo, a transformação do teosinte, com menor grau de domesticação, em milho, um cereal de importância vital para a alimentação dos povos das Américas (Goodman, 1988). Outro exemplo foi a domesticação do trigo, cujas sementes eram outrora coletadas no chão e que, após a intervenção humana, passaram a ser coletadas da planta diretamente (IFT Expert Report, 2000). Cruzamentos entre plantas de espécies diferentes levaram à produção de híbridos - estéreis, o que limitava a aplicação dessa técnica (ainda que ela servissse para ampliar a variedade genética disponível para os criadores). Posteriormente, algumas plantas férteis resultaram desses cruzamentos por meio da duplicação espontânea dos cromossomos, a exemplo do triticale, um híbrido fértil do trigo e do centeio. Mais tarde, o sistema de cultura de tecidos in vitro permitiu o resgate de embriões de híbridos de curta viabilidade (desenvolvem-se por curto espaço de tempo e depois se degeneram e morrem). Com essa técnica de cultura de tecidos, o embrião consegue amadurecer e se desenvolver numa planta fértil. Mais recentemente, tanto a radiação ionizante quanto os agentes químicos têm sido empregados para induzir mutações genéticas e expandir a faixa de variação genética de plantas disponíveis para cultivo. Esses e outros métodos convencionais de melhoramento genético tradicional 6 apresentam a desvantagem de serem imprecisas, imprevisíveis e mal sucedidas. No entanto, enquanto não se exige uma avaliação sistemática da toxicidade para os alimentos derivados de melhoramento genético tradicional, o potencial de toxicidade dos alimentos derivados da biotecnologia rDNA é rigorosamente avaliado dentro de um processo global de avaliação de segurança alimentar (IFT Expert Report, 2000). A importância da biotecnologia rDNA para o Brasil As empresas brasileiras de biotecnologia consideram fundamental a aplicação da biotecnologia rDNA para o desenvolvimento sustentável da agricultura (Costa, 1999), bem como para a expansão da agroindústria de alimentos. O Brasil detém tecnologia para o aumento de respostas positivas na transformação de plantas por rDNA (Rech & Aragão, 1999) e no enriquecimento nutricional de alimentos básicos da dieta dos povos dos países em desenvolvimento (Aragão et al., 1992). Recentemente, uma equipe de pesquisadores de São Paulo publicou a seqüência completa do genoma da bactéria Xylella fastidiosa, fitopatogênica a todas as variedades de laranja doce comercializadas no Brasil (Simpson et al., 2000). Pela primeira vez no mundo foi realizada a seqüência de uma bactéria fitopatogênica. O agente transmissor dessa bactéria são cigarrinhas das espécies Dilobopterus costalimai, Acrogonia terminalis e Oncometopia facialis (Roberto et al., 1986). As frutas afetadas são pequenas, enrigecidas e sem nenhum valor comercial. Atualmente, o controle dessa praga está limitado à poda da planta nas áreas infectadas, à aplicação de inseticidas e ao completo replantio, com graves conseqüências, tanto para a citricultura quanto para a agroindústria da laranja. A análise completa do genoma permitiu determinar não somente o metabolismo e as características de replicação daquela bactéria, como também uma série de mecanismos patogênicos em potencial (Simpson et al., 2000). A informação contida nessa seqüência genética poderá servir de base para determinar a seqüência de interações entre a bactéria e o hospedeiro (cigarrinha), e seus mecanismos de ação sobre a planta, com possíveis aplicações comerciais, para se buscarem variedades de plantas mais resistentes à praga, mais ricas em nutrientes e mais adaptadas aos processos tecnológicos industriais. Segurança de alimentos Historicamente, no que se refere à tecnologia de alimentos, a introdução de novas tecnologias sempre foi acompanhada de controvérsia (IFT Expert Report, 2000). Os alimentos enlatados (apertizados) foram vistos, por mais de 100 anos, com apreensão e com razão pelos consumidores, técnicos e cientistas, numa época em que não se conheciam as bases da bacteriologia. A pasteurização do leite, uma tecnologia que permitia salvar vidas e eliminar os microorganismos causadores da tuberculose, foi inicialmente vista com enorme suspeita. A inseminação artificial de animais de criação tecnologia que permitiu a seleção das raças para melhoria na oferta de carne, leite e ovos foi vista como uma afronta à natureza. Todo tipo de ameça à saúde pública foi atribuída ao uso de microondas. A margarina, na época em que foi lançada, foi combatida, em parte por uma necessidade legítima de se avaliar a segurança daquele produto antes da sua liberalização para consumo, mas, sobretudo, por ser uma ameça comercial à indústria de laticíni- 5 Essa nomenclatura visa a diferenciar as várias técnicas utilizadas na obtenção de alimentos oriundos dos recentes avanços da biotecnologia daquelas utilizadas para se obterem alimentos oriundos do DNA recombinante (biotecnologia rDNA), ou alimentos oriundos de organismos geneticamente modificados (OGM). 6 Melhoramento genético tradicional se refere aos melhoramentos genéticos onde a modificação genética da planta não é realizada pela inserção de genes exógenos por engenharia genética, ou seja, não é oriunda da biotecnologia rDNA. Biotecnologia Ciência & Desenvolvimento 35 os. Nos anos 70, a segurança de aditivos alimentares foi altamente debatida. Na década de 80, o foco de discussão foram os resíduos de pesticidas e a irradiação de alimentos (Felberg et al., 2000). Assim, por que se esperar que a introdução da tecnologia do rDNA na produção de alimentos (biotecnologia rDNA) viesse a causar menos controvérsia? Para compreender o significado de segurança alimentar, devemos definir os termos perigo e risco. Segundo as definições elaboradas pela FAO/OMS, perigo é um agente biológico, químico ou físico presente no alimento, ou condição do alimento, com potencial para causar um efeito adverso à saúde; o risco é definido em função da probabilidade de um efeito adverso à saúde, e a severidade desse efeito, ocorrer como consequência de um perigo. Dessa forma, o risco depende do nível de exposição ao perigo, e a existência do perigo, por si só, não implica em risco apreciável (Walker, 2000). Em ciência, não se fala em risco zero ou na ausência total de que possa ocorrer efeito negativo. Na ausência de efeitos prejudiciais, podemos concluir apenas que não ocorrem danos sob certas condições, e devemos garantir que o alimento não causará danos à saúde do consumidor quando preparado e/ou consumido de acordo com o seu uso intencional, ou seja, conforme as condições previstas para seu consumo (Felberg et al., 2000). Um alimento é, então, considerado seguro, se houver certeza razoável de que nenhum dano resultará de seu consumo sob as condições previstas de uso (OMS, 2000). Segurança alimentar e biotecnologia rDNA A avaliação de produtos derivados da biotecnologia rDNA não implica em alterações significativas nos princípios estabelecidos para a avaliação de segurança alimentar de produtos convencionais (Felberg et al., 2000). Para a avaliação da segurança alimentar é fundamental que estes alimentos derivados da biotecnologia rDNA sejam comparados com seus análogos convencionais (IFT Expert Report, 2000b). Este é o principal critério utilisado para se avaliar a segurança alimentar dos alimentos derivados da biotecnologia rDNA e que levou a elaboração do conceito de equivalência 36 Biotecnologia Ciência & Desenvolvimento substancial (ES). Se um alimento ou ingrediente derivado da biotecnologia rDNA for considerado substancialmente equivalente a um alimento ou ingrediente convencional, aquele alimento ou ingrediente poderá ser considerado tão seguro quanto esse (FAO / OMS, 1996). A determinação da ES engloba (Belem et. al., 2000): avaliação molecular; avaliação das características fenotípicas do organismo; l avaliação da composição do alimento; l e avaliação do potencial de alergenicidade. l l Aspectos moleculares A biotecnologia rDNA permite a introdução específica e precisa de um ou mais genes, previamente caracterizados, em um organismo receptor. Este organismo receptor contém, geralmente, milhares de genes. Devido à especificidade do gene e de uma maior precisão na inserção do gene no organismo receptor, a biotecnologia rDNA apresenta grandes vantagens em relação às técnicas de melhoramento genético convencional - muitas vezes aleatórias e imprecisas. Auxiliados pela grande quantidade de informação disponível em bancos de dados (NCBI, 1999), tanto sobre a seqüência do DNA do genoma de plantas e microorganismos quanto sobre a seqüência das proteínas expressas por esses genes, bem como pelo conhecimento acumulado sobre as diversas vias do metabolismo bioquímico, os biologistas moleculares podem adicionar um ou mais genes sem que haja uma alteração fundamental no microorganismo ou na planta de interesse, exceto pelas características introduzidas (previstas e desejadas) pelo gene exógeno (IFT Expert Report, 2000). Por outro lado, a biologia evolucionária e a árvore filogenética dos organismos vivos permitem prever a estabilidade e o grau de sobrevivência das quimeras criadas pela biotecnologia rDNA. Assim, a introdução de uma nova característica fenotípica em uma planta, por exemplo, é facilmente detectada antes de seu plantio comercial (IFT Expert Report, 2000). Ainda, a conversão de um organis- mo não patogênico em um organismo patogênico pela biotecnologia rDNA é muito pouco provável, posto que a patogenicidade não é uma característica oriunda de um só gene, mas de múltiplos genes (IFT Expert Report, 2000b). Tanto a fonte genética quanto a estrutura e função da proteína expressa pelo gene inserido devem ser conhecidos detalhadamente antes de se propor a liberação para comercializar o alimento derivado da biotecnologia rDNA. Qualquer potencial de insegurança deve ser intensivamente analisado (IFT Expert Report, 2000b). Avaliação de segurança do material genético introduzido A primeira etapa na avaliação da segurança alimentar é a completa caracterização do material genético inserido. Isso inclui a identificação da fonte do material genético, para se verificar se ele é proveniente de uma fonte patogênica, tóxica ou alergênica. Os principais parâmetros a serem avaliados são: o tamanho do material genético inserido, o número de genes inseridos, a localização da inserção, e a identificação das seqüências marcadoras do material genético construído para ser inserido e que permitem sua detecção (genes marcadores) e expressão (promotor) (IFT Expert Report, 2000b). Uma vez que todos os alimentos contêm DNA, que esse é rapidamente digerido pelo trato gastrointestinal, e que não há nenhuma evidência de transferência de DNA do alimento para as células intestinais ou para os microorganismos da flora intestinal, não precisam ser realizados testes de avaliação de segurança do DNA do alimento (IFT Expert Report, 2000b). Avaliação de segurança da proteína expressa pelo gene inserido Uma vez que o material genético tenha sido completamente caracterizado, é preciso avaliar a segurança da proteína expressa pelo gene inserido geralmente uma enzima. A avaliação de segurança da proteína expressa inclui: identificação da composição e da estrutura da proteína; quantificação da proteína expressa; busca de similaridade com outras toxinas, alergênicos, fatores antinutricionais e outras proteínas funcionais; termoestabilidade da proteína expressa; digestibilidade da proteína expressa; testes toxicológicos in vitro e in vivo sobre a proteína expressa; e avaliação do potencial alergênico in vivo e in vitro da proteína expressa (IFT Expert Report, 2000b). Avaliação de segurança da composição do alimento Análises para determinar a composição dos alimentos derivados de OGMs devem focar o conteúdo de nutrienteschave (macro e micronutrientes), de componentes tóxicos-chaves e de fatores antinutricionais-chaves (The Commission of the European Communities, 1997). A planta ou o alimento convencional (planta/alimento-referência) utilizado na comparação pode ser a linhagem ou cepa parental e/ou linhagem ou cepa comestível da mesma espécie. Para alimentos processados, a comparação pode também ser realizada entre o alimento processado derivado de um OGM e um alimento com processamento análogo, mas convencional (FAO/OMS, 1996). A escolha adequada de um alimento-referência para se estabelecer a equivalência substancial (ES) em termos de composição depende de alguns fatores. É mais apropriado se comparar matérias-primas não processadas. Entretanto, se o alimento só for consumido uma vez processado (ex: óleo refinado de soja , farelo de soja), a comparação pode ser realizada entre o alimento derivado de OGM e o alimento convencional processado da mesma maneira. O alimento-referência deve refletir a composição centesimal média encontrada em alimentos convencionais semelhantes, seu consumo, sua importância na dieta e seus efeitos no processamento (Huggett et al., 1996). Dados da literatura, no que se refere à composição do alimento convencional, só podem servir de base de comparação se as técnicas analíticas tiverem sido validadas (OCDE, 1998). Muitas vezes porém, esses dados indicam apenas as médias dos resultados de composição e podem subestimar variações naturalmente encontradas (OMS, 1995). A comparação para avaliar os efeitos não intencionais devido à inserção genética em alimento derivado de OGM é mais apropriada e útil se for realizada com sua linhagem/cepa parental nas condições mais próximas possíveis do plantio (plantas GM), da alimentação (animais GM), do manejo e transporte (plantas e animais GM), e do processamento (microorganismos, plantas e animais GM). No caso de safras comerciais de grãos, muitas vezes não são possíveis linhagens de plantas geneticamente modificadas (PGMs), isogênicas à linhagem parental. Assim, para comparação, a linhagem mais próxima possível deve servir de referência (OCDE, 1998). O estabelecimento da ES para os alimentos derivados da biotecnologia rDNA segue procedimentos diferenciados caso a caso. O conceito de ES pode ser aplicado de maneira mais ou menos abrangente (OCDE, 1998). Diferentes formas de avaliações de ES foram propostas e publicadas (OCDE, 1992). Padgette et al. (1996), cujo trabalho representa um marco na avaliação da segurança alimentar de PGMs, compararam soja GM tolerante ao herbicida glifosato com sua linhagem parental, com uma linhagem controle e com o espectro de variações de composição encontrado na literatura, através de 1.422 análises dos grãos, 858 análises do farelo de soja desengordurada, 60 análises do farelo de soja desengordurado não tostado, 114 análises do óleo de soja refinado, 12 análises da lecitina de soja, com delineamento experimental em blocos aleatórios, com uma análise por amostra sem replicata para cada local de plantio. Fuchs (OCDE, 1998) relata que há variações de composição entre diferentes locais de plantio, muito maiores do que entre análises de amostras com replicata, e entende que uma comparação entre as PGMs e os dados encontrados na literatura deve ser realizada quando, porventura, se verificam diferenças estatisticamente significativas entre a PGM e sua análoga parental. Este autor considera crítico um bom delineamento experimental, para que haja uma interpretação criteriosa dos resultados de composição e para que se realize uma comparação efetiva. Belem et al. (2000) propuseram uma rede para se tomarem decisões e um modelo para se estabelecer a ES de plantas derivadas da biotecnologia rDNA ao compará-las com as plantas parentais ou de linhagens próximas, seguras para consumo alimentar, se- guindo um delineamento experimental em blocos aleatórios. Aqueles autores também propuseram procedimentos para os casos em que não seja constatada a ES entre as PGMs e suas análogas convencionais, e aonde não se observe nenhum risco à saúde do consumidor. Avaliação do potencial alergênico As alergias alimentares atingem 2% da população mundial, e, em alguns casos, podem levar a choques anafiláticos (OCDE, 1997). Uma vez que os alimentos geneticamente modificados usualmente contêm novas proteínas, a segurança desses alimentos deve incluir a avaliação da alergenicidade de tais proteínas (OMS, 2000). Até o momento, não se tem conhecimento de nenhum produto agrícola ou alimento geneticamente modificado, aprovado para consumo, que tenha causado alergias. No entanto, ao se tentar enriquecer a qualidade nutricional de grãos de soja com metionina 2S albumina através da inserção genética de gene da castanha do Pará (Nordlee et al., 1996), foi constatado que esta planta geneticamente modificada era potenciamente alergênica. Tal fato fez com que o estudo fosse interrompido. Se um novo produto da biotecnologia realmente causar alergias, o mesmo não deveria ser proposto para comercialização ou, então, deveria ser devidamente rotulado (Avery, 2000). Para se estabelecer a segurança alimentar de uma PGM, compara-se a concentração de proteínas alergênicas da PGM com a concentração de proteínas alergênicas usualmente encontradas nas plantas convencionais (Metcalfe et al., 1996). Depois, é preciso comparar a seqüência de aminoácidos da proteína exógena expressa pelo gene inserido com a seqüência de quaisquer proteínas causadoras de alergia alimentar, usualmente presentes ou não naquela planta (Metcalfe et. al, 1996, Padgette et al., 1996, Sander et al., 1998). Para tal, bancos de dados (GenBank, BLAST, SWISSPROT) contendo a seqüência de aminoácidos de proteínas alergênicas devem ser consultados (NCBI, 1999). Se houver homologia entre a proteína expressa pelo gene inserido e qualquer proteína alergênica, a PGM é potencialmente alergênica. No entanto, o fato de uma proteína não ser homóloga a qualquer proteína Biotecnologia Ciência & Desenvolvimento 37 alergênica não descarta seu potencial de alergenicidade. A determinação da homologia apenas permite que se preveja o potencial alergênico da proteína exógena expressa pelo gene inserido (OCDE, 1997). Outros ensaios in vitro e in vivo são necessários (Padgette et al., 1996). O Conselho Internacional de Biotecnologia de Alimentos e o Instituto de Alergia e Imunologia do Instituto Internacional de Ciências da Vida (ILSI) desenvolveram, em 1996, uma árvore de tomadas de decisão para avaliar o potencial de alergenicidade de novas proteínas em alimentos geneticamente modificados, a qual foi adaptada pelos peritos que participaram da consulta conjunta da FAO/WHO sobre alimentos derivados da biotecnologia. Essa estratégia de ação tem sido largamente adotada pela indústria de biotecnologia. A atual árvore de decisões requer o exame de vários parâmetros que são comuns a muitos alergênicos alimentares. Os critérios mais relevantes, incluem: fonte do material geneticamente transferido (precaução especial deve ser tomada se a fonte do material contiver alergênicos conhecidos); homologia da seqüência de aminoácidos; imunoreatividade da proteína introduzida; efeito do pH e/ou digestão (a maioria dos alergênicos são resistentes à acidez gástrica e às proteases digestivas); estabilidade ao calor ou ao processamento (OMS, 2000). A tecnologia de modificação genética oferece a oportunidade de reduzir ou eliminar alergênicos protéicos que ocorrem naturalmente em alimentos específicos (OMS, 2000). Pesquisadores têm trabalhado para retirar alergênicos naturalmente presentes em trigo, leite e até mesmo amendoim. Assim, a biotecnologia tem trabalhado para reduzir problemas com alergias alimentares e não para agravá-los (Avery, 2000). Avaliação Toxicológica: Estudos com animais As dificuldades práticas para se obterem informações significativas sobre segurança alimentar a partir de estudos toxicológicos têm sido reconhecidas já há vários anos. Tal reconhecimento se tornou particularmente evidente a partir do grande número de estudos conduzidos com animais para avaliar a segurança de alimentos irradiados (Tomlinson, 2000). Estudos toxicológicos com animais 38 Biotecnologia Ciência & Desenvolvimento constituem os principais componentes da avaliação de segurança de vários compostos como pesticidas, produtos farmacêuticos, substâncias químicas industriais e aditivos para alimentos. Na maioria desses casos, entretanto, a substância teste é bem caracterizada, de pureza conhecida, de nenhum valor nutricional particular e a exposição de humanos às mesmas é geralmente baixa. Assim, animais são diretamente alimentados com esses compostos em diferentes dosagens, algumas muito superiores ao nível de exposição esperado para consumo humano, com o objetivo de identificar qualquer efeito potencial adverso à saúde. Desta forma, é possível, na maioria dos casos, determinar níveis de exposição em que efeitos adversos não são observados, e estabelecer limites seguros pela aplicação de fatores de segurança apropriados (OMS, 2000, Donaldson & May, 2000). Os alimentos, por sua vez, constituem-se em misturas complexas de vários compostos e são caracterizados por uma ampla variação na composição e no valor nutricional. Devido ao seu volume e efeito de saciedade, os alimentos são usualmente fornecidos a animais em quantidades equivalentes a um baixo número de múltiplos daquelas quantidades que provavelmente estariam presentes em uma dieta humana (OMS, 2000; Donaldson & May, 2000). Um outro fator-chave a ser considerado na condução de estudos com animais é o valor nutricional do alimento e, conseqüentemente, o balanceamento das dietas utilizadas. A detecção de quaisquer efeitos adversos potenciais e o relacionamento destes a uma característica individual do alimento pode ser, entretanto, extremamente difícil. Outra consideração a ser feita ao se decidir sobre a necessidade desse tipo de estudo é quanto a submeter animais experimentais ao mesmo, nos casos em que a obtenção de informações relevantes seja improvável (OMS, 2000). Na prática, poucos alimentos hoje consumidos foram submetidos a quaisquer testes toxicológicos. Mesmo assim, esses alimentos são geralmente aceitos como sendo seguros (Tomlinson, 2000). No Reino Unido, por exemplo, a avaliação de segurança dos milhares de produtos alimentícios lançados a cada ano se baseia na suposição de que, se os ingredientes alimentares individualmente já possuem um histórico extenso de consumo, uma nova combinação desses ingredientes será igualmente segura. Contudo, muitos alimentos hoje existentes provavelmente apresentariam efeitos adversos se pudessem ser consumidos em doses suficientemente altas (Donaldson & May, 2000). As dificuldades para aplicar testes toxicológicos tradicionais e procedimento de avaliação de risco a alimentos fez com que uma abordagem alternativa fosse requerida para a avaliação de alimentos geneticamente modificados, o que levou ao desenvolvimento do conceito de equivalência substancial (OMS, 2000). Métodos de detecção de alimentos derivados da biotecnologia rDNA As duas técnicas mais comuns para detectar organismos geneticamente modificados em alimentos são: PCR (polymerase chain reaction), que detecta as seqüências de DNA geneticamente modificadas; e os imuno-ensaios, que medem os níveis de proteínas expressas por genes transgênicos. Laboratórios do mundo todo estão desenvolvendo novos métodos para a detecção de organismos geneticamente modificados em alimentos, mas não há consenso quanto à especificidade, reprodutibilidade e repetibilidade desses métodos. No momento existe a dificuldade de métodos internacionalmente reconhecidos para a quantificação de organismos geneticamente modificados em alimentos. Muitos métodos ainda se encontram em fase de validação. As técnicas de PCR e de imunoensaios têm papéis complementares nos testes utilizados na análise de alimentos geneticamente modificados. Embora resultados quantitativos têm sido reportados, os críticos argumentam que nenhum dos métodos é capaz de produzir resultados reproduzíveis, sendo que a falta de padrões internacionalmente aceitos de organismos geneticamente modificados é apontada como a maior razão para a variabilidade dos resultados. O teste ELISA não é designado para detectar organismos geneticamente modificados em produtos alimentícios acabados, uma vez que o mesmo detecta proteínas, as quais são facilmente degradadas durante o processamento. Existe controvérsia se a técnica de PCR é capaz de detectar organismos geneticamente modificados no produto alimentício final e não apenas nos ingredientes utilizados para a produção do mesmo. Isto porque as moléculas de rDNA podem ser desnaturadas, parcialmente digeridas e hidrolisadas durante o processamento. Este argumento favorece aqueles que entendem que seria mais representativo a avaliação dos ingredientes para detecção de rDNA. (Erickson, 2000) . A verificação de que produtos alimentícios não geneticamente modificados realmente não contêm organismos geneticamente modificados, continuará provavelmente, a curto prazo, a direcionar a demanda por testes de detecção de rDNA e das proteínas expressas. A longo prazo, o mercado crescente de alimentos nutricionalmente melhorados através da biotecnologia rDNA vai constituir uma área que, provavelmente, terá um efeito dramático na demanda por esses testes, pois, à medida que o mercado começar a aceitar as novas características expressas por modificação genética em alimentos como benéficas ao consumidor, o nível das mesmas se tornará muito importante; nesse ponto, a quantificação da modificação será crítica (Erickson, 2000). No entanto, a extrema sensibilidade de novas técnicas de PCR capazes de detectar a presença de resíduos específicos de DNA (nested PCR) em alimentos processados pode levar a falsas conclusões e interpretações. Em Israel, foram detectados resíduos de rDNA na farinha de trigo utilizada na fabricação de peru à milanesa. Como aquele país importa dos Estados Unidos praticamente todo o trigo que consome, a detecção de rDNA na farinha por PCR foi inicialmente interpretada como uma contaminação dos grãos de trigo por trigo GM. No entanto, através de estudos mais complexos, pôde-se constatar que, na realidade, os grãos de trigo haviam sido contaminados por resíduos de grãos de soja GM durante o armazenamento nos silos e durante o transporte nos containers dos navios. Farinhas de trigo preparadas com resíduos de soja GM apresentarão invariavelmente presença de rDNA (Stram, et al., 2000). Rotulagem Um dos grandes desafios relacionados com a biotecnologia rDNA envolve a rotulagem de alimentos geneticamente modificados. Na Europa, os consumidores foram encorajados a exigir rótulos que identifiquem os alimentos derivados da biotecnologia rDNA (Hoban, 2000). A rotulagem de produtos alimentícios geneticamente modificados passou a ser obrigatória para a soja e o milho resistente a insetos. Contudo, a rotulagem pode não ser requerida para alimentos que não contêm quantidades mensuráveis da nova proteína ou DNA, uma vez que não é possível a verificação dos alimentos oriundos de PGM e de seus análogos convencionais (Beever and Kemp, 2000). Esse é o caso de alguns ingredientes alimentares altamente refinados, como, por exemplo, sacarose e óleos vegetais. O processo de refino destrói e remove qualquer material genético e proteína que possam estar presentes; o produto final que entra na composição do alimento não é, em si, modificado e, portanto, não pode ser distinguido daquele produzido através de meios convencionais (Donaldson & May, 2000). Recentes trabalhos nos Estados Unidos têm demonstrado que as frases utilizadas em rótulos têm efeito significativo na compreensão e aceitação da biotecnologia rDNA por parte do consumidor. Muitos consumidores americanos já se sentem oprimidos pela quantidade de detalhes dos rótulos de alimentos e, na verdade, não desejam mais informação que não tenha uma justificativa científica. Basicamente, o consumidor quer saber como um produto foi modificado e se tal modificação foi aprovada por uma agência governamental. Qualquer informação no rótulo deve ser simples, relevante e clara. A rotulagem de alimentos processados apresenta vários desafios de logística e custos para todos os envolvidos na sua produção. (Hoban, 2000). Ainda não existe um consendo quanto à rotulagem de alimentos derivados da biotecnologia rDNA. Na União Européia, os alimentos que contêm uma porcentagem superior a 1% de soja ou milho geneticamente modificados devem ser rotulados geneticamente modificados (Erickson, 2000). A proposta brasileira, em consulta pública (n0 02 do DPDC/SDE/MJ de 1/ 12/99), é semelhante à proposta da União Européia, pois considera obrigatória a rotulagem quando presente rDNA ou proteína resultante de modi- ficação genética (Felberg et. al., 2000). No momento, o Governo brasileiro realiza estudos de viabilidade da implementação dessas normas de rotulagem, de maneira a não transferir mais esse custo para o consumidor final. No Japão, foi estabelecido o nível de 5% para a soja, mas no caso do milho, devido à polinização cruzada, nenhuma porcentagem foi estabelecida. Nos Estados Unidos, não existe nenhum requerimento obrigatório para a rotulagem de alimentos que contenham organismos geneticamente modificados. O FDA mantém a posição de que, se alimentos geneticamente modificados são substancialmente equivalentes aos seus análogos convencionais, nenhum tipo de rotulagem é requerida, a não ser nos casos em que o conteúdo nutricional tenha sido alterado ou quando o produto contenha alergênicos conhecidos (Erickson, 2000). Referências: Aragão, F. J. L., Grossi, M. F., Almeida, E. R., Gander, E. S., Rech, E. L. (1992). Particle bombardment-mediated transient expression of a Brazil nut methionine-rich albumin in bean (Phaseolus vulgaris L.). Plant Mol. Biol. 20: 357-359. Avery, D. T. (2000) Why we need food biotechnology? Food Technology, 54 (9): 132. Beever, D. E.; Kemp, C. F. (2000) Safety issues associated with the DNA in animal feed derived from genetically modified crops. A review of scientific and regulatory procedures. Nutrit. Abs. Rev. Series B: Livestock Feeds and Feeding, v. 70, n. 3, p. 175192. Belem, M. A. F., Felberg, I., Gonçalves, E. B., Cabral, L. C., Carvalho, J. L., Sundfeld, E. , Nutti, M. R. (2000). Equivalência substancial da composição de alimentos derivados de plantas geneticamente modificadas (PGM). Biotecnol. Ciênc. Des., 3 (14): 140-149. Belem, M. A. F. (1999). Application of biotechnology in the product development of nutraceuticals in Canada. Trends Food Sc. Technol., 10: 1-6. Costa, F. C. (1999) Resumo da posição da EMBRAPA sobre plantas transgênicas. Cad. Ciênc. Tecnol., 16 (1): 11-16. Donaldson, L.; MAY, R. (1999) Health implications of genetically modifiBiotecnologia Ciência & Desenvolvimento 39 ed foods. Site do Department of Health. URL: http://www.doh.gov.uk/ gmfood.htm. Consultado no dia 13/ 07/2000. Erickson, B. E. (2000) Detecting genetically modified products in food. Analyt. Chem. 7: 454A-459A. FAO/OMS (1996) Biotechnology and food safety. In: Report FAO/OMS, FAO Food Nutrition Paper, 61. Roma. 31 p. Felberg I., Cabral L. C., Nutti, M. R. (2000) Segurança alimentar de produtos derivados de plantas transgênicas. Ação Ambiental, abr/maio (11): 25-26. Goodman, M. M. (1988) The history and evolution of maize. Crit. Rev. Plant Sc., 7: 197-220. Hoban, T.J. (1999) Public perception and understanding of agricultural biotechnology. Site da US Information Agency. URL: http://www.usia.gov/ journals/ites/1099/ijee/bio-toc.htm. Consultado em 02/10/2000. Huggett, A. C. & Verschuren, P. M. (1996) The safety assurance of functional foods. Nutrition Reviews, 54 (11): S132-S139. IFT Expert Report on Biotechnology and Foods (2000). Benefits and concerns associated with recombinant DNA biotechnology-derived foods. Food Technology, 54 (10): 61-80. IFT Expert Report on Biotechnology and Foods (2000b). Human food safety evaluation of rDNA biotechnology-derived foods. Food Technology 54 (9): 53-61. Metcalfe, D. D., Fuchs, R. L., Townsend, R., Sampson, H. A., Taylor, S. L., Fordham, J. R. (1996) Allergenicity of foods produced by genetic modification. Crit. Rev. Food Sc. Nutr. 36: S165S186. NCBI (1999), National Center for Biotechnology Information. Disponível: NCBI site. URL: http:// ncbi.nlm.nih.gov. Consultado em 20/ 11/99. Nordlee, J. A., Taylor, S. L., Towsend, J. A., Thomas, L. A. , Bush, R. K. (1996) Identification of a Brazil-nut allergen in transgenic soybeans. New Eng. J. Med. 334: 688-692. OCDE (1992) Safety evaluation of foods derived from modern biotechnology, concepts and principles. Paris. 74 p. Disponível: OCDE site.URL: http:/ /www.oecd.org/subject/biotech/ . Consultado em 8/11/99. OCDE (1997) Safety Assessment of 40 Biotecnologia Ciência & Desenvolvimento new foods: resulting of an OCDE survey of serum banks for allergenicity testing, and use of databases. Paris. 32 p. Disponível: OCDE site. URL: http:/ /www.oecd.org/subject/biotech/. Consultado em 12/11/99. OCDE (1998) Report on the OCDE workshop on the toxicological and nutritional testing of novel foods. Paris. 48 p. Disponível: OCDE site. URL: http://www.oecd.org/subject/biotech/ . Consultado em 10/10/99. OMS (1995) Application of the principles of substantial equivalence to the safety evaluation of foods or food components from plants derived by modern biotechnology. Report of a WHO Workshop. Genebra. 80 p. OMS (2000). Safety aspects of genetically modified foods of plant origin. Report of a Joint FAO/WHO Expert Consultation on Foods Derived from Biotechnology. Geneva: WHO, 2000. OTA (1984) Commercial biotechnology: an international analysis. OTABA-218, p. 3. US Congress, Office of Technology Assessment. U. S. Govt. Printing Office, Washington, DC. Padgette, S. R., Taylor, N. B., Nida, D. L., Bailey, M. R. , Macdonald, J. , Holden, L. R. & Fuchs, R. L. (1996) The composition of glyphosate-tolerant soybean seeds is equivalent to that of conventional soybeans. J. Nutr. 126: 702-716. Rech, E. and Aragão, F. J. L. (1999) A process for obtaining transgenic leguminuous plants (Leguminosae) containing exogenous DNA. EMBRAPA, Brasília. Patente: WO 99/18223. Roberto, S. R., Coutinho, A., De Lima, J. E. O., Miranda, V. S. & Carlos, E. F. (1996) Transmissão de Xylella fastidiosa pelas cigarrinhas em citros. Fitopatol. Bras., 21, 517-518. Sanders, P. R., Lee, T. C., Groth, M. E., Astwood, J. D., Fuchs, R. L. (1998) Safety assessment of insect-protected corn In: Biotechnology and Safety Assessment, 2nd edition, Thomas, J. A., ed. (1999), 241-256. Taylor & Francis, Filadélfia. Simpson, A. J. G., Reinach, F. C., Arruda, P., Abreu, F. A., Acencio, M., Alvarenga, R. , Alves, L. M. C., Araya, J. E., Baia, G. S., Baptista, C. S., Barros, M. H., Bonaccorsi, E. D., Bordin, S., Bové, J. M., Briones, M. R. S., Bueno, M. R. P., Camargo, A. A., Camargo, L. E. A., Carraro, D. M., Carrer, H., Colau- to, N. B., Colombo, C., Costa, F. F., Costa, M. C. R., Costa-Neto, C. M., Coutinho, L. L., Cristofani, M., Dias-Neto, E., Docena, C., El-Dorry, H., Facincani, A. P., Ferreira, A. J. S., Ferreira, V. C. A., Ferro, J. A., Fraga, J. S., França, S. C., Franco, M. C., Frohme, M., Furlan, L. R., Garnier, M. , Goldman, G. H., Goldman, M. H. S., Gomes, S. L., Gruber, A., Ho, P. L., Hoheisel, J. D., Junqueira, M. L., Kemper, E. L. , Kitajuma , J. P., Krieger, J. E., Kuramae, E. E., Laigret, F., Lambais, M. R., Leite, L. C. C., Lemos, E. G. M., Lemos, M. V. F., Lopes, S. A., Lopes, C. R., Machado, J. A., Machado, M. A., Madeira, A. M. B. N., Madeira, H. M. F., Marino, C. L., Marques, M. V., Martins, E. A. L., Martins, E. M. F., Matsukuma, A. Y., Menck, C. F. M., Miracca, E. C., Nunes, L. R., Oliveira, M. A., de Oliveira, M. C., de Oliveira, R. C., Palmieri, D. A., Paris, A., Peixoto, B. R., Pereira, G. A. G., Pereira Jr., H. A., Pesquero, J. B., Quaggio, R. B., Roberto, P. G., Rodrigues, V., Rosa, A. J. M., de Rosa Jr., V. E., de Sá, R. G., Santelli, R. V., Sawasaki, H. E., da Silva, A. C. R., da Silva, A. M., da Silva, F. R., Silva Jr., W. A., da Silveira, J. F., Silvestri, M. L. Z., Siqueira, W. J., de Souza, A. A., de Souza, A. P., Terenzi, M. F., Truffi, D., Tsai, S. M., Tsuhako, M. H., Vallada, H., Van Sluys, M. A., VerjovskiAlmeida, S., Vettore, A. L., Zago, M. A., Zatz, M., Meidanis, J., Setubal, J. C. (2000). The genome sequence of the plant pathogen Xylella fastidiosa. Nature, 406 (13): 151-157. Stram, Y., Vilk, A., Klinger, I. (2000) Detection of residues of genetically modified soybeans in breaded fried turkey cutlets. J. Food Sc. 65 (4): 604-606. The Commission of the European Communities (1997) Recommendations concerning the scientific aspects of information necessary to support applications for the placing on the market of novel foods and novel food ingredients. OJ L 253, 16. 9. 1997. Official Journal of the European Communities, ed. Bruxelas. Tomlinson, N. (2000) The concept of substantial equivalence, its historical development and current use. Joint FAO/ WHO Expert Consultation on Foods Derived by Biotechnology. Walker, R. (2000) Safety testing of food additives and contaminants as the long term evaluation of foods produced by biotechnology. Joint FAO/WHO Expert Consultation on Foods Derived by Biotechnology. Topic 6. ANÚNCIO NOVO (Fotolito em anexo) Colocar o anúncio nº 02 (foram enviados 02 anúncios) Biotecnologia Ciência & Desenvolvimento 41 A atualização do debate ciência - sociedade está hoje centrada nos temas que discutem os efeitos negativos e positivos das tecnologias disponíveis. Nesse aspecto, a Biossegurança abraça essa preocupação, pois cabe a ela garantir cientificamente as bases dos controles dos efeitos positivos e negativos, considerando a relação entre risco e benefício dessas tecnologias. Na construção da Biossegurança, identificamos como área do conhecimento científico um lastro cognitivo que, historicamente, está associado aos processos que resultaram na confirmação do que hoje chamamos de estruturas científicas e tecnológicas, nas quais onde se apoiam as ciências da vida e suas possibilidades experimentais. Considerando a consolidação desse lastro, remontamos aos processos que contribuíram para dar forma à ciência moderna, processo este que, em sua origem, segundo a História da Ciência, estava mais próximo do Renascimento do que da Modernidade. Encontramos algumas importantes correlações, que podemos atribuir às questões impostas à Biossegurança e aos processos de legitimação da ciência moderna, nas indagações colocadas a partir das proposições existentes, já evidenciadas pela perspectiva do universo newtoniano e suas possibilidades de afirmação, voltadas agora para a compreensão e decodificação científica da natureza, cujo enfoque considerava até então, prioritariamente, as propriedades físico-mecânicas do universo para explicar seus fenômenos. O Universo de Newton estava pleno de forças fora do alcance do plano racional, possibilitando brechas que colocavam para sua ciência a existência de possíveis forças ocultas impossíveis 42 Biotecnologia Ciência & Desenvolvimento Marli B. M. de Albuquerque Doutora em História da Ciência pela Université Paris X Pesquisadora da FIOCRUZ/Casa de Oswaldo Cruz Colaboradora do Núcleo de Biossegurança da FIOCRUZ [email protected] de serem mensuradas e demonstradas no plano físico. Também as ciências de Kepler e Copérnico estavam imbuídas de pressupostos metafísicos provenientes da vertente ocultista do pensamento Renascentista, pois o homem do Renascimento estava francamente dividido entre Deus e a razão, que colocava dúvidas relativas ao plano de respostas, que poderiam estar ao alcance do postulado da Física como ciência, capaz de decodificar a natureza do mundo a partir de teorias apoiadas no instrumental técnico como recurso demonstrativo e probatório. Hoje, uma das questões basilares do novíssimo campo de conhecimento da Biossegurança é a sua capacidade de assegurar, de forma demonstrativa e objetiva, as possibilidades de controle capazes de definir segurança e risco para o ambiente e para a saúde humana, associados à liberação dos Organismos Geneticamente Modificados, os OGMs. Grande parte das manifestações opositoras dos projetos biotecnológicos relativos aos OGMs nos remete a forças que estão ocultas na natureza, minimizando a importância e a eficácia dos monitoramentos propostos pela ciência e colocando, no âmbito do universo natural, os desafios sobre os quais, a priori, a ciência poderá declarar sua impotência. Por outro lado, outros componen- tes, igualmente relevantes, não são claramente considerados nos processos de construção da ciência, pois, historicamente, as afirmações que tendem a consagrar a ciência moderna como triunfo absoluto da razão tendem a minimizar a importância desse movimento como integrado na história da cultura. O aparato ideológico que, nos dias atuais, elabora e executa ações militantes contra os processos bioctenológicos, em especial, contra a tecnologia do DNA recombinante, base da produção dos OGMs, estrutura seus argumentos pautados numa percepção que tende a enfatizar o distanciamento entre os processos estabelecidos pela ciência e as demandas e desejos da sociedade, e entre o estabelecimento de novas tecnologias e a preservação de tradições culturais, entre outras. Nesse contexto, podemos também colocar uma questão essencial, que parece faltar aos debates, ou seja, a recuperação da história recente da sociedade inserida num mundo globalizado, no qual a tecnologia se apresenta como um dos mais valorizados ícones da cultura ocidental, alcançando, mesmo de maneira anacrônica, grupos menos complexos em termos de organização social. É o caso do fascínio que a tecnologia exerce sobre indígenas, por exemplo, cujos membros de vários grupos, usam relógios digitais, televisões, rádios, com- putadores e outros produtos fornecidos pela nova era tecnológica. Vários fatores estão associados às estratégias dos grandes interesses políticos e econômicos embutidos na questão, mas o fato contundente é a relação entre o fascínio tecnológico e a manutenção dos valores tradicionais das sociedades. Negar os processos científicos, mesmo os que causam mais impacto na sociedade, como é aquele gerado pela bioctenologia em curso, seria descartar ou diminuir a importância dos grandes investimentos destinados ao avanço do conhecimento sobre a vida e sobre o homem, tal como foi o fato associado à história recente da ciência, projetado pela descoberta da estrutura do DNA, realizada por Watson e Crick em 1953. A partir desse fato científico, concretizouse irreversivelmente o avanço da Biologia Molecular, abrindo novas fronteiras para a ciência, inclusive a possibilidade da arquitetura de novas formas de vida. Diante dessa realidade, pergunta-se: O homem está brincando de Deus? Ao abordarmos, nesta reflexão, a projeção do impacto das inovações técnicas e científicas na sociedade que foi contemporânea da estruturação da ciência moderna, podemos verificar um questionamento semelhante àquele formulado no século XVI: O homem está negando Deus? E foi com base nessa questão, que, aparentemente, opunha a ciência ao contexto mental da sociedade da época, que muitos homens de ciência tiveram que negar suas teorias, enquanto outros foram julgados e executados pelo Tribunal do Santo Ofício. É imperativo ressaltar que essa negação expressa também a desconsideração da ciência como valor cultural da sociedade. É sonegar, sobretudo, que, por um lado, a tecnologia do DNA recombinante passou a suscitar preocupações e até pânicos, acelerando a necessidade da formalização de um campo do conhecimento científico mais preciso, a Biossegurança, a partir das decisões tomadas na Conferência de Asilomar, de 1975, quando aquele fórum sistematizou questões que estavam na pauta dos cientistas desde 1973. Aquele evento serviu de marco para registrar as preocupações pontuais de um grupo de pesquisadores, cujas principais indagações estavam centradas nos riscos e nos benefícios que envolviam a ciência da recombinação, preocupações estas explicitadas na reunião realizada no Massachusetts Institute of Tecnology. Em Asilomar, declarou-se que os experi- mentos de clonagem continham riscos, em maior ou menor grau, e que os mais preocupantes eram os biológicos. Diante dessa complexidade, acordou-se que os projetos que envolviam as técnicas de recombinação ficassem sob observação até que fossem ajustados cientificamente métodos de controle de riscos laboratoriais. Assim, um outro grande resultado de Asilomar foi a franca demonstração da capacidade que tem a comunidade científica de absorver e de acatar preocupações apontadas pela sociedade, além de empenhar esforços para construir suportes para responder positivamente a essas preocupações, tanto no tocante à segurança dos espaços laboratoriais, como no tocante à aplicação de novas tecnologias, mais precisamente a biotecnologia, dando atenção especial à liberação dos OGMs, com base, sobretudo, nos instrumentos previstos nos Estudos de Impacto Ambiental e nos Relatórios de Impacto Ambiental. Tomando como exemplo as questões mais atuais colocadas pelo surgimento acelerado de novas tecnologias, o desenvolvimento dessa proposta reflexiva pretende destacar os grandes processos de construção da cultura científica, com a intenção clara de destacar que a ciência em si pode optar, pode construir seus próprios objetos, pode propor suas linhas de investigações e formular diferentes métodos, pois o conhecimento em si é um valor, e a ciência, em sua estrutura, está livre dos condicionamentos ideológicos. No entanto, se a ciência não pode estar presa a uma rigidez moral e ética, pode e deve estar ao uso que dela se faça, considerando suas implicações sociais. Essa questão, como veremos, sempre esteve presente no desenvolvimento da ciência e da tecnologia, pois, não nos esqueçamos, a construção das bases da ciência moderna registrou eventos e fatos tidos hoje como cruéis. Em nome da manutenção das tradições, Giordano Bruno foi queimado, Galileu Galilei enfrentou a Inquisição. Ao resgatar os processos cognitivos das revoluções científicas no que se refere à constituição das bases da ciência moderna, devemos considerar a perspectiva cultural, que registra com vigor a passagem da percepção do mundo baseado no neoplatonismo, que considerava como categorias fundamentais a matéria e o espírito, para a percepção que seria imperativa na ciência moderna, ou seja, o deslocamento daqueles esses fundamentos para as categorias de SUJEITO-OBJETO em busca da OBJETIVIDADE RACIONAL. O cenário cultural e científico do Renascimento conjugou as expectativas da sociedade originadas nas transformações da vida material com o plano mental e cultural dos homens a fim de confirmar os espaços abertos, que resultaram na constituição de um processo que levaria à consolidação de condições favoráveis para a formalização da ciência moderna, conjugando, nesse processo, as contradições e as percepções paradoxais entre o desejo do avanço para novos padrões e valores sociais, e os temores justificados pela guarda das tradições. A ambiência material, mental e cultural possibilitou a concepção da idéia de um mundo físico organizado a partir das bases da teoria heliocêntrica de Nicolau Copérnico (1473-1543), mundo este até então organizado segundo a percepção geocêntrica de Aristóteles-Ptolomeu, que entendia os fenômenos do mundo dividos entre passageiros e corruptíveis (esfera sublunar) e perfeitos, eternos e absolutos (esfera supralunar), estando os primeiros associados aos atos humanos e os segundos, associados ao plano divino. Essa noção de organização dos fenômenos do mundo atendia plenamente à compreensão cosmológica legitimada pela igreja católica, que confirmava, assim, a existência de um universo regido pela manifestação da onipresença, da onipotência e da onisciência de Deus. As bases dadas pela teoria de Copérnico iriam construir um novo rumo para a compreensão do espaço e dos fenômenos físicos, pois propunha uma perspectiva baseada na objetividade e na concretude para a observação destes, e uma perspectiva subjetiva e mental destinada à leitura dos anseios e das expectativas humanas. A intercessão entre as demandas materiais, o contexto da transformação dos valores culturais e a configuração de novos quadros mentais, processados entre os séculos XIV e XVI, estava contemplada por um conjunto de eventos amparados e possibilitados pelas conquistas realizadas no campo científico, que caracterizam uma revolução cognitiva que trazia em si consonância com os desejos instalados na sociedade. A partir dessas transformações introduzidas pela ciência, o mundo passa a adquirir uma conformação mais integrada, mais globalizada. Novas percepções dos fenômenos físicos confirmados pela Física Mecânica modificaram a percepção da inserção do Biotecnologia Ciência & Desenvolvimento 43 homem no mundo, assim como modificaram dramaticamente a inserção do mundo no universo, abrindo novas dimensões e novos parâmetros para a avaliação da potencialidade humana diante do universo físico e natural. Concretamente, no rastro das inovações colocadas pela ciência renascentista, efetivaram-se importantes iniciativas que modificaram totalmente a noção sobre o mundo, como foram, por exemplo, as grandes navegações e o desenho de uma nova cartografia do mundo; mundo mais diverso em termos de sua natureza e de sua cultura. Esses fatos causaram um grande impacto e transformaram substancialmente o mundo europeu, consolidando também a ciência como valor essencial para o processo civilizatório num mundo, agora, definitivamente ampliado. Essas transformações manifestadas pelas necessidades da vida material e pela ansiedade cognitiva dos processos de transformação dos valores e da cultura possibilitaram distinções entre o alcance do conhecimento interior e o do conhecimento exterior, e aceleraram a percepção do mundo com características distintas, onde o homem material se apresentava, na sua relação com o conhecimento, sendo portanto o homem racional, mas este mesmo homem era também subjetivo, no tocante a sua relação com Deus. Essa perspectiva da percepção humana diante dos fenômenos do mundo promoveria a separação do conhecimento científico da religião, e conduziria a um processo que resultou na dessacralização do mundo. As progressivas descobertas propiciadas pela Física com base na observação da mecânica dos corpos abririam o caminho de uma nova percepção dos fenômenos do mundo e da natureza. A criação do método experimental proposto por Francis Bacon (1561-1626) e por Galileu Galilei (1564-1642) foi fundamental para dinamizar os processos de pesquisas e de descobertas científicas acompanhados pelo valor do rigor e da objetividade científica. Os grandes marcos que definiram a separação entre o racional e o sagrado centraram-se nas pesquisas e descobertas sobre as macro-estruturas do universo, demonstradas especialmente nos estudos de Kepler (1571-1630); sobre a forma elíptica dos astros, que consolidou a idéia da ausência da perfeição divina que caracterizavam a idéia, até então vigente, da criação divina para explicar o universo e tudo que nele 44 Biotecnologia Ciência & Desenvolvimento existe. A busca da precisão técnica para ajustar e confirmar as novas proposições sobre a organização cosmológica do mundo também seria essencial para legitimar os processos de consolidação da percepção científica a respeito dos fenômenos da natureza. O alargamento da busca científica sobre o movimento mecânico dos astros e dos corpos sobre a superfície da Terra começou a ganhar mais consistência a partir do uso da luneta, inventada por Galileu. Esse recurso tecnológico consolida o campo do conhecimento da Física, favorecendo a criação de leis voltadas para a concepção da noção de um universo uniforme. Essa linha de percepção do universo e de seus fenômenos ganha um novo reforço a partir da perspectiva de visualização dessa uniformidade, através da geometria, proposta por Descartes (1596-1650), quando este congrega os recursos da matemática, fundindo a álgebra, a aritmética e a geometria para organizar a estrutura do raciocínio matemático, e abrir novas possibilidades de demonstração padronizada voltadas para os métodos baseados na experimentação. A idéia de um mundo uniformizado, regido pelas leis da Física Mecânica, permite o avanço de observações e definições padronizadas dos fenômenos ocorridos no universo, tal como a gravidade, proposta, como Lei da Mecânica, por Isaac Newton, e contribui para a construção da percepção do mundo, cujos movimentos reguladores de sua ordem eram agora baseados na razão matemática, que os visualizava como máquina, e substituíam a vontade voluntariosa e misteriosa dada por Deus. O racionalismo configura uma forma de compreensão do mundo, dos objetos e das coisas, mas o movimento mental e ideológico do homem continua ligado à valorização da criação divina, fato que será também objeto de preocupação da ciência e de seus filósofos. Para resolver essa dicotomia entre o racional e o divino, Descartes propõe a distinção entre o mundo objeto manipulado (res extensa), e o mundo subjetivo e pensante (res cogito), e separa o conceito de homem do conceito de natureza, sugerindo que os fenômenos humanos estão fora do âmbito da natureza, pois a idéia de homem passa a ser correlata ao conceito de espírito, onde reside o mundo subjetivo do pensamento. O conceito de natureza está fora do homem e o homem, fora do conceito de natureza. No âmbito da reorganização do conhe- cimento, o estudo e a reflexão da natureza caberá à ciência, e a reflexão sobre o homem caberá à Filosofia; ao homem caberá o status de sujeito pensante e à natureza o status de objeto manipulável e controlado pela razão científica. Essa dimensão do alcance da ciência, do lugar do homem e da importância de Deus se volta para a definição do homem segmentado em corpo, mente e espírito, e contribui para a constituição de campos científicos mais especializados. A Medicina se preocupará com os fenômenos do corpo humano, sobretudo a partir do avanço das pesquisas sobre anatomia realizadas por Vesálio (1514-1564); os fenômenos mentais, que caracterizam a produção do pensamento, passam ao domínio da Filosofia; e as questões espirituais ficam sob o domínio da Teologia. A ciência, que irá se ocupar dos fenômenos da natureza, irá investigá-la, percebendo-a basicamente como uma coleção de corpos dotados de movimentos mecânicos, e procederá, a partir dessa noção, à sua classificação, atributos e utilização, favorecendo a construção de uma lógica utilitária dos recursos encontrados na natureza em benefício do progresso material da sociedade, consolidando que se perceba a natureza como estoque de recursos, e lapidando noções que iriam se concretizar verticalmente durante os processos das revoluções industriais. No entanto, também o avanço industrial criou uma nova demanda para a ciência, abrindo-lhe caminho para a estruturação de outros campos especializados da ciência, em particular para a Química e para a Biologia, ciências fundamentalmente apoiadas no método experimental baseadas na observação isolada do fenômeno em laboratório, para confirmar regularidades do fenômeno observado ou provocar repetições. O método, ancorado na necessidade incondicional do experimento, foi supervalorizado pelos estudos promovidos por essas ciências, e realizou uma transformação paradigmática na percepção do mundo e de seus fenômenos. Os experimentos liderados pelos laboratórios de química e de biologia comprovaram, enquanto fato essencial da ocorrência dos fenômenos da natureza, o movimento interno da matéria, superando a predominância da visão que considerava essencialmente a externalidade dos mesmos pelo movimento regido pelas leis da mecânica. Dentro dessa nova percepção dos fenômenos da natureza, algumas passa- gens constituíram marcos para a construção do paradigma que percebia a natureza como estrutura interna vital. Em Lavoisier (1743-1794), a Química iria afirmar esse movimento interno e dinâmico dos fenômenos, apontando para a existência de uma natureza cíclica, por intermédio da clássica afirmação que traduzia o movimento interno da matéria: na natureza, nada se perde, nada se cria, tudo se transforma. Nessa linha de preocupação, Newton avançaria em seus estudos, procurando perceber o movimento interno da matéria, investindo nas pesquisas sobre a luz e a ótica, contribuindo com a formulação da teoria dos movimentos ondulatórios. Também Lineu (1741-1783) contempla, em seu estudo de sistematização da classificação das espécies vegetais, a noção de evolução, e Lamarck, ao dedicar-se ao estudo dos seres vivos, desenha a idéia de evolução natural, que será, posteriormente, desenvolvida por Charles Darwin (1809-1882), estudo que abrangeria os campos das ciências naturais e humanas, como a biologia, a história, a antropologia e a filosofia, favorecendo a construção de percepções interdisciplinares nos estudos sobre a natureza e a dinâmica da vida, enfatizando uma relação mais estreita entre o homem e a natureza, dentro da perspectiva do pensamento científico, reabilitando o homem como parte integrante do mundo natural, dando aos fenômenos naturais uma conotação orgânica no sentido de sua continuidade. Um outro importante marco foi elaborado pelas observações e pesquisas realizadas por Louis Pasteur, de formação química, que funda a doutrina microbiana para explicar o princípio microbiano das doenças, deixando a vacina disponível para a sociedade como terapêutica preventiva das moléstias de caráter epidêmico, e contribuindo decisivamente para a organização de uma medicina voltada para a saúde coletiva, atendendo às demandas do crescimento urbano e das urgências sanitárias como conseqüência do aceleramento da produção industrial. O contexto definido pelo progresso industrial verticaliza a percepção e a conseqüente utilização da natureza como fonte de recursos, traduzida em solos férteis, ocorrência de minérios, existência de mananciais, de florestas, etc., itens classificados como riqueza e potencial econômico das nações. A construção dessa visão da natureza, agora, sem a intervenção direta da ciência, vai estimu- lar a mercantilização dos espaços naturais para atender aos projetos industriais, criando as condições necessárias para a eclosão de conflitos e disputas entre os Estados, na luta pela conquista dos melhores territórios. Nesse contexto, valorizam-se os estudos e os levantamentos baseados nas pesquisas amparadas pelo campo científico das geociências, como lastro seguro do método cartográfico ou georeferenciado para determinar as fronteiras naturais dos Estados. Por outro lado, esta conjuntura e as preocupações bem pontuais impõem a percepção do espaço natural associado à história dos territórios, contemplando seus aspectos culturais para estabelecer as diferenças territoriais. As proposições metodológicas de Carl Ritter (1779-1859) marcam essa perspectiva da percepção do espaço natural, o espaço intimamente relacionado com as intervenções das necessidades humanas, tanto no plano objetivo de sua sobrevivência, como no plano de sua identificação subjetiva e cultural. Os estudos elaborados por Ritter e, mais tarde, por Friedrich Ratzel (1844-1905) lançariam as bases para a formulação de uma outra percepção do espaço natural, ou seja, aquela que concebia o homem como resultado do meio natural, e considerava a construção civilizatória do homem incluída no quadro geral da natureza por ele conhecida e onde ele se encontra adaptado biologicamente e mentalmente, delineando, assim, a prénoção daquilo que seria posteriormente uma vertente teórica para a construção do paradigma ecológico. O paradigma ecológico retomaria criticamente a lógica do racionalismo cartesiano para redefinir a percepção do movimento do universo natural, minimizando a importância hierárquica da dinâmica da vida, mas, sobretudo, reintegrando o homem nessa dinâmica, e valorizando acentuadamente, a diversidade da natureza, incluindo os aspectos da diversidade cultural humana com base no pressuposto teórico que conduziria a percepção de que o processo natural se realiza por sínteses, através da produção e da reprodução da vida, sendo, portanto, o fator sintetizador, o ponto, ao mesmo tempo, unitário e diversificador do mundo, e considerando que o movimento vital congrega, simultaneamente, o orgânico, o inorgânico, o fragmentário e o unitário, onde a evolução é a condição fundamental para a existência do diverso que caracteriza a unidade em escala planetária. O que parece ser um contexto de encantamento ou de desencantamento diante das potencialidades, projetos e promessas da ciência solidifica a estruturação mental do desejo de uma natureza lúdica, de um planeta igualitário, enfim, do sonho do Éden. Essas bases ideológicas deságuam de várias maneiras nos discursos e nas ações que se afirmam ecológicas. No entanto, devemos salientar que a relação entre ciência e sociedade possui uma história que faz parte da história do homem. A atualização do debate ciência sociedade está hoje centrada nos temas que discutem os efeitos negativos e positivos das tecnologias disponíveis. Nesse aspecto, a Biossegurança abraça essa preocupação, pois cabe a ela garantir cientificamente as bases dos controles dos efeitos positivos e negativos, considerando a relação entre risco e benefício dessas tecnologias com o objetivo de cuidar da segurança da vida e de diminuir assim, a distância histórica que se construiu entre a sociedade e os laboratórios. Devemos estar atentos às implicações dos atos que anunciam e agem para desconstrução da ciência e da tecnologia, ou que reeditam visões e percepções enraizadas na tradição religiosa ou em quaisquer outras apoiadas em posições dogmáticas, para bloquear o alcance da ciência. Lembramos que, quando Charles Darwin publicou seu livro A Origem das Espécies, a sociedade revelou medo e pânico diante das heresias que negavam a idéia criacionista sobre a origem do homem e do mundo. Em termos contemporâneos, essa ideologia preparadora do pânico, arquitetada para conduzir enfrentamentos com as perspectivas dos avanços científicos e tecnológicos, pode redefinir e legitimar pensamentos e ideologias que ingenuamente pretendem decretar o fim da ciência. Referências Koyré, A. Do mundo fechado ao unuverso infinito. 1957, ed. Forense. Jacob, François. A lógica da vida (uma história da hereditariedade). 1983, Graal, RJ Mason, S.F. História da ciência. 1962. Ed. Globo, Porto Alegre. Morin, Edgar. O método, 3 volumes. S/ d, Zahar Editores, RJ Moreira, Ruy. O círculo e a espiral. A crise paradigmática do mundo moderno. 1993, ed. Cooautor, RJ Wilson, Edward O. L´enjeu Écologique. http://www.larecherche.fr/view/333/ 03330141.html. Biotecnologia Ciência & Desenvolvimento 45 Vacinas são administradas a pessoas sadias e, por isso, devem ter um alto padrão de biossegurança. Vasco Azevedo Prof. Adjunto do Departamento de Biologia Geral do Instituto de Ciências Biológicas da Universidade Federal de Minas Gerais- UFMG. Membro Titular da CTNBio. [email protected] Sérgio Costa Oliveira Prof. Adjunto do Departamento de Bioquímica e Imunologia do Instituto de Ciências Biológicas da Universidade Federal de Minas Gerais-UFMG. Membro Titular da CTNBio. [email protected] Foto cedida pelos autores As duas medidas de saúde pública que tiveram maior impacto no controle das enfermidades infecciosas e parasitárias no mundo foram as de tratamento da água e a vacinação, sendo a segunda a que apresenta o melhor custo-benefício. Há duzentos anos atrás, Jenner criou uma nova era na medicina quando intencionalmente infectou uma criança com o vírus da varíola bovina. Esse experimento, que hoje seria considerado pela comunidade científica como anti-ético, foi o começo para a erradicação da primeira doença infecciosa no mundo, a varíola humana (Foto 1). Várias outras doenças e enfermidades consideradas de maior gravidade para a saúde humana estão sendo controladas com vacinas tradicionais ou de primeira geração (Tabela 1). Apesar do sucesso dessas vacinas convencionais, ainda existem muitas doenças que debilitam ou levam à morte, como, por exemplo, a AIDS, a malária, a dengue e a hepatite C, para as quais 46 Biotecnologia Ciência & Desenvolvimento não existem vacinas disponíveis ou as que existem não são efetivas e apresentam riscos inaceitáveis. Com o tremendo avanço da biologia molecular, que permite manipular, inserir e expressar genes heterólogos em diferentes organismos, novos tipos de vacinas estão sendo desenvolvidas como alternativas para o controle dessas enfermidades. Dessas vacinas recombinantes , a imunização genética ou vacina de DNA é a mais promissora. Essa tecnologia, de menos de uma década, envolve a administração direta do DNA plasmidiano carreando o gene codificador da proteína antigênica, a qual será expressa no interior da célula do hospedeiro. Recentemente, foram publicados nesta revista vários artigos sobre o assunto (1-3) e na literatura existe uma infinidade de exemplos que demonstram a importância desse novo instrumento na pesquisa biomédica (4,5). Vacinas são administradas a pessoas sadias e, por isso, devem ter um alto padrão de biossegurança. Os testes clínicos das vacinas de DNA são similares aos de outros produtos biológicos (Tabela 2), sendo o seu controle de qualidade mais fácil e menos oneroso pois necessita apenas da certificação da pureza do DNA. Contudo, existem riscos potenciais de biossegurança, como uma possível integração no genoma da célula hospedeira do DNA plasmidiano, que pode causar ativação de oncogenes ou inibição de genes supressores de tumor, e indução de autoimunidade, que devem ser exaus- tivamente investigados. Entretanto, poucas evidências existem de que as vacinas gênicas possam apresentar riscos superiores aos desencadeados pelo uso das vacinas convencionais (6). Neste artigo, daremos ênfase ao tema risco de integração do DNA vacinal no genoma da célula hospedeira. A integração do DNA plasmidiano em cromossomos de células somáticas pode potencialmente gerar efeitos patológicos. A mutagênese por inserção levaria a um câncer, caso esse evento ative (proto-oncogenes) ou inative genes (supressores de tumor) implicados na regulação do ciclo celular. Essa inserção pode ocorrer ao acaso ou por meio da recombinação homóloga, sendo que o primeiro evento seria o mais freqüente. Para tentar diminuir a possibilidade destes eventos ocorrerem, deve-se evitar, se possível, que existam seqüências nucleotídicas homólogas ao do genoma humano no plasmídio vacinal e que este não se replique nas células hospedeiras. Plasmídios usados na imunização genética possuem uma estrutura com elementos regulatórios como promotores, acentuadores, terminadores, e sítios de poliadenilização reconhecidos pelas células eucarióticas, marcadores de seleção, que são, na maioria, antibióticos, e uma origem de replicação que não é funcional em células de mamíferos (7). Apesar dos elementos regulatórios serem funcionais nessas células, as seqüências nucleotídicas desses plasmídios não devem possuir homologias significativas com o DNA genômico dos mamíferos iguais ou superiores a 0,6 kilobases (kb), o que evitaria uma maior eficiência na inserção do DNA, ao acaso. Na recombinação homóloga, além do requisito anterior, os dois genomas, o plasmidiano e o do hospedeiro, devem ser replicativos; como os plasmídios mais utilizados nas vacinas de DNA não se replicam, a eficiência desse evento ficaria comprometida. Esses argumentos teóricos são indicativos de que a taxa de integração é baixa, e se esta ocorresse, a probabilidade de mutação deveria ser insignificante, e isso foi comprovado pelos experimentos pré-clínicos realizados por Nichols e colaboradores (8) e Martin e colaboradores, (9) que utilizaram a técnica de PCR (Polymerase Chain Reaction). Como essa técnica é extremamente sensível, foi necessário realizar algumas adaptações para serem evitados resultados falso positivos. Para que o DNA genômico extraído de tecidos musculares dos quadríceps dos camundongos vacinados geneticamente fosse separado do DNA plasmidiano (vacina gênica), este foi digerido com uma enzima rara, cujo sítio de clivagem foi inserido no plasmídeo vacinal para evitar a formação de concatâmeros, eliminando uma migração em géis de agarose conjunta com o DNA genômico. Foram também tomados os clássicos cuidados para evitar contaminações na PCR, e, quando o resultado era positivo, ou seja, havia a ocorrência do evento de integração do plasmídeo no genoma, foi necessário repetir os ensaios com variantes da técnica de PCR, como LMPCR ( Ligation-mediatedPCR), ou PCR inversa, para a sua validação. Nichols e colaboradores não detectaram nenhuma evidência de integração usando de 1 a 7,5 cópias de plasmídeos por 150.000 células como limite de sensiblidade, porém Martin e colaboradores detectaram que entre 330 cópias de plasmídeos ficavam associados ao DNA genômico dos animais vacinados. Apesar de resultados conflitantes em relação à integração, a conclusão dos dois grupos foi unânime no cálculo de freqüência de muta- ção induzida pela integração do plasmídeo no genoma do hospedeiro. A probabilidade de uma mutação ocor- Figura 1: Homem com varíola. Foto da coleção do CDC (Center for Disease Control and Prevention) autorizada para divulgação rer em um dado gene devido à imunização gênica, seria 3.000 vezes menor do que a freqüência de mutação espontânea que ocorre no genoma das células dos mamíferos. Entretanto, Tabela 1. Datas da utilização em seres humanos de vacinas de primeira geração. Ano 1798 1885 1897 1923 1926 1927 1927 1935 1955 1962 1964 1967 1970 1981 Enfermidade Varíola Raiva Peste bubônica Difteria Coqueluche Tuberculose (BCG) Tétano Febre amarela Poliomielite injétavel Poliomielite oral Sarampo Papeira Rubéola Hepatite B* De acordo com Plotkin & Mortiner (15). * Vacina de segunda geração (proteina recombinante purificada de células) mesmo sendo a probabilidade tão baixa para que eventos oncogênicos ou patogênicos ocorram, somente um longo período de avaliação com um grande número de voluntários permitiria determinar, em seres humanos, a ocorrência desses fenômenos biológicos. O que significa que os testes clínicos são tão imprescindíveis para as avaliações desses riscos teóricos quanto para certificar os benefícios potenciais dessa nova tecnologia. A agência reguladora americana FDA (Food and Drug Administration) agora requer que testes com o uso de PCR sejam feitos com as adaptações descritas anteriormente nos ensaios préclínicos, mas ainda não estabeleceu os níveis aceitáveis de integração plasmidiana no genoma. Essa mesma agência possui um documento bem complexo que estabelece normas para os experimentos em animais e testes clínicos em humanos com a utilização de vacinas de DNA (10) . Na legislação brasileira de biossegurança, ainda não existe uma instrução normativa que seja específica e completa no trato dessa matéria. Testes clínicos na fase I e II em seres humanos já estão sendo realizados com vacinas de DNA contra as seguintes enfermidades: AIDS, malária, linfoma das células B, melanoma, hepatite B, e infecção pelo herpes vírus. Calarota e colaboradores (11) publicaram recentemente, na revista The Lancet, o resultado de testes clínicos na fase I, onde indivíduos imunizados com genes do HIV-1 induziram resposta imune celular específica, sem que efeitos colaterais tenham sido observados. O grupo de Stephen Hoffman (12), na fase I dos testes clínicos com a vacina de DNA contra a malária, relatou que a administração foi bem tolerada, sem problemas de biossegurança aparente e com uma excelente indução da resposta celular. Esses resultados deram suporte à passagem para a fase II, onde serão feitos testes de proteção contra essa enfermidade. Nos tratamentos de câncer, as vacinas de DNA estão sendo usadas em pacientes quando os tumores são refraBiotecnologia Ciência & Desenvolvimento 47 Tabela 2. Testes Clínicos Fases I II III Número de pacientes Tempo 20 a 100 Algumas centenas Algumas centenas até alguns milhares Alguns meses Alguns meses até 2 anos Alguns meses até 2 anos Avaliação da biossegurança Teste de proteção e efeitos colaterais +++ +++ +++ +++ +++ O primeiro passo para uma vacina ser aprovada para comercialização é o teste em animais de laboratório; se esses não apresentarem reações adversas, as etapas posteriores podem ser prosseguidas. O passo seguinte são testes clínicos em seres humanos, que são divididos em três fases de avaliação do nível de proteção conferido por estas vacinas e a sua biossegurança. Se nas últimas fases, for comprovada que essas vacinas são efetivas e seguras, então a indústria farmacêutica pode solicitar aos órgãos competentes a licença para a comercialização do produto tários às terapias tradicionais. Em um desses testes clínicos, pacientes com melanoma receberam injeções de DNA complexados a lipossomos diretamente nos tumores. Em alguns desses pacientes houve regressão do tumor e de suas metástases (13). Os testes clínicos relatados anteriormente foram realizados através da injeção direta de DNA no músculo do indivíduo ou nos tumores, porém o teste com a vacina de DNA contra a hepatite B foi realizado por meio da imunização pelo processo da biobalística, utilizando-se o gene gun ou arma de genes (14). O gene gun é um aparelho que promove a aceleração e a introdução de micropartículas de ouro encobertas com o DNA plasmidiano recombinante na derme dos indivíduos. Os voluntários vacinados não se queixaram de dor ou de qualquer outro desconforto devido à utilização desse aparelho. Uma resposta eritematosa moderada e transiente foi observada, o que consiste em uma resposta inflamatória natural da pele após a imunização. Esse estudo demonstra que essa via de administração das vacinas de DNA, utilizando a arma de genes gene gun, pode viabilizar a imunização de um grande número de indivíduos quase que automatizando esse processo. As vacinas de DNA em menos de uma década têm dado uma contribuição real no campo da vacinologia, e possuem uma grande vantagem em relação às vacinas tradicionais, o que torna essa tecnologia um instrumento importante no combate às doenças infecciosas que afetam a nossa sociedade. 48 Biotecnologia Ciência & Desenvolvimento Referências bibliográficas 1. Silva, C.L. Vacinas gênicas. O impacto sobre o controle das doenças infecciosas (1997). Biotecnologia Ciência & Desenvolvimento. 3:32-34. 2. Silva, C.L. Tuberculose. Uso da biotecnologia para o desenvolvimento de uma vacina de DNA que previne e cura a doença. Vacinas gênicas (1998). Biotecnologia Ciência & Desenvolvimento. 4. 3. Azevedo, V., Oliveira, S.C. (1998) Vacinas de DNA: o paradigma das vacinas gênicas. Biotecnologia Ciência & Desenvolvimento. 5: 40-43. 4. Oliveira SC, Rosinha GM, deBrito CF, Fonseca CT, Afonso RR, Costa MC, Goes AM, Rech EL, Azevedo V (1999). Immunological properties of gene vaccines delivered by different routes. Braz J Med Biol Res. Feb;32(2):207-14. 5. Oliveira SC, Harms JS, Rosinha GM, Rodarte RS, Rech EL, Splitter GA. (2000). Biolistic-mediated gene transfer using the bovine herpesvirus-1 glycoprotein D is an effective delivery system to induce neutralizing antibodies in its natural host. J Immunol Methods. Nov 1;245(1-2):109-18. 6. Donnelly, J.J., Ulmer, J.B. DNA vaccines for viral diseases. Brazilian Journal of Medical and Biological Research, 32(2) 215-212. 7. Azevedo V., Levitus G., Miyoshi A., Cândido A.L, Goes A.M., and Oliveira S.C. (1999). Main features of DNAbased immunization vectors. Brazilian Journal of Medical and Biological Research, 32:147-153. 8. Nichols WW., Ledwith BJ., Manam SV., Troilo PJ. (1995). Potencial DNA vaccine integration into host cell genome. Annals of the New York Aca- demy of Sciences, 94:30-39. 9. Martin T., Parker SE., Hedstrom R., Le T., Hoffman SL, Norman J., Hoblew D.(1999). Plasmid DNA malaria vaccine: The potencial for genomic integration after intramuscular injection. Hum Gene Ther, 10(5): 75968. 10. Points to consider on plasmid DNA vaccines for preventive infectious disease indications. http:// www.fda.gov/cber/ptc/plasmid.pdf 11. Calarota S., Bratt G., Nordlund S., Hincula J., Leandersson A-C., Sandstrom E., Wahrem B. (1998). Cellular cytotoxic response induced by DNA vaccination in HIV-1-infected patients. Lancet, 351: 1320-1325. 12. Wang R., Doolan DL., Le TP., Hedstrom RC, Coonan KM., Charoenvit Y, Jones TR., Hobart P., Margalith M., NG J., Weiss WR., Sedegah M., De Taisne C., Norman JA., Hoffman SL. (1998). Induction of antigen specific cytotoxic T lymphocyte in humans by a malaria DNA vaccine. Science, 282:476-479. 13. Benton PA., Kennedy RC.(1998) DNA vaccines for the treatment of cancer. Curr Top Microbiol Immunol.;226:1-20. 14. Roy MJ, Wu MS, Barr LJ, Fuller JT, Tussey LG, Speller S, Culp J, Burkholder JK, Swain WF, Dixon RM, Widera G, Vessey R, King A, Ogg G, Gallimore A, Haynes JR, Heydenburg Fuller D. (2000) Induction of antigenspecific CD8+ T cells, T helper cells, and protective levels of antibody in humans by particle-mediated administration of a hepatitis B virus DNA vaccine. Vaccine. 22;19(7-8):764-78. 15. Plotkin SA., Mortiner EA.(1994). Vaccines. Philadelphia WB Saunders. ANBIO Associação Nacioal de Biossegurança (Repete Fotolito) Saiu na página 29 da última edição (ED. 17) Biotecnologia Ciência & Desenvolvimento 49 Transferência de Tecnologia Durante o processo de desenvolvimento tecnológico, raramente incorporamos o conhecimento prático do produtor. A crítica é feita pelo pesquisador da Embrapa Gado de Corte, Ivo Martins Cezar, da área de socioeconomia. Ele desenvolveu uma pesquisa que comprovou o quanto os produtores rurais estão, cada vez mais, dependentes de informação e tecnolo- Ivo Martins Cezar gia para tomarem decisões . De acordo com o pesquisador, o distanciamento que possa existir entre o conhecimento gerado nos centros de pesquisa, as tecnologias desenvolvidas e a real necessidade do produtor ou as possibilidades concretas do pecuarista em adotar tais tecnologias, acontece devido à falta de integração entre produtores e técnicos. Estes últimos, segundo sua opinião, tendem a interpretar os problemas de acordo com seus pontos-de-vista, não considerando a vivência dos produtores. Segundo Cezar, o produtor decide pela adoção de determinada tecnologia por dois motivos básicos: observação (ele reage como o cético São Tomé: é ver para crer!) e indicação, a partir da referência de uma pessoa de sua confiança, que funciona como formador de opinião e avalista tecnológico. Já no processo de transferência de informação, Cezar chama a atenção dos técnicos para a necessidade de revisão de alguns procedimentos, uma vez que 50 Biotecnologia Ciência & Desenvolvimento 50 Biotecnologia Ciência & Desenvolvimento o setor produtivo é formado por diferentes grupos sociais. Não se deve generalizar porque, hoje, é imperativo democratizar a informação. Ivo ressalta a existência de uma barreira entre produtores e técnicos: muitas vezes, desenvolvemos tecnologias que acabam não sendo utilizadas pelos produtores, seja porque sua realidade socioeconômica não se ajusta à tal tecnologia, seja porque ele ,simplesmente, não foi envolvido no processo que a originou. Para o pesquisador outro empecilho está na tendência dos difusores em repassar a informação tecnológica usando a mesma receita para divulgação ao público urbano. Segundo ele, a principal diferença entre o fluxo de informação no campo e na cidade é que o produtor rural precisa ver os resultados; tem de observar para se convencer de que determinada tecnologia pode ser aplicada em sua propriedade. É justamente nesta etapa que os técnicos devem buscar meios alternativos e informais de chegar até este público, comenta o pesquisador. Conversas, visitas às propriedades, dias de campo, tudo é válido na tentativa de difundir tecnologias que possam se ajustar ao ambiente socioeconômico de todos os grupos que integram o setor produtivo. Thea Tavares e Christiane Reis Embrapa - CNPGC [email protected] Mariposa Transgênica Está previsto para Maio a liberação de um inseto transgênico na natureza para testes no combate à pragas. A Mariposa, geneticamente modificada, foi criada por Thomas Miller, da Universidade da Califórnia e é estéril. Expedição Científica Paleontólogos farão uma expedição científica por três sítios geológicos nacionais. A equipe, formada por 30 pessoas incluindo cinegrafistas e produtores para filmagem , levarão pouco mais de um mês para o trabalho, que foi orçado em 600 mil reais. A expedição Em busca dos dinossauros, foi idealizada pelo Departamento de Paleontologia do Museu Nacional do Rio. Projeto Genoma Humano Saiu a publicação de dados sobre o genoma humano. Foi estimado em 30 mil o número aproximado de genes do corpo humano - quase o número de genes de um camundongo, que é em torno de 29,7 mil e não muito diferente da maioria das plantas, que têm em torno de 25mil genes. O sequenciamento completo deverá estar pronto em 2003, mas levará muito mais tempo para ser completamente compreendido. Vale lembrar que o Brasil deu uma importante contribuição ao Projeto Genoma Humano Internacional, produzindo mais de 1 milhão de fragmentos de genes humanos e colocando o Brasil como o segundo país que mais contribuiu com informações para o Projeto. Muito desse sucesso se deve à estratégia desenvolvida pelos pesquisadores do Instituto Ludwig de Pesquisas sobre o Câncer, a chamada Estratégia Orestes, na qual permite a obtenção preferencial de regiões codificadoras do genoma humano. - Para saber mais sobre o Projeto Genoma do Câncer, procure na edição número 12 da Revista Biotecnologia o artigo escrito pelo Dr. Emmanuel Dias Neto do Instituto Ludwig, ou acesse www.biotecnologia.com.br. italiano decidiu formar um painel de especialistas para relatar as pesquisas que estão sendo feitas sem preconcei- Adriana Bruno Casa da Imprensa CTNBio A Comissão Técnica Nacional de Biossegurança (CTNBio) liberou a continuidade das pesquisas na estação experimental da empresa Monsanto, em Não- Me- Toque (RS). A área, onde havia uma plantação experimental de soja transgênica RR, foi alvo da invasão promovida pelo MST, no dia 28 de Janeiro. O relato sobre a situação no local foi apresentado na 45º reunião da CTNBio, encerrada nesta quinta-feira, 8 de Fevereiro, em Brasília. O representante do Ministério da Agricultura na Comissão, Paulo Borges, foi o responsável pela inspeção realizada no último dia 5. Segundo ele, a destruição da lavoura experimental não causou prejuízos ao meio-ambiente. Borges explicou que a cultura ainda não havia produzido sementes que pudessem se espalhar, mas confirmou que houve perda de dados científicos, o que pode prejudicar as pesquisas sobre transgênicos. Ministério da Ciência e Tecnologia CTNBio. Itália retoma pesquisa de biotecnologia após protesto de 1.500 cientistas O governo da Itália anunciou, em 13 de fevereiro, que cancelou a proibição que o país vinha impondo às pesquisas com plantas geneticamente modificadas depois de um protesto de cientistas realizado em Roma, na mesma data. O governo sam graves danos à balança comercial italiana, já que os produtos agrícolas perdem competitividade no mercado externo, diminuindo as exportações. Nossa agricultura só se salvará se for baseada nas inovações, afirmou Magnifico ao jornal italiano Il Foglio. Transgênicos e Agrotóxicos tos ou paixão e instalar uma comissão autônoma que, dentro de dois meses, estabelecerá novas regras no que concerne à biotecnologia. A decisão junta-se ao anúncio do Parlamento Europeu de colocar fim à moratória de três anos sobre o plantio de novos cultivos de plantas geneticamente modificadas na União Européia, ao apresentar dia 14 de fevereiro novas regras para o setor. As informações foram veiculadas pelas agências internacionais Bloomberg e AP/Dow Jones. O manifesto protestando contra o banimento parcial de novas pesquisa na área de biotecnologia e de plantas geneticamente modificadas com mais de 1.500 assinaturas de cientistas de diversas especialidades foi lançado em Roma no dia 13 de fevereiro, na mesma data do anúncio do governo da Itália. Encabeçaram o protesto os cientistas Renato Dulbecco, Prêmio Nobel de Medicina de 1975, e Rita Levi-Montalcini, Prêmio Nobel de Medicina em 1986. O manifesto defende a liberdade de pesquisa e é contra o veto a experimentos com organismos geneticamente modificados. Para Angelo Spena, especialista em biotecnologia vegetal pela Universidade de Verona e um dos cientistas a assinar a declaração pública, a biotecnologia aplicada à agricultura leva a uma drástica diminuição do uso de agroquímicos nas lavouras, o que gera plantas e alimentos mais saudáveis para a população. Para Vitangelo Magnifico, diretor do Instituto Experimental de Horticultura do Ministério da Agricultura italiano, as proibições às inovações tecnológicas, incluindo a biotecnologia, cau- A China reduziu em oito vezes a aplicação de pesticidas na cultura de algodão. O relatório foi divulgado recentemente pelo Ministério da Agricultura chinês e revela que o país plantou mais de um milhão de hectares de algodão transgênico, em 1999. O resultado foi a diminuição em até oito vezes da aplicação de pesticida nas plantações. Este foi um dos exemplos citados pela presidente da Comissão Técnica Nacional de Biossegurança (CTNBio), Leila Oda, ao falar sobre os avanços da Biossegurança no Brasil e no mundo, no I Encontro Norte-Nordeste de Biossegurança, que aconteceu recentemente em Recife. Do ponto de vista ambiental e de saúde, este é um dado importantíssimo, ressaltou Oda, lembrando que a maioria dos países onde se desenvolvem pesquisas com transgênicos são trabalhados genes de tolerância a herbicidas, o que causará uma diminuição significativa do uso de agrotóxicos. Estamos dando mais um passo na melhoria da qualidade nutricional. Em pouco tempo o consumidor poderá optar, quando for ao supermercado, entre os alimentos orgânicos, transgênicos ou os que possuem aplicações de agrotóxicos. Ela lembrou ainda que a polêmica que envolve hoje a rotulagem nada tem a ver com a segurança do alimento. O rótulo, diz ela, servirá apenas para o consumidor decidir se vai ou não optar por aquele tipo de alimento. A CTNBio existe para dar à sociedade a segurança de que nenhum alimento transgênico que possa prejudicar a saúde humana será aprovado para comercialização. Se o alimento estiver no supermercado é porque a CTNBio concluiu que não representa risco para o homem, disse Leila Oda. Ministério da Ciência e Tecnologia CTNBio Biotecnologia Ciência & Desenvolvimento 51 Biotecnologia Ciência & Desenvolvimento 51 Agência Iris (Repete Fotolito) Saiu na página 37 da última edição (Ed. 17) 52 Biotecnologia Ciência & Desenvolvimento COBRAFI Conselho Brasileiro de Fitossanidade (Repete Fotolito) Saiu na página 23 da última edição (Ed. 17) Biotecnologia Ciência & Desenvolvimento 53 Por cerca de um século, o melhoramento convencional tem desenvolvido e liberado novas variedades sem riscos, ou com mínimos riscos, para o meio ambiente. As evidências e os resultados até então encontrados sugerem que a maioria dos OGM não apresentam riscos para o ambiente. Três tipos de riscos podem ser distinguidos: - riscos diretamente perceptíveis: andar de bicicleta em um trânsito caótico. - riscos perceptíveis com auxílio de métodos científicos: exposição a patógenos. - riscos virtuais: quando os conhecimentos existentes não permitem consenso: baixo nível de radiação, resíduos de defensivos agrícolas. Esses três tipos de riscos são ilustrados na Figura 1 por três círculos, que apresentam áreas de sobreposição indicando que os limites deles são, em determinados casos, indistinguíveis. Aluízio Borém Eng.-Agrônomo, MS, Ph.D., Pós-doutor, Professor do Departamento de Fitotecnia da Universidade Federal de Viçosa [email protected] Figura 1 Três tipos de riscos 54 Biotecnologia Ciência & Desenvolvimento Os riscos diretamente perceptíveis são controlados instintiva e intuitivamente. Não são necessários métodos científicos para se saber dos riscos de andar de bicicleta, por exemplo. Intuitivamente já se conhece esses riscos. Outros riscos só são detectados por meios científicos. Com um microscópio, por exemplo, podese ver e medir objetivamente o nível de contaminação de um alimento com microorganismos patogênicos. Existem ainda muitos riscos sobre os quais os cientistas ainda discordam. Muitos desses riscos relacionam-se com a saúde. Os críticos aos transgênicos têm elaborado uma longa lista de possíveis riscos de um eventual escape de um transgene para espécies silvestres, sugerindo conseqüências com implicações ecológicas, sociais, culturais, religiosas, econômicas e éticas. Entretanto, até a presente data, nenhum desses riscos foi cientificamente confirmado entre as milhares de liberações de transgênicos já realizadas. Muitos cientistas vêem esses riscos como possibilidades muito remotas (Schuster 1991), enquanto os críticos mantêm sua opinião de que, devido ao incompleto conhecimento da ação do transgene, o risco dessa tecnologia não pode ser acuradamente estimado (Breyer, 1991). Mackenzie e Henry (1990) argumentam que risco é função da exposição e do perigo. No contexto dos transgênicos, a exposição é medida pela capacidade de escape do transgene da variedade transgênica. conseqüentemente, há necessidade de se estimar a probabilidade de o escape persistir, aumentar e se espalhar no ambiente, colonizando-o. O perigo é inerente à característica e referese ao impacto que o transgene poderia ter no ambiente. Para quantificar a exposição, é necessário estimar a probabilidade do escape em função da distância entre indivíduos/populações, bem como do tamanho da população fonte do escape e sua persistência. A quantificação do perigo ou do impacto do escape no ecossistema não tem sido o principal alvo dos estudos de fluxo gênico. A quantificação do perigo deve envolver aspectos biológicos e sócio-econômicos. Visando a identificar e a medir os riscos em potencial no uso de variedades transgênicas, muitos projetos de pesquisa estão sendo conduzidos em laboratórios, casa de vegetação e em campo (Woohrmann et al. 1993). Muitos desses projetos são direcionados para o entendimento: I) do modo de reprodução das plantas, especialmente os sistemas de incompatibilidade e os mecanismos de dispersão de pólen; II) da hibridação e a introgressão gênica; III) da colonização; IV) da especiação e V) da evolução, associados ao uso comercial das variedades transgênicas. A falta de estudos abrangentes, que envolvam simultaneamente, genética de populações e ecologia, tem sido alvo de crítica dos ecólogos (Gabriel, 1993). Mecanismos Evolucionários Em genética de população, as forcas evolucionárias são estudadas por meio dos seus efeitos sobre as freqüências gênicas. Observando uma população em equilíbrio, de HardyWeinberg, os fenômenos que podem afetar as freqüências gênicas são: I) mutação; II) seleção; III) sistemas de acasalamento; IV) migração; V) deriva genética; VI) competição entre populações; VII) co-evolução. Mutação Mutação, no sentido amplo, significa o aparecimento de novos tipos hereditários. Ao nível do DNA, a maioria das mutações é de simples substituição de nucleotídeos, deleções, inserções e inversões. As tentativas de induzir alterações genéticas nas espécies cultivadas por meio de mutação, em geral, resultaram em mudanças detrimentais. A transformação gênica é uma forma de introduzir alterações genéticas nas plantas, de forma direcionada e não aleatória. Ela não é direcionada no sentido da região de inserção do transgene no genoma receptor ou do número de cópias introduzidas, mas o é no sentido de resultar em uma função pré-estabelecida. Seleção A seleção natural é o mecanismo pelo qual a população se adapta ao ambiente. O coeficiente de seleção é definido como o desvio da adaptação relativa ideal. Talvez a seleção natural seja a força evolucionária menos entendida, uma vez que: I) a adaptabilidade do indivíduo depende de inúmeros genes e da interação entre eles e deles com o ambiente; II) a maioria das mutações são neutras para a adaptação e sujeitas somente à deriva genética; III) mutações favoráveis não são selecionadas e fixadas em curto prazo; IV) alterações profundas no fenótipo normalmente reduzem a capacidade de adaptação, uma vez que o organismo é um sistema integrado. Para avaliar os riscos dos transgênicos, deve-se analisar o efeito do transgene no fenótipo do indivíduo receptor. O estabelecimento e a colonização por um OGM dependerá da natureza do gene introduzido, da sua interação com outros genes do receptor e com o meio ambiente. Variedades transgênicas tendem a ser mais fracas competidoras do que seus correspondentes não transgênicos, uma vez que os genes introduzidos estabelecem um novo dreno metabólico, além de resultarem em novas intera- ções epistáticas no indivíduo. Adicionalmente, o ambiente em que eles eventualmente manifestem superioridade competitiva tende a ser menor do que aquele onde seus correspondentes não transgênicos possuem maior habilidade de sobrevivência. Modo de Reprodução O isolamento reprodutivo entre diferentes populações fundamentase em barreiras geográficas e genéticas estabelecidas no processo evolucionário. Em uma população panmitica em equilíbrio de Hardy-Wernberg, o isolamento não é observado, uma vez que todos os indivíduos se cruzam livremente. Alterações no sistema de acasalamento na população podem levar a um forte isolamento, com conseqüente risco de extinção dos indivíduos transgênicos com baixa capacidade de competição. No caso do escape de transgênicos devido ao menor tamanho da população desses indivíduos em relação à população nativa, a influência da deriva genética aumenta as probabilidades de desaparecimento da população com o transgene. Deriva Genética Deriva genética é a alteração na freqüência gênica devido ao acasalamento tendencioso decorrente, exclusivamente, do tamanho da população. Se um transgene possui adaptabilidade neutra, a deriva genética altera a sua freqüência aleatoriamente, levando-o à fixação ou à eliminação. A deriva genética em pequenas populações pode ter maior força do que a seleção natural e definir sua extinção ou fixação. Migração A freqüência gênica em um sistema com subpopulações pode ser alterada pela migração de indivíduos entre elas ou pela dispersão do pólen. A migração em sentido amplo incluia troca gênica entre espécies (transferência gênica horizontal), mas o isolamento reprodutivo entre as espécies normalmente exclui esse intercâmbio. Biotecnologia Ciência & Desenvolvimento 55 Competição A persistência de uma planta transgênica no campo depende da sua habilidade de competir no ecossistema. A habilidade de competição ou a agressividade das variedades transgênicas devem ser estimadas para que se possam fazer inferências sobre o seu risco de colonização em um hábitat. Por cerca de um século, o melhoramento convencional tem desenvolvido e liberado novas variedades sem riscos, ou com mínimos riscos, para o meio ambiente. As evidências e os resultados até então encontrados sugerem que a maioria dos OGM não apresentam riscos para o ambiente (Regal, 1994). Espécies exóticas, quando introduzidas em novo hábitat, podem causar impacto no ecossistema. O mesmo poderia ocorrer com as variedade transgênicas, mas a maioria dos OGMs não apresentam elevada habilidade de competição, especialmente sem a interferência do homem. Evidências evolucionárias sugerem que, quanto mais domesticada ou melhorada é a espécie, menor habilidade de competição ela apresenta em sistemas silvestres. Coevolução O comportamento evolucionário dos indivíduos nativos em uma comunidade com variedades transgênicas deve ser analisado para se estimarem os possíveis impactos do processo coevolucionário no contexto das interações interespecíficas. Modelos para Avaliar Fluxo Gênico Vários modelos podem ser adaptados para o estudo do risco em potencial de escape gênico em variedades transgênicas. Entre eles, dois modelos, um derivado da genética de populações e outro, da teoria do melhoramentos de plantas, serão discutidos a seguir: Modelos Derivados da Genética de População 56 Biotecnologia Ciência & Desenvolvimento O fluxo gênico pode ser estimado com modelos que consideram as forças evolucionárias: seleção, migração, deriva genética e mutação. Para cada uma dessas forças, uma série de considerações devem ser feitas para validação do modelo: I) somente um transgene é considerado; II) o transgene é dominante sobre a forma alternativa no indivíduo receptor. Deve-se reconhecer, entretanto, que, em muitos casos, o híbrido é hemizigoto, uma vez que o receptor não possui forma para a alternativa do gene. Seleção e Migração O fluxo gênico pode ser estimado usando-se o modelo de ilha-continente para a migração, onde o transgene migraria do continente, a partir de uma variedade transgênica, para uma outra espécie da ilha. Nesse caso, a mudança na freqüência gênica (∆q) é: onde q e Q são as freqüências do alelo A no receptor e nos indivíduos imigrantes, respectivamente; m é a proporção de imigrante a cada geração; s1 e s2 são as vantagens seletivas dos genótipos AA e Aa, comparado com aa. Seleção e Mutação O fluxo gênico de uma variedade transgênica para um parente silvestre pode ser descrito como um evento de mutação recorrente em uma população. Novamente, as mesmas considerações devem ser assumidas. Nesse caso, o fluxo do transgene depende de três fatores: taxa de mutação, isto é, taxa de escape gênico por cruzamento natural; tamanho efetivo da população; e vantagem seletiva conferida pelo transgene. Considere que A seja um transgene dominante com freqüência q, e a, seu alelo correspondente, não existente no receptor, com as seguintes vantagens seletivas: WAA=WAa=1 e Waa=1-s Adicionalmente, considere n a taxa de mutação de A para a, isto é, a taxa com a qual o transgene A entra na população receptora. Nesse caso, podem-se também considerar as mutações reversas como nulas ou inexpressivas. Em uma população finita de tamanho N, a deriva genética é uma das forças evolutivas e Wright (1969) fornece as fórmulas para a taxa de mudança e de distribuição de q; a freqüência do transgene A é: A probabilidade de fixação de um gene com diferentes valores de vantagem seletiva e freqüência inicial é ilustrada na Figura 2. Figura 2. Probabilidade de fixação do transgene para diferentes valores de vantagem seletiva (S) e freqüência inicial do alelo (q). Modelos Derivados da Teoria do Melhoramento A forma mais provável de um escape gênico, eventualmente, ocorrer a partir de uma variedade transgênica é por meio do cruzamento interespecífico com seus parentes silvestres sexualmente compatíveis. A constituição genética do híbrido formado dependerá do modo de cruzamento. No caso de espécies muito aparentadas, os híbridos formados apresentam pareamento meiótico normal e há permuta genética entre cromossomos homólogos. O cruzamento entre entidades filogeneticamente mais distantes depende de eventos mais complexos como a duplicação cromossômica e a formação de anfidiplóides (Khush e Brar, 1992), o que não só reduz a taxa de formação do híbrido, como também a de retrocruzamento do híbrido com seus genitores. A poliploidização também afeta a dinâmica das mudanças genéticas (Hekmsen, 1992). Dessa forma, o escape gênico por meio da introgressão é aqui analisado como o caso de híbridos entre entidades filogeneticamente próximas apenas. As culturas são geralmente consideradas possuir pequena força competitiva ou seletiva, quando em ambiente silvestre. A domesticação e o melhoramento das espécies tem sido direcionados para outras características que não adaptativas. Muitas das características que conferem vantagem competitiva às espécies são indesejáveis para os modelos da agricultura moderna como: a maturação desuniforme, dormência de sementes, deiscência de vagens, crescimento indeterminado, sementes pequenas, etc. Muitas dessas características, relevantes para uma forte vantagem competitiva, são controladas por genes maiores, de forma qualitativa. Se for confirmado que o híbrido entre uma espécie cultivada e seu parente silvestre apresenta geralmente baixa capacidade de adaptação ao ambiente silvestre quando comparado com o tipo silvestre, então o genótipo que oferece maior risco de colonização é aquele que possui a forma selvagem, e o transgene, e sua capacidade de adaptação, pode se estimado por onde WH e WT são a adaptabilidade do híbrido e a adaptabilidade do híbrido com a presença do transgene, respectivamente representa a adaptabilidade geral do híbrido sem o transgene, expressa como um produto, em que WHi é a adaptabilidade do híbrido nos seus n locos. Adicionalmente, considere WW a adaptabilidade geral do parente silvestre e WWi os valores da adaptabilidade dos seus n locos de interesse, de forma que seguindo o argumento anterior, dessa forma, o caso que deve ser considerado é: into é, quando a vantagem adaptativa WT conferida por um alelo do transgene mais do que compensa para a desvantagem adaptativa geral do híbrido, comparado com seu parente silvestre. Esse seria o caso quando o transgene confere elevada resistência a uma praga presente no hábitat. Existe a possibilidade de que o escape do transgene, embora não compense a baixa adaptabilidade geral do híbrido, permaneça na população silvestre devido à deriva genética ou devido ao contínuo escape em gerações sucessivas. Se a adaptabilidade líquida do híbrido inicial é maior que a adaptabilidade média do parente silvestre, as condições seriam favoráveis para colonização do habitat. Genes que codificam para tolerância a herbicida somente conferem vantagem adaptativa se os seus portadores são cultivados sob pressão de seleção do herbicida. De forma semelhante, genes que codificam para resistência a doenças ou pragas conferirão vantagem seletiva aos indivíduos somente se estes forem cultivados em habitat com forte pressão pelos patógenos ou pragas. O conhecimento da dispersão gênica decorrente do movimento de pólen entre indivíduos ou populações é de especial interesse para agrônomos, geneticistas e ambientalistas . A contaminação de campos de produção de sementes por pólen de outras variedades ou outras espécies sexualmente compatíveis desencadeou uma série de estudos com o objetivo de estabelecer distâncias requeridas para a manutenção da pureza genética. Os pesquisadores têm também desenvolvido outros mecanismos para assegurar o isolamento genético: barreiras vegetais, eliminação de faixas de bordadura, controle de polinizadores, assincronia de época de florescimento, entre outras. Métodos de Análises A maioria dos métodos para mo- nitorar o escape gênico descritos na literatura não definem níveis mínimos que podem ser detectados com cada procedimento. Na maioria dos estudos, os indivíduos amostrados constituem apenas um pequeno número dentro da unidade experimental, o que pode justificar as pequenas distâncias sugeridas para o escape de transgênicos (Scheffler et al. 1993). Ainda, a maioria dos trabalhos nessa área apresentam os resultados em forma de histogramas ao invés de apresentarem uma distribuição espacial do escape gênico. Freqüentemente, os dados da freqüência do marcador são apresentados como uma percentagem dos genes amostrados, o que não é apropriado, uma vez que a distribuição é dependente da escala (Kareiva et al. 1994). Métodos de Estimação Os métodos indiretos envolvem o uso de técnicas desenvolvidas em genética de populações (Raybould et al. 1997). Esses métodos são difíceis de ser aplicados, uma vez que eles requerem populações naturais. Entretanto, nos casos onde o risco envolve a dispersão do transgene para parentes silvestres da espécie cultivada, esses métodos apresentam a vantagem de combinarem os efeitos da taxa de dispersão de ambos. Os métodos diretos envolvem a estimativa dos parâmetros de campo. Tradicionalmente, consideram-se a dispersão como tendo uma distribuição normal bidimensional (Wright 1943; Haldane, 1948). Entretanto, a dispersão de pólen a partir de plantas é mais complexa e segue uma função exponencial da forma (Bateman, 1947; Kareiva et al. 1994). Ao invés de usar essa distribuição, Lavigne et al. (1996) e Tufto et al. (1997) sugerem o uso de métodos baseados em movimentos Brownianos em três dimensões. Obviamente, a variação da velocidade do vento e da sua direção, durante o experimento é melhor descrita por funções exponenciais que por funções bidimensionais. Para as espécies de polinização entomófila, o tipo e a densidade da vegetação vizinha, o estádio de floBiotecnologia Ciência & Desenvolvimento 57 rescimento de outras espécies, além das condições meteorológicas, devem ter importante papel na dispersão do pólen. O desenho experimental no caso de espécies de polinização entomófila pode ter grande efeito sobre os resultados. Embora as variedades transgênicas sejam cultivadas nos mesmos ambientes em que as variedades não transgênicas, são plantadas sem problemas, os riscos de impacto ambiental decorrentes do uso dos OGMs têm sido estimados para cada tipo de variedade liberada. Doebley et al. 1990 analisou a descendência do cruzamento entre milho e seu ancestral teosinto para determinar o número de genes responsáveis pela natureza invasora desse ancestral silvestre do milho. Os resultados sugerem que apenas um pequeno número de genes associados às características morfológicas são suficientes para causar profundas modificações fenotípicas. O teosinto, por exemplo, poderia ser transformado em um biótipo semelhante ao milho cultivado, pela introdução de cinco regiões genômicas do milho. Entretanto, adicionalmente a esses genes que produzem significativa alteração na morfologia da planta, muitos outros genes teriam que ser introduzidos para induzir a natureza invasora no milho cultivado. A Figura 3 ilustra algumas características morfológicas do milho, do teosinto e do híbrido entre eles. Ambas as espécies possuem 2n=20 entretanto a espiga do milho possui 8 fileiras de grãos e é facilmente debulhável. A espiga do teosinto possui 2 fileiras de grãos e é protegida por um involucro rígido (não mostrado na Figura 3). A Figura 4 ilustra outros aspectos morfológicos contrastantes entre essas duas espécies. Figura 3. Comparação entre espigas de milho, teosinto e do híbrido entre eles 58 Biotecnologia Ciência & Desenvolvimento Figura 4. Características morfológicas contrastantes entre o milho e seu ancestral teosinto Literatura Consultada Bateman, A.J. 1947. Contamination in seed crops. III. Relation with isolation distance. Heredity 1:303-336. Baulcombe, D.C e English, J.F. 1996. Ectopic pairing of homologous DNA and post transcriptional gene silencing in transgenic plants. Current Opinion in Biotechnology 7: 173-180. Beck, U. 1996. Risk society and the provident state. In: Lash, S. (ed.). Risk, environment and modernity. Londres: Sage Press. pp. 27-43. Brandle, J.E.; McHugh; S.G.; James L.; Labbe, H.; e Miki, B.L. 1995. Instability of transgene expression in field grown tobacco carrying the crs1-1 gene for sulfonylurea herbicide resitance. Bio/Technology 13:994-998. Broer, I. 1996. Stress inactivation of foreign genes in transgenic plants. Field CropsResearch 45: 19-25. Brubaker, C.L; Brown, A.H.D; Stewart, J.M; Kilby, M.J; Grace, J.P. 1999. Production of fertile hybrid germplasm with diploid Australian Gossypium species for cotton improvement. Euphytica 108: 199-213. Burrows, P. 1999. Deliberate release of genetically modified organisms: the UK regulatory framework. In: Gene flow and agriculture: relevance for transgenic crops. Proceedings of a symposium held at Keele, UK 13-21pp. BCPC Symposium Proceedings No.72. British Crop Protection Council; Farnham; UK. Carvalho, N.F.; Frendo, P. e Montagu, M.; Cornelissen, M.1995. Post-transcriptional cosuppression of -1, 3-glucanase genes does not affect accumulation of transgene nuclear mRNA. The Plant Cell 7: 347-358. Chevre, A.M.; Eber, F.; Baranger, A.; Hureau, G.; Barret, P.; Picault, H.; e Renard, M. 1998. Characterisation of backcross generations obtained under field conditions from oilseed rape wild radish F1 interspecific hybrids: an assessment of transgene dispersal. Theoretical and Applied Genetics 97: 90-98. Daniell H.; Datta, R.; Varma, S.; Gray, S. e Lee S. B. 1998. Containment of herbicide resistance through the gentic engineering of the chloroplast genome. Nature Biotechnology 16: 345-348. Depicker A. e Montagu, M. 1997. Post-transcriptional gene silencing in plants. Current Opinion in Cell Biology 9: 373-382. Desplanque, B.; Boudry, P.; Broomberg, K.; Saumitou; Laprade, P.; Cuguen, J.; Dijk, H. Dijk, H. 1999. Genetic diversity and gene flow between wild, cultivated and weedy forms of Beta vulgaris L. (Chenopodiaceae), assessed by RFLP and microsatellite markers. Theoretical and Applied Genetics 98: 1194-1201. Dietz, A. 1993. Risk assessment of genetically modified plants introduced into the environment. In: Wohrmann, K. e Tomiuk, J. (eds). Transgenic Organisms: Risk Assessment of Deliberate Releases. Basel: Birkhauser Verlag pp. 209277. Dix, P.J. e Kavanagh, T.A. 1995. Transforming the plastome: genetic markers and DNA delivery systems. Euphytica 85: 29-34. Doebley, J.; Stec, A. ; Wendel, J. e Edwards, M. 1990. Genetic and morphological analysis of a maize-teosinto F2 population: implications for the origin of maize. Proc. Natl. Acad. Sci. USA 87: 9888-9892. Elmayan, T. e Vaucheret, H. 1996. Expression of single copies of a strongly expressed 35S transgene can be silenced post-transcriptionally. The Plant Journal 9: 787-797. Gabriel, W. 1993. Technologically modified genes in natural populations: some sckeptical remarks on risk assessment from the view of population genetics. In: Wohrmann, K. e Tomiuk, J. (eds): Transgenic Organisms: Risk Assessment of Deliberate Release. Basel: Birkhause Verlag. pp. 109116. Gatz, C. e Lenk, I. 1998. Promoters that respond to chemical inducers. Trends in Plant Science 3: 352-358. Gliddon, C.; Boudry, P.; Walker, D.S. 1990. Gene flow - a review of experimental evidence. In: Gray, A.J.; Amijes, F. e Gliddon, C.J. (eds.). Environmental impact of genetically modified crops. Genstically Modified Organisms Research Report 10-pp 67-81. Londres:DETR. Gliddon, C.J. 1999. Gene flow and risk assessment. In: Gene flow and agriculture: relevance for transgenic crops. Proceedings of a symposium held at Keele, UK 49-56pp. BCPC Symposium Proceedings No.72; British Crop Protection Council. Greef, W. 1999. A long term perspective on Ag-biotech. In: Gene flow and agriculture: relevance for transgenic crops. Proceedings of a symposium held at Keele, 33-37pp. BCPC Symposium Proceedings No.72. British Crop Protection Council. Haldane, J.B.S. 1948. The theory of a cline Journal of Genetics 48: 277284. Hersnsen, J. G. T. 1992. Introductory considerations on distant hybridization. In: Kalloo, G. e Chowdhury, J. B. (eds.): Distant Hybridization of Crop Plants. Berlin: Springer Verlag pp. 1-14. Kaff, N.S.; Covey S.N.; Kreike M.M.; Pinder R; e Dale P.J. 1998. Transcriptional and postranscriptional plant gene silencing in response to a pathogen. Science 279: 2113-2115. Kareiva, P.; Morris, W. e Jacobi, C. M. 1994. Studying and managing the risk of cross-fertilization between transgenic crops and wild relatives. Molecular Ecology 3: 15-21. Khush, G. S. e Brar, D. S. 1992. Overcoming the barrier of hybridization. In: Kalloo, G. e Chowdhury, J. B. (eds.): Distant Hybridization of Crop Plants. Berlin: Springer Verlarf pp. 4761. Kumpatla, S. P.; Chandrasekharan, M.B.; Iver, L.M.; Li, G e Hall, T.C. 1998. Genome intruder scanning modulation systems and transgene silencing. Trends Plant Science 3:97-104. Lavigne, C.; Godelle, B.; Reboud, X. e Gonyon, P.H. 1996. A method to determine the mean pollen dispersal of individual plants growing within a large pollen soure. Theoretical and Applied Genetics 93: 1319-1326. Levin, D.A. e Kerster, H. 1974. Gene flow in seed plants. Evolutionary Biology 7: 139-220. Loop, C.B.; Buttel, F.H.; Hoban, T.J.; Gould, F.; Beachy, R.N.; Bendahmane, M.; Nickson, T.E.; McKee, M.J.; Ho, M.W.; Matten, S.R.; Robinson, M; Hardy, R.W.F. 1998. Agricultural biotechnology and environmental quality: gene escape and pest resistance. In: Segelken J.B. (ed.); NABC-Report. No. 10, 165 pp. National Agricultural Biotechnology Council Press. Mackenzie, D.R. e Henry, S.C. 1990. Towards a consensus. In: The Biosafety Results of Field Tests of Genetically Modified Plants and Microorganisms. Proceding of the Kiawah Research Institute Bethesda. 159p. Matzke, M.A.; Park, Y.D.; Papp, I.; Vaucheret, H. e Matzke, A.J.M. 1996. Features of promoter homology-dependent gene silencing in transgenic plants. In: Grierson, D.; Lycett, G.W. e Tucker, G.A. (eds.). Mechanisms and applications of gene silencing Nottingham: Nottingham University Press, pp.33-42. Matzke, M.A.; Primig, M.; Trnovsky, J. e Matzke, A.J.M. 1989. Reversible methylation and inactivation of marker genes in sequentially transformed tobacco plants. EMBO Journal 8: 643649. Meyer, P. 1995. Understanding and controlling transgene expression. Tibtech 13: 332-337. Meyer, P.; Linn, F.; Heidmann, I.; Meyer, H.; Niedenhof, I. e Saedler, H. 1992. Endogenous and environmental factors influence 35S promoter methylation of a maize A1 gene construc in transgenic Petunia and is colour phenotype. Molecular & General Genetics 231: 345-352. Neumann, K.; Droge-Laser, W.; Kohne, S. e Broer, I. 1997. Heat treatment results in loss of transgene encoded activities in several tobacco lines. Plant Physiology 115: 939-947. Pohl; Orf, M; Brand, U.; Driessen, S.; Hesse, P.R.; Lehnen, M.; Morak, C.; Mucher, T.; Saeglitz, C.; Soosten; C, von.; Bartsch, D.; von, Soosten, C. 1999. Overwintering of genetically modified sugar beet, Beta vulgaris L. subsp. vulgaris, as a source for dispersal of transgenic pollen. Euphytica 108: 181-186. Regal, P.J. 1994. Scientific principles for ecologically based risk assessment of transgenic organisms. Mol. Eco. 3:5-13. Rieger, M.A.; Preston, C.; Powles, S.B. 1999. Risks of gene flow from transgenic herbicide-resistant canola (Brassica napus) to weedy relatives in southern Australian cropping systems. Australian Journal of Agricultural Research 50: 115-128. Sage, G.C.M. 1999. The role of DNA technologies in crop breeding. In: Gene flow and agriculture: relevance for transgenic crops. Proceedings of a symposium held at Keele, 23-31pp. BCPC Symposium Proceedings No.72. British Crop Protection Council. Scheffler, J.A.; Parkinson, R. e Dale, P.J. 1993. Frequency and distance of pollen dispersal from transgenic oilseed rape (Brassica napus). Transgenic Research 2: 356-364. Schuster, H. J. 1991. Interview on safety aspects of GMOs. Ec Magazine 11:13. Sikdar, S. R.; Serino, G.; Chaudhuri, S. e Maliga, P. 1998. Plastid transformation in Arabidopis thaliana. Plant Cell Reports 18: 20-24. Tufto, J.; Engen, S. e Hindar, K. 1997. Stochastic dispersal process in plant populartion. Theoretical and Applied Genetics 28: 114-138. Vaucheret, H.; Elmayan, T.; Thierry, D.; Geest, A.; Hall, T.; Conner, A.J.; Mlynarova, L. e Nap, J.P. 1998. Flank matrix attachemnt regions (MARs) from chicken, bean, yeast or tobacco do not prevent homology-dependent trans-silencing in trangenic tobacco plants. Molecular & General Genetics 259: 388-392. Walter, C.; Broer, I.; Hillemann, D. e Puhler, A. 1992. High frequency, heat treatment induced inactivation of the phosphinothricin resistance gene in transgenic single cell suspension cultures of Medicago Sativa. Molecular and General Genetics 235: 189-196. Wohrmann, K.; Tomiuk, J.; Pollex, C. e Grimm, A. 1993. Evolutionsbiologische Risiken bei Freisetzungen genetechnish veranderter Organismen in die Unwelt. Berlin: Bundesminister fur Unwelt. 183p. Wright, S. 1943. Isolation by distance. Genetics 28: 114-138. Wright, S. 1969. Evolution and the Genetics of Populations-Vol.2: The Theory of Gene Frequencies. Chicago: The University of Chicago Press. 279p. Biotecnologia Ciência & Desenvolvimento 59 FUNDAÇÃO GIACOMETTI (Repete Fotolito) Saiu na página 60 da última edição (Ed. 17) 60 Biotecnologia Ciência & Desenvolvimento EMBRAPA (Repete Fotolito) Saiu na 4ª Capa da última edição (Ed. 17) Biotecnologia Ciência & Desenvolvimento 61 MONSANTO (Repete Fotolito) Saiu na 3ª Capa da última edição (Ed. 17)
Baixar






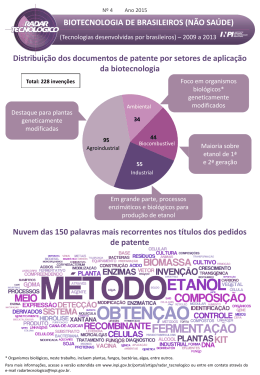
![[br - 2] estado/opinião/páginas 20/12/06](http://s1.livrozilla.com/store/data/000407654_1-7f734dbe0ff92299e0d15220e3bb5330-260x520.png)
