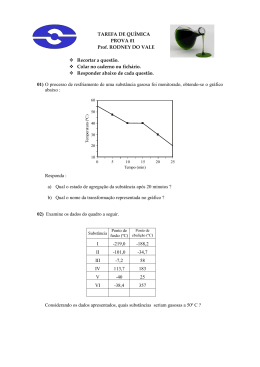
Prof. Alfredo Neto Mistura → forma por mais de um componente. Substância Simples e Composta. Substância Simples → possuem apenas um elemento químico. As misturas podem ser classificadas como homogêneas e heterogêneas. Homogênea → apresenta uma única fase. Ex.: O3, S8, O2, etc. Substância Compostos → possuem mais de um elemento químico. Ex.: Gasolina + Querosene Água + Acetona Ex.: CaCO3, H2SO4, CO2, etc. Fenômenos Químicos e Físicos. Fenômeno Químico → altera a natureza da matéria. Ex.: Combustão da gasolina, digestão dos alimentos, formação de ferrugem, ets. Heterogênea → apresenta mais de uma fase. Ex.: Gasolina + Água Fenômeno Físico → não altera a natureza da matéria. Ex.: Fundir uma barra de ouro, precipitação da chuva, dissolver sal em água, etc. OBS: Mudanças de Estado Físico. As misturas não apresentam PF e PE Gráficos Sublimação T (ºC) Fusão Vaporização Sólido Líquido Solidificação Gasoso Liquefação t (min) Sublimação T (ºC) Substância Pura e Mistura. PE Substância Pura → formada por um único componente. As substâncias puras, durante as mudanças de estado físico, não apresentam variação de emperatura, isto é, apresentam ponto de fusão (PF) e ponto de ebulição (PE). t (min) Gráfico T (ºC) T (ºC) PE PF PF t (min) t (min) Prof. Alfredo Neto Exercício 1. A glicose, importante açúcar na alimentação de muitos seres vivos, possui fórmula igual a C6H12O6. Sobre a glicose é possível afirmar que: a) é uma substância simples. b) possui 24 elementos químicos c) possui três átomos d) é uma mistura de três elementos químicos e) é uma substância composta, formada por três elementos químicos. 2. Ao observarmos uma mistura de sal e açúcar com uma simples lente de aumento, percebemos que os cristais do sal são diferentes dos cristais do açúcar. Nessas condições, é possível dizer que o sistema é constituído por: a) uma fase e um componente b) duas fases e dois componentes c) uma fase e dois componentes d) duas fases e um componente e) milhares de fases e dois componentes. 7. O número de substâncias simples com atomicidade par entre as substâncias O3, H2O2, P4, I2, C2H4, CO2 e He é: a) 5 b) 4 c) 3 d) 2 e) 1 8. Observe atentamente os processos cotidianos abaixo: I. secagem de roupa no varal II. fabricação caseira de pão III. filtração da água pela vela do filtro IV. avermelhamento do bombril V. formação da chama do fogão, a partir do gás de cozinha. Constituem fenômenos químicos: a) II e V apenas d) I, II e III apenas b) II, IV e V apenas e) I, II, III, IV e V c) I, III e IV apenas 9. temperatura (ºC) 60 3. Qual das alternativas a seguir contém apenas substâncias compostas? d) H2O, Cl2, I2 a) N2, P4, S8 b) N2, O3, H2O e) CO2, H2O, C6H12O6 c) CO, He, NH3 4. O tratamento da água consiste basicamente na adição de sulfato de alumínio, cloro, flúor e outros produtos químicos. A água, após o tratamento, classificase como: a) mistura homogênea d) mistura azeotrópica b) mistura heterogênea e) substância pura c) substância simples 5. Sejam os fenômenos: I. Formação da neve. II. Fusão do chumbo. III. Queima do álcool. IV. Atração de uma agulha por um imã. V. Obtenção do iogurte a partir do leite. 40 20 1 2 3 4 5 6 7 8 tempo (min) Analisando o gráfico acima, referente ao aquecimento de uma substância sólida, podemos afirmar que: a) quando t = 2 minutos, tem-se um sistema monofásico. b) quando t = 4 minutos, coexixtem substâncias sólida e líquida c) em t = 1 minuto inicia-se a liquefação da substância d) a substância tem ponto de fusão igual a 40 ºC e) no intervalo de 5 a 8 minutos, a substância encontra-se totalmente na forma de vapor 10. Entre as transformações citadas a seguir, aquela que não representa um fenômeno químico é: a) o cozimento de um ovo b) o azedamento do leite c) a queima do carvão d) a formação de orvalho e) o amadurecimento de uma fruta Quais deles são fenômenos químicos? a) todos d) III e V b) nenhum e) III, IV e V c) I, II e V 6. Sabendo que o ouro 18 quilates é formado por 75% de ouro e 25% de prata e cobre, em massa, identifique o gráfico que melhor representa sua fusão. Justifique sua escolha. 11. Fenômeno químico é aquele que altera a natureza da matéria, isto é, aquele no qual ocorre uma reação química. Baseado nessa informação, analise as proposições abaixo e indique (F) para fenômeno físico e (Q) para fenômeno químico. Gráfico 1 temperatura ( ) a combustão de álcool ou gasolina nos motores ( ) a queima do gás de cozinha ( ) a formação de gelo ( ) a formação de ferrugem sobre uma peça de ferro ( ) a digestão dos alimentos. ( ) o arco-íris. ( ) acender uma lâmpada ( ) obtenção de sal pela evaporação da água do mar. Gráfico 2 temperatura tempo tempo Prof. Alfredo Neto 12. Um sistema formado por água, açúcar dissolvido, álcool, pedaços de ferro e areia apresenta: a) 1 fase d) 5 fases b) 4 fases e) 3 fases c) 2 fases 17. Com relações aos sistemas abaixo, é incorreto afirmar que: a) Um sistema constituído por três pedaços de ouro puro é monofásico. b) Um sistema contendo apenas água e uma ínfima quantidade de açúcar forma uma mistura homogênea. c) Uma substancia pura sempre constituirá um sistema monofásico. d) A água limpa, como a água filtrada que bebemos, é uma sistema homogêneo. e) A água e o álcool etílico formam mistura homogêneas em quaisquer proporções. 13. No sistema representado pela figura abaixo, os números de fases e componentes são, respectivamente: 18. No sistema representado pela figura abaixo, os números de fases e componentes são, respectivamente: a) 3 e 2 a) 2 e 2 ( ( ( ( ( ( ) A queima de fogos de artifício. ) A sublimação da naftalina. ) A fermentação do leite. ) Picotar papel. ) A precipitação das chuvas. ) Dissolver açúcar no café. b) 3 e 3 c) 3 e 4 d) 2 e 2 e) 2 e 3 b) 2 e 3 c) 3 e 2 d) 3 e 3 e) 3 e 4 14. Em um balão existe um liquido transparente, inodoro e incolor. Com certeza, é possível afirma que se trata de: a) Uma substancia pura. b) Uma solução. c) Um sistema homogêneo. d) Uma mistura homogênea. e) Uma solução em que os sólidos e os líquidos presentes estão complemente dissolvidos. 19. Analise os fenômenos abaixo e marque aquele que não envolve uma transformação da natureza íntima da matéria. 15. Considere os sistemas materiais indicados abaixo: 20. Dada a tabela abaixo, em relação ao estado físico das substâncias, marque a alternativa correta. Sistema Componentes I água e óleo II areia e álcool III água e sal de cozinha dissolvido IV água e álcool V gás carbônico e oxigênio Assinale a alternativa que apresenta apenas sistemas homogêneos. a) somente I e III d) somente III, IV e V b) somente I, III e IV e) somente III e IV c) somente I e II 16. Com relação às substancias O2, H2, H2O, Pb, CO2, O3, CaO e S8, podemos afirmar que: a) Todas são substâncias simples. b) Somente O2, H2 e O3 são substâncias simples. c) Todas são substâncias compostas. d) Somente CO2, CaO e S8 são substâncias compostas. e) As substâncias O2, H2, Pb, O3 e S8 são simples. a) A queima de fogos de artifício. b) A fermentação do leite. c) A oxidação de um prego. d) O apodrecimento de uma fruta. e) A sublimação da naftalina. Substância I II III IV V Temperatura de Fusão (°C) - 218 - 63 41 801 1.535 a) I é sólido a 30 °C. b) II é líquido a 480 °C. c) III é sólido a 25 °C. Temperatura de Ebulição (°C) - 183 61 182 1.473 2.885 d) IV é líquido a 480 °C. e) V é gasoso a 2.4 00 °C. 21. A classificação da matéria é definida baseando-se em variações de certas propriedades específicas, por exemplo: Classificação substância pura mistura comum Mistura azeotrópica mistura eutética Exemplo A – água pura B – água do mar C – álcool de farmácia (96% de álcool e 4% de água) D – solda (36% de Chumbo e 63% de Estanho) Prof. Alfredo Neto Considerando as temperaturas de fusão e de ebulição, assinale a alternativa correta: a) B e C têm temperaturas constantes durante a ebulição. b) D e A têm temperaturas constantes durante a fusão. c) A, B e C têm temperaturas variáveis durante a ebulição. d) D, B e C têm temperaturas variáveis durante a fusão. e) B e C têm a mesma temperatura durante a ebulição, pois são misturas. 22. Considere a substância cuja fórmula é H3PO4. Essa substância é composta por: a) 3 átomos. b) 8 elementos.. c) 8 átomos. d) Um único elemento, variando apenas seus isótopos. e) Um único átomo, variando apenas a froma de representá-lo. 23. Considere as seguintes tarefas realizadas no diaa-dia de uma cozinha e indique aquelas que envolvem transformações físicas. I. Aquecer uma panela de alumínio. II. Acender um fósforo. III. Ferver água. IV. Queimar açúcar para fazer caramelo. V. Fazer gelo. a) I, III e V b) II e IV c) I, III e IV d) III e V e) II e III 24. Considere a substância cuja fórmula é H2SO4. Essa substância é composta por: a) 7 elementos.. b) 3 átomos. c) 7 átomos. d) Um único elemento, variando apenas seus isótopos. e) Um único átomo, variando apenas a forma de representá-lo. 25. Considere um sistema constituído apenas por água e gelo. Pode-se afirmar corretamente que esse sistema: a) apresenta 2 componentes. b) apresenta 3 fases. c) apresenta 1 componente e 1 fase. d) é constituído por uma substância. e) é homogêneo. 26. Nos diferentes materiais abaixo, expostos ao ar, verifica-se que: I. sobre uma lâmina metálica forma-se uma película escura; II. bolinhas de naftalina diminuem de tamanho; III. o leite azeda; IV. um espelho fica embaçado se respirarmos encostados a ele; V. uma banana apodrece. Podemos dizer que são observados fenômenos: a) físicos somente. b) físicos em I, II e V e químicos em III e IV. c) físicos em II e IV e químicos em I, III e V. d) físicos em III e V e químicos em I, II e IV. e) químicos somente. 27. Considere os sistemas: I. água líquida e gelo II. gás oxigênio (O2) III. álcool e areia IV. gás carbônico e gás oxigênio Relativo a esses sistemas pode-se afirmar que: a) III é uma substância pura b) II é uma substância composta c) III é uma mistura monofásica d) IV é uma mistura bifásica e) se misturarmos II com IV o sistema obtido é homogêneo. 28. Considerando a substância cuja fórmula é O3. Pode-se afirmar que: a) apresenta 3 elementos b) trata-se de uma substância composta, pois é formada por mais de um átomo. c) é um isótopo do Oxigênio d) é formada por um único elemento e) possui atomicidade par
Baixar