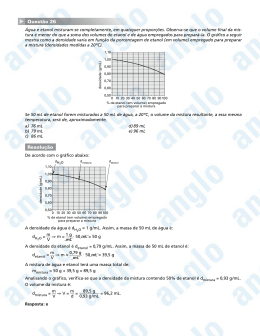
Química QUESTÃO 03 Combustível é todo produto utilizado com a finalidade de produzir energia a partir de sua queima ou combustão. O etanol (C2H5OH) é um combustível que, quando injetado nas câmaras de combustão dos veículos, reage com oxigênio e libera energia. A quantidade de calor liberada pela combustão completa de 1 mol de etanol é 300kcal. a) Escreva a equação balanceada da reação de combustão completa do etanol em uma câmara de combustão de um automóvel (reação do etanol com o O2). b) Calcule a energia produzida, na forma de calor, pela combustão de 1L de etanol, sabe-se que a densidade do etanol é de 0,828g/mL c) Calcule o volume de CO2, em litros, produzido pela combustão completa de 46Kg de etanol, massa aproximada de um tanque cheio com o combustível nas condições de temperatura igual a 27ºC e pressão de 1atm. Resolução: a) CaCO3 = CaO + CO2 b) 1L = 1000mL → usando a fórmula da densidade para o cálculo da massa de etanol, teremos: d = m/V → 0,828g/mL = m/1000mL → m = 828g cálculo da energia liberada: 1mol de etanol = 46g de etanol → 300Kcal 828g de etanol → x X = 5400Kcal c) P.V. = n.R.T → V = n.R.T/P → V = m1.R.T/M1.P → V = 46000.0,082.300/46.1 V = 24600L de CO2
Baixar