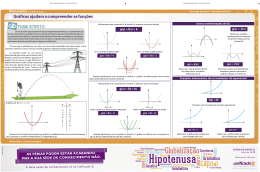
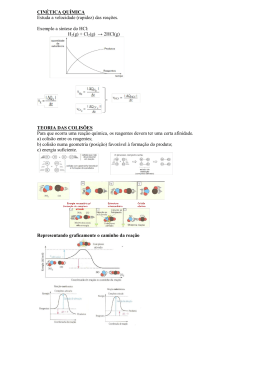
EQUILÍBRIO QUÍMICO e DESLOCAMENTO DE EQUILÍBRIO Equilíbrio Químico Equilíbrio químico é um estado alcançado por qualquer reação reversível a partir do qual a velocidade da reação direta se torna igual à da reação inversa e, conseqüentemente, as concentrações de todas as substâncias participantes passam a ficar constantes. Concentração e Equilíbrio Velocidade e Equilíbrio 38 Constante de Equilíbrio considerando as concentrações aA(g) + bB(g) cC(g) + dD(g) Kc = [C ]c.[ D]d [A ]a.[ B]b • • Kc não varia com a concentração nem com a pressão, mas varia com a temperatura. Quanto maior o Kc, maiores são as concentrações dos produtos em relação às dos reagentes, no equilíbrio. Quanto menor o Kc, menores são as concentrações dos produtos em relação às dos reagentes, no equilíbrio. • Constante de Equilíbrio considerando as pressões parciais aA(g) + bB(g) cC(g) + dD(g) Kp= (PC)c.(PD)d (PA)a.(PB)b Relação entre Kp e Kc Kp = Kc (RT)∆n ∆n = (c + d) - (a + b) Obs.: Em equilíbrios heterogêneos os participantes sólidos não entram na expressão do Kc nem do Kp . DESLOCAMENTO DE EQUILÍBRIO Princípio de Le Chatelier ou princípio da fuga Quando se exerce uma ação sobre um sistema em equilíbrio, ele desloca-se no sentido que produz uma minimização da ação exercida. Henri Louis Le Chatelier 39 • Equilíbrio e temperatura Um aumento da temperatura desloca o equilíbrio para a reação endotérmica. Uma diminuição da temperatura desloca o equilíbrio para a reação exotérmica (Regra de van't Hoff). • Equilíbrio e pressão Um aumento da pressão desloca o equilíbrio para a reação que ocorre com contração de volume. Uma diminuição da pressão desloca o equilíbrio para a reação que ocorre com expansão de volume. • Equilíbrio e concentração Um aumento da concentração de um participante desloca o equilíbrio no sentido da reação em que este participante é consumido. Uma diminuição da concentração de um participante desloca o equilíbrio no sentido da reação em que este participante é formado . • Equilíbrio e catalisador O catalisador não desloca equilíbrio pois atua tanto na reação direta como na reação inversa, apenas diminui o tempo necessário para atingi-lo. 40
Baixar