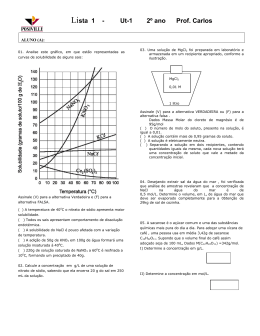
Professor: Carlos 2º ano Data: Nome: ______________________________________________________ Série: _____________ 01. Analise este gráfico, em que estão representadas as curvas de solubilidade de alguns sais: 03. Uma solução de MgCl2 foi preparada em laboratório e armazenada em um recipiente apropriado, conforme a ilustração. MgCl2 0,01 M 1 litro Assinale (V) para a alternativa VERDADEIRA ou (F) para a alternativa falsa. a) ( b) ( c) ( d) ( e) ( ) Dados Massa Molar do cloreto de magnésio é de 95g/mol. ) O número de mols do soluto, presente na solução, é igual a 0,01. ) A solução apresenta 0,01 mol de Mg 2+ e 0,02 mol de Cl-. ) A solução é eletricamente neutra. ) Separando a solução em dois recipientes, contendo quantidades iguais da mesma, cada nova solução terá uma concentração de soluto que vale a metade da concentração inicial. Assinale (V) para a alternativa Verdadeira e (F) para a alternativa FALSA. a) ( b) ( c) ( d) ( e) ( ) A temperatura de 400C o nitrato de sódio apresenta maior solubilidade. ) Todos os sais apresentam comportamento de dissolução endotérmica. ) A solubilidade do NaCl é pouco afetada com a variação de temperatura. ) A adição de 50g de KNO3 em 100g de água formará uma solução insaturada à 400C. ) 220g de solução saturada de NaNO3 a 600C é resfriada a 100C, formando um preciptado de 40g. 02. Calcule a concentração em g/L de uma solução de nitrato de sódio, sabendo que ela encerra 400 mg do sal em 250 mL da solução. 04. Desejando extrair sal da água do mar, foi verificada que análise de amostras revelaram que a concentração de NaCl na água do mar é de 0,5 mol/L. Determine o volume, em L, de água do mar que deve ser evaporado completamente para a 0btenção de 29kg de sal de cozinha. 05. A sacarose é o açúcar comum e uma das substâncias químicas mais pura do dia a dia. Para adoçar uma xícara de café, uma pessoa usa em média 3,42g de sacarose C12H22O11. Supondo que o volume final do café assim adoçado seja de 100 mL. Dados M(C 12H22O11) =342g/mol. a) Determine a concentração em g/L. b) Determine a concentração em mol/L. 06. No tratamento de madeira usada para produzir pequenos embarcações, dentre várias substâncias, usa-se uma solução de ácido bórico H 3BO3 a 25% de densidade 1,25g/mL. Determine a concentração em mol/L desta solução. Dados: H=1u, B= 11u e 0 =16u a) Determine a concentração da Solução de ácido bórico em g/L. b) Determine a concentração da solução de ácido bórico em quantidade de matéria por volume (mol/L). 07. Entre os diversos hormônios que promovem o equilíbrio das diversas funções no organismo humano, está a adrenalina, que regula o funcionamento do coração, dos brônquios e dos vasos sanguíneos. Secretada pelas glândulas supra-renais, a adrenalina apresenta a estrutura molecular representada a seguir: Dados: massas atômicas C=12u, N=14u, O=16u e H=1u e Fórmula molecular C9H 13NO3. Determine a concentração de adrenalina em g/L, sabendo que a densidade da solução é de 1g/mL e que apresenta 2% de soluto. 08. Nos postos de gasolina é comum o frentista oferecer produtos associados à manutenção interna e externa dos veículos. Um dos produtos oferecidos para evitar o aquecimento excessivo dos radiadores de automóveis apresenta como princípio ativo o eltilenoglicol, que misturado a água provoca alterações nas temperaturas de ebulição e fusão. Sabendo que em um frasco de 500 mL da solução de etilenoglicol apresenta 5 mols de etilenglicol C2H6O2. Determine a concentração em g/L desta solução. Dados: C=12, H=1 e O=16. 09. “Cólera, doença que pode provocar a morte, caso a pessoa infectada não seja tratada a tempo. Este Vibrio cholerae, ao se instalar no intestino, provoca diarréia e vômitos, que normalmente causam desidratação. Uma das formas de contrair a doença é através de ingestão de água e alimentos contaminados”. Dica de saúde, para evitar a cólera, através da ingestão de alimentos contaminados com o víbrio cholerae, recomenda-se deixar legumes e verduras em molho numa solução de um litro, formada por 10 mL de hipoclorito de sódio (NaClO) de concentração inicial de 37,25g/L e diluindo com água até o volume final de 1 litro. Dados: massas atômicas Na=23u; Cl=35,5u; O=16u Determine a concentração em mol/L da solução de hipoclorito de sódio (NaClO) inicial e a concentração em g/L após a adição de água. 10. No Brasil, o transporte de cargas é feito quase que totalmente em rodovias por caminhões movidos a diesel. Para diminuir os poluentes atmosféricos, foi implantado desde 2009 o uso do Diesel 50S (densidade média 850 g/L), que tem o teor máximo de 50 ppm (partes por milhão) de enxofre. a) Determine a massa total do Diesel 50S em um tanque de 50L. b) Determine a quantidade máxima de enxofre, em gramas, contida no tanque cheio de um caminhão com capacidade de 100 L, abastecido somente com Diesel 50S, é: Faça esta lista com muita atenção Professor Carlos
Baixar