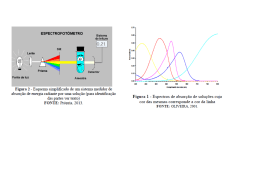
UNIVERSIDADE FEDERAL DE PERNAMBUCO CENTRO DE BIOCIÊNCIAS DEPARTAMENTO DE BOTÂNICA ECOFISIOLOGIA DE PLANTAS DA CAATINGA Introdução O Espectrofotômetro e os medidores de sais • Exames – Colesterol, triglicerídeos, glicose, ácido úrico, etc. AULA 1 Introdução a Espectroscopia, Lei de Lambert Beer • Exames Marcelo Francisco Pompelli Tipos de Espectrofotômetro – Como eles são analisados? Tipos de Espectrofotômetro Tipos de Espectrofotômetro amostra tela de cristal líquido teclado para entrada de informações tela de cristal líquido ou PC? entrada para pen drive 3 1 Lâmpada de xenon, emissora de fonte de luz Detector de referência, funciona para calibração do aparelho e desconto do “zero” de referência Funcionamento dos Espectrofotômetros 1 – bacterioclorofila a 2 – clorofila a 3 – clorofila b 4 – ficoeritrbilina 5 – β-caroteno 2 Intensidade de luz incidente I0 Monocromador, funciona como um prisma, selecionando o comprimento de onda adequado Mocrocromador Detector ou tela lâmpada emissora de luz 4 5 Intensidade de luz transmida I Detector, mostrará um valor, dependendo da absorvância Vai depender do comprimento de onda escolhido Carrossel automático para até seis cubetas, seis leituras ao mesmo tempo Funcionamento dos Espectrofotômetros • Ao passar pela cubeta é comum que a luz seja transmitida com características distintas da luz emitida (ex. maior comprimento de onda, menor energia) Cubeta com a amostra a ser analisada Lei de Lambert-Beer Lei de Lambert-Beer • Absorção de luz pelas moléculas • A fração de luz incidente absorvida por uma solução num determinado comprimento de onda é relacionada com a espessura do caminho óptico e a concentração da amostra. – uma ampla faixa de biomoléculas absorvem luz num determinado comprimento de onda • – – Ex.: o triptofano absorve luz em 280 nm Coeficiente de extinção Molar (M-1 L-1 cm-1) próprio de cada substância a ser analisada a medição da luz absorvida por uma biomolécula através do espectrofotômetro é usada para detectar, identificar e quantificar moléculas num determinado material biológico Para tanto deve-se levar em consideração a Lei de Lambert-Beer A=εcL Absorbância ou absorvância Concentração(M) Caminho ótico (cm), profundidade da cubeta, geralmente 1 cm Lei de Lambert-Beer Lei de Lambert-Beer Coeficiente de extinção molar • Quanto maior a concentração (c) ou maior o caminho óptico (L) maior será a absorbância da amostra, por isso geralmente o L é padronizado em 1 cm • Como vimos a profundidade do caminho óptico interfere na absorbância da solução • O coeficiente de extinção molar varia • Exemplo: – com base na lei de Lambert-Beer, calcule a absorbância de uma solução com concentração 0,002 mol L-1 de uma substância com absortividade molar de 313 L mol-1 cm-1, determinada em uma célula com 2,00 cm de caminho óptico. ε – A= – A = 313 L mol-1 cm-1 x 0,002 mol L-1 x 2 cm – A = 1,252 – Como visto a aborbância não tem unidade C L Pico máximo de absorção de luz • Porém, quando o caminho óptico é fixado (geralmente 1 cm) a absorbância é diretamente proporcional a concentração da amostra • Sendo assim, deve-se ter consciência que todo e qualquer objeto que interrompa o caminho óptico vai “atrapalhar” a leitura, podendo dar uma falsa impressão de aumento da concentração Pico máximo de absorção de luz 0,8 • Mas como determinar isso para uma substância desconhecida? 0,6 • Simples – varre-se a solução com diferentes comprimentos de onda – quando se desconhece completamente a natureza da substância pode-se usar comprimentos de onda que vão desde o UV até o ultravioleta. Absorbância • Como vimos toda biomolécula apresenta um comprimento de onda específico onde a absorção de luz é máxima com a natureza da substância analisada – com o tipo de solvente utilizado – com o comprimento de onda utilizado – com o pH da solução Como se calcula o coeficiente de absorção molar • Uma vez que se tenha o pico de absorção máxima da molécula, basta fazer uma sequência de diferentes concentrações e medir a absorbância respectiva. • De posse dos valores de absorbância, você pode calcular o coeficiente de extiñção molar através da fórmula A = ε c L 0,4 • Exemplo: 0,2 580 nm 0 300 – 400 500 600 700 Comprimentos de onda (nm) – 800 900 1000 A = 0,351 e C = 0,01563 mM L-1, qual será o ε? – 0,351 = ε x 0,01563 mM L-1 x 1cm – ε = 0,351 / 0,01563 – ε = 22,46 mM L-1 cm-1 Como se calcula o coeficiente de absorção molar 0,8 Absorvância (nm) 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0 0 0,005 0,01 0,015 0,02 -1 Concentração (g L) 0,025 0,03
Baixar