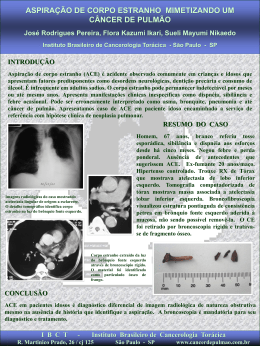
Pacientes com o mesmo diagnóstico Resposta preditiva boa para o medicamento Resposta preditiva ruim ou ausente Use outro medicamento Risco de toxicidade alto Diminuir a dose ou usar outro medicamento Tratamentos estabelecidos com alta eficácia e % dos pacientes beneficiados e não beneficiados com o tratamento Ensaio Droga Eventos (%) Placebo Tratad Benefício/100 Ausência de Benefício/100 Hope Ramipril 17.8 14 3.8 96.2 APTC Aspirina 14 10 4 96 FTT Trombolíticos 11.5 9.6 1.9 98.1 4S Simvastatina 28 19 9 91 EPIC Abciximab 12.8 8.3 4.5 95.5 CURE Clopidogrel 11.5 9.3 2.2 97.8 Farmacogenética Alvos do medicamento Transportadores Farmacodinâmica Enzimas metabolisadoras Farmacocinética Variabilidade na eficácia ou toxicidade Farmagenômica Distribuição Absorção Excreção Farmacogenômica Afinidade do receptor pela droga Droga atuando em produtos gênicos Curr Probl Cardiol, May 2003 Alelos da apo e • apo e2 • apo e3 • apo e4 Kaplan-Meier em pctes com e sem o alelo apoe4 ~Proporção Vivo 1.00 Sem e4 N=312 0.95 0.90 e4-Portadores N=166 0.85 0.80 0 500 1000 1500 2000 2500 Dias após Randomização Tratamento com Placebo Curr Probl Cardiol, May 2003 Tratamento com simvastatina reduz mortalidade em • 13% em pacientes não apo e4 • 50% em pacientes apo e4 Kaplan-Meier em pctes com e sem o alelo apoe4 Proporção Vivo 1.00 Sem e4 N=301 e4-Portadores N=187 0.95 0.90 0.85 0.80 0 500 1000 1500 2000 2500 Dias após randomização Tratamento com Simvastatina Curr Probl Cardiol, May 2003 Alelos da ACE (modulam níveis da ACE em plasma) • Alelo DD – níveis 2x • Alelo II – níveis x • Alelo ID – níveis >x e <2x Sobrevivência de transplantados Kaplan-Meier e genótipo da ACE 1.00 p = 0.04 0.80 0.60 0.40 ACE II (N=69) ACE ID (N=154) ACE DD (N=105) 0.20 0.00 0 6 12 18 24 Seguimento em Meses 30 Curr Probl Cardiol, May 2003 Sobrevivência de Transplantados Kaplan-Maier em ACE DD e uso de betabloqueadores 1.00 p = 0.007 0.80 0.60 0.40 0.20 Beta Bloqueador (N=154) Sem Beta Bloqueador (N=105) 0.00 0 6 12 18 24 30 Seguimento em Meses Curr Probl Cardiol, May 2003 Proporção de sobreviventes Receptor adrenérgico bAR - pacientes com ICC 1.0 0.9 Tre-164 0.8 0.7 0.6 0.5 0.4 Ile-164 Ajustado RR = 4.81, p < 0.001 0.3 0.2 0.1 0.0 0 100 200 300 400 500 600 700 800 900 1000 Dias após entrada no estudo Sintase de óxido nítrico endotelial - ICC % sem eventos 1.00 0.80 Glu-Glu 0.60 Asp=298 0.40 0.20 0.00 0 6 12 18 24 30 36 Seguimento em meses 42 48 54 Adenosina monofosfato deaminase ATP ADP IMP AMP AMP deaminase Adenosina Probabilidade de sobrevivência sem transplante Adenosina monofosfato deaminase - ICC 1.0 0.8 AMPD1 (+/-)/(-/-) 0.6 0.4 AMPD1 (+/+) 0.2 0 0 5 10 Tempo (anos) 15 Tiopurina Metiltransferase • • • • • • Polimorfismo TPMT Metila mercaptopurina – reduz F Leucemia linfocítica aguda 10% intermediária – maior toxicidade 0.3% não tem TMPT – fatal Genotipagem essencial UDP-glucoronosiltransferase 1A1 • • • • Irinotecan – câncer de cólon, pulmão Forma ativa inativada por glucoronidação Aumento de 4x a toxicidade Genotipagem alelo UGT1a1*28 Gene da colinesterase plasmática • • • • • Apnéia prolongada após succinilcolina 1 em 187 em Valencia 1 em 3460 europeus 1 em 25 x 106 asiáticos Complicação facilmente tratada, não há necessidade de genotipagem Leucemia mielóide crônica • • • • • Translocação no cromossoma Filadelfia Alterou localização dos genes bcr e abl bcr-abl tirosina quinase fica ativa Imatinib bloqueia especificamente Imatinib 88% resposta positiva em pctes Câncer de mama • Herceptin – ab citotóxico contra Her-2/neu. • Her-2/neu aumentada em 25% pctes • Herceptina funciona somente nestes pacientes Substratos para citocromo P4502D6 • b-bloqueadores – alprenolol, carvedilol, propranolol • Anti-arrítmicos – flecainida, mexiletina, propafenona • Neurolépticos – haloperidol, clozapina, olanzapina, risperidona • Antidepresssivos – amitriptilina, clomipramina, paroxetina • Antieméticos – ondansetrona, tropisetrona • Outros – anfetamina, codeína, debrisoquina, dextrometorfano Inibidores do citocromo P4502D6 • Neurolépticos – clomipramina, levopromazina, haloperidol • Antidepressivos – fluoxetina, paroxetina, sertralina • Antieméticos - metoclopramida • Anti-histamínicos – clorfeniramina, cimetidina, clemastina, difenilhidramina • Outros – ritonavir, quinidina, amiodarona Genótipo do citocromo P4502D6 • Metabolisadores ultrarápidos • Metabolisadores rápidos • Metabolisadores lentos Genótipo do citocromo P4502D6 • Metabolisadores ultrarápidos – muito baixa em orientais (<<1%), baixa em europeus do norte (<1%), 7% em espanhóis, 29% em etíopes • Metabolisadores rápidos • Metabolisadores lentos – muito baixa em orientais Tratamento de náusea e vômito in quimioterapia - Tropisetron • 42 pacientes, 30% tiveram náusea e vômito • CitP4502D6 – maior frequência dos demais pacientes • Genotipagem recomendável – evitaria emese severe em 1/50 pacientes. Frequeência (no de indivíduos) Polimorfismo genético (acetiladores rápidos e lentos) 25 20 15 10 5 0 0 1 2 3 4 5 6 7 8 9 10 11 12 Concentração ionizada (mg/mL) A superfamília do citocromo P450 Isoenzima Substrato típico Comentários CYP1A CYP2A Teofilina Testestorona Induzida por tabagismo Induzida por tabagismo CYP2B CYP2C Numerosos Numerosos Induzido por fenobarbital Apresenta polimorfismo genético CYP2D Debrisoquina Apresenta polimorfismo genético CYP2E CYP3A Induzida por álcool Nitrosaminas Nifedipina/ciclosporina Induzida por carbamazepina CYP4 Ácidos graxos Induzida por clofibrato Diferenças Farmacogenéticas das Enzimas que metabolizam medicamentos Enzima Pseudocolinesterase plasmática Desidrogenase alcoólica CYP2C19 CYP2D6 CYP2C? Acetil-N-transferase Metiltransferase a Para caucasianos Incidência de deficiência ou metabolizadores lentosa 1 in 3000 Substratos típicos Suxametônio (succinilcolina) 5-10% (approx. 90% em Asiáticos) Etanol 5% (approx. 20% em Asiáticos) S-Mefenitoína, omeprazole 5 - 10% Debrisoquina, espartina, metoprolol, dextrometorfan Fenitoína Muito raro Isoniazida, hidralazina, Approx. 60% (approx. 5% em procainamida japoneses) 6-Mercaptopurina 0.5 % Cmin = Cmax . -kτmax e τmax = ln ( Cmax / Cmin ) k
Baixar