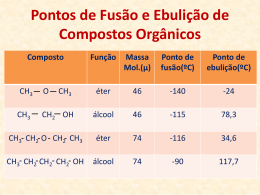
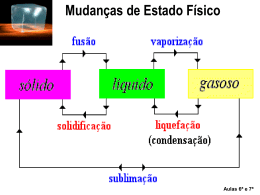
TRANSFORMAÇÕES QUÍMICAS E FÍSICAS Transformações Físicas e Químicas Físicas Dissolver o sal em água; Partir um copo de vidro Triturar os grãos de sal; Transformações Físicas e Químicas Químicas Maçã a apodrecer; Madeira a arder ; Bolo; Transformações Físicas e Químicas Transformações Física não há formação de novas substâncias Transformações Químicas há formação de novas substâncias, ou seja, formam-se substâncias diferentes das existentes inicialmente. Lição sobre a água Este líquido é água. É um bom dissolvente. Embora com excepções mas de um modo geral, dissolve tudo bem, bases e sais. Congela a zero graus centesimais e ferve a 100, quando à pressão normal. Quando pura é inodora, insípida e incolor. Reduzida a vapor, sob tensão e a alta temperatura, move os êmbolos das máquinas que, por isso, se denominam máquinas de vapor. Foi neste líquido que numa noite cálida de Verão, sob um luar gomoso e branco de camélia, apareceu a boiar o cadáver de Ofélia com um nenúfar na mão. António Gedeão Mudança de Estado Físico A mudança de estado físico (líquido gasoso) é a vaporização: Evaporação se o processo for lento. Ex: roupa a secar, estrada a secar após uma chuvada; Ebulição se o processo for rápido. Ex: água a ferver (“alta temperatura”). Mudança de Estado Físico Ponto de ebulição À mesma pressão, cada substância entra em ebulição a uma determinada temperatura, que se chama ponto de ebulição (p.e.) dessa substância. Ponto de ebulição Ponto de ebulição é diferente para cada substância, então o p.e é característico de cada substância. O ponto de ebulição de uma substância aumenta na presença de impurezas. “SE ESTIVÉSSEMOS A AQUECER A ÁGUA E TAPÁSSEMOS O TACHO, A SUBSTÂNCIA AQUECERIA MAIS DEPRESSA? PORQUÊ?” A substância aqueceria mais depressa. Quando tapamos o tacho em casa a pressão no interior vai aumentar, aumentando a temperatura à qual ocorre a ebulição; quando se baixa a pressão, a temperatura diminui. Ponto de Ebulição “SE TIVERMOS VAPOR DE ÁGUA A 250ºC E DIMINUIRMOS A TEMPERATURA ATÉ AOS 100ºC, OCORRERÁ ALGUMA MUDANÇA DE ESTADO?” A água continua no estado gasoso, logo não houve mudança de estado Ponto de Ebulição “E ENTRE OS 100 ºC E 0 ºC, OCORRERÁ ALGUMA MUDANÇA DE ESTADO? A água no estado gasoso passou para estado líquido e que θ (ebulição) = θ (condensação) “Congela a zero graus centesimais (…), quando à pressão normal” Material: almofariz, pilão, tubo de ensaio, termómetro Reagente: gelo, sal. 1. Num almofariz triturar gelo e deitá-lo num tubo de ensaio; 2. Noutro almofariz, triturar gelo misturado com sal e deitá-lo num outro tubo de ensaio; 3. Introduzir um termómetro em cada um dos tubos de ensaio e medir a temperatura dos dois sistemas, registando-a ; 4. Medir e registar a temperatura nos dois sistemas ao fim de 3 minutos “Congela a zero graus centesimais (…), quando à pressão normal” Prevê os resultados que esperarias nos dois casos, fundamentando. Observa a experiência e confronta os resultados com as tuas previsões. Ponto de Fusão À mesma pressão, cada substância entra sempre em fusão a uma determinada temperatura, que se chama ponto de fusão (p.f.) dessa substância. Durante a fusão, se a pressão não variar, a temperatura da mistura sólida e líquida permanece constante. Ponto de Fusão e Ponto de Ebulição Ponto de Fusão e Ponto de Ebulição o p.f. e o p.e. são diferentes para cada substância e que, além de nos permitir identificar essas substâncias, são também critérios de pureza. A presença de impurezas faz aumentar o p.e. e baixar o p.f. As misturas não têm p.f nem p.e. tabelados (no intervalo de tempo em que se dá a ebulição ou a fusão de uma substância na mistura, a temperatura não permanece constante). Questão Problema 1 “Denis Papin, físico francês (1674-1714), tornou-se célebre por ter inventado a “Marmita de Papin”, vasilha que antecedeu a panela de pressão. Este invento, útil ainda nos dias de hoje, é muito importante para as populações que vivem em zonas muito elevadas, onde a pressão atmosférica é baixa”. R: O uso da panela de pressão faz aumentar a pressão e, consequentemente, o ponto de ebulição, conseguindo-se uma cozedura mais rápida dos alimentos. Em zonas onde a pressão atmosférica é baixa, o ponto de ebulição da água é inferior a 100ºC, não permitindo uma cozedura eficaz dos alimentos. Questão Problema 2 R: Como sabes, é habitual deitar sal nas estradas com gelo ou com neve para evitar acidentes. Se deitarmos sal no gelo, o ponto de fusão baixa, isto é, o gelo derrete a temperaturas inferiores a 0ºC.
Baixar