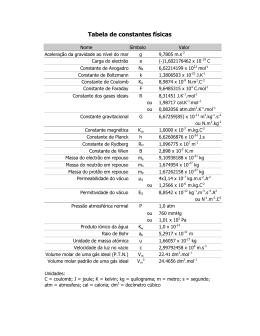
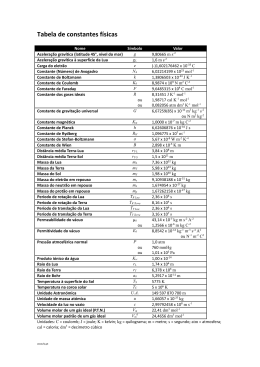
Capítulo 10 - Exercícios adicionais Espontaneidade das transformações 1. Sabendo-se que o cloreto de sódio (NaCℓ) se dissolve em água espontaneamente, pode-se afirmar que este é um processo exotérmico? Justifique. NaCℓ → Na+(aq) + Cℓ–(aq) 2. Segundo M. Berthelot, um químico do século XIX, todos os processos exotérmicos ocorrem de maneira espontânea. À luz dos conhecimentos atuais, o que se pode dizer sobre essa afirmação? Explique. 3. Avalie se cada um dos processos abaixo é espontâneo ou não: a) Dissolução de açúcar em água. b) Flagrância de um perfume espalhando-se pelo ambiente. c) A água caindo em uma cachoeira. Entropia 4. Considere um processo que ocorreu com uma variação de entropia de –8 J K-1 no sistema. De acordo com a segunda lei da termodinâmica, o que se pode concluir sobre a variação de entropia do ambiente? 5. Por que a entropia do sistema aumenta quando o cloreto de sódio sólido é dissolvido em água? Localize, em tabelas de dados termodinâmicos, os valores de Sº [NaCℓ(s)] e Sº [NaCℓ(aq)]. 6. Em algumas situações, ouvimos dizer que os organismos vivos contrariam a segunda lei da termodinâmica, pois são sistemas altamente organizados. A vida contraria essa segunda lei? Justifique. 7. Calcule a entropia-padrão de formação do etano, C2H6(ℓ), a 25 ºC. 8. Deduza o sinal de ∆S para as seguintes transformações: a) C(grafite) → C(diamante). b) O2(g) (5 atm) → O2(g) (1 atm). c) Formação da neve. d) Um gás saindo do extintor de incêndio. 9. Deduza o sinal de ∆Sº para as seguintes transformações: a) 2H2(g) + O2(g) → 2H2O(ℓ). b) 2H(g) → H2(g). c) 2C8H18(ℓ) + 25O2(g) → 16CO2(g) + 18H2O(g). 10. Calcule o valor de ∆Sº para as seguintes transformações: a) C(grafite) → C(diamante). b) 2H2(g) + O2(g) → 2H2O(ℓ). 2007 Pearson Education do Brasil — Química geral 11. Utilize uma tabela de entropia-padrão para calcular o ∆Sº para as seguintes reações: a) S8(rômbico) + 8O2(g) → 8SO2(g). b) 2SO2(g) + O2(g) → 2SO3(g). c) SO3(g) + H2O(g) → H2SO4(ℓ). Energia livre de Gibbs 12. Consulte uma tabela de energia livre e calcule o ∆Gº para as seguintes reações: a) S8(rômbico) + 8O2(g) → 8SO2(g). b) 2SO2(g) + O2(g) → 2SO3(g). c) SO3(g) + H2O(g) → H2SO4(ℓ). 13. Para cada uma das reações do exercício anterior, determine o ∆Gº a 100 ºC. 14. Consulte uma tabela de energia livre e calcule o ∆Gº para as seguintes reações: a) N2(g) + 3H2(g) → 2NH3(g). b) 4Aℓ(s) + 3O2(g) → 2Aℓ2O3(s). 15. O gás oxigênio, O2, pode ser obtido em laboratório por meio da reação do peróxido de sódio com água, de acordo com a equação: 2Na2O2(s) + 2H2O(ℓ) → 4NaOH(s) + O2(g) ∆H = -126 kJ; ∆So = 160,4 J K-1 mol-1 a) Calcule ∆Gº a 25 ºC para essa reação. b) Em que temperatura essa reação entra em equilíbrio à pressão de 100 kPa? 16. O octano, C8H18(ℓ), é um dos componentes da gasolina. Na sua queima, formando gás carbônico e água, sem utilizar dados termodinâmicos, avalie se o sinal de ∆G é positivo ou negativo. Explique. 17. Verifique se cada uma das proposições abaixo é verdadeira (V) ou falsa (F) e justifique. a) Quando o ∆G é positivo, a reação não pode ocorrer. b) Uma reação endotérmica pode ser espontânea. c) Em geral, o ∆S é positivo quando há um aumento no número de mols de gases em uma reação. 18. Qual o efeito da variação de temperatura na espontaneidade das seguintes reações químicas a 1 atm: a) CO(g) → C(s) + ½O2(g) ∆H = 110,5 kJ; ∆So = -89,7 J K-1 mol-1. b) SO2(g) + ½O2(g) → SO3(g) ∆H = -99,1 kJ; ASo = -94,8 J K-1 mol-1. 19. Certa reação tem valor de ∆H = –100 kJ mol-1 e ∆S = –150 J K-1 mol-1. Considere que ∆H e ∆S não variam com a temperatura: a) Determine a temperatura na qual ∆G = 0. b) Se a temperatura for aumentada acima do valor encontrado no item ‘a’, o que acontece com a reação? 2007 Pearson Education do Brasil — Química geral 20. Sabendo que a temperatura de fusão da platina é 1.772 ºC e que sua temperatura de ebulição é 3.827 ºC, estime a entalpia de fusão e a entalpia de vaporização da platina. 21. Considerando as temperaturas abaixo, qual é a quantidade máxima de trabalho útil que pode ser obtida da reação C(s) + O2(g) → CO2(g): a) 25 oC. b) 100 oC. 2007 Pearson Education do Brasil — Química geral
Baixar