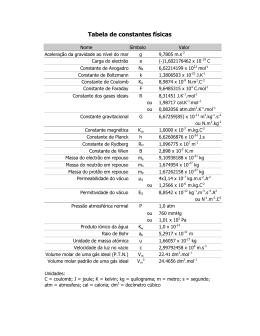
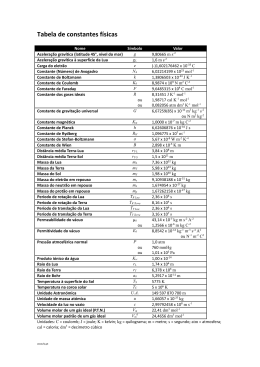
Universidade de Brasília Instituto de Ciências Biológicas Departamento de Biologia Celular Disciplina Biofísica – 121045 – – noturno - Prova 01 – 02/2007 WIrreversível = - Pop* V // para gás ideal P * V n * R * T E=Q+W para gás ideal monoatômico E = (3/2) * n*R* T WRe versível n * R * T * ln V2 V1 S sistema 1 atm*L*mol-1 = 101.39 J*mol-1 R = 8.314 J*K-1*mol-1 ou 0,082 atm.L.mol-1.K-1 X = (Xfinal – Xinicial) ou (Xproduto – Xreagente) Qrev T n * R * ln V2 V1 G= H - T* S 1 caloria = 4,184 Joules H= E + P* V Pode lápis ou caneta. Responda uma questão por página. Coloque nome e matrícula em todas as folhas. 1) Um sistema sofre uma transformação do estado inicial A ao final Z , passando pelos estados B, C e D e permanecendo 15 minutos em cada um deles. Calcule a variação de entropia do sistema entre o estado final Z e o estado inicial A. estado A : n= 1mol de gás ideal T=298K P=1atm estado B : n= 0.25 mol de gás ideal T=58,68K P=14.368atm estado C : n= 0.562 mol de gás ideal T=362.4 K P=0.87atm estado D : n = 17.1mols de gás ideal T = 298K P = 1atm estado Z : n = 1mol de gás ideal T = 298K P = 0.5 atm 2) Uma reação química ocorrendo num sistema a pressão constante transformou 3 gramas do componente A em 3 gramas do componente B. A quantidade de energia liberada elevou de 25 para 25,28 graus a temperatura dos 8,5 litros água ao redor do sistema de reação (que estava em contato térmico perfeito com este). Qual a variação de entalpia do sistema? 3) Para as reações 2 NO( g ) O2 ( g ) 4 NO2 ( g ) O2 ( g ) N 2 ( g ) O2 ( g ) NaCl(s) H 2 O(l ) 2 NO2 ( g ) 2 N 2 O5 ( g ) 2NO ( g ) NaCl(aquoso) H (kJ) - 228,2 reação 01 - 440,8 reação 02 + 180,5 reação 03 + reação 04 3,9 Faça comentários sobre as possíveis causas da variação de entalpia de cada reação, sabendo que todas ocorreram a temperatura constante e pressão de 1 atm. Qual a variação de energia interna para as reações 03 e 04 (considere para a determinação do volume do sistema apenas os componentes gasosos, e a estes como ideais)? 4) Uma planta é colocada em uma campânula de vidro transparente e completamente fechada. Na primeira situação a campânula é colocada numa sala escura onde há vácuo. Na segunda situação, junto com a planta colocamos um pássaro, e na sala de vácuo há luz. O que a segunda lei da termodinâmica pode (se é que pode) dizer sobre o desenvolvimento da planta nessas duas situações? Situação 01 Situação 02
Baixar






![Q32 01. [2,0 pontos] O ácido acetilsalicílico, C9H8O4, é uma](http://s1.livrozilla.com/store/data/001715211_1-c712818da33bf2b4628f87bb08260f0d-260x520.png)


