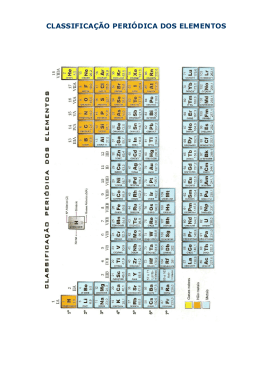
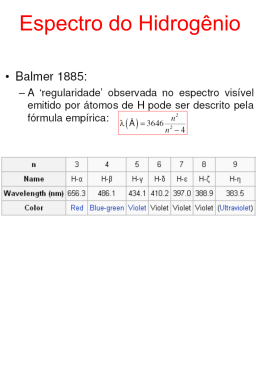
Seminário de Química Capitulo 7: Propriedades Periódicas dos Elementos Vinícius Vieira de Souza Balbi – 14474 Caio César Simões de Souza – 14428 ECO-2007 Introdução • Tabela Periódica – Organizar os diferentes elementos químicos de acordo com suas características, por exemplo, pela configuração eletrônica. • Descoberta de novos elementos – Avanços científicos trouxeram novas ferramentas para poderem isolar elementos de compostos e misturas. A Tabela Periódica Carga Nuclear Efetiva • É uma carga localizada no núcleo do átomo, que gera um campo elétrico. • É calculada com o número médio de elétrons por causa da grande quantidade de repulsões elétron-elétron. = Carga Nuclear Efetiva = Número de prótons = Número médio de elétrons • Ex: Mg – [Ne]3s² – Carga 12+ no núcleo – Carga 10- na camada mais interna, igual ao Ne – C.N.E= 12 – 10 = 2+ Tamanho de átomos e íons • Raio atômico de Van der Waals (raio nãoligante) – Medido através das colisões de átomos. • Raio atômico covalente (raio ligante) – Medido através da distância entre os núcleos dos átomos interligados. • A tendência periódica do raio atômico é crescer em direção ao elemento localizado no último período e no primeiro grupo. Ex: Da direita para esquerda há diminuição da carga do núcleo, diminuindo a atração pelos elétrons. • O tamanho dos íons em relação ao átomo de origem depende da sua carga. • No caso de um cátion, sua carga positiva diminui as repulsões elétron-elétron, sendo o íon menor que o seu átomo de origem. O contrário acontece com os ânions. Energia de Ionização • É a mínima energia necessária para se retirar um elétron de um átomo ou íon gasoso isolado em seu estado fundamental. • Em um átomo pode existir da primeira até a sétima energia de ionização, e esta é crescente no intervalo. • Tabela com energias de ionização de alguns elementos: • A tendência periódica das primeiras energias de ionização é crescer em direção ao elemento localizado no primeiro período e no último grupo. Ex: Da esquerda para direita há diminuição do tamanho do átomo, estando os elétrons mais próximos do núcleo. Configurações eletrônicas de íons • Ao retirar-se um elétron de um átomo, é escolhido o elétron que se encontra no orbital com maior número quântico principal disponível. Ex: • Ao adicionar-se um elétron a um átomo, ele é acrescido ao próximo orbital disponível de menor energia. Ex: Afinidade Eletrônica • É a energia liberada pelo átomo ao ganhar um elétron. • Quanto maior a atração entre átomo e elétron, mais negativa ela é. • À medida que caminhamos para os halogênios, os elementos apresentam um elétron a menos para preencher o sub-nível p. • Adicionar um elétron a um gás nobre é energeticamente desfavorável. O mesmo se dá com Be e Mg. Principais características dos metais • Tem brilho, várias cores, no entanto a maioria é prateada • Os sólidos são bons condutores de calor e eletricidade • Muitos óxidos metálicos são sólidos iônicos básicos • Tendem a formar cátions em soluções aquosas Metalóides • De acordo com a IUPAC, eles foram extintos da tabela periódica e foram para o grupo dos metais ou dos não-metais. • Ge (germânio), Sb (antimónio), Po (polônio) são definidos como metais. • B (boro), Si (silício), As (arsênico), Te (telúrio), de acordo com a IUPAC, são agora não-metais. Principais características de nãometais • Não tem brilho, várias cores • Sólidos normalmente são quebradiços, alguns são duros e outros macios • Pobres condutores elétricos e de calor • Muitos óxidos de não metais são substâncias moleculares que formam soluções ácidas • Tendem a formar ânions ou oxiânions em soluções aquosas Metais Alcalinos • Cor cinza • Baixa densidade e ponto de fusão • Muito reativos • Reação exotérmica em contato com água Metais Alcalino-Terrosos • Mais duros e densos que os metais alcalinos • Menos reativos e de ponto de fusão maior que os metais alcalinos, que vai aumentando de acordo com o número atômico dos elementos As tendências de não-metais Hidrogênio • Hidrogênio não pertence a nenhum grupo particular. • Na natureza é encontrado em forma de molécula diatômica incolor. Podendo ser metálico em condições de pressão extremamente alta. As tendências de não-metais da família 16 • Oxigênio é o único gasoso à temperatura ambiente; os demais são sólidos. • O polônio é o único metal e é raro. As tendências de não-metais da família 17 • Halos e gennao vem do grego e significam formadores de sal. • Todos elementos formam moléculas diatômicas. Gases nobres • Monoatômicos • Estáveis • Gases nobres também formam compostos Referências bibliográficas • Química, a ciência central. Autores: Brown, LeMay e Bursten; • Google: http://images.google.com.br ; • Wikipedia: http://www.wikipedia.org ; • Fotosearch: http://www.fotosearch.com.br FIM
Baixar