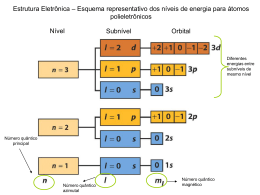
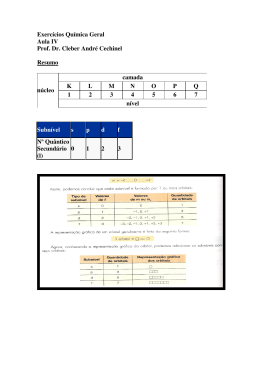
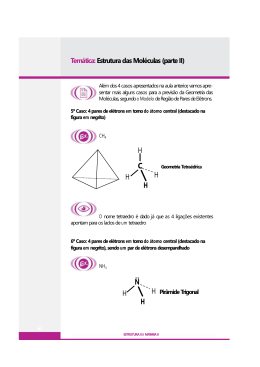
Questões – distribuição elet. , nº quânticos e mol 9º Ano Profª Andreia 1. O titânio (Z = 22) é muito utilizado atualmente, quando se deseja um material de difícil oxidação. Sobre esse elemento, são feitas as seguintes proposições: I) Possui 12 elétrons na camada M. II) Apresenta 4 camadas eletrônicas. III) Apresenta 8 elétrons no subnível “s”. IV) O seu subnível mais energético é o subnível 4s. São corretas: a) II, III e IV. d) II e III. b) II e IV. e) todas. c) III e IV. 2. Alguns elementos apresentam, no estado fundamental e no seu nível mais energético, a configuração npx. Dentre os elementos abaixo, o que apresenta maior valor de “x” é: a) Al (Z = 13). c) F (Z = 9). e) Si (Z = 14). b) N (Z = 7). d) Ne (Z = 10). 3. Quais são os quatro números quânticos dos dois elétrons mais externos do átomo de número atômico 20? 4. Indique qual é o conjunto dos quatro números quânticos do elétron mais energético do átomo do elemento Ferro (Z = 26). 5. Determine as massas moleculares das substâncias abaixo: a) N2 b) CO2 c) HNO3 d) H2SO4 e) C6H12O6 f) Ca(OH)2 g) Ca(ClO3)2 h) (NH4)2SO4 i) Ca3(PO4)2 j) Al(OH)3 H = I; C = 12; N = 14; O = 16; Na = 23; Ca = 40; Cl = 35; P =31; Cu = 63; S = 32; F = 19; Ag = 1O8; Al = 27; Fe = 56; I = 127 6. Sabendo que a massa atômica do magnésio é igual a 24 u, determine a massa, em gramas, de um átomo desse elemento. (Dado: Número de Avogadro = 6,0 . 1023). 7. Considere um copo que contém 180 mL de água. Determine, respectivamente, o número de mol de moléculas de água, o número de moléculas de água e o número total de átomos. (Massas atômicas = H = 1,0; O = 16; Número de Avogadro = 6,0 . 1023; densidade da água =1,0 g/mL). 8. 3,0 x 1023 moléculas de certa substância “A” têm massa igual à 14g. A massa molar dessa substância é: 9. Quantos mols de ácido sulfúrico (H2SO4) se tem em 294g dessa substância?
Download