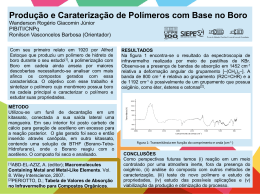
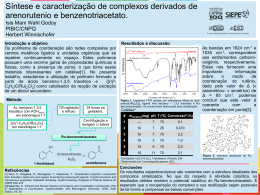
SÍNTESE E CARACTERIZAÇÃO DE COMPOSTOS DE COORDENAÇÃO PARA A FIXAÇÃO DE CO2 DE RELEVÂNCIA BIOINORGÂNICA. Daniela De Nez1*(IC), Suzana Cimara Batista 1(PG) [email protected] 1 Centro Tecnológico – Universidade do Sul de Santa Catarina – 88704-900 - Tubarão – SC. RESUMO – O complexo de cobre (II) apresenta moléculas de água coordenadas na forma trans ao íon metálico central e mostra-se eficiente para a incorporação do dióxido de carbono, podendo ser utilizado para fins ambientais. O composto de cobalto (II) que apresenta moléculas de água na forma cis na sua esfera de coordenação não é eficiente para incorporar dióxido de carbono. Palavras Chave: composto de coordenação, dióxido de carbono, esfera de coordenação. 1. INTRODUÇÃO As metaloenzimas são constituídas por cadeias de proteínas em que grupos terminais, provenientes de resíduos de aminoácidos, são constituídos pelos grupos tiol, hidroxila, aminas, amidas e ácido carboxílico. Estes grupos encontram-se ligados diretamente ao íon metálico, o que constitui o sítio ativo da metaloenzima.1 Assim sendo, metaloenzimas como a anidrase carbônica em que o sítio ativo apresenta o íon carbonato coordenado são foco de investigações.2 O atual interesse em compostos de coordenação que apresentam em sua esfera de coordenação uma ligação do tipo metal-hidróxido é devido ao fato que estes podem ser modelos para a incorporação do CO2 da atmosfera contribuindo para a proteção ambiental. 2 Para esta reação de incorporação de CO2 faz-se necessário a existência de um ânion nucleofílico que pode ser proveniente de um grupo hidroxo ou aquo coordenado ao centro metálico. A reação resulta na formação de um complexo carbonato. Essa reação é conhecida para complexos de Co, Ni, Cu e Zn.2,3 Neste sentido este trabalho apresenta a reação de inserção de dióxido de carbono em um composto de coordenação de cobre (II) que apresenta em sua esfera de coordenação o grupo aquo coordenado, tornando-se um ambiente propício para a incorporação de CO2, bem como a estrutura cristalina de um complexo de cobalto (II). Através destes compostos é possível explicar porque compostos de coordenação com estruturas semelhantes muitas vezes não incorporam dióxido de carbono em sua esfera de coordenação. 2. MÉTODOS 2.1 Obtenção do Composto [Cu(H3tea)CO2]SO4 (1) O composto de coordenação de partida para a obtenção do composto (1) foi o [Cu(H3tea)(H2O)2]SO4 que foi sintetizado e isolado e sua rota sintética e a sua estrutura cristalina foram publicados anteriormente.4,5 O composto (1) foi sintetizado a partir de 0,45 g do composto [Cu(H3tea)(H2O)2]SO4 4,5 em solução de metanol, sob agitação e a temperatura ambiente. Para iniciar a reação de inserção de Curso de Engenharia Química – Universidade do Sul de Santa Catarina. Av. José Acácio Moreira 787, Dehon –CEP: 88704-900 – Tubarão – SC – Brasil Telefone: (48) 3621-3138 – Fax: (48) 3621-3021 – e-mail: [email protected] dióxido de carbono foi adicionado 0,20 mL de uma solução em metanol de hidróxido de lítio. Houve a formação de um precipitado microcristalino de coloração azul claro. O precipitado formado foi filtrado e deixado secar em dessecador. Em seguida foi caracterizado por espectroscopia eletrônica de Uvvís e vibracional (IV). 2.2 Obtenção do Composto [Co(H3tea)(H2O)2]SO4 (2) O composto de coordenação de cobalto (2) foi sintetizado pela reação de 1,69 g (6 mmol) de CoSO4 . 7H2O com 0,8 mL (6 mmol) de H3tea em solução de metanol, sob agitação e aquecimento a uma temperatura de 60 C. O composto de cobalto foi obtido na forma de cristais violetas em que o rendimento da reação foi de 42,54%. A caracterização do composto foi realizada através de espectroscopia eletrônica (UV-vis), vibracional (IV) e estrutura cristalina através da técnica de difração de raios X. 2.3 Obtenção do Composto [Co(H3tea)(CO2)]SO4 (3) Partiu-se de 0,6g do composto [CoH3tea(H2O)2] (1) solubilizado em metanol e colocou-se sob refluxo e em seguida iniciou-se a inseto do gás CO2 no meio reacional, mantendo-se o pH em torno de 7,5 a 8 com solução de hidróxido de lítio 2.10-3 mol.L-1. Após três horas de refluxo, a solução mãe foi filtrada e em seguida deixada em repouso, condição necessária para a precipitação. 3. RESULTADOS 3.1 Espectroscopia Vibracional (IV) O espectro de infravermelho do composto 1 realizado em pastilha de KBr apresenta bandas características do ligante e do contra-íon: 3357 cm-1 (O-HH2O), 2895 cm-1 (C-HCH2), 1327 cm-1 (O-H), 1118 cm-1 (S-O). A banda em 1118 cm-1 evidência a presença do ânion SO42-. A presença do ânion carbonato coordenado pode ser verificada pela presença da banda6 em 1404 cm-1 e 1290 cm-1 que correspondem ao (C-O) do grupo CO32- a qual não se encontra presente no espectro de infravermelho do composto de partida. O espectro de infravermelho do composto 2 realizado em pastilha de KBr apresenta bandas características do ligante e do contra-íon: 3357 cm-1 (O-HH2O), 2846 cm-1 (C-HCH2), 1334 cm-1 (O-H), 1096 cm-1 (S-O). A banda em 1096 cm-1 evidência a presença do ânion SO42-. 3.2 Espectroscopia Eletrônica Uv-vís O espectro eletrônico do composto 1 foi realizado em solução de metanol e apresenta duas bandas na região de 768 nm e 291 nm. O espectro do composto 2 realizado em solução de metanol, apresenta duas bandas na região de 520 nm e 300 nm e um ombro em 483 nm, conforme apresentado na figura 1. 0,30 0,25 0,20 0,15 0,10 0,05 0,00 300 400 500 600 700 800 900 comprimento de onda (nm) Figura 1. Espectro eletrônico do composto 2 em solução de metanol. 3.3 Estrutura Cristalina O composto de coordenação de cobalto foi sintetizado e isolado na forma cristalina. Neste composto o átomo de cobalto está coordenado em uma esfera de coordenação de geometria octaédrica. A estrutura cristalina do composto 2 (figura 2) apresenta a coordenação do íon cobalto no plano equatorial a um átomo de nitrogênio amínico e a dois átomos de oxigênio do grupo álcool na forma protonada. Neste plano de coordenação apresenta ainda uma molécula de água. A esfera de coordenação se completa com a coordenação no plano axial de um átomo de oxigênio do grupo álcool (protonado) e uma molécula de água. Está forma como a água coordena-se é muito similar aquela apresentada pela metaloenzima anidrase carbônica, o que pode representar um bom sítio para o ataque nucleofílico e a posterior coordenação do ânion carbonato. As ligações Co1—O13 2.0397 e Co1—O11 2.0792 Å apresentando um ângulo O13—Cu1—O11 100.92. Os comprimentos de ligações Co1—N2 2.128 Å. No complexo (1), a distância Co1-O9 é 2.1068 e Co1-O12 é 2.1198 Å. Figura 2. Estrutura Cristalina do complexo 2. Alguns parâmetros cristalográficos importantes estão apresentados na Tabela 1. Tabela 1. Parâmetros cristalográficos para a estrutura do complexo 2. Fórmula Empírica C6H19CoNO5·O4S·H2O Massa Molecular 358.24g.mol-1 Sistema Cristalino monoclínico Grupo Espacial P21/c V 83.6 (4) Å3 Dimensões da cela unitária a = 7.4905 (14) Å b = 15.003 (3) Å c = 12.693 (2) Å 3.4 Inserção do dióxido de carbono nos compostos 1 e 2 O composto de coordenação de cobre (II) 1 que apresenta em sua esfera de coordenação moléculas de água coordenadas (trans) apresentou-se eficiente para a incorporação de dióxido de carbono, conforme foi confirmado pela análise de espectrosocpia de infravermelho. A caracterização estrutural do composto mononuclear de cobalto (II) 2 representa um importante modelo em que sua esfera de coordenação apresenta moléculas de água coordenadas. Isso representa que este composto pode ser utilizado como modelo para testes de incorporação de dióxido de carbono tal como realiza esta atividade catalítica a metaloenzima anidrase carbônica. No entanto, os testes de inserção de dióxido de carbono gasoso ao composto 2 mostraram que este não é eficiente para a coordenação deste gás à esfera de coordenação na forma de íon carbonato. 4. CONCLUSÕES O composto de coordenação de cobre (II) 1 que apresenta em sua esfera de coordenação moléculas de água coordenadas trans apresentou-se eficiente para a incorporação de dióxido de carbono, podendo portanto ser utilizado para fins ambientais. O composto mononuclear de cobalto (II) 2 foi sintetizado e caracterizado e as suas propriedades físico-químicas foram apresentadas. Este composto está sendo utilizado como precursor para a síntese de outros compostos de coordenação para a modelagem da metaloenzima anidrase carbônica. No entanto, pelo fato do composto 2 apresentar em sua esfera de coordenação moléculas de água coordenadas na forma cis ao centro metálico, isto pode estar associado a não incorporação do dióxido de carbono. 5. REFERÊNCIAS 1 Kaim, W. & Schederski, B. Bioinorganic Chemistry: Inorganic Elements in the Chemistry of Life. 1994. 2 Kitajima, N.; Hikichi, S.; Tanaka, M.; Moro-oka, Y. J. Am. Chem. Soc. 1993, 115, 5496. 3 Tanase, T.; Nitta, S.; Yano, S. et alli. Inorg. Chem. 1993, 31, 1058. 4 Batista, Suzana C.; Marques, Camila M.; XVI Encontro de Química da Região Sul. 2008, QI60. 5 Batista, Suzana C.; Marques, Camila M.; XVII Encontro de Química da Região Sul. 2009, QI 450. 6 Nakamoto, K. Infrared and Raman Spectra of Inorganic and Coordination Compounds. 3rd ed.: John Wiley: New York, 1978; p. 232.
Baixar