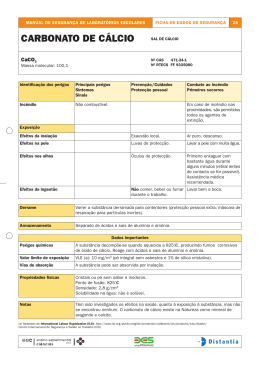
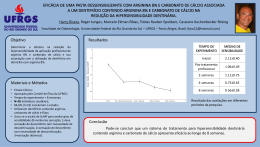
2 Vamos ver como tudo isso pode ser escrito através das equações químicas? As cavernas formam-se normalmente em áreas de rochas calcárias, embora na zona costeira possam ocorrer em outros tipos de rochas. As rochas calcárias são formadas por calcita (carbonato de cálcio, CaCO3), que se dissolvem quando entram em contato com a água que contém suficiente teor de ácidos. Estes ácidos são provenientes da chuva ácida ou do dióxido de carbono (CO2) existente na atmosfera e na decomposição da matéria orgânica, que em contato com a água formam o ácido carbónico, H2CO3. Num segundo momento, a água ácida penetrando pelas fendas do calcário ataca a rocha, produzindo o bicarbonato de cálcio (Ca(HCO3)2), que é solúvel e facilmente transportado pela água. Com a dissolução do bicarbonato de cálcio, as fendas vão alargando-se lentamente e formando as cavernas. Vamos ver a equação química que expressa este fenómeno? 3 – Precipitação do carbonato de cálcio: 1- Acidulação da água pela formação do ácido carbónico: Água 1 A gota dessa solução aquosa fica pendurada no teto até que atinja volume e peso suficiente para cair. Nesse período ocorre a liberação do gás carbônico (CO2) e, como conseqüência, ocorre a precipitação de parte do bicarbonato dissolvido. Formam-se assim os primeiros cristais de carbonato de cálcio (CaCO3), que vão dar origem à estalactite.A gota, ao cair, ainda carrega consigo bicarbonato de cálcio (Ca(HCO3)2) em solução, o qual vai sendo depositado no piso logo abaixo, formando uma estalagmite. O crescimento oposto da estalactite e da estalagmite faz com que essas peças muitas vezes se unam, dando origem à colunas. + dióxido de carbono H2O + CO2 = ácido carbónico = H2CO3 2- Dissolução da rocha pelo ácido carbónico: ácido carbónico + H2CO3 + CaCO3 carbonato de cálcio = bicarbonato de cálcio = Ca(HCO3)2 As águas da chuva, aciduladas pelo gás carbónico da atmosfera e do solo, ao penetrarem pelas fendas da rocha calcária, vão dissolvendo-a e transportando em solução o bicarbonato de cálcio, Ca(HCO3)2, até emergirem no teto de uma caverna pré-existente. Carbonato de cálcio + água + dióxido = Bicarbonato de carbono de cálcio CaCO3 + 3 H2O + CO2 Vamos rever? = Ca(HCO3)2 Bibliografia As Reações Químicas e a Formação das Cavernas Referências Bibliográficas: 1- Lino, C.F. Cavernas: o fascinante Brasil subterrâneo, Editora Rios-SP, 1989. 2- Brady, J.E. and Holum, J.R. Chemistry: The study of matter and its changes, John Wiley, 1993. 3-Beiser, A. et al A Terra, Biblioteca da Natureza- Life, Livraria José Olympio Editora-RJ, 1970. Fontes Das Imagens Retirado de: 1- http://www.ajbonito.com.br/index.php?idcanal=184 Consultado em 11/01/2012 2- http://fpslciencias.blogspot.com/2010/04/formacao-decavernas.html Consultado em 11/01/2012 3- http://www.cdcc.usp.br/quimica/ciencia/cavernas.html Consultado em 11/01/2012 “Numa caverna nada se tira a não ser fotografias (quando permitido), nada se deixa a não ser as pegadas, nada se mata a não ser o tempo.” Este é o lema internacional da espeleologia Escola Secundária da Cidadela 2011 Ano internacional do morcego Paginador: Victor Fernandes
Baixar