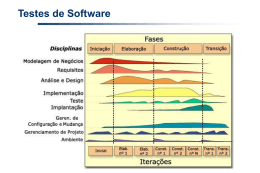
Química das Superfícies e Interfaces Interface gás/sólido Valentim M. B. Nunes Departamento de Engenharia Química e do Ambiente 2009 Química das Superfícies e Interfaces Adsorção de gases em sólidos Quando um gás/vapor entra em contacto com um sólido parte dele adsorve à superfície. Física: forças de interacção de van der Waals; energias de adsorção de 300 a 3000 Existem dois tipos de J.mol-1 adsorção Química: interacção a curta distância; calor de adsorção química maior 40 a 400 kJ.mol-1 Química das Superfícies e Interfaces Método de medição O gás a ser adsorvido ocupa uma bureta calibrada, e a pressão lê-se num manómetro. Quando o gás entra em contacto com a amostra adsorvente, pode-se calcular a quantidade adsorvida a partir da leitura de pressão, quando se atinge o equilíbrio. Química das Superfícies e Interfaces Isotérmicas de adsorção: quantidade de gás adsorvido em função de p/ps , sendo ps a pressão de vapor do adsorvido à temperatura da isotérmica. Volume de gás adsorvido/g de adsorvente N2 em sílica a 77 K (adsorção física) 0 p/ps O2 em carvão activado a 150 K (adsorção química, limitada a monocamada) 1 Química das Superfícies e Interfaces ISOTÉRMICAS DE ADSORÇÃO – CLASSIFICAÇÃO DE BRUNAUER Química das Superfícies e Interfaces Tipo I: Sólidos com poros pequenos – carvão activado. Tipo II: Sólidos que não possuem redes internas de orifícios – sílica ou alumina. Tipo III: adsorvente não poroso – Cl2 em sílica gel; CCl4 em caulino. Tipo IV e V: bastante raros. Química das Superfícies e Interfaces Adsorção física Quando p = ps ocorre condensação do gás na superfície do sólido. A quantidade de vapor adsorvido para um dado adsorvente depende de várias variáveis. xads f ( p, T , gás, sólido) O aumento de temperatura diminui a quantidade de gás adsorvido, uma vez que a adsorção física é um processo exotérmico, Hads < 0 Química das Superfícies e Interfaces IUPAC Technical Reports and Recommendations Reporting physisorption data for gas/solid systems with special reference to the determination of surface area and porosity (Recommendations 1984) K. S. W. Sing Química das Superfícies e Interfaces Due to the weak bonds involved between gas molecules and the surface (less than 15 KJ/mole), adsorption is a reversible phenomenon! No entanto, do ponto de vista teórico, é muito difícil prever a forma das isotérmicas. A maior parte das teorias baseia-se no aparecimento de monocamadas a baixas pressões, formandose multicamadas quando p ps. Química das Superfícies e Interfaces ISOTÉRMICA DE LANGMUIR Hipóteses: a) A superfície sólida possui um número fixo de centros para adsorção. O equilíbrio entre o gás e o sólido é dinâmico. A uma dada temperatura e pressão está ocupada uma fracção de centros, e uma fracção 1- estão desocupados. b) Cada centro é ocupado apenas por uma molécula. c) O calor de adsorção é o mesmo para todos os centros e não depende de . d) Não existe interacção entre as moléculas dos diferentes centros. Química das Superfícies e Interfaces A velocidade a que as moléculas ocupam os centros é igual à velocidade a que os desocupam. Á pressão p, a velocidade de ocupação dos centros é: va ka pN(1 ) onde N é o número total de centros. A velocidade de desocupação é: vd kd N Química das Superfícies e Interfaces No equilíbrio, igualando a velocidade de ocupação e desocupação, obtém-se: kp 1 kp com k = ka/kd. Química das Superfícies e Interfaces Reorganizando a expressão: Considerando agora, kp kp V Vm em que Vm é o volume correspondente a toda a superfície ocupada (ou volume de monocamada): V V kp kp Vm Vm Química das Superfícies e Interfaces Obtém-se a isotérmica de Langmuir: p p 1 V Vm kVm Fazendo p/V em função de p, obtemos uma linha recta, cujo declive é igual a 1/Vm e cuja ordenada na origem é 1/kVm. Química das Superfícies e Interfaces Química das Superfícies e Interfaces Química das Superfícies e Interfaces A velocidade de adsorção do número de centros atingidos pelas moléculas (teoria cinética de gases) NA p (1 ) 1/ 2 2MRT A velocidade de desadsorção depende de um processo de activação Zme H / RT Onde H é o calor de adsorção (simétrico do calor de desadsorção), Zm é o número de moléculas adsorvidas por área e é a frequência de oscilação das moléculas perpendicularmente à superfície. Química das Superfícies e Interfaces Igualando as duas expressões, obtém-se: NA p 1/ 2 2MRT NA p H / RT Z e 2MRT 1/ 2 m ou 1 1 1 kp com H RT N Ae k 1/ 2 Z m 2MRT Química das Superfícies e Interfaces Para baixas pressões (kp << 1): kp V kpVm Para altas pressões (kp >> 1): 1 V Vm Química das Superfícies e Interfaces k comporta-se como uma constante de equilíbrio: H 1 H ln k 2 2 2T RT T p RT Equação de van’t Hoff Química das Superfícies e Interfaces Isotérmica de Freundlich V kp 1/ n 1 log V log k log p n
Baixar