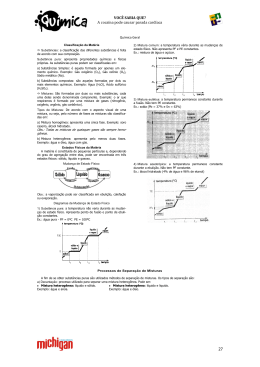
Química Geral Classificação da Matéria Substâncias: a classificação das diferentes substâncias é feita de acordo com sua composição. 2) Mistura comum: a temperatura vária durante as mudanças de estado físico. Não apresenta PF e PE constantes. Ex.: mistura de água e açúcar. Substância pura: apresenta propriedades químicas e físicas próprias. As substâncias puras podem ser classificadas em: a) Substâncias Simples: é aquela formada por apenas um elemento químico. Exemplo: Gás oxigênio (O2 ), Gás ozônio (O3), Sódio metálico (Na). b) Substâncias compostas: são aquelas formadas por dois ou mais elementos químicos. Exemplo: Água (H2O), Ácido sulfúrico (H2SO4 ). Misturas: São formadas por duas ou mais substâncias, cada uma delas sendo denominada componente. Exemplo: o ar que respiramos é formado por uma mistura de gases (nitrogênio, oxigênio, argônio, gás carbônico). 3) Mistura eutética: a temperatura permanece constante durante a fusão. Não tem PE constante. Ex.: solda (Pb = 37% e Sn = 63%) Tipos de Misturas: De acordo com o aspecto visual de uma mistura, ou seja, pelo número de fases as misturas são classificadas em: a) Mistura homogênea: apresenta uma única fase. Exemplo: soro caseiro, álcool hidratado. Obs.: Todas as misturas de quaisquer gases são sempre homogêneas. b) Mistura heterogênea: apresenta pelo menos duas fases. Exemplo: água e óleo, água com gás. Estados Físicos da Matéria A matéria é constituída de pequenas partículas e, dependendo do grau de agregação entre elas, pode ser encontrada em três estados físicos: sólido, líquido e gasoso. Mudança de Estado Físico: 4) Mistura azeotrópica: a temperatura permanece constante durante a ebulição. Não tem PF constante. Ex.: álcool hidratado (4% de água e 96% de etanol) Obs.: a vaporização pode ser classificada em ebulição, calefação ou evaporação. Diagramas de Mudança de Estado Físico 1) Substância pura: a temperatura não varia durante as mudanças de estado físico. Apresenta ponto de fusão e ponto de ebulição constantes. Ex.: água pura - PF = 0ºC PE = 100ºC Processos de Separação de Misturas A fim de se obter substâncias puras são utilizados métodos de separação de misturas. Os tipos de separação são: a) Decantação: processo utilizado para separar uma mistura heterogênea. Pode ser: Mistura heterogênea: líquido e sólido. Mistura heterogênea: líquido e liquido. Exemplo: água e areia. Exemplo: água e óleo. 27 b) Filtração: processo utilizado para separar substâncias em misturas heterogêneas envolvendo sólidos e líquidos. c) Destilação: processo utilizado para separar uma mistura homogênea. Pode ser: Destilação Simples: mistura homogênea entre sólido e líquido. Ex.: água e sal. Destilação Fracionada: mistura homogênea entre líquidos. Ex.: água e álcool. 28 Tipos de Fenômenos: a) Fenômenos físicos: é todo aquele em que não há destruição b) Fenômenos químicos: é toda transformação em que há ou formação de substâncias. Nesses fenômenos, a forma, o destruição de moléculas e formação de novas espécies químicas. tamanho, a aparência e o estado físico podem mudar, porém a Quando ocorre um fenômeno químico, uma o mais substâncias se constituição da substância não sofre alterações. Ex.: as mudanças transformam e dão origem a novas substâncias, logo podemos de estado físico. dizer que ocorreu uma reação química. Exemplo: queima de materiais. ESTRUTURA ATÔMICA Subnível s p d f CARACTERÍSTICAS DO ÁTOMO * Número Atômico (Z) : é o número de prótons presentes no núcleo de um átomo. Z=P Obs.: átomos neutros e- = p ÍONS: excesso de carga Carga positiva – cátions ( perde elétrons) Carga negativa – ânions ( ganha elétrons) * Número de Massa (A): é a soma do número de prótons e de nêutrons. A=Z+n Obs.: n = A – Z Representação geral: z XA Z = A = p = e = Isoeletrônicos: Átomos ou íons com nº e = L 8 M 18 7 níveis (camadas) O P Q 32 18 2 ou 8 N 32 s 2 4 subníveis p d 6 10 2 3 s2 0 6 p -1 0 +1 10 d -2 -1 0 +1 +2 0 +1 +2 +3 Número quântico spin (s): está relacionado à rotação do elétron. s = -1/2 s = +1/2 Obs.: cada orbital suporta no máximo 2 elétrons de spins contrários Obs.: elétron celibatário (elétron desemparelhado) ELETROSFERA K 2 1 Número quântico magnético (m): está relacionado à região de máxima probabilidade de se encontrar o elétron, denominada orbital. -3 –2 –1 n = 0 f 14 Semelhanças Atômicas Isótopos Isóbaros Isótonos Valores de l Tabela Periódica qtdade máxima de e- Na tabela, os elementos estão arranjados horizontalmente, em seqüência numérica, de acordo com seus números atômicos, resultando o aparecimento de sete linhas horizontais (ou períodos). f 14 qtdade máxima de e- Elementos Químicos: Os elementos químicos são representados por letras maiúsculas ou uma letra maiúscula seguida de uma letra minúscula. Os Símbolos são de origem latina: NÚMEROS QUÂNTICOS São os nº que caracterizam um elétron. Número quântico principal (n): está relacionado com o nível de energia do elétron. n = 1,2,3,4,5,6 ou 7 Número quântico secundário (l): está relacionado ao subnível de energia do elétron. Português Sódio Potássio Enxofre Fósforo Ouro Latim Natrium Kalium Sulphur Phosphurus Aurum Símbolo Na K S P Au 29 Períodos ou Séries: São as filas horizontais da tabela periódica. São em número de 7 e indicam o número de níveis ou camadas preenchidas com elétrons. Famílias ou Grupos: São as colunas verticais da Tabela Periódica. Em um Grupo ou Família, encontram-se elementos com propriedades químicas semelhantes. Para os Elementos Representativos, o nº do Grupo representa o nº de elétrons da última camada (camada de valência). Classificação Periódica Observações sobre a tabela: Diagrama de Linus Pauling 1 - São elementos líquidos: Hg e Br; 2 - São Gases: He, Ne, Ar, Kr, Xe, Rn, Cl, N, O, F, H; 3 - Os demais são sólidos; 4 - Chamam-se cisurânicos os elementos artificiais de Z menor que 92 (urânio): Astato (At); Tecnécio (Tc); Promécio (Pm) 5 - Chamam-se transurânicos os elementos artificiais de Z maior que 92: são todos artificiais; 6 - Elementos radioativos: Do bismuto (83Bi) em diante, todos os elementos conhecidos são naturalmente radioativos. Propriedades Periódicas - Raio e Eletropositividade - Afinidade eletrônica - Energia de ionização - Eletronegatividade* * gases nobres não apresentam eletronegatividade Ligação química: É a força de atração suficientemente forte entre os átomos a fim de mantê-los unidos. Valência: Capacidade de combinação dos átomos. Regra do octeto: Os átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Ligações Interatômicas Ligação Iônica Elementos Ligantes Metais e ametais. Metais e hidrogênio. Grande diferença de eletronegatividade. 30 Pequena diferença de eletronegatividade. Metálica Metais Alta eletropositividade Compartilhamento de pares de elétrons de valência através da formação de orbitais moleculares. Liberação parcial dos elétrons mais externos, formando uma estrutura de cátions envoltos pelos elétrons parcialmente liberados. Cristal iônico, representado Moléculas, representadas pela pelo íon-fórmula ou fórmula fórmula molecular ou cristal mínima (mínimo de cátions e covalente (macro-molécula), ânions necessários para que a representada pela reestrutura soma das cargas elétricas mínima seguida do índice n. seja zero). Cristal metálico, representado pelo símbolo do elemento. Transferência de elétrons dos metais (que formam cátions) Como ocorre a para os ametais (que formam ligação ânions). Cátions e ânions sofrem atração elétrica. Unidade formadora Covalente Ametais e ametais. Ametais e hidrogênio. Hidrogênio e hidrogênio. Cristal iônico de cloreto de sódio. íon-fórmula: NaCl. Exemplo importante Molécula de água. Cristal metálico de alumínio. Fórmula molecular: H2 O Cristal covalente de diamante. Representação: Al(s) Representação: Cn(s) Ligações Interatômicas Definição e Ocorrência As forças intermoleculares são as que mantêm a coesão das moléculas ou partículas que compõem uma substância. Na prática, as forças intermoleculares podem atuar em conjunto e a interação entre as moléculas é calculada pela soma dos diversos tipos de forças intermoleculares atuantes. Por exemplo, na água a principal força de interação molecular são as pontes de hidrogênio, embora também haja interações do tipo dipolo permanente. Forças de Van der Waals Dipolo Permanente Pontes de hidrogênio São forças de natureza elétrica de intensidade fraca. Uma das principais forças são as dispersões de London, ou seja, interações que ocorrem entre moléculas apolares e átomos de gases nobres quando, por um motivo qualquer, ocorre uma assimetria na nuvem eletrônica de uma molécula ou átomo, gerando um dipolo que induz as demais moléculas ou átomos a também formarem dipolos. Na fase sólida, formam cristais moleculares. He(l), Ne(l), CO2(S), Br2(l), I 2(s) Forças de natureza elétrica, que ocorrem entre moléculas polares, de modo que a extremidade negativa do dipolo de uma molécula se aproxime da extremidade positiva do dipolo de outra molécula. Na fase sólida, orienta a posição de cada molécula no espaço, formando os cristais dipolares. HBr, HCl, HI, H2S, PH3 Forças de natureza elétrico do tipo dipolo permanente, porém bem mais intensas. Ocorrem quando a molécula possui hidrogênio ligado a um elemento muito eletronegativo: flúor F, oxigênio O ou nitrogênio N, de modo que o hidrogênio de uma molécula estabelece uma ponte (ligação) com o átomo muito eletronegativo de outra molécula. H2 O, HF, NH3 Número de Oxidação (Nox) É o número que designa a carga elétrica real ou aparente de um átomo em função da diferença de eletronegatividade entre ele e seus ligantes. Regras Substância simples = 0 Íon simples = carga de íon A soma dos Nox de todos os átomos da molécula = 0 Metais alcalinos e a Ag = + 1 Metais alcalinos-terrosos e o Zn = +2 Alumínio, Bismuto e Boro = +3 Silício = +4 Fluor = -1 Principais ânions Monovalentes fluoreto O2- óxido Cl- cloreto O2 2- peróxido Br- brometo S2- sulfeto iodeto SO32- sulfito hipoclorito SO42- sulfato ClO2- clorito S2 O3 2- tiossulfato ClO3- clorato CO32- carbonato I - ClO- CIO4 Halogênios em qualquer halogeneto = - 1 Oxigênio: normal = -2 peróxidos= -1 superóxidos= -½ fluoretos= +1 e +2 Hidrogênio: normal= +1 Nox +7 a -7 Fe2(SO4)3 + Fe2S3O12 NH4 CaCO3 +2 +4 -2 +3 +6 -3 +1 -2 +18 perclorato SiO32- metassilicato NO3 - nitrato SiF62- fluorsilicato CN cianeto HPO3 2- fosfito OCN- cianato CrO4 2- cromato SNC- tiocianato Cr2O72- dicromato PO3 - metafosfato MnO42- manganato H2 PO2 - hipofosfito MnO32- manganito AlO2- aluminato SnO2 2- estanito 2- estanato MnO4 - permanganato hidróxido PbO2 2- plumbito H- hidreto PbO3 2- plumbato Trivalentes H+ Ag+ Mg2+ Fe2+ Al3+ Au3+ + + 2+ 2+ 3+ Li Cu Ca Mn Bi Fe3+ Na+ Au+ Sr2+ Pb2+ Co3+ Sb3+ Trivalentes PO4 33- K+ NH4+ Ba2+ Sn2+ Cr3+ As3+ AsO3 Rb+ H3O+ Ra2+ Pt2+ Ni3+ B3+ AsO4 3- 2+ 2+ + Cs Zn Cu Co2+ Ni2+ SbO3 Pt 4+ 4+ Sn 4+ Pb Pentavalentes 4+ Mn 3- 5+ As 5+ Sb zincato S2 O6 2- hipossulfato S2 O7 2- pirossulfato Tetravalentes fosfato P 2O74- pirofosfato arsenito P 2O64- hipofosfato arseniato SiO44- silicato 4- ferrocianeto antimoniato BO33Fe(CN)6 ZnO2 2- antimonito Fe(CN)6 SbO4 3- Cd2+ Tetravalentes SnO3 OH- -24 = 0 Bivalentes oxalato nitrito Principais Cátions Monovalentes C2 O4 2- NO2 - -3 +4 = +1 +2 +4 -6 = 0 +6 - - hidretos iônicos = -1 Bivalentes F- borato 3- ferricianeto 31 Funções Inorgânicas: Veja o quadro que resume as principais funções inorgânicas Função Ácidos: Conceito de Arrhenius Bases: Conceito de Arrhenius Sais Óxidos Peróxidos Superóxidos Hidretos Definição e Exemplos São soluções aquosas iônicas que possuem como único cátion o hidrônio H3 O+, formado pela reação entre a água e determinados compostos covalentes. Exemplos: HCl(aq), H2SO4(aq), H3PO4(aq) São compostos capazes de se dissociarem na água liberando íons, mesmo que muito poucos, dos quais o único ânion é o hidróxido OH1Exemplos: NaOH, Ca(OH)2, Al(OH)3 Propriedades Conduzem corrente elétrica, possuem sabor azedo e mantêm incolor uma solução de fenolftaleína. Só conduzem corrente elétrica as bases de metais das famílias 1 e 2. Possuem sabor adstringente e mudam a cor de uma solução de fenolftaleína para vermelho. Só os sais predominantemente iônicos São compostos capazes de se dissociaconduzem corrente elétrica, na fase rem na água liberando íons, mesmo que líquida ou em solução aquosa. Possumuito poucos, dos quais pelo menos um em sabor salgado e mantêm ou cátion é diferente de H3O+ e pelo menos mudam a cor de uma solução de um ânion é dirente de OH1-. fenolftaleína conforme o caráter ácido Exemplos: NaCl, NaHCO3, Mg(OH)Cl ou básico. Os óxidos de caráter iônico conduzem São compostos binários (formados por corrente elétrica na fase líquida. Com dois elementos), onde o oxigênio é o exceção do CO, NO e NO2 , que são elemento mais eletronegativo e apresenneutros, podem manter ou mudar a ta NOX= 2-. cor de uma solução de fenolftaleína Exemplos: CO2 , CaO, Al2O3 conforme reajam com a água formando ácido ou base. São compostos binários formandos pelo O H2 O2 é molecular e se decompõem oxigênio ligado a metais da família 1 ou em meio básico em O2 e H2O. os 2 prata ou zinco, onde o oxigênio apredemais são iônicos, reagem com água senta NOX = 1-. produzindo base e H2 O2 e com ácido Exemplos: H2O2, Na2O2, ZnO2 produzindo sal e H2 O2. São compostos binários formandos pelo São extremamente instáveis. Reagem oxigênio e metais das famílias 1 ou 2, onde com água produzindo base, H2O2 e O2 . o oxigênio apresenta NOX médio 1/2Reagem com ácido, produzindo sal, Exemplos: Na2O4, K2O4, CaO4 H2O2 e O2 . Os hidretos metálicos são instáveis e São compostos que possuem o hidrogêreagem com água de modo violento nio como elemento mais eletronegativo. produzindo base e H2 . Os hidretos Exemplos: NaH, MgH2, LiAlH4 moleculares são estáveis e tóxicos. Características Gerais dos Ácidos Característica Definição Exemplos Nomenclatura Ácido + nome do ânion com terminação: trocada de eto para ídrico trocada de ito para oso trocada de ato para ico H2S(aq): ácido sulfídrico H2 SO3(aq): ácido sufuroso H2 SO4(aq): ácido sulfúrico Presença de oxigênio Oxiácidos possuem oxigênio na fórmula. Hidrácidos não possuem oxigênio HClO3(aq), H3 PO4(aq), HNO3(aq) HCl(aq), HCN(aq), H2 S(aq) Grau de ionização Fortes: > 50% ou R > ou = 2 Semifortes: 5% < ou = < ou = 50% ou R < 2 Fracos: < 5% ou R < 2 Onde R = y - x para HxEz Oy Fortes: HCl(aq), HI (aq), H2SO4(aq). Semifortes: HF, H3PO4 Fracos: HCN, H3BO3 Ponto de ebulição Ponto de ebulição alto: ácidos fixos Ponto de ebulição baixo: ácidos voláteis H2SO4(aq) (340°C) e H3PO4(aq) (213°C) HCl(aq) (-85°C), HCN(aq) (26°C) Características Gerais das Bases Nomenclatura Solubilidade em água Força ou grau de dissociação 32 Definição Exemplos Hidróxido + de + nome do cátion NaOH: hidróxido de sódios Fe(OH)2: hidróxido de ferro II Fe(OH)3 : hidróxido de ferro III São solúveis as bases de metais alcalinos e de amônios. As bases de metais alcalino-terrosos são pouco solúveis e as demais são praticamente insolúveis. São fortes as bases de metais alcalinos. Semifortes as bases de metais alcalinoterrosos. As demais bases são fracas. O hidróxido de amônio é instável NaOH: 0,95 (mol/L)2 Ca(OH)2: 1,3 . 10-6 (mol/L)3 Fe(OH)3: 6,0 . 10-38 (mol/L)4 Fortes: LiOH, NaOH, KOH Semifortes: Mg(OH)2 , Ca(OH)2 Fracas: AgOH, Zn(OH)2 , Al(OH)3 <NH4 OH(aq)> NH3(g) + H2 O(l) Características Gerais dos Sais Característica Definição Exemplos Nomenclatura Nome do(s) ânion(s) + de + nome(s) do(s) cátion(s) MgBr2 : brometo de magnésio Caráter em solução aquosa Solubilidade em água O caráter do sal depende do cátion e do ânion dos quais ele é formado. Sabendo que o cátion do sal vem da base e o ânion do sal vem do ácido, temos: Sal ácido: cátion de base fraca e ânion de ácido forte Sal básico: cátion de base forte e ânion de ácido fraco Sal Neutro: cátion de base forte e ânion de ácido forte ou cátion de base fraca e ânion de ácido fraco De modo geral são solúveis os sais que contêm cátion de metal alcalino, metal alcalino-terroso e amônio, e também os sais que contêm ânion nitrato, e halogenetos (com exceção dos halogenetos de Ag1+, Pb2+ e Cu1+). Os demais são poucos soluveis ou praticamente insolúveis. Sal ácido: Al2 (SO4)3. sulfato de alumínio Sal básico: NaHCO3, bicarbonato de sódio ou carbonato "ácido" de sódio Sal Neutro: NaCl, cloreto de sódio Solúvel: NaCl, KNO3 , MgSO4 Pouco Solúvel: PbCl2, CaSO4 Quase insolúvel: BiS, Ba3(PO4)2 Características gerais dos Óxidos Característica Óxidos Iônicos Óxidos Covalentes Exemplos Nomenclatura óxido + de + nome do cátion Óxido + de + prefixo de quantidade + nome do elemento Na2 O: óxido de sódio CuO: óxido de cobre II CO2 dióxido de (mono)carbono SO3: trióxido de (mono)enxofre Caráter básico ácido (anidridos) Na2 O e CuO são básicos CO2 e SO2 são ácidos Reações Reagem com água produzindo base e reagem com ácido produzindo sal e água Reagem com água produzindo ácido e reagem com base produzindo sal e água Na2O(s) + H2 O(l) 2NaOH(aq) CO2(g) + H2O(l) H2CO3(aq) SO3(g) + 2KOH K2 SO4(aq) + H2O(l) Além dos óxidos descritos, temos: Óxidos neutros: Não possuem caráter ácido nem básico. São todos covalentes: Ex: CO, NO e N2 O. O gás N2 O e conhecido como gás hilariante, pois ao ser inalado produz uma sensação de euforia. Óxidos anfóteros: reagem com água formando base, reagem com base como se fossem ácido formando sal e água e reagem com ácido com se fossem bases, formando sal e água. São formados por elementos de eletronegatividade média, que podem ser metais ou semimetais. Classificação das Reações Químicas Equação química: É a representação gráfica e abreviada da reação química. 2H2 reagentes (1° membro) + ½ O2 2H2O produtos (2° membro) Equação iônica: É a equação química em que aparecem íons, além de átomos e moléculas. H+ + OH- H2O Reação de Síntese ou Adição CaO+H2O Ca(OH)2 Reação de Análise ou Decomposição H2 O2 H2 O + O2 Pirólise: calor Fotólise: luz Eletrólise: eletricidade Reação de Deslocamento ou Simples Troca Fe + 2HCl FeCl2 + H2 Reação de Dupla Troca ou Dupla Substituição NaCl + AgNO3 AgCl + NaNO3 Reações de óxi-redução - aumenta o nox: oxidação (perde elétrons) - diminui o nox: redução (ganha elétrons) - agente oxidante: substância onde encontra-se o elemento que reduz - agente redutor: substância onde encontra-se o elemento que oxida Relações de Massa 1 Mol --- M --- 6,02x1023 entidades químicas 1 Mol --- 22,4 L (CNTP) Estequiometria - Lei de Lavoisier: a reação deve estar sempre balanceada. - Pureza e Rendimento: valores teóricos equivalem a 100% Soluções: São misturas de duas ou mais substâncias que apresentam aspecto uniforme. As soluções são sistemas homogêneos formados por uma ou mais substâncias dissolvidas (soluto) em outra substância em maior proporção na mistura (solvente). Aspectos quantitativos das Soluções massa da solução = massa do soluto + massa do solvente m = m1 + m2 Unidades de Concentração 1) Concentração comum (C) C m1 V Unidades: g/L, g/mL, g/cm3 , g.L-1 Obs.: 1 L = 1000 mL = 1000 cm3 2) Densidade (d) d m V Unidades: g/L, g/mL 3) Título e porcentagem em massa (τ ou T) T m1 m1 m2 Ex.: O soro glicosado possui 5 g de glicose em 95 g de água. Calcule o título e a porcentagem em massa. 33 T= 5 = 0,05 x 100 = 5 % 5+95 Obs.: Título ou porcentagem em volume Ex.: o álcool é formado por 96 mL de etanol e 4 mL de água. T = 96 = 0,96 x 100 = 96% 96 + 4 4) Molaridade ou Concentração molar ou Concentração em mol/L (M) M= m1 Mol x V(L) Obs.: o volume deve ser necessariamente em Litros. Unidades: mol/L ou M (molar) Relações entre C, T, d, M C = d x T = M x Mol Obs.: C e d em g/L calor absorvido ou liberado na formação de 1 mol de substância, a partir das substâncias simples no estado padrão. Entalpia de calor liberado na combustão total de combustão 1 mol de substância no estado Hc padrão. calor liberado na neutralização de 1 Entalpia de equivalente-grama de um ácido por neutralização um equivalente-grama de uma base Hn no estado padrão Entalpia de formação H0f Energia de ligação É a quantidade de calor absorvida na quebra de um mol 23 (6,02.10 ) de ligações no estado padrão. H>0 Lei de Hess A quantidade de calor liberada ou absorvida numa reação química depende dos estados inicial e final da reação. TERMOQUÍMICA É o estudo das quantidades de calor liberadas ou absorvidas durante as reações químicas. Exotérmicas: São as que liberam calor. CH4(g) + 2O2(g) CO2(g) + 2H2O(l) + 212,8 Kcal/Mol CINÉTICA QUÍMICA É o estudo da velocidade das reações químicas e dos fatores que nela influem. Velocidade média: Vm t Fatores que influem na velocidade das reações: Temperatura, Eletricidade, Estado físico, Pressão, Luz, Concentrações dos reagentes Catalisador: É a substância que aumenta a velocidade da reação, sem ser consumida durante o processo. O catalisador diminui a energia de ativação e não altera o H da reação. EQUILÍBRIOS QUÍMICOS Reação reversível é aquela que se processa simultaneamente nos dois sentidos. aA + bB V1 cC + dD V 2 Endotérmicas: São as que absorvem calor. Cl2(g) 2 Cl(g) - 57,9 Kcal/Mol V1 = velocidade da reação direta V2 = velocidade da reação inversa Constante de equilíbrio: KC [C]c. [D]d [A]a. [B]b Kc = constante de equilíbrio em função das concentrações molares [ ] = concentrações molares no equilíbrio. Kp d p cC. pD p aA pbB Kp = constante de equilíbrio em função das pressões parciais p = pressões parciais no equilíbrio ECA = energia do complexo ativado Hf = entalpia final Hi = entalpia inicial H = variação de entalpia H H f Hi EA = energia de ativação energia mínima que as moléculas devem possuir ao se chocarem, para haver reação. Estado padrão (convenção) Temperatura: 25°C ou 298 K Pressão: 1 atm ou 760 mmHg Estado físico: mais comum Forma alotrópica: mais estável Entalpia das substâncias simples: H = 0 Deslocamento do equilíbrio Concentração A adição de uma substância desloca o equilíbrio no sentido em que será consumida (lado oposto). A retirada de uma substância desloca o equilíbrio no sentido em que será refeita (mesmo lado). Pressão Um aumento de pressão desloca o equilíbrio no sentido do menor volume. Uma diminuição de pressão desloca o equilíbrio no sentido de maior volume. Temperatura Um aumento de temperatura desloca o equilíbrio no sentido endotérmico. Uma diminuição da temperatura desloca o equilíbrio no sentido exotérmico. ESCALAS DE pH E pOH [H+] . [OH- ] = 10-14 [H+] = [OH-] solução neutra [H+] > [OH-] solução ácida [H+] < [OH-] solução básica pH + pOH = 14 pH = 7 solução neutra pH > 7 solução básica pH < 7 solução ácida Tipos de entalpia 34 ELETROQUÍMICA sp3: 4 lig. simples (tetraédrica) sp2: 1 lig. dupla (trigonal plana) sp: 1lig. tripla ou entre 2 duplas (linear) Pilhas Oxidação Redução Ânodo Cátodo Pólo negativo Pólo positivo Corrosão Deposição Elétrons migram da oxidação para a redução - Representação oficial de uma pilha: ânodo//cátodo - Cálculo da voltagem: ∆E = ERed maior – ERed menor Química Orgânica Classificação de cadeias Aberta (alifática ou acíclica): Normal ou ramificada Saturada ou insaturada Homogênea ou heterogênea Fechada (cíclica): Alicíclica ou aromática Alicíclica (sat. ou insat. e homog. ou hetg.) Aromática (mononucleada ou polinucleada) Destilação Fracionada do Petróleo Hibridação e geometria do Carbono Funções Orgânicas 35 Isomeria plana 36 Isomeria espacial Reações Orgânicas * Esterificação ácido carboxílico + álcool éster + água * Oxidação de Álcool álcool primário aldeído ácido carboxílico álcool secundário cetona álcool terciário não sofre oxidação * Hidrogenação de alcenos e alcinos Quebra de ligação dupla ou tripla e acréscimo de H2 Bioquímica * Glicídios oses (monossacarídeos): aldoses (glicose) cetoses (frutose) osídios: dissacarídeos (sacarose) polissacarídeos (amido e celulose) * Lipídios - óleos: obtido a partir de ácido graxo insaturado - gordura: obtida a partir de ácido graxo saturado 37
Baixar