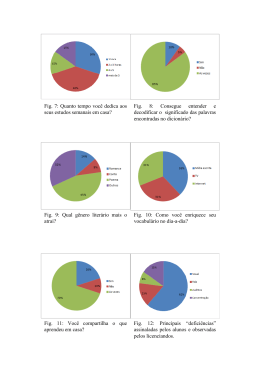
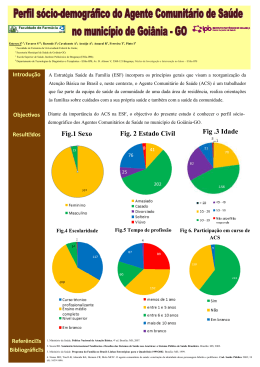
A propagação in vitro de plantas. CULTURA DE TECIDOS O que é isso? Cultura de tecidos vegetais - uma ferramenta fundamental no estudo da biologia moderna de plantas. L. Pedro Barrueto Cid Biólogo M.Sc. Ph.D Embrapa/Cenargen - Área de Biologia Celular Autor do livro "O método científico, o cientista e a sociedade", pela editora da Universidade do Amazonas. [email protected] Fotos do autor Definição Antecedentes históricos A propagação in vitro de plantas, Figs.1 e 2, chamada também micropropagação, é uma técnica para propagar plantas dentro de tubos de ensaios ou similares de vidro (por isso, o termo in vitro), sob adequadas condições de assepsia, nutrição e fatores ambientais como luz, temperatura, 02 e CO2. É uma parte importante de biotecnologia, conjuntamente com outras duas áreas: DNA recombinante e fermentação. A cultura in vitro, apresenta diferentes modalidades conforme os objetivos de sua aplicação, como por exemplo, cultura de protoplastos; anteras; calos (Fig. 3); células em suspensão (Fig. 4); sementes (Figs. 5 e 6),etc. A teoria da totipotencialidade formulada por Matthias Schleiden & Theodor Schwann, em 1838, pode ser dita que constitui um dos primeiros fundamentos da cultura in vitro, embora seus formuladores nem tenham imaginado uma metodologia como essa. A teoria afirma que a célula é autônoma, portanto, que contém o potencial necessário para originar um organismo completo; nesse caso, uma planta completa. É claro que essa capacidade deve manifestar-se sob especiais condições de estímulo. Em decorrência desta teoria, células com diferentes fenótipos dentro da planta têm idéntico genótipo. Haberlandt, um fisiólogo vegetal austro-húngaro, por volta de 1902, imbuído dessa teoria, foi o primeiro a manipular um sistema de cultura in vitro de plantas, procurando estabelecer e consolidar um sistema de micropropagação. Infelizmente, por limitações técnicas da época, seus esforços falharam. Contudo, alguns anos mais tarde a partir dos trabalhos de Robbin (1922) e White (1934) em ponta de raízes; cultura de embriões, por La Rue (1936); cultura de calos, por Gautheret Nobécourt (1939); enriquecimento de meios nutritivos com leite de coco, por van Overbeek, 1941; uso de plantas de tabaco como modelo experimental para estudo de morfogênese, por Skoog, desde 1944, e uso de meristemas apicais na obtenção de plantas livres de vírus, por Morel & Martin, 1952, abriram-se as estradas que a cultura de tecido de plantas percorreria triunfalmente ao longo de todo o século XX, com mais e mais descobertas e aplicações. Importância Fig.1: Plântula de café cv Rubi, crescida in vitro e obtida a partir 16 Biotecnologia Ciência & Desenvolvimento de gema axilar de uma outra plântula similar a ela. Assim por diante, outros clones podem ser obtidos A cultura in vitro de plantas, é uma técnica que não apenas apresenta importância prática na área florestal e agrícola, mas, também na científica básica. Dentro do campo da biologia de plantas talvez seja uma das técnicas mais polivalentes. Assim, através da cultura de protoplastos, podem-se hibridizar variedades diferentes, vencendo barreiras genéticas. Através da cultura de anteras, podem-se obter plantas haplóides, que logo depois podem-se diploidizar e transformar-se em homozigotos, isto é, indivíduos que produ- zem um só tipo de gameta para um determinado locus. Com a cultura de células em meio líquido, podem-se obter mutantes, isto é, genótipos que ganharam ou perderam alguma característica específica. Com a cultura de embriões e meristemas, podem-se fazer trabalhos de criopreservação para conservar materiais em bancos de germoplasmas, com economia de espaço e dinheiro, especialmente em espécies de reprodução assexuada como batata, mandioca, abacaxi etc. Com a cultura de meristemas apicais, pode-se pensar em obter plantas livres de vírus, e com a cultura de gemas axilares (Fig.7), propagar milhares de plantas, com genótipos superiores, por exemplo resistentes a nematóides, Fusarium etc. (Fig.8). Na mesma linha de raciocínio, a embriogênese somática (Fig.9), pode fornecer grandes quantidades de plântulas que podem servir de base para plantios no campo, tanto na área florestal quanto na agronômica e na hortigranjeira. Por outro lado, a cultura de tecidos dá suporte técnico a trabalhos de transformação na área da genética e na obtenção de plantas transgênicas, hoje, assunto da moda e muito controvertido. No campo da aplicação básica, a cultura de tecidos dá suporte técnico também à bioquímica, à fisiologia vegetal, à fitopatologia e à citogenética. Na bioquímica, para estudo e dilucidação de rotas metabólicas. Na fisiologia, para estudos de crescimento e desenvolvimento, efeito de metais pesados etc., na fitopatologia, para estudos de toxinas; e na citogenética, para estudos de cromossomos ou aberrações cromossômicas (quebras cromossômicas). Apesar de toda essa diversidade de técnicas, a cultura de tecido é uma só, e o denominador comum de todas elas é: a assepsia, o explante, o meio nutritivo e os fatores ambientais: luz, temperatura, C02 e 02. Assepsia Será entendida como um conjunto de procedimentos para tornar um explante livre de microrganismos (bactérias, fun- Fig.2: Plântula de banana obtida in vitro e transferida para terra em casa de vegetação gos filamentosos, leveduras etc). A respeito de como evitar microrganismos que possam contaminar o explante, é inevitável o uso de antissépticos, sejam estes bacteriostáticos ou germinicidas. Esses antissépticos podem ser antibióticos ou de outra natureza, como álcoois (álcool etílico); halogênios (hipoclorito de sódio); sais de metais pesados (bicloreto de mercúrio), fungicidas orgânicos etc. Em relação à vidraria e aos meios de cultura, estes devem ser esterilizados para que se destruam todos os microrganismos, por calor seco (forno, ar quente) ou úmido (autoclave). Pinças bisturis e Fig.3: Calo friável oriundo de raízes de plântulas de eucalipto in vitro (Eucalyptus grandis x E.urophylla) demais utencilios metálicos para a manipulação do tecido podem ser esterilizados por flambagem direta, como por exemplo: lamparina com álcool ou bico de Bunsen na câmara de fluxo laminar, ambiente este axênico (livre de germes) portanto, adequado para o trabalho in vitro. Explante Dentro da terminologia da cultura de tecidos, em geral, explante é qualquer segmento de tecido oriundo de uma planta para iniciar uma cultura in vitro, geralmente com as vistas a estabeler um protocolo de plantas de genótipo superior. Assim, o explante pode ser um ápice radicular ou caulinar, uma gema axilar (Fig.7), um segmento de folha jovem (Fig. 10), uma antera, um ovário, um embrião zigótico, etc. Esses explantes poderão devir plantas diretamente, ou passar por uma etapa intermediária de calo, antes de a planta ser obtida. Um calo é uma massa de células não diferenciadas do ponto de vista organogênico (brotos, raízes, frutos etc), que está em contínua proliferação celular, podendo ser compactos, friáveis, esbranquiçados ou amarelados Fig. 3, etc. Podemos realizar indução de plântulas a partir de um calo, com hormôBiotecnologia Ciência & Desenvolvimento 17 Fig.4: Aspecto microscópico de um conglomerado de células em suspensão, obtidas a partir de calos friáveis de raízes de plântulas de eucalipto in vitro nios vegetais ou reguladores do crescimento (estes últimos de ação hormonal, mas de origem sintética). Assim, numa reviravolta espetacular (morfogênese) o calo começa a induzir brotos, mas a base molecular do fenômeno na célula, ainda não é especificamente conhecida, por isso também a dificuldade de extrapolar protocolos de micropropagação de uma espécie para outra, ou de uma variedade para outra. Contudo, muitas vezes, a incapacidade de induzir brotos pode estar relacionada com a poliploidia ou com aberrações cro- mossômicas. Por outro lado, discute-se muito se a obtenção de plantas via calo é um bom sistema para clonar plantas com fins comerciais. Embora a preocupação seja pertinente, há também nessa preocupação muita carga especulativa. Dentro da biologia, clone é um termo de origem botânica e representa a idéia de plantas que se originam de uma mesma matriz e, supostamente, possuem o mesmo genótipo. Em cultura de tecidos, isso não necessariamente pode ser verdade, por isso, então, essa dificuldade de aceitar sem suspeitas plantas via calo. Quando essa variabilidade morfogenética acontece a denominamos variação somaclonal, embora ela seja indesejável para a propagação clonal, ela possui muito potencial no estudos de melhoramento de plantas. Meio nutritivo a) sais minerais Se uma planta no solo precisa para crescer de elementos minerais que são absorvidos pelas raízes, quanto mais um explante, que é, por definição, um pedaço de tecido separado da planta mãe. E que elementos minerais são esses? Os estudos da nutrição de plantas provenientes do âmbito da fisiologia vegetal informam que os elementos que compõem o meio nutritivo da cultura in vitro devem pertencer à categoria dos essenciais, isto é, a planta não se desenvolve na ausência deles. Existem dois grupos deles: os macronutrientes e os micronutrientes. Entre os primeiros, podem-se citar: fósforo, magnésio, nitrogênio etc.; entre os segundos, boro, manganês, cobre etc. Os primeiros são adicionados em forma de sal, acima de 100 mg/l até o máximo de 2.500, como no caso de KNO3 em B5, enquanto os segundos, na quantidade de fração de miligramas, uns poucos miligramas por litro (máximo 27 mg no caso do Fe em FeSO4. 7H2O). Não sendo o selênio, rubídio e outros, essenciais para a planta, não formam parte dos meios nutritivos mais utilizados: tais como MS, B5, White, Heller. Embora a manipulação desses meios constitua um processo de receituário, existe muito fundamento fisiológico na sua utilização; por exemplo, balanço líquido de cátions e ânions na solução; antagonismo iônico (o aumento da absorção de um diminui a do outro); percentagem crítica de um elemento (consumo de luxo); influência do pH na disponibilidade dos sais para a planta; absorção diferencial de íons entre tipos de planta, exemplo: árvores e gramíneas, estas últimas mais exigentes em bases; transporte ativo de íons a nível celular; enfim, são conhecimentos que podem auxiliar de modo importante no estabelecimento de um protocolo de cultura de tecidos para uma espécie. b) componentes orgânicos: Fig.5: Fruto de mamão (Carica papaya L. cv tainung 1) mostrando aspectos e quantidade de sementes por fruto 18 Biotecnologia Ciência & Desenvolvimento sacarose Um meio nutritivo também possui componentes orgânicos, entre eles, sacarose, vitaminas e inositol, para citar os mais utilizados. A sacarose é importante como fonte de carbono para alimentar a glicólise e o ciclo de Krebs, devido a que, inicialmente, o tecido, explante, não é suficientemente autotrófico. De um outro ponto de vista, a sacarose, quando em presença de auxina, pode contribuir para a diferenciação do câmbio em benefício de novas formações de xilema e floema. Em alho, altas con- centrações de sacarose (6%) têm melhorado ostensivamente sua bulbificação. Sua concentração normalmente varia entre 1% a 3 %, mas, por efeito da autoclavagem e do pH, sua concentração no meio pode variar, já que é hidrolizada em glicose e frutose, sendo que esses limites não são claros e esse problema pode tornar-se limitante para o explante ou para a planta. vitaminas São substâncias requeridas por animais e plantas, embora estas últimas sejam mais autônomas quanto à sua Fig.6: Germinação de sementes de mamão sob condições in vitro, após síntese. As vitaminas são importantes ter-se retirado a sarcotesta e realizado sua assepsia fatores catalíticos de rotas metabólicas na célula. Nos trabalhos pioneiros da cultura de tecido, os requerimentos de ser encontrado como pertencente ao mentos variam segundo as plantas, senvitaminas foram satisfeitos mediante su- complexo vitamínico B e necessário ao do que, no meio de cultura, as monocoplementos de composição pouco co- crescimento de leveduras e de células tiledôneas são muito sensíveis à sua nhecidos, como extrato de leveduras, de animais (mamíferos) in vitro. falta. No MS, o meio mais universalmenleite de côco, hidrolizado de proteínas, Na área de cultura de tecidos vege- te utilizado, sua prescrição é 100 mg/ extrato de malte, etc. Hoje, apesar de tais, muitos o consideram uma fonte litro. essa tendência não haver desaparecido, complementar de carboidrato, mais o mais freqüente, é que, os meios nutri- que um composto vitamínico, e que agentes gelificantes tivos incorporem vitaminas específicas desempenha um papel importante na São necessários, considerando que o como B1 (tiamina), B6 (piridoxina), áci- formação de pectinas e hemicelulose explante e as plantas obtidas devem do pantotênico, ácido nicotínico, ácido na parede celular. Seu uso data, apro- ficar sobre um suporte, para não afundaascórbico etc. ximadamente, de 1951, e é decorrente rem. Em geral, os meios sólidos são Não obstante as plantas sepreferidos aos de cultura líquirem capazes de sintetizar suas da, sendo que estes últimos são próprias vitaminas, fica a dúvida mais caros pelo fato de exigirem se a incorporação no meio é um agitador para evitar o afogasempre necessária. Contudo, em mento ou a hipoxia do explante. se tratando de drenos, raízes, por O agente gelificante forma exemplo, a suposição de que com a água um gel que funde a nem todos os seus requerimen100°C e que solidifica por volta tos nutricionais orgânicos sejam dos 45°C; não é hidrolizado por sintetizados ficou evidenciada já enzimas e, aparentemente, não em 1930, quando pesquisadores reage com o resto de ingrediencomo Bonner, Robbins, White tes do meio. etc, observaram que, na presença O ágar-ágar é um tipo de de algumas vitaminas (tiamina, agente gelificante de natureza Fig.7: piridoxina, ác. nicotínico, etc.), o polissacarídica produzido por Prévia assepsia, gema caulinar de abacaxi (Ananas algas (Gelidium amansii), sencrescimento das raízes (tomate, ervilha e rabanete) melhorava comosus L. Merr. Cv Pérola) cultivada in vitro do que sua composição em posensivelmente. lisacarídeo pode variar de 50% a Com respeito à quantidade a ser do fato de que, em muitos casos, sua 90 %, por isso, a procedência do mesmo incorporada, ela varia desde fração de incorporação ao meio de cultura pro- é importante. Por outro lado, a autoclamiligramas até 10 miligramas por litro, moveu diferentes eventos: formação vagem pode hidrolizá-lo se o pH do podendo ser esterilizada por filtração ou de gemas, crescimento de calos etc. meio está ácido, fazendo com que perca autoclavagem. Convém lembrar que, em algumas plan- firmeza e, dependendo da marca, o tas, o myo-inositol está conjugado com agente gelificante pode apresentar immyo-inositol a auxina, sendo essa uma forma de purezas, como cloro, bário, sulfato etc, Este composto também descrito como estocar ou transportar aquele hormô- que podem afetar o crescimento dos meso-inositol, é um isômero do inositol nio, ou, conjugado, em alguns tipos de explantes. o que, apresenta importância biológica, sementes, com o ácido fosfórico, forGelrite (Merck) é um outro tipo de já que participa da internalização de mando o ácido fítico. agente gelificante. Produzido pela bacestímulos externos a partir de receptores A respeito da sua aplicação, a infor- téria Pseudomonas elodea, é usado em de membrana. Na literatura médica, pode mação disponível é que os requeri- menor quantidade (2,5 g/l); uma vez Biotecnologia Ciência & Desenvolvimento 19 solidificado, é transparente, o que facilita a observação da raiz e focos de contaminação. Com íons, como Ca++ e Mg++, forma um elo mais firme do que com cátions monovalentes (K+ e Na+). Devem-se ter cuidados porque, às vezes, os agentes gelificantes, incluída a agarose, podem induzir hiperhidricidade (vitrificação) nos brotos ou plântulas obtidas. A hiperhidricidade é uma anomalia do tecido, na qual este fica rígido e quebradiço (glassy shoot), havendo malformação de estômatos na plântula e dificuldade para enraizar. É um fenômeno complexo e depende também de outros fatores como umidade, amônia, citocinina, pH etc. hormônios Estes representam o alma mater da cultura de tecido, porque são eles que direcionam o processo morfogenético. Agrupam-se tradicionalmente em 5 grupos: auxinas, citocininas, giberelinas, etileno e ac. absícico, sendo, os três primeiros os mais usados na micropropagação. Por exemplo, sob condições in vitro, uma planta de abacaxi pode ser clonada através de uma gema axilar, a qual, é induzida a produzir inúmeros brotos com citocinina, que, depois de alongados com giberelinas, podem ser enraizados com auxina e transferidos para terra em casa de vegetação. Quando se fala de hormônios, é sempre oportuno registrar uma diferenciação terminológica importante. Trata-se dos chamados reguladores de crescimento, que são substâncias que têm ação similar aos hormônios, porém, têm origem sintética. Assim, o ácido indol acético (AIA) e o Picloram são duas auxinas, mas, enquanto o primeira é hormônio, a segunda é um regulador de crescimento, que, na prática laboratorial, terminam sendo chamados de hormônios. Em geral, tanto uns como outros são usados na ordem de uns poucos µM até 40 µM. No caso do meio ter carvão ativado, pode-se aumentar a concentração em até 100 µM. Por outro lado, as auxinas e giberelinas 20 Biotecnologia Ciência & Desenvolvimento tidas em freezer ou refrigerador. Fatores ambientais: Fig.8: Plântula de abacaxi oriunda de uma gema caulinar. Por micropropagação milhares dessas plântulas (clones) podem ser obtidas podem ser dissolvidas em NaHO (0,1 1 N) e as citocininas em HCl também na faixa de 0,1 - 1 N. Em doses maiores produzem efeitos tóxicos ou teratológicos ou ainda inibirem a fotosíntese, como é o caso da auxina sintética 2,4D ( ácido 2,4-diclorofenoxiacético). No caso de seu uso em quantidades pequenas, é aconselhável obtê-los de soluções estoques que devem ser man- Fig.9: Embriões somáticos de café, obtidos a partir de explantes foliares de cv Rubi luz Luz e temperatura são dois fatores importantes nas salas de cultura, onde devem ser controlados para que as plantas ali mantidas se desenvolvam adequadamente. São raras as salas de cultura com iluminação constante. A luz é importante para a planta sob três pontos de vista. Do ponto de vista da fotossíntesse, da fotomorfogênese e do fototropismo; por isso, a sua inclusão numa sala de cultura. Nessa sala, a luz deve seguir um determinado fotoperíodo, por exemplo, 16 h luz e 8 de escuro, sendo que, nas prateleiras a irradiância (densidade de fluxo radiante por superfície, W m-2, ou densidade de fluxo de fótons, µmol m-2 s-1)1 pode variar de 8 a 15 W m2 . Embora nas salas seja usada luz branca fluorescente, a composição espectral pode variar conforme as marcas comerciais oferecidas. Algumas podem apresentar mais irradiação na região do azul / violeta (perto de 71 kcal/Einstein ); outras, na região do laranja / vermelho ( cerca de 43 kcal/Einstein) Essas variações podem representar impactos diferentes na cultura in vitro, segundo a espécie em questão. Assim, em alguns casos, uma luz mais rica em vermelho que azul pode, por exemplo, estimular melhor a indução de raízes adventícias. Já em outros casos, a luz azul pode estimular mais a brotação de calos que outros comprimentos de onda, mas esta também pode contribuir a quebrar a molécula de AIA. De modo geral, a luz branca estimula a indução de brotos, porém, tende a inibir a indução de raízes. Entretanto, é bom lembrar que o nível de irradiância é importante na resposta morfogenética. Sendo assim, uma irradiância baixa (3 W m-2) pode ser mais efetiva que uma irradiância alta (12 W m-2) na indução de brotos a partir de calos, ou vice-versa. Pode-se contornar o problema de se obterem maiores ou menores irradiâncias com o número de lâmpadas por pra- teleira ou determinando que altura deverá ter a prateleira. Para a cultura in vitro, irradiâncias maiores que 15 W m-2 podem reduzir a fotosíntesse das plantas, o que não necessariamente pode acontecer em condições de campo. Irradiâncias maiores na sala de cultura obviamente contribuirão para elevar a temperatura dos frascos, embora se saiba que, em café, irradiâncias altas não reduziram a fotosíntesse quando a temperatura foliar permaneceu constante a 25 °C. temperatura Em geral, nas salas de cultura, a temperatura a ser usada varia entre 24º e 27°C. É importantíssimo contar com um sistema de refrigeração acionado por termostato para manter fixa a temperatura. O fato de os reatores das lâmpadas ficarem fora da sala de cultura, ajuda, ou senão, o uso de reatores eletrônicos, que não esquentem. Mesmo com todas as precauções de manter as variações de temperatura sob controle, sempre temos nas placas ou tubos de ensaios problemas de condensação da água nas paredes desses materiais. Existem câmaras ou incubadoras que evitam esse problema, mas seu preço é proibitivo. Com respeito às necessidades eventuais de temperaturas alternadas entre o dia e a noite, é preferível usar incubadoras para lograr isso. 02 e C02 Existe pouca informação sobre o microclima gasoso dentro do tubo de ensaio. De qualquer maneira, a presença deles é importante para a respiração do explante ou para a fotossíntesse da plântula. No que diz respeito à respiração aeróbica-(glicólise + ciclo de Kreb), considerando apenas um tecido heterotrófico, e em se tratando de tubos de ensaio, podemos supor que, no volume disponível acima do meio sólido, existe, inicialmente, uma concentração e uma pressão parcial do 02 equivalente à atmosférica (25 °C e 1 atmosfera); isso é:, 8,6 mM e 0,2 atmosfera, respectivamente, embora esse valor, no decorrer do tempo, possa Fig.10: Explante foliar de café, mantido no escuro, insinuando, após 30 dias, formação de calo pela ação de um regulador de crescimento presente no meio nutritivo diminuir no interior do tubo e a respiração anaeróbica, supostamente, não começará a operar antes da repicagem seguinte do material. É provável que, em níveis de 0,3 mM e 0,07 atmosfera de pressão parcial do 02 no espaço interior do tecido (explante, calo etc.) essa respiração rapidamente comece a operar e, com isso, iniciar-se a morte do explante. Isso levanta a questão sobre a transferência periódica do material, o volume do frasco e a permeabilidade ou não da tampa. A concentração de C02 de 350 µl / l no ambiente externo não necessariamente reflete a concentração de C02 no ambiente interno do tubo de ensaio. Muitas vezes ela pode ser maior no tubo, devido à respiração da plântula no período noturno. Por outro lado, no caso de uma plântula com irradiância de 60 µm m-2 s-1 e aquela quantidade de C02 rapidamente deveria ultrapassar o ponto de compensação. Contudo, parece que essas interações são mais complexas do que parecem, porque existem evidências de que a presença de sacarose no meio pode deprimir a rubisco, reduzir a fotosíntesse e, conseqüentemente, a utilização de C02 e, dessa forma, a plântula não apresentará sinais de crescimento satisfatório e provocará reações de desconcerto no observador, sobre as possíveis causas de seu não crescimento. Tentou-se aqui apresentar uma visão sinóptica do que seja a cultura de tecido in vitro e sua importância para a biologia de plantas. No campo econômico, sem ir muito longe, basta lembrar que, através dessa técnica, a floricultura movimenta milhões de dólares e de plantas anualmente. Na Embrapa /Cenargen (Brasília DF) usamos essa técnica em quatro frentes: na micropropagação , na criopreservação, na conservação de germoplasma e na transformação, todas elas, visando a uma agricultura mais moderna e competitiva para o país. Bibliografia BARRUETO CID, L.P. (Ed.). Introdução aos hormônios vegetais. Brasília: Embrapa Recursos Genéticos e Biotecnologia,2000. 205 p. No prelo. BARRUETO CID, L.P.; MACHADO, A. C.G.; CARVALHEIRA, S.B.C.; BRASILEIRO, A.C.M. Plant regeneration from seedling explants of Eucalyptus grandis x E. urophylla. Plant Cell, Tissue Organ Culture, v.56:17-23,1999. BUCHANAN, B.B.; GRUISSEM, W.; JONES, R.L. Biochemistry & molecular biology of plants. Rockville: American Society of Plant Physiologist, 2000. 1367 p. DODDS,J.H.; ROBERTS, L. Experiment in plant tissue culture. London: Cambridge Unv. Press, 1982. 178 p. FOSKET, D.E. Plant growth and development. A molecular approach. San Diego: Academic Press, 1994. 580 p. GEORGE, E.F. Plant propagations by tissue culture. Part 1-2. Edington: Exegetics Ltd, 1993/1996. 1361 p. PIERIK, R.L.M. In vitro culture of higher plants. Drodrecht: Martinus Nijhoff Pub.,1987. 344 p. REDLIN, S.C.; CARRIS, L.M. Endophytic fungi in grasses and woody plants. Minnesota: APS Press, 1996. 223 p. Biotecnologia Ciência & Desenvolvimento 21
Baixar