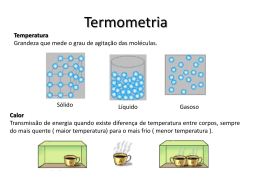
Unidade VI - Temperatura, Calor e Transferência de Calor fig. VI.1. Temperaturas em nosso planeta. Na segunda parte da figura podemos ver o calor intenso da superfície solar. 1. Situando a Temática Calor é uma das formas de energia mais fáceis que o homem pode detectar em seu meio ambiente, pois temos a sensação de frio, quente, suamos, tomamos líquidos quando sentimos calor, vemos o motor de um carro esquentar, tomamos banho de água aquecida por um chuveiro elétrico ou uma caldeira, etc. Os conceitos de calor, temperatura e transferência de calor são fundamentais, além de nosso cotidiano, na física, na engenharia e nos processos industriais. Nestes últimos podemos citar as máquinas térmicas, as quais têm como base a transferência de energia produzida pela diferença de temperatura. 2. Problematizando a Temática Calor é uma forma de energia, ele é a energia cinética e potencial do movimento aleatório das moléculas, átomos, elétrons e outras partículas. Hoje em dia o calor é chamado de energia térmica. Entretanto no passado os cientistas não tinham uma ideia clara do que era o calor. Propôs-se ser um fluido, chamado fluido calórico. O primeiro experimento que veio a dar uma evidência do calor como uma forma de energia, foi o experimento de Rumford, que mostrou que a energia mecânica perdida no atrito é convertida em calor. Nesta unidade vamos definir temperatura, incluindo escalas de temperatura e métodos para determinar a temperatura. Depois vamos discutir como as dimensões e o volume de um corpo, se alteram com a variação de temperatura. Passamos a estudar o conceito de calor, o qual descreve a transferência de energia produzida pela diferença de temperatura, calculando a taxa dessa diferença. O objetivo desta unidade é mostrar como os conceitos de temperatura e calor se relacionam, com objetos macroscópicos, deixando para as unidades seguintes os aspectos microscópicos. Esta unidade também servirá de base conceitual para estudarmos a termodinâmica: a qual estuda a energia interna dos sistemas – energia térmica - e como essa energia é transferida de um sistema a outro. 57 3. Temperatura Temperatura, do nosso cotidiano, é a medida de como alguma coisa está quente. Na verdade veremos que a temperatura é proporcional a energia cinética média dos átomos em uma substância. O calor é a energia que flui entre dois objetos devido à diferença de temperatura. Se dois objetos estão em contato eles deverão, após um certo tempo, ter a mesma temperatura. Dois objetos em uma mesma temperatura estão em equilíbrio térmico. Esta é a base para podemos ter uma medida física de temperatura e para construirmos um termômetro usamos: Se um corpo A está em equilíbrio térmico com um corpo C e um corpo B está em equilíbrio térmico com o corpo C, então A está em equilíbrio térmico com B. Muitas vezes esta afirmativa é chamada de lei zero da termodinâmica. Para associarmos um número à medida de temperatura, arbitrariamente toma-se 273,15 K como sendo o ponto triplo da água. Este ponto ocorre quando coexistem as fases: líquido, sólido e vapor da água. Essa escala de temperatura é chamada Kelvin ou absoluta. Nessa escala, 0 K é o zero absoluto, o ponto em que classicamente os átomos param de se movimentar. Um termômetro padrão é feito com uma quantidade pequena de gás contido em um frasco. A pressão do gás é proporcional a sua temperatura numa escala Kelvin e ele é calibrado de forma que o ponto triplo da água seja 273,15 K. Em uma escala Kelvin a água ferve a 1 atm numa temperatura de 373,15 K, isto é, 100 K acima do ponto triplo. A escala de temperatura Celsius é definida como TC TK 273,15 eq. VI. 1 Assim o zero absoluto está a uma temperatura degelo da água está a 273,15 0 C ou 0 K, e o ponto de ebulição da água é de 100 0 C ou 373 K. A escala Fahrenheit é definida por TF 9 TC 320 5 eq. VI. 2 4. Expansão Térmica Quando a temperatura de um sólido ou líquido aumenta, os átomos vibram de forma mais intensa, tendendo a expandir. Algumas exceções 0 existem, como por exemplo a água que contrai entre 0 0 C e 4 C. Se um corpo está a uma temperatura T0 e tem um comprimento L0 , quando ele passa a ter uma temperatura T, L L0 T onde é o coeficiente de dilatação térmica. 58 eq. VI. 3 A área e o volume de um corpo também variam com a variação de temperatura, A 2A0 T eq. VI. 4 onde A0 L0 L0 a uma temperatura T0 e 1 . De forma similar para um pequeno cubo de lado L0 , o volume V0 L30 varia para um volume V, com a mudança de temperatura. Então, para um coeficiente de dilatação volumétrica 3 , V 3V0 T eq. VI. 5 5. Calor e Energia Térmica A energia interna, também chamada energia térmica de um sistema é o movimento aleatório de átomos e moléculas do sistema e está associada à energia cinética e potencial desse sistema. Quando um sistema a uma temperatura T é colocado em uma vizinhança em que a temperatura é diferente, a energia é transferida para dentro ou para fora do sistema. Calor é a energia transferida entre um sistema e suas vizinhanças por causa das diferenças das temperaturas. O fluxo de calor Q > 0 quando o fluxo é para dentro do sistema e Q < 0 quando o calor vai para fora do sistema. O calor tem como unidade o Joule. Temos que 1 cal = 4,186 J e 1 Btu = 252 cal. Note que a energia interna de um sistema muda se calor é adicionado ao sistema ou se um trabalho é realizado sobre ele. Enquanto pressão, volume e temperatura são propriedades de um sistema, calor e trabalho não são. 6. Capacidade Calorífica e Calor Latente Quando calor é adicionado a uma substância, ela se aquece a menos que ela mude de fase ( por exemplo gás, líquido ou sólido). A diferença de temperatura T depende da massa da substancia, do calor adicionado e da espécie do material. A quantidade de calor requerida para aumentar a temperatura de uma substância para 10 C é chamada a capacidade calorífica. A quantidade de calor necessária para aumentar a temperatura de de um 1g de uma substancia é chamado de calor específico c. Se Q é o calor que causa à massa m um aumento na temperatura de T , então c Q / mT , Q mcT eq. VI. 6 Note que o calor específico da água, c = 1 cal/g. 0 C é muito maior do que muitas das outras substâncias. As fases da matéria são sólido, líquido e gás (ou vapor). Um gás em contato com a forma líquida da mesma substância é dito um vapor. Energia deve ser adicionada a uma substância de maneira a mudar o estado da 59 matéria. A energia que deve ser adicionada ou removida para causar a transição de sólido para líquido em 1 kg de um dado material é chamada de calor latente de fusão L f . Se a transição for de líquido para gás similarmente teremos calor latente de vaporização L v . 7. Transferência de Calor Quando dois sistemas ou objetos interagem e estão a temperaturas diferentes, a energia térmica fluirá daquele mais quente para o mais frio. Ao pegarmos uma panela quente no fogo podemos queimar nossa mão, já que o calor da panela pode passar para nossa mão que está a uma temperatura mais baixa. Existem três mecanismos de transferência de calor que veremos a seguir. Se aquecermos uma barra de metal, por condução, os átomos começam a vibrar mais intensamente e transmitir isto de forma aleatória. Os metais possuem muitos elétrons livres que podem contribuir para a condução do calor. fig. VI.3. Transferência de calor por radiação, Considere uma barra de um material de área de convecção e condução. secção transversal A e espessura x . Uma face é mantida a uma temperatura T1 e a outra face a uma temperatura T2 como mostra a fig. VI. 2. Experimentalmente a energia térmica Q que flui na barra num tempo t é Q kA(T / x) , onde T T2 T1 e k é a condutividade térmica do material. Podemos escrever para o fluxo de calor na barra para uma mudança de temperatura T H dQ dT kA dt dx eq. VI. 7 fig. VI.3. Barra de um certo material aquecida a duas temperaturas diferentes. A transferência de energia térmica por movimento de material é chamada de convecção. A convecção natural resulta do fato de quando um gás ou líquido é aquecido ele expande e ascende carregando energia térmica com ele. Esse processo é que determina de forma geral o tempo climático. Esse também é o mecanismo para circulação da água nos oceanos, rios e lagos, essencial para vida. Todos os objetos emitem radiação eletromagnética, e essa radiação carrega energia. A potência radiada de uma superfície de área A a uma temperatura T é dada pela lei de Stefan-Boltzmann, P eAT 4 eq. VI. 8 A emissividade e, que depende da natureza da superfície, está entre 0 e 1 e não tem dimensão. A constante 5,57 10 8 W / m 2 K , com a temperatura sendo expressa em K. Quando a temperatura aumenta, as 60 frequências de radiação aumentam seus valores. Se um objeto está a uma temperatura T e em sua vizinhança a temperatura é T0 , a taxa de energia perdida é P eA(T 4 T04 ). Exercícios Resolvidos Exemplo VI. 1 Em qual temperatura na escala Fahrenheit é lida: (a) a mesma na escala Celsius; (b) a metade da escala Celsius; (c) duas vezes aquela da escala Celsius? Solução: TF TC em TF 9 TC 32 , então 5 TF 40 0 F . O restante se faz de forma análoga. Exemplo VI. 2 0 0 Ouro derrete a uma temperatura de 1064 C e entra em ebulição a 2660 C. Expresse essas temperaturas em Kelvin. Solução: Use a equação TC TK 273 para calcular as temperaturas em kelvin e não em gruas Kelvin. Exemplo VI. 3 0 Uma barra de aço tem 12 m de comprimento quando instalada num portão a 23 C. 0 De quanto seu comprimento muda quando sua temperatura muda de -32 C para 0 55 C? Para o aço 1,1 10 5 / 0C . Solução: L L0 T 0,011m Exemplo VI. 4 Um reservatório de 200 cm 3 feito de vidro é preenchido com mercúrio. Qual 0 volume de mercúrio que transborda quando a temperatura aumenta para 30 C? Solução: O volume de mercúrio crescerá por VHg Hg V0 T 0,18 10 3 / 0 C 200cm 3 30 0 C 1,08cm 3 O volume do reservatório de vidro crescerá por Vvidro 3 vidroV0 T 3 11 10 6 / 0 C 200cm 3 30 0 C 0,20cm 3 3 A diferença 0,88 cm é o volume que transborda. Exemplo VI. 5 0 Uma luva de latão de diâmetro interno 1,995 cm a 20 C está sendo mal colocada em um eixo de diâmetro 2,005 cm. Para qual temperatura deve a luva ser aquecida para ajustar ao eixo? 1,9 10 6 / 0C . Solução: L L0 T T L L L0 = 263 0 C T T T 283 0C 0 L0 L0 61 Exemplo VI. 6 Um nova engrenagem é composta por um pistão que contém 0,60 kg de aço, com calor específico 0,11 kcal/kg. 0 C e 1,2 kg de alumínio (calor específico = 0,214 0 kcal/kg . C ). Quanto de calor é requerido para aumentar a temperatura do pistão de 0 0 20 C para a temperatura de 160 C? Solução: Q m aço c aço T m al c al T 45,19 kcal. Exemplo VI. 7 Enquanto uma pessoa dorme ela tem uma taxa de metabolismo de aproximadamente 100 kcal por hora. Essa energia flui do corpo como calor. Suponha que a pessoa mergulha em um tanque com 1200 kg de água a uma 0 temperatura de 27 C. Se o calor flui para água, de quanto a temperatura da água aumenta ao passar 1h? Solução: Temos que o calor perdido pela pessoa em uma hora é igual ao calor ganho pela água em uma hora. Então teremos, 0 100 mágua c água T 1200 1 (T 27) T 27,08 C. Logo a água 0 aumenta 0,08 C. Exemplo VI. 8 Uma bala de chumbo de 4 g vai a uma velocidade de 350 m/s e se choca com um bloco de gelo a uma temperatura de 0 0 C. Se o calor gerado pelo atrito derrete o gelo, quanto de gelo é derretido? O calor latente de fusão do gelo é de 80 kcal/kg e 0 seu calor específico é 0,5 cal/g. C. Solução: A energia cinética perdida pela bala é igual a energia ganha pelo gelo. Daí teremos, 1 m b v 2 m gelo L f m gelo 0,17 g . 2 Exemplo VI. 9 Uma barra de cobre de 24 cm de comprimento tem uma área de seção transversal de 2 4 cm . Um dos extremos é mantido a 24 0 C e o outro a uma temperatura de 0 184 C. Qual é a taxa de fluxo de calor na barra? O condutividade do cobre é 397 0 W/m C. Solução: H Q T 184 24 kA 397 4 10 4 106W , onde W é a unidade de t x 0,24 potência e o sinal indica a direção do fluxo com relação ao eixo x. Exercícios Propostos Exercício VI. 1 o 0 Expresse as temperaturas abaixo nas outras escalas. 98 C, -40 F e 77 K. 0 0 0 0 Resposta: 371 F e 208 K; -40 C e 233 K; -196 C e -321 F 62 Exercício VI. 2 Para manter inteira uma laje de concreto, muitas vezes é colocada madeira entre as 0 0 fendas. As variações de temperatura entre o inverno e verão são de -10 C e 35 C. Se a laje tem um comprimento de 10 m na temperatura do inverno, quanto aumenta o comprimento no verão? Resposta: 4,5 10 3 10 5 / 0 C. m. Exercício VI. 3 Rebites de alumínio são usados na construção de aviões e são confeccionados 0 maiores do que os buracos e levados ao resfriamento por gelo seco (CO 2 ) a -78 C antes de serem colocados nos buracos. Quando eles são deixados no lugar à 0 0 temperatura de 23 C eles se ajustam perfeitamente. Se um rebite a -78 C está inserido em um buraco de 3,2 mm de diâmetro, qual será o diâmetro do rebite a 2,4 10 5 / 0 C. 0 23 C? Para o alumínio, Resposta: 3,21 mm. Exercício VI. 4 0 Um tanque de gasolina de um caminhão tem 25 gal a uma temperatura de 23 C. 0 Depois expoem-se o tanque de aço e a gasolina ao sol a temperatura de 35 C. O coeficiente do volume de expansão para a gasolina é de 96 do o do aço 1,1 10 5 / 0 10 5 / 0 C que é maior C e assim alguma gasolina transborda o tanque. Qual a quantidade de gasolina que transbordou? 1 gal = 3,785 L. Resposta: 0,28 gal. Exercício VI. 5 0 0 A oitenta gramas de latão, calor específico 0,092 cal/g. C, a 292 C, é adicionado 0 200 g de água, calor específico 1 cal/g C, a 14 0 C, em um tanque isolado de capacidade calorífica desprezível. Qual a temperatura final do sistema? 0 Resposta: 23,9 C Exercício VI. 6 0 0 0 A 160 g de água a 10 C é adicionado 200 g de ferro (c = 0,11 cal/g C) a 80 C e 0 0 80 g de mármore (c = 0,21 cal/g C) a 20 C. Qual é a temperatura final da mistura? 0 Resposta: 18,6 C. Exercício VI. 7 Um coletor solar colocado sobre um telhado de uma casa consiste de uma folha de 2 plástico preto de área 5 m e por baixo está uma bobina de cobre pelo qual passa a água por dentro dos tubos dela. A intensidade de luz solar no coletor é de 1000 2 0 W/m . A água circula através da bobina e se aquece a 38 C. Supondo que toda a energia solar aquece a água, a que taxa, em litros por minuto, a água circula através da bobina? Resposta: 1,87 l/min. 63 Exercício VI. 8 Quantos cubos de gelo devem ser adicionados a uma vasilha contendo 1 litro de água em ebulição à temperatura de 100 0 C, desde que a mistura resultante alcance 0 uma temperatura de 40 C? Suponha que cada cubo de gelo tem uma massa de 20 g e que a vasilha e o ambiente não trocam calor com a água. Resposta: aproximadamente 25 cubos de gelo. Exercício VI. 9 Duas lajes de espessura L 1 e L 2 e área A, estão em contanto com suas superfícies a temperaturas T 1 e T 2 . Qual a temperatura na interface entre as duas lajes? Qual é a taxa do fluxo de calor? Resposta: T k1 L2T1 k 2 L1T2 , k1 L2 k 2 L1 H A(T2 T1 ) L1 / k1 L2 / k 2 Exercício VI. 10 A superfície do sol tem uma temperatura de 5800 K e o raio do sol é cerca de 7 8 10 m. Calcule a energia total radiada pelo sol a cada dia, supondo a emissividade 1. Resposta: 1,75 10 25 J. 64
Baixar