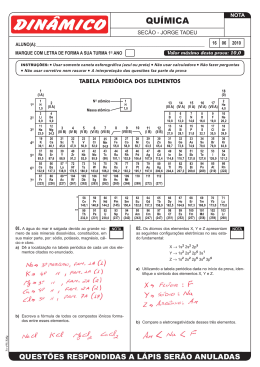
CENTRO EDUCACIONAL SIGMA :: 2ªsérie 2.2 QUÍMICA 1º período Dados: 1H, 2He, 3Li, 4Be, 5B, 6C, 7N, 8O, 9F, 10Ne, 11Na e 12Mg Constante de Planck (h) = 6,6.10-34J.s Velocidade da luz no vácuo (c) = 3,0x108 m/s. Convenciona-se que o 1º elétron a ocupar um orbital possui número quântico spin igual a - 1 2 QUESTÃO 1 Considere as seguintes informações sobre os átomos A, B e C. Seus números atômicos são 3x + 4, 4x – 1 e 2x + 10, respectivamente. Os íons A+ e C2+ são isoeletrônicos; A e C são isótonos; B e C são isóbaros; A soma dos números de nêutrons de A, B e C é igual a 61. Com base nas informações e apresentando os cálculos necessários, determine. (A) O número de massa de B: (0,3) (B) O número de atômico de A: (0,2) (C) O número de nêutrons de C: (0,2) (D) O somatório do número de prótons de A, B e C: (0,3) (A) Defina eletroafinidade. (0,3) (B) Escreva os elementos do quarto período em ordem decrescente de energia de ionização. (0,3) (C) Escreva os elementos do sexto período em ordem crescente de eletronegatividade. (0,2) (D) Escreva os Calcogênios em ordem decrescente de caráter metálico. (0,2) QUESTÃO 5 Indique a hora que o relógio marca, quando: QUESTÃO 2 As propriedades magnéticas das espécies químicas variam com alguns fatores como, por exemplo, a configuração eletrônica. (A) Faça a distribuição, em ordem crescente de energia, para o 23V3+ (0,5) (B) Qual íon gasoso, no estado fundamental, deve ser mais susceptível à atração de um campo magnético: 2+ ou 33As+? Justifique. (0,5) 23V QUESTÃO 3 Um dos grandes problemas enfrentados pela Química era construir uma teoria consistente que explicasse como os elétrons eram distribuídos nos átomos. Linus Pauling (1901-1994) desenvolveu um método baseado nos cálculos da mecânica quântica que comprovou experimentalmente que os elétrons são dispostos nos átomos em ordem crescente de energia. Baseando-se no diagrama de Linus Pauling e admitindo que a configuração eletrônica de um átomo é dada por [X]ns2(n – 1)d10npn+1, em que X é um gás nobre, determine o número atômico e o valor de n, para que a configuração eletrônica represente um elemento químico da família dos halogênios. (1,0) QUESTÃO 4 Na tabela a seguir, os elementos químicos são representados pelas letras que não correspondem aos seus verdadeiros símbolos. Analise-a e faça o que se pede. AVALIAÇÃO DISCURSIVA DE QUÍMICA :: 1º período | 2ª SÉRIE :: ENSINO MÉDIO | 22M1Qui_2014_pro.lwp (A) O ponteiro dos minutos aponta para o elemento de menor número atômico e o ponteiro das horas aponta para o elemento mais eletronegativo. (0,5) (B) O ponteiro dos minutos aponta para o metal alcalino terroso de menor raio atômico e o ponteiro das horas aponta para o gás nobre do segundo período. (0,5) QUESTÃO 6 Com base na configuração eletrônica, em ordem geométrica, 1ª Energia de ionização ( 1ª E.I) e Afinidade Eletrônica (A.E) dos elementos hipotéticos contidos na tabela a seguir, responda. Elemento A B C D E F Configuração eletrônica 1s22s2 2p6 3s2 3p6 4s1 1s2 2s2 2p6 3s2 3p1 1s1 2s2 1s2 2s2 2p6 3s2 3p6 3d3 4s2 1s2 2s2 2p4 1s2 2s2 2p6 3s2 3p5 1° E.I (KJ/mol) A.E (KJ/mol) 418,8 48,0 577,5 42,5 899,5 <0 650,3 <0 1.313,9 140,97 1.251,2 349,0 PÁG. 1 CENTRO EDUCACIONAL SIGMA :: (A) A que grupo e período pertence o elemento D? (0,2) (B) Qual dentre os elementos apresentados possui a maior tendência de formar cátion? (0,2) (C) Qual dentre os elementos apresentados possui a maior tendência de formar ânion? (0,2) (D) Escreva a equação de ionização para o elemento A. (0,2) (E) Escreva o nome da família ou o grupo do elemento A. (0,2) QUESTÃO 7 O molibdênio metálico tem de absorver radiação com frequência mínima de 1,00 % 1015 s–1 antes que ele emita um elétron de sua superfície via efeito fotoelétrico. (A) Calcule a energia mínima, em joule, para retirar 1 elétron de uma placa de molibdênio metálico. (0,5) (B) Calcule o comprimento de onda, em nm, associado a radiação. (0,5) QUESTÃO 8 O último elétron de um átomo neutro apresenta o seguinte conjunto de números quânticos: n=3; l=1; m=0; s=+ 1 . Determine o número atômico (Z) desse átomo. 2 (1,0) :: AVALIAÇÃO DISCURSIVA DE QUÍMICA :: 1º período | 2ª SÉRIE :: ENSINO MÉDIO | 22M1Qui_2014_pro.lwp PÁG. 2 CENTRO EDUCACIONAL SIGMA :: 2ªsérie 2.2 QUÍMICA 1º período :: 27 de março de 2014 QUESTÃO 1 QUESTÃO 3 (A) (0,3) (B) (0,2) (C) (0,2) (D) (0,3) Número atômico _______________________________________ (0,5) n: ________________________________________________________ (0,5) QUESTÃO 4 (A) (0,3) (B) (0,3) (C) (0,2) (D) (0,2) QUESTÃO 5 QUESTÃO 2 (A) (0,5) (B) (0,5) (A) (0,5) (B) (0,5) QUESTÃO 6 (A) (0,2) (B) (0,2) (C) (0,2) AVALIAÇÃO DISCURSIVA DE QUÍMICA :: 1º período | 2ª SÉRIE :: ENSINO MÉDIO | 22M1Qui_2014_pro.lwp PÁG. 1 CENTRO EDUCACIONAL SIGMA :: (D) (0,2) (E) (0,2) QUESTÃO 7 (A) (0,5) (B) (0,5) QUESTÃO 8 (1,0) AVALIAÇÃO DISCURSIVA DE QUÍMICA :: 1º período | 2ª SÉRIE :: ENSINO MÉDIO | 22M1Qui_2014_pro.lwp PÁG. 2
Baixar