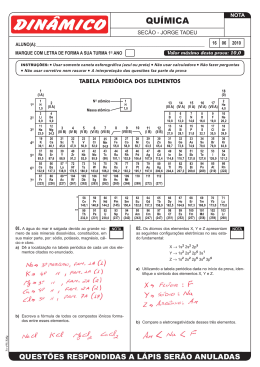
CENTRO FEDERAL DE EDUCAÇÃO TECNOLÓGICA DE SANTA CATARINA UNIDADE CURRICULAR: FUNDAMENTOS DE QUÍMICA ALUNO:................................................................................... DATA:......../........./........... Conceito:............................. 1) Dê o nome dos seguintes elementos, consultando a tabela periódica. O:...................................... Na:........................................ F........................................ Th:........................................ 2) (MackenzieSP) Pertence aos metais alcalinos o elemento: a) ferro b) cobre c) potássio d) oxigênio e) magnésio 3) (UFRS) Considerando a classificação periódica dos elementos, a afirmação correta é: a) O manganês é um metal e seu número atômico é 34,9. b) O bromo é um semimetal e pertence à família dos halogênios. c) O criptônio é um gás nobre e seu número atômico é 19. d) O zinco é um metal que, no estado fundamental, apresenta elétrons distribuídos em 3 camadas eletrônicas. e) O enxofre é um não metal com 6 elétrons na última camada. 4) (UFPA) Um átomo, cujo número atômico é 18, esta classificado na tabela periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 5) (UnimepSP) Um determinado elemento químico está situado no quarto período da tabela periódica e pertence à família 6A. O número atômico desse elemento é: a) 52 b) 34 c) 35 d) 33 e) 53 6) (PUC/CampinasSP) Robert Curl, Richard Smalley e Harold Kroto foram premiados com o prêmio Nobel de Química em 1996 por estudos relacionados com o fulereno, substância simples formada pelo elemento químico de configuração 1s2, 2s2, 2p2. Com essa configuração é possível afirmar que o elemento químico: a) está localizado no quarto período da classificação periódica. b) pertence à família dos halogênios. c) tem número atômico 12. d) é menos eletronegativo que o flúor. 7) Abaixo são mostradas quatro configurações eletrônicas, segundo o diagrama de Linus Pauling: I 1s2, 2s2, 2p6, 3s1 I 1s2, 2s2, 2p6, 3s2, 3p6, 4s2 III1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p5 IV 1s2, 2s2, 2p6, 3s2, 3p4 Os elementos químicos representados na sua configuração são: a) Na, Ba, Fe e Ne b) Ti, Zn, Hg, O c) Ti, Zr, Hg, F d) Na, Ca, Br, S e) Na, Ca, F, Mg 8) Qual é a fórmula do composto resultante da união de um elemento A, da família 1A, com outro B, da família 5A? 9) Considere as substâncias formadas pelas formadas a seguir: Ag, Fe, Zn, F2, H2, HF, CaCl2, HCl, NH3, H2O, NaF Sobre elas responda: a) Quais delas são substâncias iônicas? b) Quais delas são moleculares? c) Quais delas conduzem corrente elétrica no estado sólido? 10) Das seguintes substâncias, a única que não apresenta ligação covalente é: a) HCl b) H2O2 c) NH3 d) CO2 e) Al2O3 11) Um átomo X se liga a um átomo Y de número atômico igual a 20 através de ligação iônica. O átomo X é um metal ou um ametal? 12) Diga quais substâncias são polares e quais substâncias são apolares. a) HCl b) O2 c) CO2 d) F2 e) H2 13) A fórmula N=N indica que os átomos de nitrogênio estão compartilhando dois: a) prótons b) elétrons c) pares de prótons d) pares de elétrons e) pares de nêutrons 14) Os íons são formados a partir das propriedades dos elementos químicos. Observe as propriedades periódicas e as configurações eletrônicas dos elementos abaixo e indique o íon que será formado a partir de cada um deles. a) Cl b) Ca c) Zn
Baixar