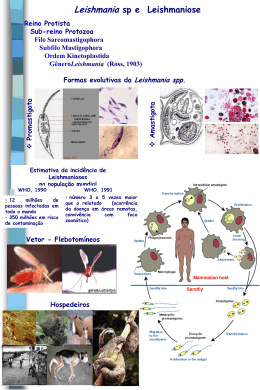
Leishmania e Leishmanioses Classificação Leishmania sp. Filo Sarcomastigophora Sub-filo Mastigophora Ordem Kinetoplastida Família Trypanosomatidae Gênero Leishmania Características gerais •Protozoário flagelado •Dois hospedeiros obrigatórios (igual ao T. cruzi /brucei ), heteroxénico • Habitat: - Vetor: lúmen do trato digestivo (Subgenus Leishmania: intestino anterior/médio) (Subgenus Viannia: intestino anterior/médio/posterior) - Hospedeiro vertebrado: células do sistema mononuclear fagocitário (SMF), principalmente Macrófagos Leishmaniose: Aspectos históricos e sociais • Doença benigna ou mortal, na forma cutânea deixa cicatrizes grandes (“botão do oriente”), doença conhecida na America do Sul antes da chegada dos espanhóis • Agente etiológico descrito primeiramente por Borovsky em 1898 em um paciente no Usbequistão • Leishman e Donovan (1903) descreveram o parasita independente- mente em um caso de calazar da Índia • Ross (quem descreveu o cíclo de vida do plasmódio) batizou o parasita em 1903 Leishmania donovani, e Wright denominou um parasita vindo de uma criança da Armênia (forma cutânea) Leishmania tropica • Em 1909, Lindenberg, Paranhos & Carini demonstraram a presença dos parasitos em lesões de pacientes brasileiros, Gaspar Vianna denominou-os Leishmania braziliensis e detectou em 1912 a ação curativa do tártaro emético • Em 1987, Lainson e Shaw sugerem um novo subgênero de Leishmania: o subgênero Viannia, que inclui espécies das Americas •Polimórfico: Promastigota Paramastigota Inseto Promastigota metacíclico Amastigota • Reprodução por divisão binária. Macrófago com amastigotas Hospedeiro mamífero Organização celular - Genoma com 36 chromossomos (L. major, Projeto genoma completo), 8305 genes identificados (4/2005). - K(C)inetoplasto, trans-splicing. Ciclo de vida Formas promastigotas metacíclicas regurgitadas por mosquitos são depositadas na derme, onde são fagocitados por macrófagos Vetores: Diptera, Phlebotomidae: Lutzomiya, Phlebotomus. Brasil: Lutzomiya longipalpis, L. wellcomei e outros Promastigotas dentro do fagolisossomo se transformam em amastigotas, que se multiplicam no macrófago. A célula hospedeira é rompida liberando amastigotas que são fagocitados por outros macrófagos ou DCs Macrófagos infectados com Leishmanias do subgênero Viannia (espécies das Américas) contém menos parasitas em vários vacúolos parasitóforos. Ajuda no diagnóstico por microscopia Subgênero Leishmania Subgênero Viannia Macrófagos infectados são ingeridos por Lutzomiya Após ingestão, amastigotas se transformam em promastigotas e se multiplicam dentro de uma membrana formada pelo vetor Promastigotas se desenvolvem para paramastigotas os quais aderem-se em pontos diferentes no trato digestivo. A proliferação é estimulada se a fêmea ingere sucos vegetais. (Critério da localização: subgenênero de Leishmania) Após 3-5 dias, promastigotas metacíclicos migram ativamente para partes anteriores do tubo digestivo. Assim, o parasita parece interferir ativamente com a capacidade de ingestão do hospedeiro mosquito! A saliva do flebotomíneo é muito importante para a infecciosidade da Leishmania (efeito imunomodulador). Somente promastigotas metacíclicos são infecciosos para os hospedeiro vertebrado! Patogenia e interação parasita-hospedeiro Após deposição de promastigotas na pele, o sistema complemento se liga na superfície do parasita, mais a clivagem de C3b em iC3b não permite ligação do complexo lítico. Proteína gp63 cliva o fator do complemento C3b para iC3b. iC3b Figure 1. Immune response against intracellular pathogens. Khan N, Gowthaman U, Pahari S, Agrewala JN (2012) Manipulation of Costimulatory Molecules by Intracellular Pathogens: Veni, Vidi, Vici!!. PLoS Pathog 8(6): e1002676. doi:10.1371/journal.ppat.1002676 http://www.plospathogens.org/article/info:doi/10.1371/journal.ppat.1002676 Figure 2. Pathogens modulate the expression of costimulatory molecules for their survival. Khan N, Gowthaman U, Pahari S, Agrewala JN (2012) Manipulation of Costimulatory Molecules by Intracellular Pathogens: Veni, Vidi, Vici!!. PLoS Pathog 8(6): e1002676. doi:10.1371/journal.ppat.1002676 http://www.plospathogens.org/article/info:doi/10.1371/journal.ppat.1002676 O sistema complemento ajuda na aderência das promastigotas nos macrófagos (receptor principal CR3). Interação de LPGs e gp63 com fibronectina também ocorre. Esta via de internalização não leva a produção de radicais de oxigênio ou NO (“silent entry”). Porque uma célula profissional do sistema fagocitário não consegue eliminar um parasita dentro do fagossomo? 1. A sinalização para ativação do macrófago está impedida pela ação do LPG: Tradução de sinais, mobilização de cálcio, ativação da proteína kinase C. Essentials of Glycobiology 2. Indução de resposta disfuncional: inibição da produção de radicais de OH e NO. Falha na apresentação em MHC2 após estimulação com IFN . Fosfoglicanos bloqueiam produção de IL-12. IFN 3. Proteina-tirosina quinases também são bloqueados Secreção de EF1 da Leishmania para o citossol. Ativação de SHP-1 (uma Phosphotirosina fosfatase). Inativação da Fosfotirosinaquinase: reação atenuada a IFN . A espécie infectante é importante para o fenótipo da patologia desenvolvida em indivíduos imunocompetentes (Leishmanias que no Brasil) (Leishmanias queocorrem ocorrem no Brasil) A expressão diferencial ou presença/ausência de genes provavelmente causa as diferenças nas patologias observadas Os diferentes tipos de Leishmaniose na clínica • Visceral ou Calazar (L. donovani, L. infantum, no Brasil causada por L. chagasi ): - Enfermidade crônica - Caracterizada por: • Febre irregular e de longa duração. • Hepatoesplenomegalia. • Linfoadenopatia. • Anemia com leucopenia. • Hipergamaglobulinemia. • Emagrecimento. • Edema. • Caquexia e morte se não for tratado, dentro de 2 anos. - Formas clínicas calazar: assintomática, oligossintomática, aguda e crônica •Tegumentaria: a) Cutânea: - Infecção confinada na derme, com epidermis ulcerada. - Velho mundo, L. tropica, L. major e L. aethiopica. - Novo mundo, leishmanias do complexo mexicana e braziliensis. - No Brasil: L. braziliensis, L. guyanensis, L. chagasi, L. lainsoni Leishmaniose cutânea (“oriental sore” “botão do oriente”, “Úlcera de Bauru”) Fonte SVS/MS b) Muco-cutânea: - Infecção na derme (úlceras), invasão de mucosa e destruição da cartilagem. - No novo mundo: L. braziliensis, L. guyanensis, L. mexicana (“espundia”), no Sudão/Etiópia L. major, L. tropica c) Cutânea difusa: - Infecção confinada na derme, formando nódulos não ulcerados. Disseminação por todo o corpo - Associado a deficiência imunológica do paciente - Novo mundo, L. pifanoi, L. amazonensis - Velho mundo, L. aethiopica Responsável pela patologia é o estado imunológico do hospedeiro. A predominância da resposta celular (Th1) leva a imunidade e cura, resposta humoral (Th2) leva às formas crônicas. Combate da infecção 1. Lise por complemento 2. Produção de IFN- 3. Ativação de macrófagos 4. Síntese de óxido nítrico (NO) Quais são os motivos para tanta diversidade de patologias na infecção? Forma Cutânea Há uma inflamação ativa. Células dentríticas apresentam antígenos em MHC2 e expressam ICAM-1. Ativação de Th1 por IFN e TNF resulta no recrutamento de células T CD8+ para a região infectada. Cura. Forma mucocutânea Forma Visceral Não há resposta Th1 e nem aumento da atividade Th2. Macrófagos infectados deixam de expressar ICAM1 e CD80 – falha na estimulação da resposta de células T-CD8+. Possivelmente, lipofosfoglicanos da Leishmania estão envolvidos. Diagnóstico: As Leishmanias são vistas nas formas amastigotas Diagnóstico Leishmaniose Tegumentaria • Clínico Características da lesão e dados epidemiológicos. • Laboratorial - Exame direto de esfregaços corados (Romanowsky, Giemsa ou Leishman). - Exame histológico. - Cultura. - Inóculo em animais. - PCR (reação em cadeia da polimerase, permite a identificação da espécie infectante). • Importante para exclusão de tuberculose cutânea, hanseníase, infecções por fungos, úlcera tropical, neoplasmas Diagnóstico Leishmaniose Tegumentaria • Imunológicos - Teste de Montenegro (teste da resposta contra formas promastigostas mortas do parasita, resposta celular). - Reação de imunofluorescência indireta (RIFI) (resposta humoral). - Hemaglutinação indireta. Diagnóstico Leishmaniose visceral (Calazar) CLÍNICO: Sintomas Febre baixa recorrente, envolvimento linfohepático, esplenomegalia, caquexia e dados epidemiológicos LABORATORIAL: 1. Exames Parasitológicos a) Demonstração direta do parasita Esfregaços corados com Giemsa ou Leishman de: -Material obtido por punção de medula óssea, fígado ou baço - Fase aguda 80-90% de positividade. - Fase sub-clínica 10%. - Co-infectados com HIV recomendado exame de medula ossea. - Aspirado esplênico 100 %, sangue periférico 30%. b) Isolamento em cultivo in vitro Aspirado ou biopsia LIT, MEM, Schneider’s e Evans (Meio monofásico) a 26ºC Exame microscópico ( 2x semana/4 semanas) c ) Isolamento em cultivo in vivo • Inoculação em animais - Hamsters ou camundongos isogênicos (BALB/c) - Cepas dermatotrópicas: pata ou tocinho dos animais (positivo após 2 a 4 semanas) - Cepas vicerotrópicas via intraperitoneal (positivo após 6 meses) - Recomendado para o isolamento do parasita nas formas subclínicas • Xenodiagnóstico - Flebótomos - Usado em pacientes com AIDS portadores de Leishmaniose visceral 2. Testes Imunológicos a) Teste de Montenegro. b) Testes serológicos. •Antígenos (parasitas inteiros, inativados) - Reação de aglutinação direta Cave: Reatividade cruzada com Chagas e tuberculose. Visualiza títulos até de 1:51.200. Leishmaniose visceral título > 1:1.600. (sensibilidade 100%) no Brasil o título > 1:6.400. c) Detecção do antigeno rK39 na urina. 3. Análise do DNA de material recolhido a) Por reação em cadeia da polimerase (PCR) Usa oligonucleotídeos espécie-específicos do DNA dos minicírculos do DNA do cinetoplasto. 100% sensível e mais específico que sorologia. b) Possibilita discriminação de espécies. Tratamento Leishmaniose Tegumentaria 1. Quimioterapia • Antimoniais Tártaro emético Antimonial trivalente. Glucantime (antimoniato de N-metil-glucamina) Antimonial pentavalente. Pentostan (estibogluconato de sodio) •Antimonial pentavalente •Inibe glicolise e síntese •Administração intramuscular ou intravenosa absorção rápida - Excreção rápida e pela urina, vida media 24 horas - Droga recomendada para os três tipos de leishmaniose * Pentamidina •Liga ao DNA, inibindo a replicação. •Inibe a dihidrofolate reductase, interfere com o metabolismo de poliaminas. •Administração intramuscular. •Excretado lentamente, é seqüestrado nos tecidos (tem uso profilático contra tripanossomiase). •Produz hipo- ou hiperglicemia. Anfotericina B •Lipofílico •Liga a esteróis (ergosterol) da membrana formando poros. Funciona como um ionóforo. •2-5% excretado na urina. •90% ligado a proteínas do plasma. •Meia vida 18 horas •Muito eficiente em nanopartículas mas muito caro (500-1000 USD)! Outras opções tratamento Leishmaniose Tegumentaria 2. Imunoterapia Leishvacin seriado. Leishvacin associado ao BCG. Leishvacin seriado associado ao BCG. Leishvacin associado ao BCG com Glucantime . Interferon gamma humano recombinante (Rhifn-) anti-IL10-receptor. Tratamento Leishmaniose visceral 1. Quimioterapia • Antimoniais Tártaro emético Glucantime • Pentamidina • Anfotericina B • Miltefosin 2. Imunoterapia Interferon gamma recombinante (Rhifn-) Br Med Bull. 2006 Jul 17;75-76:115-30 Ecologia dos Phlebotomíneos: Desenvolvimento e comportamento • 40-70 ovos por desova, agrupados em lugares humidos, eclodem depois 6-17 dias. • Larvas se nutrem de matéria orgânica por mais 15-70 dias, depois pupa (7-14 dias). • Adultos são ativos no crepúsculo ou a noite, durante o dia permanecem em lugares tranquilos: tocas, arvores ocas, currais, moradias. • Não sobrevivem bem em ambientes que não tenham pelo menos um mes T acima de 20°C “Mosquito palha” Macho Fêmea Medidas de prevenção • Identificação de focos de Leishmania. Animais infectados proximos aos domicílios Silvestres e domésticos: erradicação • Imunização em massa de cachorros (Leishvaccin) • Vacinas para seres humanos? Gold standard: uma infecção curada protege contra infecção homóloga com a mesma espécie • Componentes da saliva de Phlebotomíneos como vacina? Medidas de prevenção • Uso de repelentes, telas de proteção • Borrifação frequente de ambientes • Tratamento de sintomáticos e assintomáticos em regiões com alta incidência de flebotomíneos Dentistas Atenção na hora do tratamento de pacientes em área endêmica: eventuais lesões na boca Med. oral patol. oral cir.bucal (Internet) v.12 n.4 Madrid ago. 2007 Literatura L. Rey: Parasitologia Markell´s & Voge´s Medical Parasitology Vários reviews de Trends in Parasitology e outras revistas Links interessantes: http://www.hhmi.ucla.edu/parasite_course/Default.htm http://www.genedb.org/genedb/leish/index.jsp http://www.leishmaniasis.info/ Perguntas “Take home message” T. cruzi Qual é a forma infectante do T. cruzi para o ser humano? Por que o T. cruzi não é lisado dentro do fagolissomo? Além da infecção contaminativa, quais são outras vias de infecção com T. cruzi? Em qual ou quais ponto(s) do ciclo de vida o T. cruzi se multiplica? Cite três manifestações clínicas da infecção crônica por T. cruzi. Perguntas “Take home message” Leishmania 1. A cura de todas as pessoas portadores de Leishmania com a eliminação temporária de todos os flebotomineos irá eliminar a chance de infecção num município? 2. Qual é a forma infectante da Leishmania para seu hospedeiro mamifero? 3. Tratando alguém com Leishmaniose, como poderia se infectar? 4. Quais formas da Leishmaniose existem? 5. Porque o macrófago infectado muitas vezes não elimina o parasita infectante? IL-4 Leva a diminuição da expressão da subunidade da IL-12 nas células Th1. (Leva ao desenvolvimento de Th2) IL-12 Ativa as células NK, e células T (CD4+ e CD8+) para produzirem IFN-. IL-10 Abaixa a apresentação de antígenos e de produção de IFN-. Inibe a ativação do macrófago. NK IFN- Representam uma fonte inicial de IFN- Mediador da resistência inata contra o parasita, é uma citocina pró-inflamatória. No modelo L. major e camundongo
Baixar