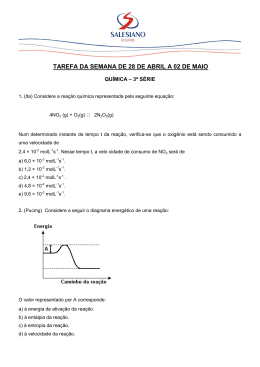
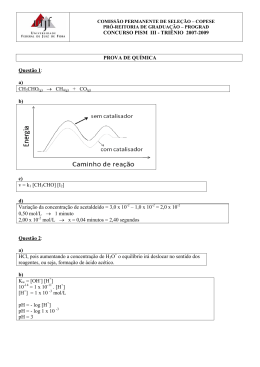
1º Q22 Esta prova contém T 5 B 14/04/10 questões. INSTRUÇÕES: Verifique se sua prova está completa. Preencha corretamente todos os dados solicitados no cabeçalho. Resoluções e respostas somente a tinta, azul ou preta. Utilize os espaços determinados para respostas, não ultrapassando seus limites. Evite rasuras e o uso de corretivos. Resoluções com rasuras ou corretivo não serão revisadas. Resoluções e respostas que estiverem a lápis não serão corrigidas. Boa prova! 01) [2,0 pontos] A velocidade da reação: Mg(s) + PbCl2(aq) → MgCl2(aq) + Pb(s) Depende dos dois reagentes. Indicar e explicar como a velocidade dessa reação é perturbada quando: a) a temperatura do sistema é diminuída. b) a pressão é aumentada. 02) [2,0 pontos] O gráfico a seguir foi construído de acordo com dois experimentos feitos a partir da equação: 3M+N→3Q+P a) Qual experimento foi mais rápido? b) Sabendo que o reagente M não participa da velocidade da reação, mas o reagente N triplica a velocidade da reação quando sua concentração é triplicada, defina a equação da velocidade da reação. c) Qual a ordem geral da reação? d) Se a reação fosse elementar, qual seria a equação da velocidade? 03) [2,0 pontos] Observe o seguinte diagrama: Com base nesse diagrama e considerando a reação direta A + B → C + D, responda as questões: a) Qual o valor da energia de ativação da reação química sem catalisador. b) Qual o valor da energia de ativação da reação química com catalisador. c) Qual o valor da variação de entalpia da reação química. d) Esse processo é endotérmico ou exotérmico? 04) [2,0 pontos] Os dados a seguir referem-se à cinética da reação entre o monóxido de nitrogênio (NO) e o oxigênio (O2), produzindo o dióxido de nitrogênio (NO2): NO (mol/l) 2,0.10-2 4,0.10-2 2,0.10-2 O2 (mol/l) 1,0.10-2 1,0.10-2 4,0.10-2 Velocidade (mol/l.s) 1,0.10-4 4,0.10-4 4,0.10-4 Com base nos dados: a) Calcule as ordens dos reagentes. b) Determine a expressão de velocidade para a reação. c) Calcule o valor da constante de velocidade. 05) [2,0 pontos] No laboratório, o hidrogênio pode ser preparado pela reação de alumínio com solução de ácido bromídrico. Observe as condições específicas nas experiências a seguir: Experiência Temperatura (ºC) Alumínio 1 2 3 4 5 70 70 70 80 80 Em pó Granulado Em raspas Em pó Em raspas Concentração do ácido em mol/l 1,5 2,0 2,0 2,0 1,5 a) Determine em qual dos experimentos a velocidade da reação é maior. b) Explique, através dos fatores que alteram a velocidade da reação, como você fez esta determinação.
Baixar

![[2,0 pontos] O gráfico abaixo refere](http://s1.livrozilla.com/store/data/000905646_1-195eb4a910ccbf5921989706f9439278-260x520.png)




![01)[2,0 pontos] O ácido acetilsalicílico, C9H8O4 , é uma substância](http://s1.livrozilla.com/store/data/001715210_1-a19b3f347349d7f82e11e8ccac3207fe-260x520.png)

