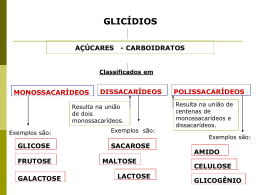
MACROMOLÉCULAS As macromoléculas poliméricas, embora longas, são entidades químicas altamente ordenadas, com sequencias específicas de subunidades monoméricas que dão origem a discretas estruturas e funções A estrutura única de cada macromolécula determina sua função. As subunidades monoméricas nas macromoléculas poliméricas ocorrem em sequencias específicas, representando uma forma de informação sobre a qual o estado de vida ordenada depende Relação entre estrutura e função em macromoléculas Nas proteínas, que exibem uma grande diversidade de funções, por exemplo: ◦ Uma sequencia de aminoácidos polimérica particular produz uma estrutura fibrosa forte, encontrada no cabelo e na lã ◦ Uma outra produz uma proteína que transporta oxigênio no sangue ◦ Uma terceira se liga a outras proteínas e catalisa a clivagem de ligações entre os seus aminoácidos Os açúcares unidos tornam-se armazéns de energia, fibras estruturais e ponto de reconhecimento molecular específicos Os núcleotídeos enfileirados no DNA ou RNA fornecem o projeto para um organismo inteiro Os lipídeos agregados formam membranas Composição Química da Célula CARBOIDRATOS • Os carboidratos são as biomoléculas mais abundantes na natureza. – A fórmula geral é: [C(H2O)]n, daí o nome "carboidrato", ou "hidratos de carbono“ – São moléculas que desempenham uma ampla variedade de funções, entre elas: • • • • Fonte de energia Reserva de energia Estrutural Matéria prima para a biossíntese de outras biomoléculas Características Existem três classes principais de carboidratos: ◦ monossacarídeos ou açúcares simples uma única unidade de poliidroxialdeído ou poliidroxicetona (D-glicose) ◦ Oligossacarídeos Cadeias curtas unidas por ligações glicosídicas (os mais comuns são os dissacarídeos) ◦ Polissacarídeos Mais de 20 unidade (amido, celulose, glicogênio) Monossacarídeos Cadeia carbônica não ramificada - todos os átomos de carbono estão unidos por ligações covalentes simples Livremente solúvel em água e insolúveis nos solventes não polares. A maior parte tem sabor doce Um átomo de carbono une-se por dupla ligação ao oxigênio formando o grupo carbonila O grupo carbonila em uma das extremidades Aldose O grupo carbonila Está em qualquer outra posição Cetose Os outros átomos de carbono têm ligados à grupamentos hidroxila Monossacarídeos 4 5 6 7 carbonos carbonos carbonos carbonos – – – – tetroses pentoses hexoses heptoses D-glicose (aldoexose) e D-frutose (cetoexose) são os monossacarídeos mais comuns na natureza Monossacarídeos Os monossacarídeos mais comuns ocorrem em formas cíclicas Os monossacarídeos com cinco ou mais carbonos ocorrem na forma cíclica (em sol.aquosa) O grupo carbonila forma uma ligação covalente com o oxigênio de um grupo hidroxila ao longo da cadeia A reação entre aldeído ou cetona e alcoóis formam derivados chamados hemiacetais ou hemicetais O átomo hemiacetal chamado anomérico de carbono do ou hemicetal é de carbono Essas formas cíclicas são chamadas de piranoses e furanose Os anéis de 6 átomos derivados do aldeído são chamados piranoses, pois se assemelham ao anel de 6 elementos do pirano. As aldohexoses também existem em formas cíclicas com 5 átomos e devido a semelhança com o furano são chamadas de furanoses O anel aldopiranosídico é muito mais estável que o anel aldofuranosídico e predomina nas soluções de hexoses LIGAÇÃO GLICOSÍDICA As ligações glicosídicas entre as unidades monossacarídicas são a base para a formação de oligo e polissacarídeos Um grupo hidroxila de um açúcar reage com o carbono anomérico de outro açúcar. As ligações glicosídicas podem ter várias formas, pois o C anomérico de um açúcar pode estar ligado a qualquer um dos grupo OH de um segundo açúcar para formar uma ligação α ou ß glicosídica. Os grupos OH são numerados e o esquema de numeração segue o dos átomos de C nos quais estão ligados. OLIGOSSACARÍDEOS Oligo = poucos. Os oligossacarídeos são formados pela união de 2 a 10 monossacarídeos, que se separam por hidrólise. Os mais importantes são os dissacarídeos - Quando duas moléculas de um açúcar simples (hexoses) se unem e liberam uma molécula de água • Sacarose= Glicose + Frutose • Lactose = Glicose + Galactose • Maltose = Glicose + Glicose POLISSACARÍDEOS ◦ Os monossacarídeos podem se combinar e formar macromoléculas, com longas cadeias de de frutose, glicose ou galactose. Estes são os chamados polissacarídeos. ◦ Os polissacarídeos são moléculas com mais de 10.000 unidades de açúcares. Existem centenas de polissacarídeos mas as mais comuns são o amido, a celulose, quitina e glicogênio. AMIDO Função de reserva nas células vegetais São polímeros de α-D-glicose. Contém dois tipos de polímeros da glicose: ◦ A amilose que consiste de cadeias longas não-ramificadas de unidades de D-glicose conectadas por ligações (α1→4) ◦ A amilopectina que consiste de uma cadeia altamente ramificada. As ligações glicosídicas unindo os resíduos de glicose são (α1→4) mas os pontos de ramificação (24 a 30 resíduos) são ligações (α1→6) Celulose Função estrutural nas células vegetais. Principal componente da parede celular. Substância fibrosa, resistente e insolúvel em água Maior massa da madeira e algodão Homopolissacarídeo linear e não-ramificado de 10 mil a 15 mil unidades de glicose Parece com amilose e com as cadeias principais de glicogênio Diferença: na celulose, os resíduos de glicose têm a conformação β Quitina Função estrutural Principal componente do exoesqueleto de aproximadamente 1 milhão de espécies de artrópodes Homopolissacarídeo composto por resíduos de N-acetil-D-glicosamina em ligação β Glicogênio Armazenamento nas células animais É um polímero de subunidades de glicose unidas por ligações (α1→4) e (α1→6) nas ramificações O glicogênio é mais extensamente ramificado (8 ou 12 resíduos) e mais compacto que o amido É abundante no fígado (7% do peso úmido do órgão) está também presente no músculo esquelético É hidrolisado por α-amilase • A glicose é o centro do metabolismo dos carboidratos, pois praticamente todos os glicídios podem ser convertidos em glicose. • Quase todas as células são capazes de atender as suas demandas energéticas apenas a partir da glicose. • A glicose constitui uma fonte de energia livre, que pode ser conservada como ATP, a principal forma de energia utilizável pelos seres vivos PROTEÍNAS PROTEÍNAS Diversas funções biológicas. Componentes mais abundantes nas células após a água (7% a 15%). Composta por aminoácidos. Os aminoácidos ligam-se entre si por ligações peptídicas. Monômeros – Polímeros. Vegetais são autônomos na produção de aminoácidos enquanto que os animais produzem alguns e outros obtém pela nutrição. Aminoácidos Naturais – Aminoácidos Essenciais (varia de espécie para espécie) FUNÇÃO ESTRUTURAL Construção de estruturas celulares e histológicas. Ex.: colágeno – resistência à tração (ossos, tendões, cartilagem e pele). Queratina – impermeabilizante (pele, unhas, cabelo) Albumina – viscosidade (sangue) Hormonal Estimular ou inibir a atividade de determinados órgãos. Ex.: insulina – manutenção da taxa de glicemia. Defesa Proteção do organismo. Antígeno – proteína invasora presente no organismo invasor. Anticorpo – proteína defensora combinase quimicamente com os antígenos neutralizando-os. Nutritiva Proteínas obtidas através da nutrição indispensáveis para os seres vivos produzirem outras proteínas. Ex.: vitelina (ovo) – formação do embrião. Reguladora Proteínas agregadas a vitaminas (co-enzima). Hipovitaminose – carência de vitaminas. Hipervitaminose – excesso de vitaminas. Enzimática Função catalítica Substrato – substância que sofre a ação de uma enzima. Condições para ação das enzimas (pH e temperatura). PROTEÍNAS São macromoléculas cujos monômeros são os aminoácidos Uma cadeia de aminoácidos é chamada de peptídeo as quais são classificadas em: O termo proteína é dado quando na composição do polipeptídio entram centenas, milhares ou milhões de aminoácidos AMINOÁCIDOS – ESTRUTURA BÁSICA Ligação Peptídica Aminoácido 1 Aminoácido 2 dipeptídeo Até 50 aminoácidos peptídeo Mais de 50 aminoácidos proteína LIGAÇÃO PEPTÍDICA AMINOÁCIDOS Essenciais – são aqueles aminoácidos que o organismo não consegue sintetizar. Logo a única forma de que dispomos para os obter é através da ingestão de proteínas. Não essenciais - são aqueles que o nosso organismo consegue produzir, mais concretamente, que o nosso fígado sintetiza. ESSENCIAIS NÃO ESSENCIAIS Arginina Alanina Histidina Asparagina Isoleucina Aspartato Leucina Cisteína Lisina Glutamato Metionina Glutamina Fenilalanina Glicina Triptofano Prolina Valina Serina Treonina Tirosina Estrutura da Proteína Primária Secundária Terciária Quaternária
Baixar