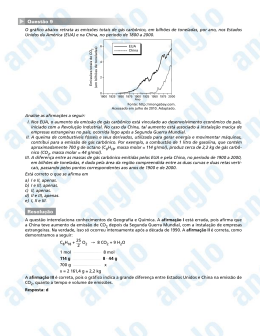
ACAFE – 2012/2 - Resolução da Prova de Química 33. Alternativa (A) Afirmação I. Correta. O termo carboidrato, apesar de antigo, ainda é usado para indicar os açúcares. Afirmação II. Correta. Observe as estruturas abaixo: Tanto a glicose quanto o etanol possuem o grupo hidroxila em suas moléculas. Afirmação III. Correta. Observe a estrutura abaixo. Afirmação IV. Correta. Durante a fermentação a bactéria aumenta a velocidade da reação. 34. Alternativa (C) A análise da estrutura do alginato revela que estão presentes os grupos hidroxila e carboxila, sua fórmula molecular é a citada na afirmação e é um copolímero pois é formada por dois monômeros diferentes, portanto estão corretas as afirmações I, II e II. Contudo a ligação entre os monômeros se dá pelos carbonos 1 e 4 das estruturas conforme figura abaixo. 35. Alternativa (D) Observando a quantidade de CO2 formada nas reações de combustão, nota-se que o etanol é menos poluente. Gasolina: C8H18 + 12,5 O2 → 8 CO2 + 9 H2O Etanol: C2H5OH + 3 O2 → 2 CO2 + 3 H2O 36. Alternativa (B) Somando e balanceando as reações teremos: C12H22O11 + H2O → 6 C2H5OH + CO2 342g ....................... 184 g 855g ....................... X g X = 460 gramas de álcool 37. Alternativa (C) Afirmação I. Errada. A geometria do CO2 é linear. Afirmação II. Correta. No CO2 ocorrem duas ligações duplas, logo possui elétrons PI em ressonância. Afirmação III. Correta. Nos refrigerantes e cervejas tem a função de gaseificar e acidular, nos extintores de incêndio tem a função de abafar e resfriar e no estado sólido é conhecido como gelo seco por sofrer sublimação. Afirmação IV. Errada. Em altas concentrações diminui o pH da água pois tende a formar o ácido carbônico. 38. Alternativa (C) Afirmação I. Correta. O principal constituinte do biogás é o metano. Afirmação II. Errada a estrutura do metano é tetraédrica. Afirmação III. Correta. Os momentos de dipolos das ligações C – H se anulam Afirmação IV. Correta. CH4 + 2 O2 → CO2 + 2 H2O 16g ..................................... libera 890 x 103J 5,6 x 103g ............................ liberam X J X = 3,11 x 10 8 J. 39. Alternativa (A) Primeiramente determinamos o volume do recipiente: P x V = m/mol x R x T; 3 x V = 72/16 x 0,082 x 300 (não esqueça que a temperatura é em Kelvin: 273 + 27 = 300). V = 36,9 litros. Depois determinamos a pressão exercida pelos 40 g de gás metano adicionado. P x V = m/mol x R x T; P x 36,9 = 40/16 x 0,082 x 300; P = 1,67 atm. Somando com a pressão inicial teremos; 3,0 + 1,67 = 4,67 atm.
Baixar