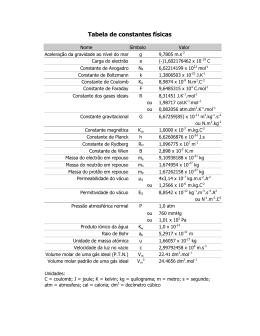
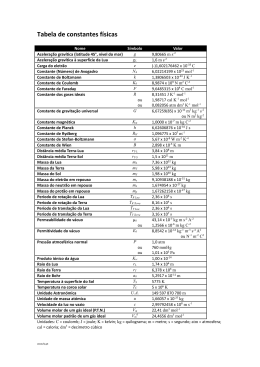
EXAME DE SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUIMICA - UFSCar CURSOS DE MESTRADO ACADÊMICO E DOUTORADO NO 2º SEMESTRE DE 2013 Questão 01 O íon cianato (NCO-), como o íon tiocianato, tem três estruturas de ressonância possíveis. a) desenhe as três estruturas de ressonância para o NCO- e atribua as cargas formais aos átomos, em cada estrutura do íon cianato. b) Baseando-se em cargas formais, qual a estrutura de ressonância seria a preferida para o íon cianato? Questão 02 A acetona, CH3 C(O) CH3, é o principal componente de alguns removedores de esmalte. (a) Desenhe a estrutura de Lewis da acetona. (b) Qual o número total de elétrons de valência na molécula de acetona? (c) Quantos elétrons de valência são usados para fazer ligações σ na molécula de acetona? (d) Quantos elétrons de valência são usados para fazer ligações π na molécula de acetona? (e) Qual é a hibridização no átomo de carbono central da molécula de acetona? Questão 03 A certa quantidade de água pura mantida a 25ºC foi adicionado cromato de prata, sendo que parte do sal permaneceu no fundo do frasco, na forma sólida. A mistura foi agitada por vários dias, de modo a assegurar que o equilíbrio entre a solução e o Ag2CrO4(s) remanescente tivesse sido alcançado. A análise da solução obtida depois de estabelecido o equilíbrio, mostrou uma concentração de íons prata igual a 1,3X10-4 mol L-1. Calcule o Kps para o Ag2CrO4. Dados: Ag = 108 g mol-1, Cr = 52 g mol-1, O = 16 g mol-1. Questão 04 A solubilidade do CO2 em água pura a 25ºC e 0,1 atm de pressão é de 162,8 mg L-1, sendo a prática usual, assumir que todo o CO2 dissolvido passa para a forma de ácido carbônico, H2CO3. a) Qual é o pH da solução de H2CO3 resultante? b) Qual é a concentração de CO32- (mol L-1) resultante? Dados: H = 1 g mol-1, C = 12 g mol-1, O = 16 g mol-1, pKa1 = 6,37 and pKa2 = 10,25 Questão 05 Calcule a constante de equilíbrio para a reação química balanceada abaixo: 1 2 2 Tabela 1 – Energia de Gibbs padrão de formação a 298,15 K. Substância , Fe(s) 0 O2(g) 0 H+(aq) 0 Fe2+(aq) -78,90 H2O(l) -237,13 !" 1/2 Questão 06 A depolimerização de poli(tereftalato de etileno) – PET pode ser alcançada dissolvendo-se o polímero em soluções concentradas de NaOH (aq). Foram obtidas as constantes cinéticas (k) da depolimerização do PET em várias temperaturas, como mostra a tabela abaixo: k (L mol-1 s-1) 3,32 x 10-7 8,31 x 10-7 22,4 x 10-7 Temperatura (°C) 120 140 160 A partir destes dados: a) calcule a energia de ativação (Ea) para a depolimerização de PET; b) calcule a constante cinética para a depolimerização do PET a 25ºC. Dados: R = 8,31JK-1mol-1 Questão 07 Nas duas partes de 1, você deve classificar a força relativa de ácidos e bases. Use seus conhecimentos em ressonância e efeito indutivo para responder estas perguntas. Parte A: Para essa série de bases mostradas abaixo, coloque em ordem decrescente de basicidade, justificando sua resposta. MeNH2 NH2 A B N H N C D Parte B: Para essa série de ácidos mostrados abaixo, coloque em ordem decrescente de acidez, justificando sua resposta. O O MeOH F3C OH A B OH Me C OH D Questão 08 No esquema abaixo, mostre a estrutura química do composto A e os reagentes para síntese dos compostos B, C e D. Em todos os casos, mostrem o mecanismo reacional HO Br B Br C HBr A D estireno 2/2
Baixar