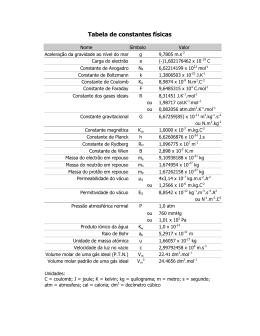
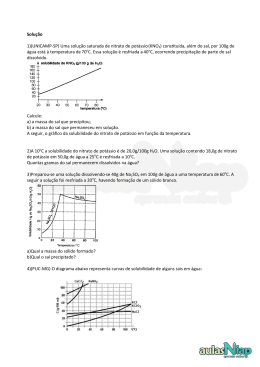
Prova Bimestral de Química Geral e quantitativa – Professora Mirian Nome ________________________________________________________________ 1. A combustão incompleta do etanol (C2H6O), também chamado de álcool combustível está representada pela equação que não está balanceada. __C2H6O + __O2 __ CO + __H2O Dados de massa molares : etanol= 46./mol-1; O2 = 32 g.mol-1, CO= 28g.mol-1 Responda: a)Faça o balanceamento da equação química b)Qual é a massa de etanol (C2H6O) necessária para produzir 90g de água? 2. Soro fisiológico é uma solução aquosa de cloreto de sódio a 0,9% (m/V). Qual é massa de NaCl em gramas necessária para preparar 2 litros de soro fisiológico ? (R:18g) 3) Qual é o volume necessário para preparar 100 mL de solução de NaOH com concentração de 0,5 mol.L-1 partindo de uma solução 2 mol.L?(R: 25 mL) 百 4. Qual é a massa de K presente em 100g de K2O? (R: 82,98 g) Dados de massa molares: K2O = 94 g.mol-1, ; K=39 g.mol-1 5. O gráfico apresenta a curva de solubilidade de 3 sais: a) Qual é a relação entre temperatura e solubilidade para NaNO3, KNO3 e NaCl? ( ) Diretamente proporcional ( ) Inversamente proporcional ( ) A temperatura não influencia a solubilidade dos sais. b) Qual é a substância mais solúvel a uma temperatura de 80o C em 100g de água? ( ) NaNO3 ( ) KNO3 ( ) NaCl c) Foram colocados 50 g e NaCl em 100g de água a uma temperatura de 20oC. A solução resultante será: ( )insaturada ( )saturada sem corpo de fundo ( )saturada com __g de corpo de fundo a. b. c. d. e. f. g. Assinale verdadeiro (V) ou falso (F): ( ) o átomo de Dalton era maciço e indivisível ( ) Cátion é o íon negativo formado pelo ganho de elétrons ( ) o número atômico corresponde a quantidade de prótons no núcleo. ( ) os elétrons são partículas negativas que se encontram no núcleo do átomo ( ) Na diluição o volume inicial (V1) sempre é maior que o volume 2(V2). ( ) A água é chamada de solvente universal pois dissolve todas as substâncias ( ) Na suspensão o tamanho das partículas dispersas são maiores que em uma solução verdadeira. h. ( ) A diluição sempre parte da solução com menor concentração i. ( ) As soluções são somente misturas líquidas que formam uma única fase
Baixar