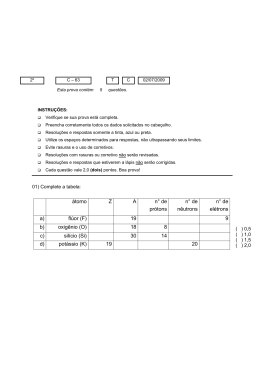
Lista de Exercícios III - Química Prof. Douglas Supletivo São Benedito Q1 - (UFJF-MG) Associe as afirmações a seus respectivos responsáveis. I. O átomo não é indivisível e a matéria possui propriedades elétricas. II. O átomo é uma esfera maciça. III. O átomo é formado por duas regiões denominadas núcleo e eletrosfera. a) I - Dalton, II - Rutherford e III - Thomson. b) I - Thomson, II - Dalton e III - Rutherford. c) I - Dalton, II - Thomson e III - Rutherford. d) I - Rutherford, II - Thomson e III - Dalton. e) I - Thomson, II - Rutherford e III - Dalton. Q2 - (UFMG) Os diversos modelos para o átomo diferem quanto às suas potencialidades para explicar fenômenos e resultados experimentais. Em todas as alternativas, o modelo atômico está corretamente associado a um resultado experimental que ele pode explicar, EXCETO em: a) O modelo de Rutherfod explica por que algumas partículas alfa não conseguem atravessar uma lâmina metálica fina e sofrem fortes desvios. b) O modelo de Thomson explica por que a dissolução de cloreto de sódio em água produz uma solução que conduz eletricidade. c) O modelo de Dalton explica por que um gás, submetido a uma grande diferença de potencial elétrico, se torna condutor de eletricidade. d) O modelo de Dalton explica por que a proporção de massa dos elementos de um composto é definida. Q3 - (FUVEST) A densidade da água comum, , e da água pesada, , medidas na mesmas condições de pressão e temperatura, são diferentes. Isso ocorre porque os átomos de hidrogênio e deutério diferem quanto ao: a) número atômico. b) número de elétrons. c) número de nêutrons. d) número de oxidação. e) número de prótons. Q4 - (Cesgranrio-RJ) Um gás nobre tem número atômico 18 e número de massa 40. O número de elétrons de um ânion é igual ao do átomo do gás nobre. O número atômico do elemento X é: a) 22 b) 20 c)18 d) 16 e) 14 Q5 - (CEFETMG - 2014/2) Suponha que uma mistura heterogênea (M1) seja submetida a um processo de separação (P1) resultando em uma mistura homogênea líquida (M2) e um sólido puro (S1). Em seguida, M2 é submetida a um processo de separação (P2), gerando um líquido puro (L1) e um sólido puro (S2). Considerando-se essas informações, é correto deduzir que a) L1 é uma solução líquida. b) P1 corresponde a um processo de levigação. c) P2 equivale a um processo de decantação. d) M2 apresenta temperaturas de fusão e ebulição constantes. e) M1 é constituída de limalha de ferro, cloreto de sódio e água. Q6 - (UFMG-2006) No fim do século XIX, Thomson realizou experimentos em tubos de vidro que continham gases a baixas pressões, em que aplicava uma grande diferença de potencial. Isso provocava emissão de raios catódicos. Esses raios, produzidos num cátodo metálico, deslocavam-se em direção à extremidade do tubo (E). (Na figura, essa trajetória é representada pela linha tracejada X.) Nesses experimentos, Thomson observou que: I) a razão entre carga e massa dos raios catódicos era independente da natureza do metal constituinte do cátodo ou do gás existente no tubo; e II) os raios catódicos, ao passarem entre duas cargas carregadas, com cargas de sinais contrários, se desviavam na direção da placa positiva. (Na figura, esse desvio é representado pela linha tracejada Y.) Considerando-se essas observações, é CORRETO afirmar que os átomos são constituídos de A) elétrons. B) ânions. C) prótons. D) cátions. Q7 - (UFMG-2007) Analise este quadro, em que se apresenta o número de prótons, de nêutrons e de elétrons de quatro espécies químicas: Considerando-se as quatro espécies apresentadas, é INCORRETO afirmar que A) I é o cátion . B) II é o ânion . C) III tem massa molar de 23 g/mol. Q8 - (CEFETMG-2011/2) Um átomo A, isótono de situação, a massa atômica de A é a) 79. b) 80. D) IV é um átomo neutro. , ao receber um elétron, torna-se isoeletrônico de c) 81. d) 82. . Nessa e) 83. Q9 - (Unicamp-2012) Em algumas extrações de ouro, sedimentos do fundo de rio e água são colocados em uma bateia, recipiente cônico que se assemelha a um funil sem o buraco. Movimentos circulares da bateia permitem que o ouro metálico se deposite sob o material sólido ali presente. Esse depósito, que contém principalmente ouro, é posto em contato com mercúrio metálico; o amálgama formado é separado e aquecido com um maçarico, separando-se o ouro líquido do mercúrio gasoso. Numa região próxima dali, o mercúrio gasoso se transforma em líquido e acaba indo para o leito dos rios. Os três segmentos acima grifados se referem, respectivamente, às seguintes propriedades: a) peso, temperatura de gaseificação e temperatura de liquefação. b) densidade, temperatura de sublimação e temperatura de fusão. c) peso, temperatura de fusão e temperatura de ebulição. d) densidade, temperatura de ebulição e temperatura de liquefação. Q10 - De modo simplificado, pode-se dizer que o modelo atômico prevê a existência de três partículas: prótons, nêutrons e elétrons, as quais não estão distribuídas ao acaso. Essas partículas podem interagir entre si e essa interação produz um conjunto organizado chamado átomo. Das afirmações abaixo, quais são verdadeiras em relação ao átomo ? Corrija a(s) alternativa(s) falsa(s). a) Prótons e nêutrons são encontrados no núcleo, que é a parte do átomo que apresenta carga elétrica positiva e na qual se encontra praticamente toda sua massa. b)O átomo eletricamente neutro possui o mesmo número de elétrons e de prótons. Se o número de elétrons for maior, forma-se um ânion. Se o número de elétrons for menor, forma-se um cátion. c) O número atômico (Z) informa o número de prótons de um átomo. d) O núcleo de qualquer átomo sempre conta com o mesmo número de prótons e elétrons.
Baixar