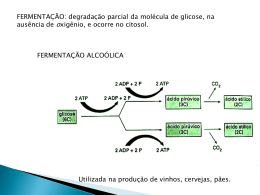
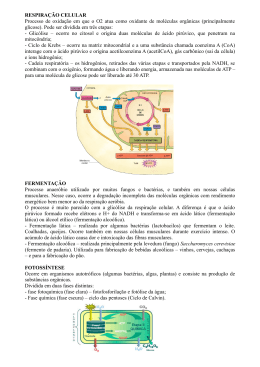
DIVULGAÇÃO TÉCNICA Dosagem de ácido lático na produção de etanol a partir da cana-de-açúcar. DOSAGEM DE ÁCIDO LÁTICO NA PRODUÇÃO DE ETANOL A PARTIR DA CANA-DE-AÇÚCAR A.L. Moreira, W.S. Almeida, R.J.A. Scabbia, R.R.P. Teixeira Faculdade de Ciências da Saúde de São Paulo, Rua D. Inácia Uchôa, 399/411, CEP 04110-021, São Paulo, SP, Brasil. E-mail: [email protected] RESUMO Na década de 1970, devido à crise internacional do petróleo, o etanol passou a ser uma alternativa de fonte de energia, por ser considerado adequado para substituir a gasolina. Isto se deveu ao fato de existirem, no Brasil, indústrias sucro-alcooleiras com potencial para a produção em grande escala, pela disponibilidade de áreas para cultivo da cana-de-açúcar e também por ele ser menos poluente e uma fonte renovável de energia. Existem três vias para a obtenção do álcool: a degradativa, a sintética e a fermentativa, sendo esta última a mais importante. A competição entre leveduras, principalmente Saccharomices cereviseae, e microrganismos contaminantes pela sacarose, pode resultar em queda na produção final de etanol. Por esse motivo, a dosagem de ácido lático (produto da ação de microrganismos contaminantes), durante a fermentação pode ser um diferencial, indicando se há um desequilíbrio entre a fermentação da garapa e a produção de etanol, decorrente de contaminação microbiana. O presente estudo tem como objetivo verificar a intensidade da presença de ácido lático no processo de produção de etanol em 3 usinas sucroalcooleiras no Estado de São Paulo. PALAVRAS-CHAVE: Cana-de-açúcar, fermentação, ácido lático, etanol. ABSTRACT DOSAGE OF LATIC ACID IN THE PRODUCTION OF ETHANOL FROM SUGAR CANE. Since the world oil crisis in the early 70s, ethanol has become an alternative source of energy, once it has proved to be an appropriate substitute for gasoline. This is true particularly in Brazil, since there are several sugar cane mills with great potential production, huge growing areas and mainly due to the fact that ethanol is less environmental aggressive, in addition to being a renewed source of energy. There are basically 3 different ways for generating ethanol, degrading, synthetic and fermentation, which is the most relevant procedure. The competing behavior between brews, mainly Saccharomices cereviseae and micro-organisms contaminated by sucrose can lead to a decreasing final ethanol production. Thus, lactic acid measurements (which is a result of contaminating micro-organisms) during the fermentation process can be a critical issue, since it can indicate any cross-contamination unbalance between the sugar cane juice fermentation and ethanol production. The objective of this study was to identify any lactic acid presence during the ethanol production process in 3 different sugar cane mills in the State of São Paulo. KEY WORDS: Sugar cane, fermentation, lactic acid, ethanol. A história da produção de bebidas destiladas a partir da cana-de-açúcar está intimamente relacionada à história do Brasil, desde os grandes descobrimentos (STANDAGE, 2005). O cultivo da cana-de-açúcar, tanto no Brasil quanto na América central e no Caribe, exigia grande quantidade de mão-de-obra: este foi um dos fatores que levaram à escravidão nestas regiões para o trabalho tanto no cultivo da cana quanto na sua moagem e na extração da garapa nos antigos moinhos de engenho: “Não tivesse sido a demanda de açúcar, é provável que nosso mundo fosse muito diferente hoje. Afinal, foi o açúcar que estimulou o tráfico escravista, levando milhões de africanos negros para o Novo Mundo e, foram os lucros obtidos com ele que, no início do século XVIII, ajudaram a estimular o crescimento da Europa” (COUTEUR, 2006). Muitos escravos levavam a garapa para a senzala, armazenando-a. Com o passar do tempo, eles perceberam que, ao envelhecer, a garapa adquiria sabor agradável e proporcionava – quando bebida – uma alteração da consciência, tornando o trabalho duro mais suportável. Desde aquela época, a produção de álcool de cana-de-açúcar vem ganhando espaço no mercado nacional e internacional. Isso faz Biológico, São Paulo, v.71, n.1, p.69-76, jan./jun., 2009 69 70 A.L. Moreira et al. com que as grandes usinas e os produtores de canade-açúcar busquem estratégias para otimizar o plantio, a colheita e a produção de álcool. Atualmente, o Brasil é um dos maiores produtores de álcool combustível no mundo, juntamente com os Estados Unidos e a África do Sul. Com isso o cultivo de cana-de-açúcar tem sido alvo de grandes especulações mundiais, não somente pela preocupação com o meio ambiente devido as crescentes preocupações associadas ao efeito estufa produzido pela queima de combustíveis fósseis, mas também devido ao crescente custo do petróleo. A região Centro-Sul do país é responsável pela maior parte da produção nacional de cana-de-açúcar e o Estado de São Paulo se destaca pelo volume produzido. O álcool pode ser produzido por três vias: a via degradativa, a via sintética e a via fermentativa (ROITMAN, 1987). A via fermentativa é a mais importante e a mais rentável (LIMA, 1975) e é esta via que será analisada neste trabalho. Nela, a levedura Saccharomyces cerevisiae é a principal responsável pela fermentação do substrato e consequente produção de álcool. A fermentação da sacarose é uma etapa importantíssima na produção do etanol e sua degradação pode ser feita por leveduras ou ainda por microrganismos contaminantes. Por esse motivo, a dosagem de ácido lático durante a fermentação da garapa pode ser um diferencial, indicando se há contaminação no processo de produção de etanol. Este trabalho visa estudar a presença de ácido lático no processo de produção de etanol a partir da cana-de-açúcar, utilizando-se, para isto, medidas da dosagem em amostras durante este processo. A CANA-DE-AÇÚCAR E A PRODUÇÃO DE ÁLCOOL NO BRASIL A cana-de-açúcar tem origem asiática e pertence a uma das mais importantes e maiores famílias de angiospermas, a Poaceae. Das seis espécies mais conhecidas, duas são consideradas silvestres (Saccharum robustum Brandes & Jewiest e Saccharum spontaneum L.) e quatro cultivadas (Saccharum officinarum L., Saccharum sinense Roxb., Saccharum edule Hassk e Saccharum barberi Jewiest.) ( DANIELS; R OACH, 1987). São herbáceas, perenes, caule do tipo colmo cheio, com nós (de onde saem gemas) e entrenós, epiderme característica, raiz fasciculada e flores monóclinas (JOLY, 2002). As folhas da cana-de-açúcar são alternas ou opostas, possuem nervuras paralelinérvias e bainhas largas, são lineares e podem chegar a 140 centímetros de comprimento. Já o fruto é bem pequeno, do tipo cariopse. Dentre seus constituintes químicos estão o ácido hidrociânico, o ácido ascórbico, sais minerais (sobretudo de cálcio e de ferro), fibras e sacarose. Em termos históricos, segundo VARNHAGEN (1978), em 1526, o primeiro carregamento de açúcar teria chegado a Lisboa, originário do atual Estado de Pernambuco, o que pressupõe a existência de canaviais no Brasil, naquele ano. Porém, paraAZEVEDO (1943), as primeiras plantações de cana-de-açúcar ocorreram já em 1502, anteriormente à vinda de Martim Afonso de Souza ao Brasil. ParaMATSOUKAet al. (1999), foi Martim Afonso quem trouxe a primeira muda de cana-de-açúcar ao Brasil em 1532 e, na Capitania de São Vicente, iniciou seu cultivo. Divergências históricas à parte, foi a partir da Zona da Mata pernambucana, que os canaviais conquistaram a Terra de Santa Cruz: Olinda foi a sede dos primeiros engenhos nordestinos (DIÉGUES, 1954). A disseminação desta cultura ocorreu em menos de um século e as lavouras se desenvolveram principalmente em faixas costeiras ou ainda próximas a rios navegáveis. O primeiro governador do Estado de Pernambuco foi o responsável pela expansão dos canaviais, já que tinha o poder de conceder terras a serem cultivadas. Santos e São Vicente foram capitanias pioneiras no Estado de São Paulo, em lavouras de cana-de-açúcar, sendo que a segunda já contava com seis engenhos em apenas dezesseis anos de fundação. As famílias, na grande maioria portuguesas, se instalavam e se multiplicavam ao redor dos engenhos, unidades econômicas características daquela época, ocupando terras e contribuindo para o adensamento demográfico e o início do processo de urbanização. Estas comunidades eram estratificadas em forma de uma pirâmide social, com os senhores de engenho posicionados no seu ápice e os escravos na base desta pirâmide (BRANDÃO, 1985). Formavam-se verdadeiros grupos populacionais com toda a complexidade social e material associada, incluindo moendas para espremer a cana, caldeiras fornecedoras de energia para o processo de purificação da garapa, a casa de purgar para aperfeiçoar o processo de purificação, a casa-grande, símbolo do poder econômico e social, a senzala, moradia dos escravos e uma capela, símbolo religioso. Os altos custos gerados para manter esta organização fizeram com que a indústria do açúcar no Brasil ficasse conhecida como “uma empresa cara”. A construção, a montagem e a manutenção dos engenhos para a produção do açúcar, bem como o plantio, a colheita e a estocagem da cana-de-açúcar exigiam muito capital (BARLÉU, 1974). Em 1974, devido à crise mundial do petróleo, se iniciou uma nova fase na produção de álcool no Brasil. Em pouco tempo, a produção de etanol do país passou dos 700 milhões de litros/ano para 15 bilhões de litros/ano. Este aumento levou à ampliação de canaviais, à modernização das destilarias e à geração Biológico, São Paulo, v.71, n.1, p.69-76, jan./jun., 2009 Dosagem de ácido lático na produção de etanol a partir da cana-de-açúcar. de grande quantidade de empregos. O Programa Nacional do Álcool (Próalcool) foi criado por Decreto Presidencial, no final de 1975, com o objetivo de atender as necessidades do país quanto aos combustíveis automotivos. Este programa foi a continuidade de um programa de uso do álcool que teve início em 1931 (LIMA, 2001). O crescimento da produção de álcool no país tem sido sustentado também devido ao seu amplo emprego nas indústrias farmacêutica, alimentícia e cosmética, além do seu uso como combustível automotivo. PRODUÇÃO DE ETANOL A observação empírica de que somente líquidos açucarados são capazes de entrar em fermentação alcoólica remonta a séculos, mas foi Lavoisier (VANIN, 1994) em 1789, um dos primeiros pesquisadores a estudar o processo de fermentação alcoólica quantitativamente, formulando uma equação que julgara representar o fenômeno químico deste processo. Porém, apenas em 1857, Pasteur (GEISON, 2002) esclareceu a natureza da fermentação alcoólica, identificando seres vivos (leveduras) como agentes causais deste processo. A fermentação alcoólica depende do tipo de substrato: há aqueles que são diretamente fermentescíveis, como o melaço e o caldo de cana, e há outros que são indiretamente fermentescíveis, como as matérias primas amiláceas ou celulósicas (ROITMAN, 1987). O produto da fermentação depende diretamente do tipo de microrganismo que atua no processo, do substrato existente e das enzimas ativas presentes (TORTORA, 2000). A fermentação é um processo no qual há liberação de energia de açúcares ou moléculas orgânicas tais como aminoácidos, ácidos orgânicos, purinas e pirimidinas e que não necessita de oxigênio para ocorrer, mas que pode ocorrer na presença deste. Para LEHNINGER (1984) fermentação é um termo que significa degradação da glicose e de outros nutrientes orgânicos em condições de anaerobiose. Existem diferentes formas de fermentação e a fermentação lática é um exemplo típico deste processo. Nela, alguns microrganismos metabolizam a glicose até ácido lático, que se acumula no meio como único produto da fermentação. Pela glicólise, uma única molécula de glicose é convertida em duas moléculas de ácido pirúvico, com a produção concomitante de dois pares de elétrons. A sequência de reações da glicólise pode ser diferente apenas na forma em que sua velocidade é regulada e no destino metabólico do piruvato formado. Este piruvato pode seguir três vias importantes: a fermentação alcoólica, a fermentação lática em condições anaeróbicas e o ciclo do ácido cítrico em condições aeróbicas. Na via do ácido cítrico, o piruvato origina- do da glicólise é oxidado, perdendo seu radical carboxila na forma de CO2 e formando o grupo acetil. Em seguida, este grupo é completamente oxidado, sofrendo intervenção do oxigênio molecular. Esta é a via realizada nas células aeróbicas vegetais e animais. Na via da fermentação lática ou do ácido lático, o piruvato, em condições de anaerobiose, não pode ser oxidado e é reduzido a lactato. Durante a atividade física muito intensa de seres humanos, este processo (glicólise anaeróbica) é uma importante fonte de ATP. A degradação do açúcar por microrganismos tendo como produto final o ácido lático, também é chamada de fermentação lática. Em outras palavras, uma molécula de glicose é oxidada a duas moléculas de ácido pirúvico. Esta oxidação gera energia para a formação de duas moléculas de ATP. A etapa seguinte consiste na redução das duas moléculas de ácido pirúvico a duas moléculas de ácido lático que, por ser produto final, não sofre mais oxidação. A energia gerada por esta reação permanece armazenada no ácido lático. Streptococcus e Lactobacillus são dois gêneros importantes de bactérias que realizam a fermentação do ácido lático. A via que resulta na produção de etanol, também ocorre em condições de anaerobiose. É a chamada fermentação alcoólica que é realizada por microrganismos como leveduras (Saccharomyces cereviseae). Neste processo, de uma molécula de glicólise obtémse duas moléculas de ácido pirúvico e duas moléculas de ATP. Na etapa seguinte, duas moléculas de acetaldeído e duas de CO2 são originadas a partir da conversão das duas moléculas de ácido pirúvico. A partir da redução das duas moléculas de acetaldeído, formam-se duas moléculas de etanol. Assim como a fermentação do ácido lático, a fermentação alcoólica é um processo de baixo rendimento energético no qual o etanol permanece com a maior parte da energia contida na molécula de glicose, energia esta que estará armazenada e que será utilizada quando o etanol queimar como combustível. FERMENTAÇÃO ALCOÓLICA E PRODUÇÃO DE ÁCIDO LÁTICO Fermento alcoólico As leveduras são agentes biológicos ativos responsáveis pela fermentação alcoólica e a escolha da linhagem correta é fundamental para o processo da fermentação. Apenas algumas espécies são utilizadas na fabricação do álcool, como por exemplo o S. cereviseae, se o substrato for constituído por hexoses, e Candida utilis, quando uma parcela do substrato for constituído por pentoses (CRUEGER, 1993). As bactérias Biológico, São Paulo, v.71, n.1, p.69-76, jan./jun., 2009 71 72 A.L. Moreira et al. Zymomonas mobilis e Thermoanaerobacter ethanolicus também podem conduzir com eficácia a fermentação alcoólica. Os seguintes critérios são utilizados para a escolha da linhagem: velocidade de fermentação, resistência ao álcool, eficiência de conversão e resistência ao pH e a antisépticos, bem como estabilidade genética (CASTRO, 1995). Atualmente, a biotecnologia permite a hibridação de duas ou mais características de linhagens diferentes em uma única linhagem e tem por consequência resultados positivos (ROITMAN, 1987). Preparo do substrato O preparo do substrato difere de acordo com a matéria prima. Em se tratando de substrato fermentescível (mosto ou melaço), dilui-se o melaço em água para se obter uma concentração de açúcar de 14 a 18%. Esta diluição faz-se em tanques com dispositivos para adequada homogeneização que pode ser manual ou mecânica e é feita com o uso de agitadores que se utilizam de paletas ou de ar comprimido (WARD, 1991). Para obtenção do caldo de cana ou de sorgosacarino, a cana é esmagada e, após a moagem, coase ou filtra-se o caldo para separar o bagacilho, que dificulta a destilação. Para obter-se um processo melhor de fermentação, aquece-se o caldo em trocadores de calor, decantando-os para que haja precipitação e remoção de colóides, gomas e materiais nitrogenados. Este tratamento do caldo desfavorece a formação de espuma durante a fermentação, provocando menos acúmulo de detritos nas colunas de destilação e reduzindo a presença de microrganismos indesejáveis. O bagacilho separado neste processo é queimado, posteriormente, com o bagaço, em caldeiras e convertido em energia ou utilizado como cobertura para a lavoura e na alimentação de porcos. O caldo resultante é muito rico em açúcar e por isso há a necessidade de diluí-lo, devido à tolerância da levedura ao álcool, o que irá impedi-la de utilizar todo o açúcar para a transformação em álcool. O teor de açúcar no caldo é determinado pelo aerômetro de Brix (o valor ideal para fermentação está entre 18 e 22 graus Brix), que mede o teor de sólidos solúveis no caldo, cujo valor, no caso do caldo de cana, é próximo ao teor da sacarose. Esta diluição é feita com a própria água de embebicação na moenda (GA V A, 1998). No caso de matérias primas não fermentescíveis, primeiramente ocorre a hidrólise de substratos amiláceos ou celulósicos, por processo ácido ou enzimático. Esta etapa influencia diretamente no rendimento do álcool. A temperatura e pressão também são fundamentais na eficiência da conversão do açúcar em álcool. Em cozedores e digestores ocorre o cozimento do amido e a digestão da celulose sob pressão de vapor, enquanto a sacarificação do amido e da celulose é conduzida à pressão atmosférica. Correção do mosto O mosto, que será submetido à fermentação alcoólica, é constituído pelo melaço diluído, pelo caldo de cana-de-açúcar e por substâncias amiláceas e celulósicas. Conhecendo a fisiologia e as exigências nutricionais das leveduras, criam-se condições ótimas para esses microrganismos o que, por consequência, favorece que a fermentação alcoólica para este seja um processo rápido e regular. Isto é possível, se ao mosto forem adicionados nutrientes necessários, empregando-se antibióticos e mantendo a temperatura adequada. Estes nutrientes, suas quantidades e a necessidade de se adicionar ou não elementos corretivos dependem diretamente do tipo de mosto. Os carboidratos são as fontes de carbono na fermentação alcoólica. As fontes de nitrogênio e fósforo também são imprescindíveis neste processo. Como o caldo de cana e a maioria dos hidrolisados amiláceos ou celulósicos são carentes destes elementos, é imprescindível a adição de sais destes elementos, como o sulfato de amônio. A adição de sulfato de magnésio, sulfato de cobalto, sulfato de manganês e farelo de arroz, torna a fermentação mais eficiente. No Brasil, o mosto não é comumente esterilizado, de modo que sempre está presente uma população microbiana natural que compete com a levedura pelo substrato, o que diminui o rendimento do álcool. Mostos que foram aquecidos, apresentam uma população microbiana reduzida e por consequência menor interferência no processo de fermentação pelas leveduras. Para assegurar uma fermentação alcoólica pura, sem competição entre microrganismos, é obrigatória a adição de antisépticos aos mostos que não receberam tratamento térmico. O ácido sulfúrico, além de corrigir o pH do meio – que deve estar entre 4,0 e 5,0 – é utilizado também como antiséptico. Seu uso é muito comum, principalmente devido ao seu baixo custo. Devido as propriedades bactericidas, os antibióticos também agem como desinfetantes do mosto. O cloranfenicol e a tetraciclina também podem ser empregados, porém a penicilina ainda é economicamente mais viável (AQUARONE , 1975). A temperatura ideal para o processo de fermentação alcoólica está entre 25 e 36° C. Temperaturas mais baixas tornam o processo muito lento, enquanto as mais elevadas fazem com que o álcool evapore. Biológico, São Paulo, v.71, n.1, p.69-76, jan./jun., 2009 Dosagem de ácido lático na produção de etanol a partir da cana-de-açúcar. Preparo do inóculo O inóculo é a quantidade de leveduras (células) necessárias para dar início ao processo de fermentação de forma rápida e eficaz. Após a escolha da levedura, para o preparo do inóculo, é preciso obter uma determinada quantidade do fermento em atividade suficiente para manter a fermentação nas dornas. Para isto, transfere-se um tubo de cultura pura de levedura para o mosto já enriquecido e esterilizado. Estas transferências são feitas sucessivamente com assepsia em quantidades e concentrações crescentes do substrato e até que seja possível manter um volume de inóculo capaz de conduzir a fermentação nas dornas. Condução da fermentação alcoólica Após o preparo do mosto e do inóculo, inicia-se nas dornas a fermentação alcoólica principal. Esta fermentação é separada em três fases: preliminar, tumultuosa e final. A elevação ligeira da temperatura ocasiona a multiplicação da levedura, que consiste na primeira etapa, a preliminar. O açúcar consumido pela levedura nesta fase destina-se à formação de novas células de fermento; esta fase é breve e pode durar entre 4 e 6 horas. Quando há desprendimento de gás carbônico decorrente de intensa atividade fermentativa, inicia-se a fase tumultuosa. Esta fase é caracterizada pela elevação da temperatura, pela elevação do teor alcoólico e pela efervescência do mosto em agitação, dando origem ao termo fermentação. Há formação de espuma e seu aspecto e volume são dependentes da linhagem da levedura e do tipo de mosto. Esta fase dura entre 10 e 18 horas, podendo variar com o sistema de fermentação empregado, com o tipo de mosto e de levedura. Quando o aspecto do vinho se torna mais calmo, a fermentação entra na fase final, diminuindo as espumas que desaparecem ao final desta fase. Nesta fase, a temperatura diminui e o consumo de açúcar atinge o limite máximo. O processo de fermentação contínua consiste na adição constante do meio esterilizado contendo o substrato, enquanto os produtos da reação também estão sendo removidos continuamente. Um fator importante que influencia a eficiência do processo de fermentação contínua é a necessidade de reciclar os microrganismos que são colocados no reator. Dentre os produtos secundários resultantes da ação bacteriana encontram-se o ácido acético, o ácido lático, o ácido butílico, o ácido propiônico e ácidos graxos de cadeia longa, que se originam da matéria prima e passam para o destilado. Nos últimos anos, diversos trabalhos têm sido conduzidos com o objeti- vo de identificar as causas de redução da produtividade e, desta forma, aperfeiçoar o processo de fermentação etanólica (CASTRO, 1995). Assim sendo, a presença de microrganismos contaminantes pode causar a redução da produção de álcool (FRANCO, 1996). Desde que a fermentação industrial, pela dimensão do processo não é conduzida em condições de completa assepsia, a contaminação bacteriana está sempre presente e, dependendo de sua intensidade, compromete o rendimento do processo fermentativo, pois aumenta a formação de ácido lático e o tempo de fermentação. Destilação O produto contido nas dornas, assim que a fermentação é concluída, denomina-se vinho. Este é uma mistura hidroalcoólica contendo, além de água e etanol, substâncias como o dióxido de carbono (dissolvido em pequenas quantidades), células de leveduras, microrganismos contaminantes, sais minerais, açúcares não fermentados, partículas sólidas em suspensão provenientes da matéria prima, óleo fúsel, aldeídos, ésteres e ácidos orgânicos. Partículas maiores são retiradas por peneiras, enquanto que as menores, como as leveduras, normalmente são separadas por centrifugação. Da mistura líquida restante, separa-se o etanol pelo processo de destilação, que decompõe essa solução múltipla em seus constituintes. Isso se consegue ao atingir as condições de temperatura e pressão ótimas, de maneira tal que uma fase líquida e uma fase de vapor coexistam e se obtenha uma diferença na concentração relativa das substâncias a serem separadas nestas duas fases. A coleta dos dados para este trabalho ocorreu em julho de 2007 nas Usinas Santa Maria (situada na Estrada Usina Santa Maria, Bairro São Francisco, Cerquilho), Ester (situada na Rodovia SP 332, km 145, Zona Rural, Cosmópolis) e Vista Alegre (situada na Fazenda Vista Alegre, Bairro Pinhal, Itapetininga), todas localizadas no interior do Estado de São Paulo. O trabalho experimental realizado consistiu em dosar a concentração de ácido lático durante o processo de produção de etanol nestas usinas, para estudar a contaminação do processo associada à presença de ácido lático que prejudica a produção final de etanol. Em decorrência do sistema diferenciado de produção de etanol, para cada usina foi adotado um critério para a coleta de amostras e posterior dosagem, mas o número de amostras por dorna foi padronizado em três amostras por dorna. As coletas se deram durante o processo de fermentação. O intervalo de tempo entre as dosagens foi de aproximadamente dois minutos. Biológico, São Paulo, v.71, n.1, p.69-76, jan./jun., 2009 73 74 A.L. Moreira et al. Fig. 1 - Esquema de produção de etanol via fermentação contínua utilizada na Usina Santa Maria (Cerquilho). Fonte: Usina Santa Maria. Na usina Santa Maria utiliza-se o processo de produção de etanol chamado contínuo. Este processo consiste em adicionar continuamente o meio esterilizado contendo o substrato, enquanto os produtos da reação também são removidos continuamente (Fig. 1). O mosto é distribuído nas três primeiras dornas, onde será adicionada a levedura, dando início ao processo de fermentação que se dá em oito dornas no total. Foram coletadas amostras nas saídas das dornas 1, 2, 3, 4, 5, 6 ,7 e dorna 10, uma por vez, em recipientes fornecidos pela usina, para evitar contaminação. As análises foram feitas na sala de controle de produção, devido à proximidade da fonte para a coleta das amostras. Na Usina Ester, localizada em Cosmópolis, a produção do álcool também é realizada por fermentação contínua. O mosto (caldo ou melaço) e a levedura previamente tratada são despejados na primeira dorna, onde se inicia o processo de fermentação. Antes de chegar ao final, o vinho é centrifugado para separar os subprodutos e a levedura. Para este experimento foram coletadas amostras do mosto, do leite tratado (fermento), do vinho levurado e do vinho delevurado. Na usina Vista Alegre, o processo de produção de etanol se dá via fermentação por batelada. As amostras foram coletadas do mosto, do vinho levurado e do vinho delevurado. As dosagens foram realizadas utilizando o aparelho YSI 1500 da Yellow Springs, portátil, com método enzimático e tecnologia de membrana, funcionando com corrente elétrica (110V ou 220V) ou bateria própria recarregável (autonomia de 8 horas). O volume de cada amostra foi de 25 microlitros, com coletas utilizando pipeta de agulha. Cada dosagem tem duração de 30 segundos, intervalo de 60 segundos entre amostras, escala em mMol/L, amplitude de leitura de 0-30 mMol/ L, coeficiente de variação (precisão) de ± 2% e resolução de 0,01 mMol/L. O equipamento foi cedido pela TBW Importadora Ltda, empresa que atua na área da saúde, durante o período de realização dos testes. As dosagens de ácido lático no processo de fermentação alcoólica durante a produção de etanol nas usinas Santa Maria, Ester e Vista Alegre, apresentaram diferentes concentrações nas diversas etapas do processo. Na usina Santa Maria, onde o etanol é produzido pelo processo de fermentação contínua, verificou-se a presença de ácido lático em todas as etapas da produção do álcool (Quadro 1). Observou-se também que os valores mínimos de ácido lático foram obtidos no mosto e os valores máximos na etapa final (Dorna 10) da produção de etanol. Biológico, São Paulo, v.71, n.1, p.69-76, jan./jun., 2009 75 Dosagem de ácido lático na produção de etanol a partir da cana-de-açúcar. Quadro 1 - Dados referentes às dosagens de ácido lático das amostras coletadas na Usina Santa Maria (J. Pilon) em 5/7/2007. (Média Mosto ± Desvio Padrão) (Média Dorna 1± Desvio Padrão) (Média Dorna 2± Desvio Padrão) (Média Dorna 3± Desvio Padrão) (Média Dorna 4± Desvio Padrão) (Média Dorna 5± Desvio Padrão) (Média Dorna 6± Desvio Padrão) (Média Dorna 7± Desvio Padrão) (Média Dorna 10± Desvio Padrão) (2,61 ± 0,06) mMol/L (3,86 ± 0,02) mMol/L (3,61 ± 0,20) mMol/L (3,40 ± 0,13) mMol/L (3,92 ± 0,06) mMol/L (3,95 ±0 ,12) mMol/L (4,60 ± 0,05) mMol/L (4,64 ± 0,03) mMol/L (4,80 ± 0,05) mMol/L Quadro 2 - Dados referentes às dosagens de ácido lático das amostras coletadas na Usina Ester em 12/7/2007. (Média Mosto ± Desvio Padrão) (Média Leite Tratado ± Desvio Padrão) (Média Vinho Levurado ± Desvio Padrão) (Média Vinho Delevurado ± Desvio Padrão) (1,08 ± 0,02) mMol/L (2,93 ± 0,64) mMol/L (6,21 ± 0,28) mMol/L (6,84 ± 0,08) mMol/L Quadro 3 - Dados referentes às dosagens de ácido lático das amostras coletadas na Usina Vista Alegre em 20/7/2007. (Média Mosto ± Desvio Padrão) (Média Vinho Levurado ± Desvio Padrão) (Média Vinho Delevurado ± Desvio Padrão) Na Usina Ester o processo de produção do álcool também é feita por fermentação contínua, porém o processo ocorre em apenas quatro dornas, sendo que uma dorna contém o mosto, outra o leite tratado (fermento), a terceira o vinho levurado e, por fim, outra com o vinho delevurado. O leite tratado é adicionado ao mosto para dar início ao processo de fermentação e, então, ambos são destinados à terceira dorna. A última dorna contém o vinho sem a levedura (eliminada por centrifugação) que é chamado de vinho delevurado. Constatou-se, também, a presença de ácido lático em todas as etapas da produção do álcool; é possível notar que esta presença se intensifica no final do processo (Quadro 2). A Usina Vista Alegre produz etanol pelo método de fermentação descontínua (batelada) e todo o processo ocorre em apenas uma dorna, onde o mosto e o leite tratado (fermento) são misturados e a fermentação acontece. Como constatado nas outras duas usinas, nesta também se verificou a presença de ácido lático em todas as etapas da produção do etanol, com o seu crescimento no final do processo (Quadro 3). Observou-se, com este experimento, que há produção de ácido lático em todas as etapas de produção de etanol, nas usinas visitadas. Nas usinas Ester e Santa Maria, onde a fermentação é contínua, pode-se constatar que a menor concentração de ácido lático foi encon- (1,69 ± 0,15) mMol/L (3,80 ± 0,07) mMol/L (3,48 ± 0,02) mMol/L trada no mosto e a maior concentração no vinho delevurado na etapa final. Com isso, pode-se inferir que há presença de microrganismos contaminantes, principalmente nesta fase do processo. Já na usina Vista Alegre, a concentração de ácido lático no mosto também foi a menor encontrada, porém a maior concentração foi verificada no vinho levurado. Em relação às variações de concentração de ácido lático obtido em cada etapa, foram observados desvios padrões pequenos indicando uma consistência dos dados obtidos. CONSIDERAÇÕES FINAIS A produção de ácido lático ocorreu durante o processo de fermentação em todas as Usinas estudadas neste trabalho, indicando a contaminação por microrganismos láticos, resultando, assim em perdas não desprezíveis na produção final do etanol, visto que este não é fermentado pelas leveduras. Tendo em vista que uma maior produção de ácido lático implica numa menor produção de etanol, pois o lactato é um produto final que não pode ser oxidado e convertido em álcool, a sua dosagem durante o processo de produção do álcool é um fator crítico e de extrema importância, principalmente para se identificar à tempo em que etapa esta contaminação está ocorren- Biológico, São Paulo, v.71, n.1, p.69-76, jan./jun., 2009 76 A.L. Moreira et al. do. Com isso, é possível reduzir os custos com o tratamento atualmente feito com antibióticos, além de otimizar a produção, já que a perda por bactérias contaminantes é a principal responsável pela queda na produção total de uma safra. Desta forma, as dosagens de ácido lático no final do processo em cada uma das três usinas analisadas, respectivamente de 4,80 mMol/L, 6,84 mMol/L e 3,48 mMol/L, são indicadores importantes da ordem de grandeza da intensidade com que acontece a produção de ácido lático. O etanol passou a ser uma alternativa de fonte renovável de energia, mais limpa e menos agressiva ao meio ambiente, mas para que possa se tornar uma alternativa energética viável economicamente – quando comparada com combustíveis fósseis – as perdas na produção das indústrias sucro-alcooleiras, em razão de contaminações bacterianas, deverão ser gradualmente diminuídas, no futuro. Por se tratar de um tema ainda pouco explorado, serão fundamentais futuras pesquisas para criar uma metodologia capaz de detectar a forma e o momento em que ocorre a presença de microrganismos, evitando, assim, as perdas na produção do etanol, otimizando os resultados, reduzindo custos com o tratamento e buscando novas formas para a contenção desta contaminação. O cultivo da cana-de-açúcar acompanhou toda a história brasileira por cinco séculos e a história da produção de etanol nas últimas décadas tem mostrado a sua importância no uso como combustível, sobretudo a partir da crise do petróleo na década de 1970. Com a crescente importância dada às questões ambientais relacionadas ao aquecimento global, as discussões acerca da relevância da produção de álcool passaram para um patamar superior. O álcool produzido no Brasil a partir da cana-de-açúcar apresenta, portanto, vantagens ambientais e econômicas tanto em relação ao petróleo quanto em relação ao álcool produzido a partir do milho, como ocorre nos Estados Unidos. Desta forma, o aumento da eficiência no processo de produção de etanol deve ser considerado um objetivo estratégico prioritário em nosso país. CASTRO, M.M.S. Leveduras contaminantes do processo de fermentação alcoólica: diversidade taxonômica e metabólica. 1995. Dissertação (Mestrado) - Faculdade de Engenharia de Alimentos, Universidade Estadual de Campinas, Campinas, 1995. COUTEUR, P.; BURRESON, J. Os botões de Napoleão – As 17 moléculas que mudaram a história. Rio de Janeiro: Jorge Zahar, 2006. CRUEGER, W.; CRUEGER, A. Biotecnología: manual de microbiologia industrial. Zaragoza: Acribia, 1993. DIÉGUES JUNIOR, M. População e açúcar no Nordeste do Brasil. Rio de Janeiro: Comissão Nacional de Alimentação, 1954. FRANCO, B.D.G.M.; LANDGRAF, M. Microbiologia dos alimentos. São Paulo: Atheneu, 1996. GAVA, A.J. Princípios de tecnologia de alimentos. São Paulo: Nobel, 1998. GEISON, G.R. A ciência particular de Louis Pasteur. Rio de Janeiro: Contraponto, 2002. JOLY, A.B. Botânica. Introdução à taxonomia vegetal. São Paulo: Companhia Editora Nacional, 2002. LEHNINGER, A.L. Princípios de bioquímica. São Paulo: Savier, 1984. LIMA, U.A.; AQUARONE, E.; BORZANI, W. Tecnologia das fermentações. São Paulo: Edgard Blücher, 1975. v.1. (Série Biotecnologia). LIMA, U.A.; AQUARONE, E.; BORZANI, W.; SCHMIDELL, W. Biotecnologia industrial. São Paulo: Edgard Blücher, 2001. ROITMAM, I.; TRAVASSOS, L.; AZEVEDO, J.L. Tratado de microbiologia. São Paulo: Manole,1987. v.1. STANDAGE, T. História do mundo em 6 copos. Rio de Janeiro: Jorge Zahar, 2005. TORTORA, G.J.; FUNKE, B.R.; CASE, C.L. Microbiologia. Porto Alegre: Artmed, 2000. REFERÊNCIAS AQUARONE, E. Desinfecção Industrial - Tópicos de microbiologia industrial. São Paulo: Edgard Blücher, 1975. AZEVEDO, F. A cultura Brasileira. In: Instituto Brasileiro de Geografia e Estatística. São Paulo: Melhoramentos, 1943. BARLÉU, G. História dos feitos recentemente praticados durante oito anos no Brasil. Belo Horizonte: Livraria Itatiaia Editora, 1974. BRANDÃO, A. Cana-de-açúcar, álcool e açúcar na história e no desenvolvimento social do Brasil. Brasília: Horizonte Editora, 1985. VANIN, J.A. Alquimistas e químicos. São Paulo: Moderna, 1994. VARNHAGEN, F.A. História geral do Brasil. São Paulo: Melhoramentos, 1978. WARD, O. Biotecnologia de la fermentacion. Zaragoza: Editora Acribia, 1991. Recebido em 19/6/08 Aceito em 19/10/08 Biológico, São Paulo, v.71, n.1, p.69-76, jan./jun., 2009
Baixar