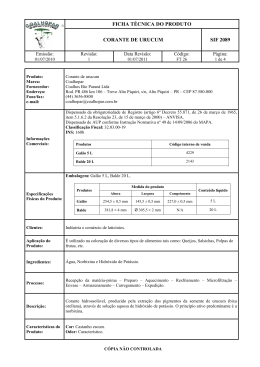
Cinética da degradação da cor de solução hidrossolúvel comercial de urucum, submetida a tratamentos térmicos1 Vera Lúcia Pupo FERREIRA2, Rodrigo Otávio TEIXEIRA NETO3,*, Silvia Cristina Sobottka Rolim de MOURA3, Marcelo Souza SILVA4 RESUMO Soluções comerciais hidrossolúveis de urucum foram submetidas a diferentes tratamentos de tempo/temperatura, a fim de se investigar a estabilidade da cor nestas condições. A cor foi medida em um espectrofotômetro COMCOR 1500 Plus no sistema Lab Hunter e os resultados são discutidos neste artigo, assim como as alterações de concentração do sal de norbixina e os parâmetros de cor L, a e b Hunter. Os resultados foram analisados quanto à ordem da reação e a dependência da temperatura pôde ser descrita pelo modelo de Arrhenius, com valores de energia de ativação entre 11 e 25 kcal/mol. As alterações de cor observadas foram o aumento de luminosidade do amarelo e diminuição do vermelho. As reações de degradação do sal de nobixina foram de 2a ordem e de 1a ordem para os outros parâmetros de cor. Palavras-chave: sal de norbixina, cinética da degradação de cor, tratamento térmico, urucum. SUMMARY KINETICS OF COLOR DEGRADATION OF WATERSOLUBLE COMMERCIAL ANNATTO SOLUTIONS UNDER THERMAL TREATMENTS. Commercial water-soluble annatto solutions were submitted to different time/temperature treatments to investigate the stability of the color in these conditions. The color was measured in a COMCOR 1500 Plus spectrophotometer in the Hunter Lab System and the results are discussed, as well as the changes in the norbixin salt concentration and L, a, b color parameters. Data were analised for order reaction and the temperature dependence being well explained by the Arrhenius model, with activation energy values between 11 and 25 kcal/mol. The changes in color showed increase on lightness and yellow color and decrease on red color. Norbixin salt degradation reaction follows the second order and for other color parameters, the first order. Keywords: norbixin salt, kinetic color degradation, thermal treatment, annatto. 1 – INTRODUÇÃO Os corantes de urucum (Bixa orellana L.) têm sido usados há muitos anos para a produção de produtos de maquilagem, de tintura de tecidos e de alimentos. Os corantes são encontrados recobrindo a superfície externa das sementes de urucum e são constituídos na sua maioria (cerca de 80%) de α-bixina que é um monometilester do ácido carboxílico da α-norbixina [7]. Para uso em alimentos, a extração do corante lipossolúvel é feita, usualmente, em óleo comestível sob a ação do calor, cujo pigmento principal continua sendo a bixina, apesar da formação de compostos de degradação e de isomerização [9]. Para a aplicação de corantes em produtos como queijos, torna-se necessária a utilização de corantes hidrossolúveis de urucum, que são obtidos pela hidrólise da bixina com soluções de álcalis de sódio ou potássio, formando um sal hidrossolúvel da norbixina com máxima absorbância a 453nm e 483nm [4, 9]. A cor do extrato hidrossolúvel varia de castanho avermelhado a castanho, sendo a estabilidade desta coloração de grande importância nas aplicações industriais durante os processos térmicos. FERREIRA et al. [2], em estudos da cor e do teor de sal de norbixina de solução hidrossolúvel de urucum, de marca comercial, submetida a binômios de tempo x temperatura de 29,8 a 270,2 minutos sob 79,9oC a 200,1oC e de 30,1 a 139,9 minutos sob 70,1oC a 119,9oC, utilizando delineamento de superfície de resposta, mostraram que, de maneira geral, ocorreu diminuição dos teores de norbixina e que as variáveis de cor observadas foram, basicamente, aumento da luminosidade, diminuição do vermelho e aumento ou diminuição dos teores de amarelo. Os intervalos de tempo e temperatura onde ocorreram as menores variações de cor das amostras tratadas em relação à original foram de 30 a 63 minutos na faixa de 70oC a 107oC e de 120 a 140 minutos na faixa de 70oC a 90oC. Em vista disto, o presente trabalho foi realizado com o objetivo de investigar a estabilidade desta solução, quando submetida a diferentes tratamentos de tempo/temperatura, que poderiam ser utilizados pela indústria tanto de alimentos, como de outros produtos, como de tingimento em tecidos, utilizandose um sistema modelo em água. 2 – MATERIAL E MÉTODOS 2.1 – Material Solução hidrossolúvel do corante de urucum, de marca comercial, foi homogeneizada em banho ultrassônico e submetida a tratamentos térmicos de 90oC, 100oC, 120oC e 140oC em cinco períodos de duração variando de 90 a 450 minutos. As amostras (10mL) acondicionadas em tubos de aço inox vedados e acoplados a termopares do tipo T foram aquecidas em banho termostático de óleo e a temperatura controlada por meio de termômetro digital. Imediatamente após tratamento térmico as amostras foram resfriadas com água corrente até temperatura ambiente, acondicionadas em tubos de vidro protegidos da luz e estocadas a 5 ± 2 oC (máximo de 4 dias) até serem analisadas. 2.2 – Métodos 2.2.1 - Cor Foi empregada a diluição de 0,2mL de corante previamente homogeneizado para cada 100mL de água destilada. Cor objetiva As amostras foram analisadas, em duplicata, quanto à cor (reflexão) por meio de um espectrofotômetro COMCOR 1500 Plus, configuração DREOL, ângulo de observação 10o, iluminante C, sistema Lab Hunter, espessura da amostra de 15mm controlados por anteparo branco (LH = 89,09, aH = -1,41 e bH = 3,23) (Comunicação pessoal, V.L.P. Ferreira e colaboradores, Instituto de Tecnologia de Alimentos, Campinas-Brasil. 1995). O sistema Lab Hunter é um sistema de coordenadas retangulares que define a cor em termos de luminosidade (L), vermelho versus verde (a) e amarelo versus azul (b). Foi calculada a diferença total de cor (∆E) [3], de acordo com a equação: ∆E = [ (∆L)2+(∆a) 2 +(∆b) 2 ]1/2 em que ∆ = diferença entre cada parâmetro de cor das amostras com e sem tratamento. Não foi necessária a análise estatística dos resultados, pois se desejava testar apenas a repetibilidade da análise e não do tratamento. Cor subjetiva Cada grupo de amostras tratadas e a amostra não-tratada foram avaliadas visualmente sob iluminante C, por equipe de 3 a 5 julgadores com discriminação superior para cor, pela ordenação em termos de intensidade maior para menor, dos parâmetros luminosidade, vermelho/verde e amarelo, sob delineamento estatístico de blocos completos. Os dados obtidos foram analisados estatisticamente pelo teste de Friedmann, empregando-se a tabela de Newel e Mac Farlane [8]. 2.2.2 - Teor de norbixina A concentração do sal de norbixina nas diferentes amostras tratadas termicamente foi determinada pela diluição das amostras em solução de KOH 5% (E1%1cm= 2850 ± 40, λ = 453nm), de acordo com método da FAO/WHO [1] em espectrofotômetro Varian. 2.2.3 - Parâmetros cinéticos Os dados obtidos da concentração de sal de norbixina e dos parâmetros de cor L, a, b Hunter, para cada tratamento, foram analisados quanto à ordem de reação de degradação e calculadas as respectivas constantes de reação (k) a diferentes temperaturas, as energias de ativação (Ea) e o quociente entre as velocidades de reação a uma determinada temperatura e a uma temperatura 10 oC mais baixa (Q ) [10]. 10 3 – RESULTADOS E DISCUSSÃO 3.1 – Cor objetiva A amostra original apresentou valores de LH = 44,2; aH = 20,8 e bH = 30,5 (Tabela 1) e foi observada a formação de precipitado branco em todas as amostras tratadas termicamente que foram homogeneizadas para as determinações de pigmento. A quantidade de precipitado é mínima não interferindo assim na determinação espectrofotométrica já que esta envolve comprimentos de onda específicos. Supõe-se que deva ocorrer o mesmo em alimentos. Os aumentos dos valores de luminosidade (LH) foram muito pequenos nas amostras tratadas a 90 oC, mas elevaram-se com o tempo nas outras temperaturas, representando um clareamento das amostras. Os valores de vermelho (aH) diminuíram, sendo esta diminuição mais intensa quanto mais alta a temperatura, representando a degradação praticamente total do sal de norbixina, e a 140 oC/270 min. passaram a apresentar valores de aH negativos, indicando a presença do componente verde da cor. Houve aumento dos valores de amarelo (bH) para todas as temperaturas, com exceção para os tempos maiores que 180 min. a 140 oC. O aumento do amarelo (bH), segundo MCKEOWN [6], é devido à formação de compostos de degradação da cor amarela e a sua diminuição a T= 140 oC é devida à degradação dos pigmentos amarelos a altas temperaturas. Observou-se aumento dos valores de DE com o aumento da temperatura e do tempo, representando perdas significativas da cor da amostra original. Houve redução dos teores de sal de norbixina (Tabela 1) em todas as temperaturas e períodos de tempo. Conforme esperado, a temperatura de 140 oC, nos períodos de tempo estudados, foi muito mais agressiva que as demais ao sal de norbixina, reduzindo drasticamente o seu teor após 90 minutos de tratamento. Observou-se também, dos dados da Tabela 1, que na faixa de 90 a 100oC as variáveis de cor são mais dependentes da temperatura e menos dependentes do tempo e na faixa de 120 a 140oC são dependentes tanto da temperatura quanto do tempo, fato este que já havia sido observado em estudos anteriores [2]. 3.2 – Cor subjetiva Na Tabela 2, os maiores valores significam amostras mais claras para a luminosidade e mais vermelhas ou amarelas para estes parâmetros. A partir de 360 min a 100oC e 120oC, os tratamentos diferiram (α = 5%) dos demais quanto à luminosidade, ao vermelho e ao amarelo e quanto à luminosidade a 140 oC. Os resultados obtidos visualmente apresentaram a mesma tendência dos dados da análise objetiva da cor. 3.3 – Parâmetros cinéticos Com base nos dados obtidos (Tabela 1), determinou-se a ordem das reações (Tabela 3, Figura 1): para a porcentagem de sal de norbixina - 2a ordem; para LH, aH e bH - 1a ordem e para a diferença total de cor (∆E) - ordem zero. No caso dos valores de amarelo (bH), a representação do modelo de Arrhenius foi feita em duas partes (Figura 2 d,e), de zero a 180 minutos, representando os valores crescentes de bH e, de 270 a 450 minutos, representando os valores decrescentes de bH a 140oC, em função das alterações ocorridas na formação de diferentes pigmentos oriundos da degradação do sal de norbixina. FIGURA 1. Modelos cinéticos da solução hidrossolúvel de urucum: a) degradação de sal denorbixina; b) luminosidade (LH); c) vermelho/verde (aH); d) amarelo (bH); e) diferença total de cor (∆E). l 90 oC; n 100 oC; 120 oC; ¹ 140 oC. Deve-se levar em conta que os testes realizados a 120 oC (Tabela 3) acarretaram resultados melhores (r2 maiores) na determinação da velocidade da reação (k), indicando que os parâmetros de cor e teores de pigmentos apresentaram um comportamento cinético mais uniforme do que nas demais temperaturas. Com base nos dados obtidos neste estudo, o processo a 120oC da solução hidrossolúvel apresenta melhor controle, porém não significando menores alterações de cor do que a 90 ou 100oC. Os valores da energia de ativação (Ea) foram calculados para os parâmetros de cor e teor de norbixina (Tabela 3, Figura 2), tendo todos seguido o modelo de Arrhenius com coeficientes de correlação (r2) superiores a 88%. Os valores de energia de ativação foram supe-riores para as reações de degradação do sal de norbixina (23,9 kcal/mol) e de aH (24,4 kcal/mol). As reações de alteração dos valores de luminosidade LH, amarelo bH e de diferença total de cor DE apresentaram valores de energia de ativação entre 11 e 18 kcal/mol. As energias de ativação calculadas para a degradação do sal de norbixina e a diminuição do teor de vermelho foram mais que o dobro necessário para o início das reações de aumento de luminosidade e uma vez e meia maior do que para a reação de aumento dos teores de amarelo. Significa dizer que a degradação do sal de norbixina ou a diminuição dos teores de vermelho é muito mais dependente da temperatura que as reações de clareamento da solução, aumento do amarelo e, conseqüentemente, da diferença total de cor, ou seja, com o aumento da temperatura houve muito mais degradação do sal de norbixina ou aumento dos teores de vermelho do que aumento da luminosidade ou do amarelo, em um mesmo tempo. FIGURA 2. Dependência da temperatura – Modelo de Arrhenius: a) degradação do sal de norbixina; c) luminosidade (LH); c) vermelho/verde (aH); d) amarelo (bH) 0 a 180 min; e) amarelo (bH) 270 a 450 min; f) diferença total de cor (∆E). Os valores de energia de ativação obtidos encontram-se dentro da faixa de 10 a 30 kcal/mol, como mencionado por LUND [5] para cor de alimentos. Os valores de Ea equivalem a Q10 na faixa de 1,5 a 2,3 para a faixa de temperatura de 90 a 140oC (Tabela 3), significando que as reações são aceleradas apenas moderadamente pela temperatura, isto é, a cada 10oC de aumento na temperatura nesta faixa, praticamente as reações no máximo alcançam um pouco mais que o dobro de velocidade. Deve-se observar que sendo as energias de ativação maiores para as reações de degradação do sal de norbixina (2,2) e de alteração de vermelho (2,3), os valores de Q10 para estas reações foram um pouco superiores aos alcançados para as reações de alteração de luminosidade (1,5), para o amarelo (1,8/1,4) e para a diferença total de cor (1,5). 4 – CONCLUSÕES Nas condições do estudo observou-se que as alterações de cor e diminuição dos teores de sal de norbixina são dependentes da temperatura e do tempo de tratamento. Nas temperaturas de 90 e 100oC as reações são menos dependentes do tempo do que nas de 120 e 140oC, quando as amostras tornaram-se mais claras, menos vermelhas e mais amarelas, chegando a esverdeadas a 140oC/270 minutos. Esta informação é relevante para as aplicações industriais já que é de fundamental importância a estabilidade do pigmento. Pôde-se também observar que os testes realizados a 120oC acarretaram resultados melhores para a determinação da velocidade da reação, indicando que os parâmetros de cor e os teores de pigmentos apresentaram um comportamento cinético mais uniforme do que nas demais temperaturas. As reações de degradação de cor e os teores de pigmentos foram moderadamente afetados pela temperatura, praticamente dobrando sua velocidade a cada 10oC de aumento, sendo que a degradação do sal de norbixina e o parâmetro aH são mais influenciados que os demais parâmetros analisados, apresentando valores de energia de ativação maiores. 5 – REFERÊNCIAS BIBLIOGRÁFICAS [1] FAO/WHO Specifications for identify and purity of some food additives. FAO Nutrition Meetings Reporting Series, n. 54B, p. 4-10, 1976. [2] FERREIRA, V.L.P.; YOTSUYANAGI, K; CARVALHO, P.R.N.; TEIXEIRA NETO, R.O. Comportamento do sal de norbixina (Bixa orellana, L.) frente a diferentes binômios de tempo e temperatura. Anais do III Congresso Brasileiro de Corantes Naturais e III Simpósio Brasileiro sobre Urucum, Porto Seguro: Editora Bahia, 1999 (no prelo). [3] FRANCIS, F.J.; CLYDESDALE, F.M. Food colorimetry: theory and applications Westport;, AVI., 1975. 477 p. [4] HERNANDEZ C.P.; RUSIG, O.; CARVALHO, P.R.N. Influence of heating time on thermal degradation of bixin in alkaline extracts of annatto (Bixa orellana L). Arq. Biol. Tecnol., v. 36, n. 4, p. 819-838, 1993. [5] LUND, D.B. Effect of commercial processing on nutrients. Food Technol., v. 33, n. 2, p. 28-35, 1979. [6] MCKEOWN, G.G. Composition of oil-soluble annatto food colours. II Thermal degradation of bixin J. Assoc. Off. Anal. Chem., v. 46, n. 5, p. 790796, 1963. [7] MCKEOWN, G.G.; MARK, E. The composition of oil-soluble annatto food colours J. Assoc. Off. Anal. Chem., v. 45, p. 761-766, 1962. [8] NEWEL, G.J.; MAC FARLANE, J.D. Expanded tables for multiple comparison procedures in the analyses of ranked data J. Food Sci., v. 52, n. 6, p. 1721-1725, 1987. [9] REITH J.F.; GIELEN, J.W. Properties of bixin and norbixin and the composition of annatto extracts J. Food Sci, v. 36, n. 6, p. 861-864, 1971. [10] [VITALI, A.A; TEIXEIRA NETO, R.O. Introdução à cinética de reação em alimentos. In: Teixeira Neto, R.O; Vitali, A.A (Coord.) Reações de transformação e vida de prateleira de alimentos processados, 2. ed. Campinas: Instituto de Tecnologia de Alimentos, 1996. p. 2.1-2.13. (Manual Técnico no.6) 6 – AGRADECIMENTOS Projeto apoiado pelo Programa de Bolsa de Produtividade em Pesquisa do Conselho Nacional de Desenvolvimento Científico e Tecnológico – CNPq para o autor principal, e financiado pelo Governo do Estado de São Paulo. 1 Recebido para publicação em 15/05/98. Aceito para publicação em 13/04/98. 2 Common Sense - Serviços e Assessoria em Análises Físicas e Sensoriais. Fone/Fax: (019) 241-6741, Campinas-SP 3 Instituto de Tecnologia de Alimentos, Av. Brasil 2880, CEP 13073-001. Fone: (019) 241-5222 ramal 170 Fax: (019) 242-3104. Campinas-SP, [email protected] [email protected] 4 Bolsista de Iniciação Científica - CNPq. * A quem a correspondência deve ser enviada.
Baixar