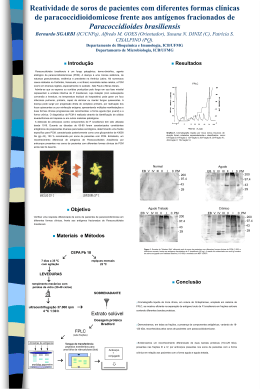
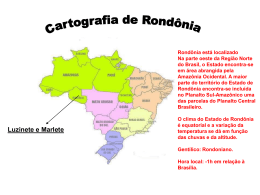
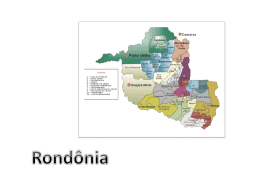
UNIVERSIDADE FEDERAL DE RONDÔNIA - UNIR NÚCLEO DE SAÚDE - DEPARTAMENTO DE MEDICINA PROGRAMA DE PÓS - GRADUAÇÃO EM BIOLOGIA EXPERIMENTAL – PGBIOEXP. “Análise da Situação Epidemiológica da Paracoccidioidomicose em Rondônia 1997 a 2008 – Brasil.” Sônia Maria Dias de Lima PORTO VELHO 2010 Sônia Maria Dias de Lima “Análise da Situação Epidemiológica da Paracoccidioidomicose em Rondônia, 1997 a 2008- Brasil”. Dissertação apresentada ao Programa de Mestrado em Biologia Experimental da Fundação Universidade Federal de Rondônia – UNIR – NUSAU. Para obtenção do título de Mestre em Biologia Experimental. Área Epidemiologia. Orientadora: Profª . Dra. Ana Lúcia Escobar. PORTO VELHO 2010 de Concentração “Análise da Situação Epidemiológica da Paracoccidioidomicose em RONDÔNIA 1997 a 2008 – Brasil.” Sônia Maria Dias de Lima Banca Examinadora: Profª Dra Ana Lucia Escobar (UNIR) Profª Dra. Maria Manuela da Fonseca Moura (UNIR) Prof. Dr. Reinaldo Souza Santos (ENSP-FIOCRUZ) PORTO VELHO 2010 DEDICATÓRIA Dedico este trabalho a Rodolfo meu filho que compreendeu a minha ausência e que soube entender meus dias de reclusão e tristeza. AGRADECIMENTOS Durante a realização deste trabalho fui auxiliada de diversas formas e por diversas pessoas sem as quais muito pouco poderia ter sido feito. Agradeço a minha família pelo apoio e por me amparar sempre quando foi preciso. Em especial à minha orientadora professora Dra. Ana Lucia Escobar, por assumir a minha orientação do mestrado, de compartilhar seus conhecimentos, e pela possibilidade de estar no mestrado. Aos meus amigos o Professor Dr. Bodo Wanke do IPEC FIOCRUZ – Rio de Janeiro/RJ, pelo incentivo e pelas horas de discussão sobre Paracoccidioidomicose; e à Professora Dra. Maria Cristina Basílio Crispim da Silva – bióloga do DSE do CCEN-/ UFPB - João Pessoa/PB. Ao médico e amigo Rui Rafael Durlacher, pelo desafio de trabalhar com a PCM e a importância e atenção que dispensa à micologia médica em Rondônia e em Especial aos pacientes com paracoccidioidomicose. À amiga Augusta Ramalhaes pela paciência nas orientações de análises de banco de dados. À amiga Flávia Serrano pelo incentivo, força e apoio nas horas de desânimo. À Agência Estadual de Vigilância em Saúde / SESAU/RO por permitir a execução deste trabalho, autorizando o acesso ao banco de dados da Paracoccidioidomicose. Aos colegas de mestrado, turma 2008, pelos dias de aprendizado, de convívio e de divagações sobre a academia. Aos amigos pela compreensão e apoio nas horas de cansaço. Em especial, Regina Barroso, Neide Melo, Nazaré Reis, Berenice Gomes, Lucicreide Maria e Felipe Michel, pela força e incentivo. Ao Pedro Paulo F. Coutinho pela tabulação de dados e orientação do Sistema de Informação da AGEVISA. Às colegas do Departamento de Enfermagem, que me auxiliaram nas dificuldades em especial à Profª. Dra. Adailde Miranda. (...) Divêrjo de todo o mundo... Eu quase que nada não sei. Mas desconfio de muita coisa. (...) João Guimarães Rosa. RESUMO A Paracoccidioidomicose (PCM) é a micose sistêmica granulomatosa de evolução crônica, sendo considerada dentre outras a mais importante do Brasil, que representa a área de maior endemicidade no mundo, com 80% dos casos. Não é doença de notificação compulsória, o que não permite o real conhecimento da magnitude do problema. A pesquisa objetivou conhecer o perfil epidemiológico da paracoccidioidomicose em Rondônia entre 1997 e 2008. Metodologia: Foram analisados, retrospectivamente, 1856 fichas de notificação de pacientes com diagnóstico para PCM entre 1997 e 2008. A coleta das informações foi realizada em protocolo padronizado e os dados foram obtidos no Sistema de Informação do Programa Estadual PCM. Os dados foram organizados e digitados no EPI INFO versão 3.51 e analisados no aplicativo tabwin e Excel 2007. Resultados: Observou-se a alta prevalência de PCM em Rondônia e a importância da organização do serviço de Vigilância epidemiológica na promoção, prevenção e assistência do agravo. Conclusão: A incidência aumentou nos últimos 12 anos, porém com declínio nos anos 2007 e 2008. O gênero masculino em idade produtiva da região central e sul do estado foi o mais prevalente. Evidenciando um problema ao sistema público de saúde em Rondônia. A forma crônica foi a que apresentou maior percentual. A PCM foi responsável por 94 óbitos no período. A disponibilização do medicamento tem sido fator importante para o manejo terapêutico e acompanhamento clínico. Há necessidade de capacitar melhor os profissionais de saúde no diagnóstico clinico, laboratorial, tratamento e vigilância epidemiológica. Descritores: Paracoccidioidomicose, Endemia, Epidemiologia, Rondônia. ABSTRACT Paracoccidioidomycosis (PCM) is the systemic granuloma mycosis of chronic evolution, being considered among other the most important of Brazil, which represents the area of largest endemicity in the world, with 80% of the cases. It is not a disease of compulsory notification, what doesn't allow the real knowledge of the magnitude of the problem. The research aimed to evaluate the epidemiological profile of Paracoccidioides the state of Rondônia between 1997 and 2008. Methodology: They were analyzed, retrospectively, 1856 records of patients' notification with diagnosis for PCM between 1997 and 2008. The collection of the information was accomplished in standardized protocol and the data were obtained in the System of Information of the State Program PCM. The data were organized and typed in EPI INFO version 3.51 and analyzed in the application tabwin and Excel 2007. Results: The high prevalence of PCM was observed in Rondônia and the importance of the Organization of the service of epidemic Surveillance in the promotion, prevention and assistance of the offence. Conclusion: The incidence increased in the last 12 years, but with a decline in the years 2007 and 2008. The males of working age in central and southern state were the most prevalent. Indicating a problem when the public health system in Rondonia. The chronic form showed the highest percentage PCM was responsible for 94 deaths in the period. The availability of the drug has been an important factor for therapeutic management and clinical monitoring. There is need to train more health professionals in clinical diagnosis, laboratory and treatment, epidemiological surveillance. Descritores: Paracoccidioidomycosis, Endemic, Epidemiology, Rondônia. LISTA DE FIGURAS FIGURA..1. Distribuição geográfica da paracoccidioidomicose..no mundo FIGURA 2. Distribuição de casos notificados de PCM por municípios, Rondônia 1997 a 2008 ...................................................................................... 15 29 FIGURA 3. Taxa de incidência de PCM por municípios em Rondônia, 1997 – 2008..................................................................................................................... 31 LISTA DE TABELAS TABELA 1. Distribuição de casos de notificados PCM, segundo faixa etária em Rondônia, 1997 - 2008................................................................... 32 TABELA 2. Distribuição de casos de notificados PCM, segundo gênero em Rondônia, 1997 – 2008 .......................................................................... TABELA 3. Taxa de mortalidade por PCM por 32 100.000/hab. Rondônia, 1997 – 2008 .................................................................................. 38 TABELA 4. Distribuição do número de óbitos e coeficiente de letalidade. Rondônia, 1997 – 2008 ................................................................................ 39 TABELA 5. Taxa de mortalidade por paracoccidioidomicose, segundo municípios, Rondônia, 1997 a 2008.......................................................... 40 LISTAS DE GRÁFICOS GRÁFICO 1. Distribuição de tipos de micoses notificadas em Rondônia, no período de 1997 – 2008 ......................................................................................... 28 GRÁFICO 2. Taxa de incidência da PCM em Rondônia, no período de 1997– 30 2008. GRÁFICO 3. Distribuição da média mensal de casos de PCM em Rondônia, no período de 1997 – 2008 ........................................................................................... 30 GRÁFICO 4. Grau de escolaridade dos pacientes com PCM em Rondônia, no período 1997 – 2008 ................................................................................................ 33 GRÁFICO 5. Distribuição de casos de PCM segundo população da zona urbana e rural , em Rondonia, 1997 – 2008.......................................................................... 33 GRÁFICO 6. Distribuição de casos de PCM segundo ocupação em Rondônia, no período de 1997 -2008.............................................................................................. 34 GRÁFICO 7. Distribuição de casos de PCM segundo sítios anatômicos em Rondônia, no período de 1997 2008........................................................................ 35 GRÁFICO 8. Distribuição de casos de PCM segundo forma clínica em Rondônia, no período de 1997 – 2008........................................................................................ GRÁFICO 35 9. Critérios de confirmação diagnóstica da PCM , segundo ficha de notificação. Rondônia, 1997 – 2008.......................................................................... 36 GRÁFICO 10. Terapêutica antifúngica aplicada em Rondônia, no período de 1995 a 2008.............................................................................................................. 37 GRÁFICO 11 . Distribuição do número de óbitos por PCM em relação ao número de casos na Rondônia 1997 a 2008........................................................................ 38 LISTA DE ABREVEATURAS E SIGLAS AGEVISA Agência Estadual de Vigilância em Saúde FIOCRUZ Fundação Instituto Oswaldo Cruz FUNASA Fundação Nacional de Saúde PCM Paracoccidioidomicose P. brasiliensis Paracoccidioides brasiliensis PBMICOSE Micose brasiliensis PEC-PCM Programa Estadual de Controle de Micoses sistêmicas SESAU Secretaria Estadual de Saúde por Paracocidioides SUMÁRIO 1. INTRODUÇÃO............................................................................................ 13 2. REVISÃO DE LITERATURA..................................................................... 15 2.1 ECO EPIDEMIOLOGIA DA ARACOCCCIDIOIDOMICOSE..................... 15 2.2 . DIAGNÓSTICO....................................................................................... 18 2.3. TRATAMENTO........................................................................................ 19 2.4 INDICADORES EPIDEMIOLÓGICOS...................................................... 19 2.4.1 Histórico da Paracoccidioidomicose em Rondônia.......................... 23 3. OBJETIVO GERAL.................................................................................... 25 3.1 OBJETIVOS ESPECÍFICOS..................................................................... 25 4. METODOLOGIA ........................................................................................ 26 4.1 DELINEAMENTO...................................................................................... 26 4.1.1 Análise de Dados................................................................................... 26 5. RESULTADOS ........................................................................................... 28 6. DISCUSSÃO............................................................................................... 41 7. CONCLUSÕES........................................................................................... 46 8. REFERÊNCIAS.......................................................................................... 48 9. ANEXOS.................................................................................................... 60 13 1. INTRODUÇÃO A Paracoccidioidomicose (PCM) é a micose sistêmica mais relevante na área médica no Brasil, a maioria dos casos procede das regiões sul, sudeste e centro oeste (LACAZ, 1984; LONDERO 1978, PEDROSA & NOUGUEIRA 1984) que tem como agente causal o fungo dimórfico e geofílico Paracoccidioides brasiliensis, descrito inicialmente por Adolfo Lutz em 1908 (LUTZ, 1908; LACAZ, 1984). Sendo considerada rara ou inexistente no Norte do país (MORAES & FERREIRA 1967; PEDROSA & NOUGUEIRA; 1984). Também foi conhecida como micose de Lutz, “granuloma coccidioico”, “granuloma paracococcidioico”, blastomicose e blastomicose sul-americana. Foi observada pela primeira vez no Brasil por Adolpho Lutz, a quem chamou à atenção as lesões bucais encontradas nos pacientes. A denominação paracoccidioidomicose foi adotada em 1971 no Simpósio realizado em Medellín, na Colômbia, quando foi abandonada a denominação blastomicose sul-americana (LACAZ, 1982). Esta micose é causada por um fungo térmo-dimórfico, autóctone da América Latina, ocorrendo em regiões tropicais e subtropicais, encontrada Colômbia e Venezuela (ALBORNOZ, 1971) e principalmente no Brasil, sendo considerado um centro endêmico dessa doença, com maior prevalência nas regiões sul, sudeste e centro oeste (MALUF, PEREIRA, TAKAHACHI G ET AL, 2003). A distribuição desta endemia no continente americano é heterogênea, coexistindo em áreas de baixa e alta endemicidade (WANKE & LONDERO, 1994). A paracoccidioidomicose tem um alto potencial incapacitante, mas para alguns segmentos sociais específicos, como indígenas, moradores rurais, trabalhadores rurais, região periurbana e atividades que envolvem manejo com solo, essas incapacidades físicas e mortes prematuras vêem sendo observadas com maior freqüência. As manifestações clínicas da doença são decorrentes do rápido e progressivo envolvimento de órgãos do sistema mononuclear fagocitário particularmente os pulmões, tegumento, gânglios, baço, fígado e órgãos linfóides do tubo digestivo (ANDRADE, 1983). Quando não diagnosticada e tratada oportunamente, pode levar a formas disseminadas graves e letais. 14 Os primeiros estudos sobre PCM em Rondônia teve inicio em 1952 (LEITE, 1984) descreve três casos de Paracoccidioidomicose, não sendo possível comprovar sua autoctonia. Estudos realizados entre povos indígenas particularmente os Surui de Rondônia (COIMBRA Jr. ET AL., 1989), são os primeiros registros do agravo, sendo que o primeiro caso clínico autóctone publicado foi por Colombo et al. (1990), em paciente procedente do mesmo grupo. Por não ser um agravo de notificação compulsória para a vigilância epidemiológica no âmbito Nacional, os estados que têm registro de PCM fazem o acompanhamento dos casos em bancos de dados paralelos, onde se armazenam os dados de identificação do paciente, como informações clínico/laboratoriais e tratamento. Fica sob a responsabilidade dos estados a aquisição dos medicamentos. É importante ressaltar que em relação aos dados laboratoriais, somente a partir de 2006 é implantada no estado a coleta sorológica, em que as amostras são encaminhadas para o serviço de micologia da FIOCRUZ laboratório de referência nacional. Devido à falta de inclusão deste agravo no Sistema Nacional de Agravos de epidemiologia Notificação dessa (SINAN), doença, e um conhecimento objetivamos comparar completo nosso da perfil epidemiológico e demográfico, com a literatura pertinente, e analisar a situação epidemiológica da PCM em Rondônia, através de uma análise retrospectiva do banco de dados do Programa Estadual de Paracoccidioidomicose, referente ao período de 1997 a 2008, buscando contribuir com a proteção e prevenção do referido agravo no estado de Rondônia. 15 2. REVISÃO DA LITERATURA A paracoccidioidomicose no Brasil representa a área de maior endemicidade no mundo com mais 80% dos casos, segundo Naiff et al. (1986), implicando assim num grave problema de Saúde Pública conforme demonstrado na figura abaixo: Figura 1. Distribuição geográfica da paracoccidioidomicose no mundo (2006) Fonte: Consenso Nacional de Paracoccidioidomicose (2006). 2.1. ECO EPIDEMIOLOGIA DA PARACOCCCIDIOIDOMICOSE Segundo Alencar (2003), dados positivos vêm-se acumulando a partir do isolamento do P. brasiliensis nas vísceras do tatu, por Naif et al., em 1986 e 1989, no sul do estado do Pará; Macedo et al., em 1998, na região da serra da mesa em Goiás; Bagagli et al., em 1998, em diferentes regiões da área endêmica de Botucatu; Restrepo et al., em 1999, na Colômbia. Embora não definido o seu 16 papel na cadeia epidemiológica dessa patologia, os tatus (Dasypus novemcinctus) apresentam o fungo em seus tecidos (SILVA-VERGARA ET AL, 1998; 2000). Há pouco tempo apenas os humanos eram tidos como os únicos hospedeiros naturalmente infectados por este fungo (RESTREPO, 1985). Atualmente, estudos foram realizados identificando alguns animais portadores da infecção como o tatu e cães da zona urbana, periurbana e rural da região de Londrina, Paraná (ONO ET AL., 2001). Em 2002, Ricci et al., relatou o primeiro achado confirmado de paracoccidioidomicose doença em cão da raça Dobermann. Segundo Corte et al., (2007); e (COSTA, FAVA NETTO, 1978; MÓS; FAVA NETTO, 1974; ONO ET AL., 2001; SILVEIRA ET AL., 2006, 2008); a infecção por P. brasilienses tem sido demonstrada em diferentes espécies de animais domésticos como cães, bovinos, eqüinos e silvestres como macacos e felinos. Ainda que tal fato não tenha sido comprovado (BAGAGLI ET AL., 2006). Alguns estudos clínicos e laboratoriais demonstraram ser a via inalatória como porta de entrada do P. brasiliensis no homem (BORGES-WALMSLEY ET AL., 2002; MONTENEGRO & FRANCO, 1994; BRUMMER ET AL., 1993; MCEWEN ET AL., 1987) No Brasil, os Estados de São Paulo, Paraná, Rio de Janeiro, Rio Grande do Sul e Minas Gerais, apresentam maior número de casos registrados em humanos (COUTINHO ET AL., 2002). Os casos que foram relatados fora da área endêmica, são de pacientes que visitaram ou residiram por algum tempo em um país da América Latina (BICALHO ET AL., 2001; PANIAGO ET AL 2003; SPOSTO, ET AL., 1993). Segundo Shikanai-Yasuda et al (2006), o fungo P. brasiliensis apresentase na natureza como estruturas filamentosas contendo propágulos infectantes denominados conídios, que uma vez inalados, dão origem a formas leveduriformes do fungo que constituirão sua forma parasitária nos tecidos do hospedeiro. A uma temperatura de 25ºC, o fungo P. brasiliensis cresce na forma de micélio e na forma de levedura no organismo humano ou in vitro em temperatura de 37ºC. O primeiro órgão a ser afetado é o pulmão, após a inalação de propágulos do fungo, proveniente do solo, podendo haver disseminação para outros órgãos e tecidos como: fígado, baço, linfonodos, pele e mucosas 17 (BRUMMER; CASTANEDA; RESTREPO, 1993; SCULLY; ALMEIDA, 1992). A infecção pelo P. brasiliensis é adquirida nas duas primeiras décadas de vida com incidência maior entre 10 e 20 anos de idade. Pode ser classificado em: PCM-infecção e PCM-doença (FRANCO ET AL., 1987). A PCM infecção atinge indivíduos aparentemente sadios de ambos os sexos, que residem ou residiram em áreas endêmicas com resultado positivo para P. brasiliensis em teste intradérmicos com paracoccidioidina ou sorologia, mas não desenvolvem a doença. A PCM-doença acomete preferencialmente em indivíduos do sexo masculino, em áreas periurbanas, moradores e/ou trabalhadores rurais, com faixa etária entre 30 e 50 anos. Enquanto as formas agudas e subagudas têm menor freqüência e ocorrem em jovens independentemente do sexo (BLOTTA, CAMARGO, 1993; LONDERO, RAMOS, 1972; MCEWEN ET AL., 1995). Não se comprovou a distribuição inter-humana da PCM, admitindo-se que a infecção ocorre após exposição acidental ao fungo P. brasiliensis (FRANCO, 1987). No decorrer das últimas décadas, têm sido observadas importantes alterações na freqüência, nas características demográficas da população atingida e na distribuição geográfica da PCM. Dependendo da região, a incidência alterouse, sem que se possam justificar totalmente as suas causas. É provável que o processo de urbanização e melhoria do diagnóstico explique, em parte, estas alterações. Além do mais, desequilíbrios ambientais decorrentes da exploração de novas fronteiras agrícolas, como: derrubada de florestas, queimadas, sobretudo nas regiões Centro-Oeste e Norte, atingindo marcadamente a Amazônia, também contribuíram para o atual quadro da PCM. (YASUDA ET AL., 2006). São considerados fatores de risco para paracoccidioidomicose morar em área endêmica, susceptibilidade genética ainda é questionável, trabalhar com atividades agrícolas contínuas, hábitos com tabagismo e etilismo, operar maquinas pesadas em atividades de terraplanagem, preparos de solo, serviços ligados a jardinagem, transportes de vegetais entre outros. Em todas as casuísticas estudadas observou-se que nas primeiras décadas de vida dos pacientes com diagnósticos de PCM havia a associação a algum tipo de atividade agrícola; e provavelmente nesta época foram infectados. 18 Diferente de outras micoses como criptococose, candidíase, aspergilose, histoplasmose as infecções por P. brasiliensis não estão relacionadas com doenças imunodepressoras. No entanto, existem casos desta micose associados à infecção pelo HIVAIDS, tuberculose (TB) e neoplasias (YASUDA ET AL., 2006). A associação entre PCM e TB não é incomum, sendo relatada há anos, dados da literatura apontam uma freqüência dessa associação variando de 5,5 a 19% (PANIAGO ET AL., 2003; PALHETA-NETO ET AL., 2003) Para Musatti e Dannenberg (1982; 1999) a PCM e TB podem acontecer por uma infecção recente ou pela reativação de um foco quiescente endógeno e a deficiência da imunidade celular parece ser a principal responsável pelo desenvolvimento de ambas, podendo levar os pacientes a apresentar simultaneamente ou seqüencialmente, as duas doenças (PCM e TB) já que uma pode facilitar a reativação da outra devido a queda da imunidade que elas provocam. 2.2 DIAGNÓSTICO É inquestionável o fato de que o diagnóstico de certeza da paracoccidioidomicose derive da demonstração do agente em preparados histológicos, exame a fresco ou em cultivo, conhecidos como técnicas diretas de diagnóstico (MARQUES, 2003). O exame histopatológico é de grande valor por permitir visualização das formas fúngicas. Podemos ainda citar as técnicas indiretas como: sorologia, imunodifusão (ID), contro-imunoeletroforese (CIE), ensaio imunoenzimáticos (ELISA), imunofluorescência indireta (IFI) e imunoblot (IB). Estas técnicas têm sua relevância não só para auxilio do diagnóstico, como também para permitir uma melhor avaliação da resposta do hospedeiro à terapêutica especifica (BRASIL, 2009) É importante ressaltar a importância da biopsia aspirativa na obtenção de espécime para detecção citológica, ou pela polymerase chain reaction (PCR), do P. brasiliensis (SANTOS, 1998 ). 19 2.3. TRATAMENTO O plano terapêutico da PCM no Brasil segue ao protocolo estabelecido no Consenso Nacional de Paracoccidioidomicose (YASUDA ET AL 2006) porém em diferentes serviços de saúde , seguem regras e preferências próprias. Os fármacos considerados eficazes no manejo terapêutico da paracoccidioidomicose devem compreender além da utilização de drogas antifúngicas, a adoção de medidas de suporte às complicações clínicas associadas ao envolvimento de diferentes órgãos pela micose, lembrando das comorbidades, carência nutricional, anemia, adesão ao tratamento e questões socioeconômicos do paciente dever ser valorizadas (MARQUES, 2003) Os antifúngicos de escolha são: anfotericina B, sulfamidicos (sulfadiazina associação sulfametoxazol/trimetoprim oral e ou endovenoso), derivados azólicos (cetoconazol, fluconazol, itraconazol) considerando as limitações de toxicidade, de interação medicamentosa ou de custo (BRASIL, 2009). 2.4 INDICADORES EPIDEMIOLÓGICOS Por não ser uma doença de notificação compulsória, não temos dados precisos sobre a incidência da paracoccidioidomicose no Brasil. Os cálculos de prevalência, incidência e morbi-mortalidade da micose baseiam-se em relatos de casos e inquéritos sorológicos, o que é considerado uma estratégia simples, adequada e de baixo custo para avaliar a prevalência regional, devendo levar em consideração a heterogeneidade dos antígenos (PALMEIRO ET AL., 2005), como também inquéritos epidemiológicos, levantamento de prontuários e séries de casos. Até o momento, não existe nenhum instrumento que permita o real conhecimento da magnitude do problema, o que dificulta a implementação de ações de promoção e prevenção do agravo. Com base na experiência de serviços de referência no atendimento de pacientes com PCM, acredita-se que a sua incidência em zonas endêmicas varie de 3 (três) a 4 (quatro) novos casos/milhão até 1(um) a 3 (três) novos casos por 100 mil habitantes ao ano. (YASUDA, 2006) 20 No Brasil, a forma crônica da doença é a mais prevalente. Tem um longo período de latência e afeta principalmente homens adultos, entre 30 e 60 anos, em geral, trabalhadores rurais, imunossuprimidos (BETHLEM ET AL.,1991; VALLE ET AL., 1992; RESTREPO – MORENO, 1983; LONDERO, 1990). A forma aguda e subaguda corresponde a 10% dos casos, atingindo crianças e jovens adultos. Calcula-se que o período de latência na forma aguda dure de um a quatro meses, enquanto na crônica, pode atingir até 30 anos. A análise das áreas de alta incidência da doença tem grande importância epidemiológica, uma vez que pode auxiliar nas hipóteses diagnósticas clínicas e sugerir tais áreas, como alvo de investigação do habitat do fungo. As áreas de alta incidência devem corresponder às condições mais favoráveis à proliferação do patógeno e áreas de risco para a infecção humana. No âmbito do Ministério da Saúde, não existe um programa de controle específico, nem padronização dos meios de diagnóstico e tratamento como os já estabelecidos para outras doenças endêmicas como: leishmaniose, malária, dengue, tuberculose, hanseníase e outras. O que existe na literatura são dados fragmentados de sua freqüência e de seu impacto, sobre as condições de saúde da população alvo. A região Norte representa nova fronteira agrícola e vem passando por várias transformações nos últimos anos. Isso propicia intensa mobilidade social, implantações de projetos agrícolas, derrubadas e queimadas das florestas naturais, provocando grandes mudanças no meio ambiente onde o fungo se encontra, acarretando numa maior exposição aos ecotopos, e conseqüente contaminação humana nessas regiões (FONSECA, 1999). Estudos realizados de casos incidentes em crianças diagnosticadas para PCM em Belém do Pará com faixa etária entre três e treze anos comprovando sua autoctonia e estas eram de diferentes regiões do Estado do Pará, colocando definitivamente áreas da Amazônia no mapa da endemia (FONSECA ET AL., 1999). Em Campo Grande /Mato Grosso do Sul, no período de janeiro de 1980 a agosto de 1999, foram descritas as característica clínicas e epidemiológicas de 422 casos de paracoccidioidomicose atendidos no Hospital Universitário da 21 Universidade Federal do Mato Grosso do Sul, Campo Grande (PANIAGO, AGUIAR, CUNHA ET AL., 2003). Em Rio Branco, no estado do Acre, Chambô Filho et al. (2000), relatam um caso de PCM em mama, e chamam a atenção para a importância de realização de biopsia em abscesso de mama em mulheres idosas. O controle de doenças infecciosas e parasitárias, segundo Carlos Corvalan (2005), diz que a magnitude e a direção da incidência alterada de doenças infecciosas devidas às mudanças nos ecossistemas, dependem de ecossistemas específicos, do tipo de mudança do solo; da dinâmica de transmissão das doenças e da susceptibilidade dos indivíduos. Fatores antropogênicos que podem contribuir com os riscos dessas doenças são: destruição ou invasão do habitat natural, principalmente por meio de desmatamento e construção de estradas, mudanças na distribuição e disponibilidade de águas superficiais, como por exemplo, construções de represas e mudança no uso de terras, tanto para a pecuária como para plantios agrícolas, utilizando poluentes químicos bem como nutrientes, fertilizantes, agrotóxicos, urbanização desordenada e variabilidade e mudança climática; migrações e a exposição humana a esses agentes patogênicos (CORVALAN ET AL., 2005). Essas mesmas regiões apresentam deficiências em recursos sociais e em suporte tecnológico da rede dos serviços de saúde, o que possibilitaria a realização do diagnóstico etiológico precoce da paracoccidioidomicose ou outras micoses sistêmicas. A dificuldade aumenta quando se refere o acesso aos serviços de saúde pela população rural, levando estes a um diagnóstico tardio e conseqüentemente a formas graves e incapacitantes da doença. Para Wanke & Londero (1994), embora este fungo seja encontrado no solo, seu nicho ecológico ainda permanece como um enigma. Acredita-se que as condições climáticas dessa região sejam favoráveis para o habitat desse fungo, apesar do pouco conhecimento sobre seu habitat natural e ecologia. As poucas citações na literatura sobre esse aspecto apontam para que o fungo habite saprofiticamente em solo úmido, rico em proteínas e com variações mínimas de temperatura (BORELLI, 1964, 1972), entre 17- 24ºC, com invernos curtos, pluviosidade entre 500 - 2.500 mm/ano, altitude do nível do mar de 1.500 m, e 22 solos férteis com cobertura vegetal (RESTREPO, 1994; MARQUES, 1998). Sabe-se que 3.181 óbitos por PCM foram registrados no Brasil entre 1980 e 1995, resultando em uma taxa de mortalidade por PCM de 1,45 casos por milhão de habitantes. Neste estudo, os autores apontaram a PCM como oitava causa de mortalidade por doença infecciosa predominantemente crônica entre as doenças infecciosas e parasitárias, inclusive maior que a mortalidade por leishmanioses, e a mais alta taxa entre as micoses sistêmicas (COUTINHO, 1999). O estado de Rondônia encontra-se situado na região Norte, e é constituído por 52 municípios, com uma população geral de 1.493.566 (IBGE, 2008). Com extensa área demográfica de 238.512,80 km2, é limítrofe com o Estado do Amazonas, Acre, Mato Grosso e faz fronteira com a República da Bolívia. O clima é predominantemente equatorial, com chuvas abundantes e temperatura média anual de 26°C (MATIAS, 1998). Populações rurais do sexo masculino são mais vulneráveis a contrair esta doença, devido ao contato maior e prolongado com a natureza, relacionado com as suas atividades a terra e vegetais. Os indivíduos acometidos pela PCM, em sua maioria encontram-se na fase mais produtiva da vida, logo a doença leva a um impacto social e econômico. Contudo as ações de controle, pesquisa e assistência em PCM, pouco têm contribuído com as populações da área rural. A PCM, quando na sua forma progressiva provoca comprometimento de um ou mais órgãos, podendo evoluir para óbito, caso não tenha sido diagnosticada e tratada de maneira adequada. A doença acomete primariamente os pulmões, disseminando-se quase sempre para outros órgãos e sistemas, consistindo assim uma ameaça à vida do paciente (ANDRADE, 1983). Segundo Brasil (2008), não existe medidas de controle que confirmadamente previnam a doença, o que se indica é diagnosticar e tratar o doente, precoce e corretamente. Quanto aos programas oficiais de prevenção e controle, constatam-se apenas ações pontuais, isoladas e desarticuladas de outros programas tais como: programa de saúde da família, programa de controle da hanseníase, tuberculose, malária e leishmaniose e outros de importância para saúde Pública. 23 As pesquisas regionais (BARTHOLO Jr., 1999), apontam a prioridade para o combate às doenças endêmicas e infecciosas prevalentes no estado, tais como: leishmaniose, tuberculose, hanseníase, lobomicose, treponematoses ou neoplasias de pele. Ressaltando que esses agravos são prevalente na região Amazônia e que podem vir a ser confundido a PCM devido à semelhança dos sintomas (BRASIL, 2007), o que leva à necessidade da realização dos exames laboratoriais para um diagnóstico diferencial. 2..4.1 Histórico da Paracoccidioidomicose em Rondônia O registro dos primeiros casos da PCM em Rondônia remota da pesquisa de Leite em 1952 que descreveu três casos de Paracoccidioidomicose. Em 1989 Valle et al. realiza uma pesquisa entre os povos indígenas particularmente na etnia Surui com o relato de dois casos autóctones Colombo et al. (1990) relata e publica o primeiro caso clínico da doença de P. brasiliensis em pacientes da mesma tribo. A estruturação do programa de controle da paracoccidioidomicose teve início em 1995 com ações isoladas da Fundação Nacional de Saúde (FUNASA), mas com o processo de descentralização dos agravos hanseníase, tuberculose e posteriormente junto com as grandes endemias como a malária, dengue, esquistossomose e leishmaniose a partir de 1999 passou a ser coordenado pela Secretaria Estadual de Saúde/RO. Nesse período foi estabelecido um protocolo de atendimento, incluindo: diagnóstico clínico, diagnóstico laboratorial (micológico), histopatológico e sorológico, tratamento e acompanhamento aos pacientes acometidos pela paracoccidioidomicose (SESAU, 2009). Em 2001 a Secretaria Estadual de Saúde de Rondônia, através das ações de controle da PEC-PCM realizaram ações de educação permanente de recursos humanos na área de saúde como: capacitação técnica em diagnóstico clínico/epidemiológico e laboratorial, tratamento e monitoramento dos pacientes com diagnóstico positivo cadastrados no programa e avaliação do PEC-PCM. O estado Rondônia foi um dos primeiros a oficializar o uso da terapia medicamentosa com os derivados imidazólicos tendo como base o protocolo estabelecido pelo Estado do Paraná. 24 O alto custo na manutenção do tratamento levou a coordenação do Programa a buscar apoio juntamente a outros estados, com o intuito de padronizar o uso da terapia no âmbito nacional o que culminou com a realização da 1ª Reunião Nacional da Paracoccidioidomicose em 2002, quando ficou acordado a formação do Comitê Nacional da PCM e passando o agravo a fazer parte da agenda do Ministério da Saúde ligado à área das Doenças Respiratórias (SESAU, 2009). A 1ª Reunião Estadual sobre PCM foi realizada em maio de 2003 onde foi definido o manejo clínico de atendimento ao paciente e a aquisição e disponibilização do itraconazol passa a ser de responsabilidade do estado em parceria com o Ministério da Saúde/Brasil. 25 3. OBJETIVO GERAL. Conhecer o perfil epidemiológico da paracoccidioidomicose em Rondônia entre 1997 e 2008. 3.1 OBJETIVOS ESPECÍFICOS Identificar as formas clínicas da PCM em Rondônia. Analisar a distribuição de casos notificados por gênero, faixa etária e grau de escolaridade. Correlacionar a ocorrência da PCM com a distribuição geográfica X ocupação e gênero. Descrever a terapia medicamentosa e critérios de diagnósticos do agravo. Analisar a distribuição da mortalidade da PCM em Rondônia. 26 4. METODOLOGIA Este estudo foi previamente submetido e posteriormente aprovado pelo Comitê de Ética em Pesquisa/ NUSAU - Porto Velho - RO sob número de protocolo FR217525 (Anexo A). Trata-se de um estudo descritivo de caráter retrospectivo com variáveis quantitativas. 4.1 DELINEAMENTO Foram incluídos neste estudo 2116 fichas de notificação de pacientes do Programa Estadual de Controle de Micoses Sistêmicas (paracoccidioidomicose e outras micoses) da Secretaria Estadual de Saúde de Rondônia, setor da Agência de Vigilância em Saúde (AGEVISA) no período entre 1997 e 2008, compreendendo portadores de paracoccidioidomicose 1856 casos, comprovada por biópsia, micológico direto das secreções (exudato e transudato, escarro), sorologia e critérios clínicos epidemiológicos. 4.1.1 - Análise dos Dados A pesquisa utilizou dados secundários, oriundos das fichas de Notificação do Programa Estadual PCM/AGEVISA/SESAU, dados de óbitos do Sistema de informação de Mortalidade - SIM, utilizando as classificações do CID 10 de B40 a B40-9 (B40. 0 Blastomicose pulmonar aguda, B40.1, Blastomicose pulmonar crônica ,B40.2 Blastomicose pulmonar não especificada, B40.3 Blastomicose cutânea, B40.7 Blastomicose disseminada, Blastomicose generalizada, B40.8 Outras formas de blastomicose, B40.9 Blastomicose não especificada), e B41 a B41-9 (B41 Paracoccidioidomicose,B41.0 Paracoccidioidomicose pulmonar B41.7 Paracoccidioidomicose disseminada, Paracoccidioidomicose generalizada, B41.8 Outras formas de paracoccidioidomicose, B41.9 Paracoccidioidomicose não especificada). O método de cálculo da mortalidade no presente estudo será do número total de óbitos residentes sobre a população total residente multiplicado por cem mil habitantes (BRASIL, 2002). 27 Coeficiente de Mortalidade Geral (CMG): mede o risco de morte por todas as causas em uma população de um dado local e período foi calculado conforme fórmula abaixo: CMG = n.º de óbitos em dado local e período população do mesmo local e período x 100.000 Os indicadores de letalidade foram calculados conforme fórmula abaixo: n.º de óbitos de determinada doença em dado local e período x 100 CL = n.º de casos da doença no mesmo local e período. Os indicadores de incidência foram calculados conforme fórmula abaixo: Nº de casos novos de uma doença ocorridos numa população em determinado período x 100.000 INCIDÊNCIA = Nº de pessoas sob risco de desenvolver a doença durante o mesmo período Para facilitar e permitir a comparação entre as taxas calculadas para diferentes locais ou para o mesmo local em diferentes períodos de tempo utilizouse uma referência comum (100.000) que representa uma potência de base 10n5 (MEDRONHO ET AL., 2002) A média mensal de sazonalidade de PCM foi calculada pela média aritmética através da adição de um grupo de números (classes), dividida, em seguida, pela quantidade desses números (VIEIRA, 2008). Para a tabulação dos dados foi utilizado o programa TABWIN (TAB versão para Windows) e EPI-INFO (versão 3.51) para a confecção dos gráficos e tabelas foi utilizado o software Excel 2007. A análise dos dados obtidos foi realizada por meio de estatística descritiva. 28 5. RESULTADOS No período de 1997 a 2008 foram notificados 2116 casos de micoses pelo Programa Estadual de PCM, sendo 76% dos casos confirmados para PCM e 9,7% Blastomicose e 14,3% outras micoses. Neste estudo foram considerados apenas os casos de PCM e Blastomicose, com um total de 1856 casos conforme demonstrado no gráfico 1 Gráfico 1 – Tipos de micoses notificadas em Rondônia -1997 a 2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. . A distribuição geográfica dos casos notificados de PCM apresentados neste estudo mostrou uma maior concentração na região central e sul do estado, Conforme demonstrado na figura 2. 29 Figura 2- Distribuição de casos de notificados de PCM por municípios, Rondônia, 1997-2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. Os dados do programa de PCM até o ano de 1999 estavam sob a responsabilidade da Fundação Nacional de Saúde (FUNASA). Com o processo de descentralização das ações de Saúde para estados e municípios, o gerenciamento do referido programa passou a ser responsabilidade do estado. Isto levou à necessidade da capacitação técnica dos profissionais de saúde da rede estadual e municipal para a implantação do PEC-PCM e a inserção das notificações no banco de dados do estado. Somente a partir de 2007 o agravo passa a ser notificado como de relevância estadual e a sua notificação passa a ser digitada pelo SINAN-NET. Entre o período de 1999 e 2000 tivemos um declínio na incidência dos casos notificados que coincidiu com o período de transição do PEC-PCM, o aumento da incidência dos casos em 2001 e 2003 pode ter estado associado aos resultados das capacitações que culminaram com um melhor registro e detecção de casos, além da padronização da terapêutica e diagnóstica, conforme podemos observar no gráfico 2. 30 Gráfico 2- Taxa de Incidência da PCM em Rondônia no período de 1997 a 2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. Ao analisarmos a distribuição mensal dos casos notificados de PCM no período de 1997 a 2008 podemos observar que a média da distribuição do período foi de 13,3 com uma maior concentração nos meses do verão amazônico. ver gráfico 3. Gráfico 3. Distribuição da média mensal de casos notificados de PCM Rondônia 1997 -2008 30 Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. 31 A distribuição da incidência por município aponta para a concentração dos casos na região centro-sul do estado (80% dos casos) conforme figura 3. FIGURA 3 - Taxa de incidência de PCM por municípios, Rondônia 1997 – 2008. Fonte de dados do PEC-PCM-AGEVISA/SESAU/RO A PCM caracteriza-se por ser um agravo que acomete indivíduos em sua fase produtiva podendo ocorrer na infância e se manifestar na fase adulta. Os casos de PCM distribuídos por faixa etária no período entre 1997 e 2008 em Rondônia apresentaram uma maior concentração na faixa etária dos 40 aos 59 anos (57,48%), seguida da faixa de mais de 60 anos (20,52%) e 20 a 39 (19,28%), a notificação de casos na faixa etária em menores de 14 anos (2,69%), idade média de 48 anos (intervalo de 4 a 80 anos) conforme a Tabela1. 32 Tabela 1- Distribuição de casos notificados de PCM segundo faixa etária em Rondônia – Brasil, 1997 a 2008 1997 FAIXA ETARIA <14 1998 1999 11 2 2000 15 A 19 2001 2002 2003 2004 2005 2006 3 1 8 15 1 1 2 1 2 1 1 2007 2008 TOTAL 42 1 8 20 A 39 22 30 39 34 43 24 29 45 33 37 17 5 358 40 A 59 60 69 71 58 85 77 124 102 130 128 99 64 1067 ≥ 60 30 22 22 19 34 37 62 29 23 39 35 29 381 TOTAL 112 132 134 113 166 141 223 191 188 206 151 99 1856 Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. A distribuição dos casos por gênero apresentou 90% dos casos PCM no sexo masculino e 10% no sexo feminino, foram excluídos do cálculo os casos que na ficha de notificação apresentavam a classificação de sexo como ignorado (5 casos), conforme podemos observar na tabela abaixo: Tabela 2- Distribuição do número de casos notificados de PCM por gênero em Rondônia – Brasil, 1997 a 2008. MASC. FEM 1997 1998 1999 2000 2001 2002 2003 2004 2005 2006 2007 2008 100 119 116 100 149 126 200 172 166 185 147 89 12 11 18 12 16 15 22 19 22 21 4 10 1 1 113 166 191 188 206 151 99 IGNO TOTAL 2 112 132 134 1 141 223 Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. Quanto ao grau de escolaridade encontrados nas fichas de notificações dos pacientes com PCM, verificou-se que declararam ter o primeiro grau 54,5%, analfabetos 18,1%, seguidos de ignorados com 18%, segundo grau 3,8%, e nível superior 0,2%. Chama a atenção o percentual de não se aplica (5,4%), usado normalmente para identificar menores de 5 anos. Ver tabela 4. 33 Gráfico 4 - Grau de escolaridade dos pacientes com PCM em Rondônia no período de 1997 a 2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. Ao analisar-se a distribuição dos casos por população, verificou-se que 54% dos casos são da zona urbana e 45,9% da zona rural, conforme gráfico 5. Gráfico 5 - Distribuição dos casos de PCM segundo população da Zona Urbana e Rural. Rondônia-1997 a 2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. Ao analisarmos os dados referentes à ocupação dos casos notificados verificamos que a maioria não estava de acordo com o Código Brasileiro de Ocupações- CBO; com o intuito de melhor classificarmos as ocupações 34 declaradas nas fichas de notificação, separamos todas as ocupações e reagrupamos de forma que aquelas ocupações que estavam relacionadas com as atividades da área rural passaram a fazer parte do mesmo grupo, dessa forma as atividades desenvolvidas na área rural corresponderam a 83% das ocupações declaradas nas fichas de notificações, seguido das que se declararam do lar (5%) e motorista (4%) ver gráfico 6. Gráfico 6 Distribuição dos Casos de PCM , segundo Ocupação - RO 1997 a 2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. A distribuição dos casos de PCM deste estudo, relacionado com os sítios anatômicos apresentou lesões únicas acometendo mais de um sítio anatômico 84% localizavam-se no pulmão, 10% na cavidade oral compreendendo língua, seguido da cutânea 4% e linfonodos 2%, conforme demonstrado no gráfico 7. 35 Gráfico 7- Distribuição dos casos de PCM, segundo sítios anatômicos em Rondônia-Brasil - 1997 a 2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. A forma clínica mais encontrada foi à forma crônica com 84% dos casos, a Subaguda com 14%, a forma aguda representou 2%%, salientamos que usamos a classificação de forma aguda e subaguda ao invés de usar forma tipo Juvenil. Gráfico 8. Gráfico 8 - Distribuição de casos de PCM, segundo forma clinica – Rondônia- Brasil - 1997 a 2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. 36 Os dados referentes ao diagnóstico laboratorial apresentaram os seguintes resultados: por exame micológico direto em 42%, clinico epidemiológico em 37%, histopatológico 12%, sorologia 6%, cultura 3% dos casos, de acordo com o gráfico 9. Gráfico 09- Critérios de confirmação diagnóstica da PCM, segundo ficha notificação, Rondônia, 1997 a 2008. Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. O manejo terapêutico da PCM no Brasil segue um protocolo estabelecido no Consenso Nacional em Paracoccidioidomicose em 2006, em que como sugestão terapêutica de primeira escolha, são os derivados imidazólicos e como segunda escolha, os derivados sulfamidicos (sulfametoxazol-trimetoprima) e Anfotericina B para as formas graves. Na terapia medicamentosa em menores de dez anos utiliza-se sulfametoxazol em suspensão devido à dificuldade de ajuste da dose uma vez que o itraconazol tem a sua apresentação farmacêutica apenas em cápsulas o que dificulta o ajuste da dose para crianças nessa faixa etária (CONSENSO NACIONAL PCM, 2006), ressaltando que na co-morbidade Tb/PCM preconiza-se também, apenas o uso da sulfametoxazol. De acordo com o gráfico abaixo. 37 Gráfico 10 . Terapêutica Antifúngica aplicada em Rondônia – Brasil, 1995 a 2008 Fonte de dados do PEC-PCM/AGEVISA/SESAU/RO. No período de 1995 100% dos casos foram tratados com sulfametoxazol, em 1996 foram tratados com itraconazol 75% dos casos; enquanto que 25% trataram com sulfametoxazol. Em 1997 foram usadas três (3) drogas terapêuticas, 60% dos casos foram tratados com itraconazol, 20% dos casos com sulfametoxazol; 20% com cetoconazol, 18% dos casos, em 1998 foram tratados com sulfametoxazol e 4% dos casos usou outro medicamento enquanto que 78 % não receberam tratamento padronizado. Em 1999 observou-se que 97% dos casos não receberam tratamento padronizado, só a partir de 2000 quando o PEC-PCM passou a ser gerenciado pela Secretaria de Estado da Saúde (SESAU) e os medicamentos passaram a ser adquiridos pelo estado, tendo como base o protocolo estadual de terapia antifúngica, onde mais de 80% dos casos foram tratados com itraconazol como demonstrado no gráfico 10. Quanto à distribuição dos óbitos esta pesquisa utilizou o banco de dados do Sistema de Informação de Mortalidade (SIM), sendo que a inclusão das informações foi baseada no Código Internacional de Doenças (CID) tendo como referência CID 10. Dessa forma, trabalhamos com a seguinte classificação: de B40 a B40-9 e B41 a B41-9, as informações foram agrupadas e apresentadas de acordo com o gênero. Ver gráfico abaixo: 38 Gráfico 11 - Distribuição de óbitos PCM em relação ao gênero de PCM - Rondônia 1997 a 2007. Fonte de dados do SIM/AGEVISA/SESAU/RO. *Os dados do banco de mortalidade esta fechado até o ano de 2007. O coeficiente geral de mortalidade por PCM no período de 1997 a 2007 foi de 6,6. Os anos de 2001 a 2004 foram os anos de maior registro de óbitos. Tabela 3 Taxa bruta de mortalidade por PCM em Rondônia – Brasil, 1997 a 2007. (100.000/hab.) Ano Óbitos Pop Taxa de Mortalidade 1997 5 1.255.538 0,39 1998 6 1.276.181 0,39 1999 5 1.296.832 0,38 2000 6 1.379.787 0,43 2001 2002 17 14 1.407.878 1.431.776 1,2 0,97 2003 11 1.455.914 0,75 2004 12 1.479.940 0,81 2005 5 1.534.584 0,32 2006 7 1.562.406 0,44 2007 6 1.590.027 0,37 TOTAL 94 1.424.624 6,6 Fonte de dados do SIM/AGEVISA/SESAU/RO. * Os dados do banco de mortalidade está fechado até 2007. 39 Em 2001 a taxa de letalidade foi de 10,2% e em 2002 de 9,9%, a taxa de letalidade foi de 5,35%. Conforme tabela 4. Tabela 4 – Distribuição de óbitos e coeficiente de Letalidade- Rondônia - 1997 a 2007. Ano Óbitos Casos % Letalidade 1997 5 112 4.5 1998 6 132 4,5 1999 5 134 3,7 2000 6 113 5,3 2001 17 166 10,2 2002 14 141 9,9 2003 11 223 4,9 2004 12 191 6,3 2005 5 188 2,6 2006 7 206 3,3 2007 6 151 4 94 1757 5,35 Total Fonte de dados do SIM/AGEVISA/SESAU/RO. Os indicadores de mortalidade e coeficiente de letalidade foram calculados de acordo com Medronho et al (2000) e Brasil (RIPSA, 2002) A distribuição dos óbitos foi realizada considerando o município de residência, dessa forma os municípios que apresentaram a maior número de óbitos foi Cacoal (13 óbitos), Ji-Paraná (13 óbitos), Porto Velho (9 óbitos) e Ouro Preto do Oeste (7óbitos). Analisando os dados em relação à taxa de mortalidade os municípios com maior taxa foram: Chupinguaia (3,56%), Nova Brasilândia do Oeste (3,54%), Colorado do Oeste (1,89%), Costa Marques (1,89%), Presidente Médici (1,88%), Cacoal (1,71%) conforme descrito na tabela 5. 40 Tabela 5 - Taxa de mortalidade por paracoccidioidomicose por 100.000 hab. segundo municípios. Rondônia, 1997 a 2007. Municípios 0,49 Média da população 27164 Taxa de Mortalidade 1,47 0,10 0,30 13003 0,77 1 0,10 0,30 17377 0,58 2 0,20 0,40 73736 0,27 13 1,18 1,27 69069 1,71 Chupinguaia 2 0,20 0,40 5615 3,56 Colorado do Oeste Corumbiara 4 0,40 0,49 21145 1,89 1 0,10 0,30 9932 1,01 Costa Marques 2 0,20 0,40 10601 1,89 Espigão do Oeste 1 0,10 0,30 24261 0,41 Itapua do Oeste 1 0,10 0,30 8923 1,12 Jaru 3 0,30 0,64 52904 0,57 13 1,18 0,83 105977 1,12 Ministro Andreazza Monte Negro 1 0,10 0,30 10995 0,91 1 0,10 0,30 13765 0,73 Nova Brasilândia do Oeste Novo Horizonte do Oeste Ouro Preto do Oeste Pimenta Bueno 6 0,60 0,66 16950 3,54 2 0,20 0,40 12075 1,66 7 0,64 0,64 40721 1,56 4 0,36 0,64 31621 1,15 Porto Velho 9 0,82 1,27 345079 0,24 Presidente Médici 5 0,50 0,67 26635 1,88 Rolim de Moura 4 0,40 0,49 47401 0,84 São Miguel do Guaporé Vilhena 2 0,22 0,42 26129 0,85 5 0,50 1,02 56204 0,89 94 9,00 13,24 1.424.624 0.63 Alta Floresta do Oeste Alto Alegre dos Parecis Alvorada do Oeste Ariquemes Cacoal Ji-Paraná RONDONIA Nº total de óbitos 4 Média dos óbitos 0,40 Desv.pad 1 Fonte de dados do PEC-PCM/AGEVISA/SESAU 41 6. DISCUSSÃO Segundo Brasil (2009), os casos de PCM têm sido registrados em populações de zona rural, ressaltando a ocorrência em áreas de colonização mais recente, submetidas a desmatamento como em partes da Amazônia, Tocantins, Pará, Mato Grosso, Acre e Rondônia onde a PCM pode ser considerada uma micose sistêmica emergente. Considerando que PCM não é uma doença de notificação compulsória, o registro dos casos se dá apenas nos estados que considera o agravo de relevância, o que dificulta o conhecimento real sobre os aspectos epidemiológicos do agravo em âmbito nacional (BRASIL, 2009). Rondônia é um dos estados que integra a paracoccidioidomicose no rol de doenças de notificação de interesse estadual (DURLACHER e LIMA, 2003), que relataram um elevado número de registro de casos. Ao analisarmos os casos notificados em Rondônia no período de 1997 a 2008 podemos observar que 9,7% dos casos, foram notificados como Blastomicose, apesar da denominação paracoccidioidomicose ter sido adotada em 1971 no Simpósio realizado em Medellín, na Colômbia, e quando foi abandonada a denominação Blastomicose sul-americana, (LACAZ, 1982). O que nos levou a questionar a atualização dos profissionais de saúde que continuam a preencher a ficha utilizando a nomenclatura abolida. A incidência anual brasileira chega a ser de 3 casos novos para cada 100.000 habitantes. (YASUDA ET AL., 2006). A incidência do agravo em Rondônia teve um aumento em 2003 e 2006 e a partir do ano seguinte começou a apresentar um declínio na curva epidemiológica, o que podemos relacionar com uma sub-notificação ou devido ao acesso ao tratamento, que culminou com a diminuição dos pacientes que reingressavam no programa por recidiva. Na distribuição dos casos por municípios constatou-se que a região Central e Sul do estado registraram maior incidência da PCM, com destaque para os municípios de Espigão do Oeste, Pimenta Bueno, Ji-Paraná, Cacoal, Vilhena e Pimenteiras. 42 Estas regiões apresentam o maior desenvolvimento agropecuário do estado, coincidindo com áreas submetidas aos plantios agrícolas como lavouras de milho, café, soja e pecuária. O que pode ser um dos fatores que justifiquem essa incidência uma vez que a literatura associa os casos de PCM ao trabalho na área rural, lembrando que as características climáticas, fisiográficas, chuvas abundantes e florestas úmidas presentes no estado de Rondônia também são favoráveis, conforme relata Matias (1998). Ao realizar-se o cálculo da média mensal no período do estudo confirmouse a maior freqüência nos meses julho e agosto coincidindo com a época da colheita que se sucede logo após o período do inverno amazônico (SEDAM-RO, 2009). Quanto à ocupação declarada pelos pacientes, através da ficha de investigação, 83% responderam ter atividades relacionadas com agricultura ou atividade anterior na zona rural, de acordo com os autores (BOTELHO e CAMPOS, 1989; BISINELI ET AL., 1998; PAGLIARI ET AL., 1995; HANSSESSIAN ET AL., 2000). Ao relacionar as ocupações com área de residência dos pacientes concluiu-se que não houve discrepância entre zona urbana e rural, não estando restrita tão somente à área rural, tal achado está de acordo com o estudo de Silva apud Verli et al. (2007), que relataram que pessoas que residem em área urbana com atividades relacionadas com a manipulação do solo, como jardineiro e pedreiro, e, ainda mais importante, até mesmo em indivíduos dados a outras profissões, tais como comerciantes e professores, logo é importante que os profissionais de saúde levem em consideração a possibilidade de o agravo acometer habitantes da zona urbana. Em nosso estudo, não foi possível analisar se os pacientes eram ou tinha hábitos de mascar vegetais, etilismo e tabagismo, por falta da inclusão dessa informação na ficha de notificação que são dados importantes por serem fatores capazes de interferir na relação agente hospedeiro (MARQUES ET AL., 1998); Dentre as fichas de notificação analisadas, as faixas etárias mais acometidas no período de 1997 a 2008, apresentou uma maior concentração na quarta e sexta décadas de vida (57,48%), seguida da faixa etária de maior de 60 43 anos (20,52%), esse dado está de acordo com o estudo realizado por Oliveira et al.(1997), que encontrou dados semelhantes. A distribuição dos casos por faixa etária demonstrou uma parcela pequena de casos na faixa etária em menores de 14 anos (2,26 %), Valle (2001) disse que a evolução da PCM é incomum nessa faixa etária, ocorrendo mais entre adultos na faixa etária de 30 a 50 anos devido à reativação do foco endógeno latente, de acordo com Maluf (2003), esta reativação pode estar associada a fatores relacionados tanto com o agente infeccioso como com o hospedeiro. A distribuição dos casos por gênero demonstrou neste estudo maior freqüência de casos em indivíduos do sexo masculino (90 %) o que pode estar associado a fatores socioeconômicos e ocupacionais uma vez que a maioria são trabalhadores que desenvolvem atividades rurais (83%) estando estes dados de acordo com a literatura (BRASIL, 2009, YASSUDA ET AL., 2006; VERLI ET AL., 2005; HANSSESSIAN ET AL., 2006). A predileção pelo gênero masculino parece resultar de um efeito protetor dos hormônios femininos, como o estradiol, que inibem a transformação do fungo da forma de levedura para hifas patogênicas (NEVELLI ET AL., 1998). Outros autores têm comentado sem maior suporte científico, que a maior dedicação das mulheres aos trabalhos domésticos possa também contribuir para tal fato (SILVA, 2007). A distribuição dos casos, segundo a escolaridade, demonstrou baixa escolaridade em que 54% dos casos têm o primeiro grau e apenas 1% com nível superior, segundo Palheta-Neto et al. (2003), a baixa escolaridade e as precárias condições socioeconômicas dos pacientes com PCM e de outras doenças são caracterizadas nesse grupo devido à falta de acesso às informações gerais profiláticas ou terapêuticas, ao mesmo tempo em que pessoas com maior escolaridade afastam-se mais dos trabalhos braçais com a terra. A distribuição dos casos por sítios anatômicos incidiu com uma maior freqüência das lesões pulmonares (84%), que são incidentes na PCM quando ocorrem em sua forma crônica, pode ser confundida com a tuberculose devido às similaridades clínicas e radiológicas entre essas patologias, a PCM, em geral, tem evolução crônica, caráter recindivante e pode deixar seqüelas anatômicas e funcionais (MARTINEZ, 1996). Em nosso estudo, a forma crônica representou 44 78% dos casos, o que está de acordo com o estudo de Pagliari et al (1995), que relataram achados semelhantes. As lesões da cavidade oral neste estudo representam 10% dos casos, em concordância com a literatura (BISINELI; TELLES; JOSIAS ET AL., 2001; BITTENCOURT, OLIVEIRA, COUTINHO, 2005 e FORNAGEIRO, MALUF, TAKARASHI ET AL., 2005) ressaltando que estas formas podem estar associadas às formas clínicas aguda e subaguda encontradas principalmente nas faixas etárias de menores de quatorze anos e em adultos jovens (15 a 30 anos). O percentual encontrado nas lesões da cavidade oral permite apontar a importância dos profissionais das áreas de odontologia e otorrinolaringologia como imprescindíveis na identificação destas lesões, fortalecendo o atendimento multidisciplinar, uma vez que os pacientes buscam esses profissionais para tratamento dessas lesões. Dessa forma, deve-se estabelecer rotineiramente uma metodologia diagnóstica para o correto diagnóstico (ALEIXO, ET AL., 2009). Outro dado importante relacionado aos sítios anatômicos foi à identificação de co-infecção associada à PCM como HIV/AIDS (3 casos), Tuberculose (3 casos), Hanseníase (1 caso) e Leishmaniose (1 caso), o que nos faz presumir a possibilidade de ativação de focos da infecção nas áreas endêmicas para esses agravos, além de que fica claro que deve haver uma sub-notificação das comorbidades devido ao baixo percentual encontrado, uma vez que em Rondônia esses agravos são de grande relevância epidemiológica. O padrão ouro para o diagnóstico da PCM segundo Brasil (2009) é o exame micológico direto e cultura e o histopatológico para outros autores é importante principalmente para a identificação das lesões bucais (MARQUES, 2003). O exame sorológico não é realizado em Rondônia, é feito somente a coleta, e o material coletado é encaminhado para o Laboratório de Referência Nacional de Micologia Médica da FIOCRUZ para análise. Em nosso estudo 42 % dos exames foram confirmados pelo Mdpb (micológico direto para PCM), seguidos dos casos confirmados pelo critério clinico epidemiológico (37%), lembrando que de acordo com Brasil (2009) o vínculo clínico epidemiológico é apenas um diagnóstico presuntivo, este é um achado preocupante devido ao 45 grande número de casos que não tiveram confirmação laboratorial da PCM por métodos diagnósticos considerados de padrão ouro. As drogas eficazes contra PCM compreendem três grupos: anfotericina B, sulfadiziana e outros compostos sulfamidicos e o grupo de drogas azólicas (MARTINEZ, 2004). Em Rondônia o uso do itraconazol era adotado como droga de 1ª escolha e também disponibilizado para o tratamento na Atenção Básica (SESAU, 2009). antes mesmo de ser preconizado pelo Consenso Nacional em PCM em 2006. Dentre as fichas analisadas no estudo mais de 90% foram tratados com Itraconazol, um dado que chama a atenção são os pacientes com co-morbidade a exemplo da tuberculose que a indicação é apenas o uso de sulfa devido à interação entre os fármacos utilizados no tratamento da Tuberculose com os da PCM e nas fichas analisadas encontramos a associação dos dois medicamentos (BRASIL, 2009). A Mortalidade por PCM no Brasil no período de 1980 a 1995 foi de 1, 487 por milhão de habitantes, sendo responsável por 3.181 óbitos nos Pais. Com média anual de 198,81óbitos, desvio padrão = 13,61. Sendo considerada a oitava causa de mortalidade por doença infecciosa e parasitária predominantemente crônica (COUTINHO, 1999). Coutinho et al. (2002), afirmaram ainda que o Estado de Rondônia apresentou um registro de 51 óbitos com freqüência relativa acima da média brasileira com taxa de 3, 564/ milhão de habitantes. Sendo considerada a taxa mais alta da Região Norte. Ao buscarmos uma comparação dos dados de mortalidade encontrados neste estudo, com os dados de outras regiões do Brasil, constatamos que esse indicador na literatura refere-se a períodos anteriores a esta pesquisa, o que dificultou a realização de uma análise comparativa do indicador encontrado com outras regiões do país, sendo que o estudo mais recente é o de Santo em 2008, que analisou a tendência da mortalidade por PCM no Estado de São Paulo no período de 1985 a 2005, onde a taxa de mortalidade por causa básica foi de 59,7% em um estudo com 1164 óbitos por PCM. 46 A taxa de letalidade em Rondônia nos anos 2001 e 2002 foram a mais elevada em todos os 12 anos deste estudo, nesse período o estado assume a coordenação do programa e inicia a capacitação dos profissionais de saúde para o manejo adequado dos casos suspeitos, coincidindo ainda com a falta do medicamento no mesmo período (gráfico11). Brasil (2009) afirma que formas graves incapacitantes ou mortes prematuras podem estar associadas à falta de intervenção de uma terapêutica oportuna. Portanto o aumento da letalidade pode ter sido devido ao melhor preenchimento do registro dos óbitos ou à falta do tratamento adequado. 47 7. CONCLUSÕES O estudo da análise da situação epidemiológica da paracoccidioidomicose em Rondônia de 1997 a 2008 permitiu concluir que: 1. A incidência da PCM em Rondônia aumentou nos últimos doze anos, período no qual 1856 casos, foram notificados ao PEC-PCM. 2. Com este estudo o Estado de Rondônia apresentou um número expressivo de casos de PCM, caracterizando-se em uma região endêmica no Brasil, reforçando a necessidade de vigilância. 3. A PCM foi mais prevalente nos homens em idade produtiva, evidenciando um problema sócio-econômico e ao sistema público de saúde em Rondônia. 4. O trabalhador rural da região central e sul do estado foram o mais acometido, com uma taxa mais alta que a média brasileira; 5. As mulheres foram menos acometidas pela infecção; 6. A aquisição e distribuição do medicamento para tratamento por parte do estado tem sido um fator importante no manejo terapêutico adequado dos pacientes; 7. Os critérios de encerramento de casos precisam ser pautados em diagnóstico laboratoriais e não em critérios presuntivos como o vínculo clínico epidemiológico; 8. A PCM foi responsável por 94 óbitos no período estudado em Rondônia, com taxa bruta de mortalidade de 6,6 por 100.000 hab.; e o coeficiente de letalidade foi de 5,35% no mesmo período; 48 9. Em relação à escolaridade, o preenchimento inadequado da ficha não permitiu uma analise mais precisa devido ao grande número de informação registrada como IGNORADOS; 10. Não foi possível identificar fatores associados à PCM como o tabagismo, etilismo por serem informações que não constam na ficha de notificação; 11. A ficha de investigação do PEC- PCM necessita ser modificada com o intuito de inserir informações relevantes no monitoramento do agravo, como comorbidades, etilismo e tabagismo, raça e informações do gênero feminino relacionados à gravidez; sinais e sintomas; critérios de alta. 12. Mudança na nomenclatura da ficha de investigação que está identificada como ficha de Investigação de MICOSES PULMONARES para ser identificada como ficha de investigação de MICOSES SISTÊMICAS e CUTÂNEAS PROFUNDAS. 13. A forma crônica da doença foi a que apresentou maior percentual, no entanto, é necessária a inclusão da informação sobre a forma clínica aguda e subaguda na ficha de investigação para uma melhor análise. 14. Há necessidade de capacitar melhor os profissionais de saúde no diagnóstico clínico, laboratorial, tratamento, vigilância epidemiológica e ações de Educação e saúde, devendo ser implementadas de forma permanente em todos os municípios do estado uma vez que são as principais ações para controle e monitoramento do agravo. 49 8. REFERÊNCIAS 1. ALBORNOZ, M. B. Isolation of Paracoccidioides brasiliensis from rural soil in Venezuela. Sabouraudia, Edinburgh, v. 9, n. 3, p. 248-253, 1971. 2. ALEIXO, R.Q., NASCIMENTO, D.O.R., RODRIGUES, M.T.V., COSTA, M.R.S.N., Paracoccidioidomicose: lesões bucais - relato de caso clínico, Resumo do 45º Congresso da Soc.Bras. de Med. Trop. DT 251, p.110, 2009. 3. ANDRADE, A.L.S.S. – Paracoccidioidomicose linfático-abdominal. Rev. de Patol. Tropical. 12:165-256 1983. 4. BAGLAGI E., SANO, COELHO brasiliensis I et al. Isolation of Paracoccidioides from armadillos (Dasypus novemcinctus) captured in an endemic area of Paracoccidioidomycosis. Am J Trop Med Hyg 1998; 58: 505-12. 5. BARTHOLO Jr. R. S & BURSZTYN, M. - Amazônia sustentável, estratégia de desenvolvimento em Rondônia 2020. Brasília, IBAMA, 1999. 6. BETHLEM, N. M.; LEMLE, A.; BETHLEM, E. & WANKE, B., 1991. Paracoccidioidomycosis. Seminars in Respiratory Medicine, 12:81-97. 7. BICALHO, R. N., SANTO, E. M.F., AGUIAR, M. C. F., SANTOS, V. R., Oral Paracoccidioidomycosis: a retrospective study of 62 Brazilian patients. Oral Dis. Houndmillls, v. 7, n. 7, p. 56-60, 2001. 8. BISINELI, J. C.; TELLES, F. Q.; JOSIAS, A. et al., Manifestações Estomatológicas da Paracoccidioidomicose. Rev. bras. Otorrinolaringol., v. 67, n.5, set., 2001. 50 9. BISINELLI, J., MARZOLA C, FERREIRA MLS, TOLEDO FILHO JL, PASTORI CM, ZORZETTO DLG. Manifestações estomatológicas da Paracoccidioidomicose (Paracoccidioides Brasiliensis ou Enfermidade de Lutz-Splendore-Almeida): considerações gerais e apresentação de casos. Rev Fac Odontol Bauru 1998; 6(1):1-1. 10. BITTENCOURT, J. I. M.; OLIVEIRA, R. M.; COUTINHO, Z. F. Paracoccidioidomycosis Mortality in the State of Paraná, Brazil 1980/1998. Cad. Saúde Pública, v. 6, p. 1854-6, Nov., /dez. 2005. 11. BOTELHO MR, CAMPOS HR. Paracoccidioidomicose:uma doença sistêmica com repercussões bucais. Arq Bras Med Nav 1989; 50(3):5963. 12. BLOTTA, M. H. S. L., CAMARGO, Z. P. Immunological response to cellfree antigens of Paracoccidioides brasiliensis: relationship with clinical forms of Paracoccidioidomycosis. Journal of Clinical Microbiology, Washington, v 31, n. p. 671-676, 1993. 13. BORELLI, D., Concepto de reservaria. La reducida reservarea de La Paracoccidioidomycosis. Derm. Venez., 4:71-77, 1964. 14. BORELLI, D., Some ecological aspects of Paracoccidioidomycosis. In: Pan American Symposium on Paracoccidioidomycosis, I Medellin, 1971. Proceedings. Washington DC, PAHOO, Scent. Public, 1972. V 254, p. 59-64. 15. BORGES-WALMSLEY, M.I., CHEN, D., SHU, X., WALMSLEY, A. R. The patobiology of Paracoccidioides brasiliensis. Trends in Microbioloy, Cambridge, v. 10, n. 2, p. 80-87, Feb/2002. 51 16. BRASIL. Ministério da Saúde. Guia de Vigilância Epidemiológica CAD. 7 – Brasília/DF 7ª Edição, 2009. 17. BRASIL. MINISTERIO DA SAÚDE ., Secretaria de Vigilância em Saude. Vigilância em saúde no SUS: Fortalecendo a capacidade de resposta aos velhos e novos desafios. Brasilia 2006. 18. BRUMER, S. O. Paracoccidioidomycosis: CASTANEDA, E., RESTREPO, A. an update. Clinical Microbiology Reviews, Washington, v 6, n.2, p. 89-117, 1993. 19. CHAMBÔ FILHO, A., BORGES, F.L.L., CINTRA, L.C., MARTINS, R.M., Paracoccidioidomicose: Relato de Caso; Revista Brasileira de Ginecologia e Obstetrícia, vol. 22 (9): 593-596 2000. 20. COIMBRA, Jr., C.E.A. - From shifting cultivation to coffee farming: the impact of change on the health and ecology of the Surui Indians of the Brazilian Amazon. Bloomington, Indiana, U.S.A. 1989 (Tese de Doutoramento - Indiana University). 21. COLOMBO AL, FORJAZ MHH, SADER HS, PEREIRA CAP, FISCHMAN O, VIEIRA JP. Paracoccidioidomicose autóctone em Suruí, Estado de Rondônia. In: Resumos do XXVI Congresso da Sociedade Brasileira de Medicina Tropical, Natal p.277, 1990. 22. CORREDOR, GG., CASTAÑO J H ., PERALTA L A, et al. . Isolation of Paracoccidioides brasiliensis from the nine-banded armadillo Dasypus novemcinctus, in an endemic area of Paracoccidioidomycosis in Colombia. Rev Iberoan Mycol 1999; 16(4): 216-20. 23. CORTE, A. C., ITANO, E. N., FREIRE,R. L., CAMARGO, Z.P., ONO, M. A., Detection of antibodies’ to Paracoccidioides brasiliensis in horses from 52 northern Region of Paraná State. Rev. Semina: Ciências Agrárias, Londrina, v. 30, n. 2, p. 441-446, abr/jun. 2009. 24. CORVALAN, C; HALES; Mc MICHAEL. Ecosystems and human wellbeing. WHO, 2005. 25. COSTA, E. O., DINIZ, L. S. M., FAVA NETTO, C., The prevalence of positive intradermal reactions to paracoccidioidin in domestic wild animals in São Paulo, Brazil. Veterinary Research Communications, Amsterdam, v. 19, n. 2, p.127-130, Mar.1995. 26. COUTINHO, Z F, Mortalidade por Paracoccidioidomicose no Brasil1980 a 1995 – Estudo Descritivo., Dissertação (Mestrado)- Universidade Federal de São Paulo. São Paulo, 1999. 27. COUTINHO, Z.F., SILCA, D., LAZERA, M., PETRI, V., OLIVEIRA R.M., SABROZA, P.C,. WANKE, B., Paracoccidioidomycosis mortality in Brazil (1980- 1995). Cad Saúde Pública. 2002 seoct;18(5); 1441-54. 28. DANNENBERG AM. Pathophysiology: Basic aspects In: Schlossberg D. Tuberculosis and nontuberculous mycobacterial infections. 4th ed. Philadelphia: W.B. Saunders Co.; 1999. p. 17-47. 29. DURLACHER, R. R., LIMA, S. M. D, Situação da Paracoccidioidomicose em Rondônia. Anais do Congresso da Sociedade Brasileira de Medicina Tropical. Tema Livre 035. Vol. 36, supl. I. 2003. 30. FRANCO, M. , MOTENEGRO, M. R., MENDES, R. P., MARQUES, S. A., DILLON, N. L., MOTA, N. G. Paracoccidioidomycosis: a recently proposed classification on its clinical forms. Revista da Sociedade Brasileira de Medicina Tropical, Rio de Janeiro, v. 20, n. 2, p. 129- 133, 1987. 53 31. FONSECA, E.R.S; PARDAL, P.P.O; SEVERO, – L.C. Paracoccidioidomicose em crianças em Belém do Pará. Rev.Bras. de Méd. Tropical, 32:31-33.1999. 32. FORNAJEIRO, N.; MALUF, M. L. F.; TAKAHACHI, G. et al., Inquérito Epidemiológico Sobre a Paracoccidioidomicose utilizando a gp43 em Dois Municípios do Noroeste do Paraná, Brasil. Rev. Soc. bras. Med. Trop., v. 2, p. 191-3, mar.,/abr., 2005. 33. FUNDAÇÃO INSTITUTO BRASILEIRO DE GEOGRAFIA E ESTATÍSTICA (IBGE). Estimativas da População Dados do Censo Demográfico 2008.. 34. HASSESSIAN, A, ISHIKAWA EN, ALENCAR FI, MARCUCCI G. Estudo da prevalência de lesões bucais em pacientes portadores de paracoccidioidomicose na região de Campo Grande – Mato Grosso do Sul. RPG -Rev. Pós Graduação 2000; 7(3):214-8. 35. LACAZ, C.S. - Passado, presente e futuro da paracoccidioidomicose. An. Bras. Derm. 59: 83-88, 1984 36. LACAZ, C.S. – Evolução dos conhecimentos sobre a paracoccidioidomicose. Um pouco de sua história. In LACAZ, C.S.; DEL NEGRO, G.D.; FIORILLO, A. M. – Paracoccidioidomicose – Blastomicose sul-americana. São Paulo: Sarvier - EDUSP, 1982. p. 1- 37. LEITE, A.S. - Alguns casos de blastomicose sul-americana em Porto Velho, Território Federal do Guaporé. Rev. Bras Med., 9: 491-496, 1952 38. LEITE, A. S. – Alguns casos de blastomicose sul-americana em Porto Velho, Território Federal do Guaporé. Rev. Bras. Méd., 9:83-88,1984. 54 39. LONDERO AT, MELO IS. Paracoccidioidomycosis in childhood: A critical review. Mycopathologia 1993; 82(1):49–55. 40. LONDERO, A.; RAMOS, C. D. Paracoccidioidomycosis: a clinical and mycologic study in fourty-one cases observed in Santa Maria, RS Brazil. American Journal of Medicine, New York, v. 52, n. 6, p. 771-775, Dec. 1972. 41. LUTZ, A. – Uma mycose pseudococcidica localizada na boca e observada no Brasil. Rev. Bras. Méd., 22:121-44.1908. 42. MACEDO , R., LACERA M., TRILES,REIS R., Infecção natural de tatus por Paracoccidioides brasiliensis em Serra da Mesa, Goiás: Estudo preliminar. Anais do II Congresso Brasileiro de Micologia. Rio de Janeiro. 1998. Abstract 182. 43. MCEWEN JG, BEDOYA V, PATINO MM, SALAZAR ME, RESTREPO A. Experimental murine paracoccidioidomycosis and induced by inhalation of conidia. Journal of Medical and Veterinary Mycology 25:165-175, 1987. 44. MALUF MLF, PEREIRA SRC, TAKAHACHI G, et al. Prevalência de paracoccidioidomicose: infecção determinada através de teste sorológico em doadores de sangue na região noroeste do Paraná, Brasil. Rev. Soc. Bras. Med. Trop. 2003;36:11-6. 45. MARQUES, S A., Paracoccidioidomycosis: Epidemiological, clinical and Treatment up-date. An. Bras Dermatol, Rio de Janeiro, 78(2):135-150, mar/april. 2003. 46. MARTINEZ, R., Etioepidemiologia e ecologia. I: VERONESI, R., FOCACCIA, R. Veronesi Tratado de Infectologia. São Paulo: Atheneu, cap. V. 84, p.1081 – 1083, 1996.1803p., 2004. 55 47. MATIAS, F. - Ocupação Humana e Trajetória Política de Rondônia, 1998. 48. MEDRONHO R. A, ET AL (2002). Epidemiologia. Editora Atheneu. Capítulo 2. 49. MINISTÉRIO DA SAÚDE- DOENÇAS INFECCIOSAS E PARASITÁRIAS. GUIA DE BOLSO. Paracoccidioidomicose CID- B 041 - 7a edição revista. Série B. Textos Básicos de Saúde. Capitulo 53 pg.268 BRASÍLIA – DF. 2008 . 50. MÓS, E. N.; FAVA NETTO, C. Contribuição ao estudo da paracoccidioidomicose. I. Possível papel epidemiológico dos cães. Estudo sorológico e anatomopatológico. Revista do Instituto de Medicina Tropical de São Paulo, São Paulo, v. 16, n. 3, p. 154-159, 1974. 51. MORAES, M.A.P. & FERREIRA, J.L.S. - Micoses superficiais e profundas na Amazônia. In: LENT, H. - Atas do Simpósio sobre a Biota Amazônica. Rio de Janeiro, CNPq, 1967. v. 6 (Patologia), p. 189-202. 52. MUSATTI CC. Imunidade celular. In: Del Negro GD, Lacaz CS, Fiorillo AM. Paracoccidioidomicose - Blastomicose sul-americana. São Paulo: Sarvier; 1982. p. 119-26. 53. NAIFF, R D; FERREIRA, L. C; BARRET, T.V; NAIFF, M. F; ARIAS, J. R. – Paracoccidioidomicose enzoótica em tatus (Dasypus novemcinctus) no Estado de Belém do Pará. Rev. Inst. Méd. Trop. S. Paulo, 28: 1927,1986. 54. NAIFF, R D, BARRETO T. Novos registros de Paracoccidioides brasiliensis em tatus (Dasypus novemcinctus). Anais do Congresso Brasileiro de Parasitologia. Rio de Janeiro. 1989. Abstract 197. 56 55. NEVILLE, B.W., DAMM, D.D,C. M., BOUQUOT, J.E. Patologia oral e Maxilofacial. Rio de Janeiro: Guanabara koogan, 1998. 705p. 56. ONO, M.A., BACARENSE, A. P., MORAIS, H.S., TRAPP, S.M., BELITARDO, D.R. CAMARGO, Z.P.2001. Canine Paracoccidioidomycosis: a seroepidemiologic study. Med. mycol. 39 (3): 277-82. 57. OLIVEIRA PT, YURGEL LS, LORANDI CS, MORAES ACS. Estudo de 54 casos de paracoccidioidomicose diagnosticados no Serviço de Estomatologia do Hospital São Lucas da PUCRS. Rev . Med PUCRS 1997; 7(4):161-6. 58. PAGLIARI, A.V, ARCE GAT, PIAZZETTA CM. Aspectos clínicos das lesões de paracoccidioidomicose na mucosa bucal. DENS 1995; 11:41-8. 59. PALHETA-NETO, F. X., MOREIRA,J. S.; MARTINS,A. C. C et. al. Estudo de 26 casos de Paracoccidioidomicose avaliados no Serviço de Otorrinolaringologia da Fundação Oswaldo Cruz. Rev. Bras Otorrinolaringol. V.69, n.5, 622-627, set./out. 2003. 60. PALMEIRO, MARIANA, CHERUBINI, K., YURGEL, L. S. Paracoccidioidomicose – Artigo de Revisão da Literatura. Rev. Scientia Medica, Porto Alegre: PUCRS, v.15,n. 4, out/dez.2005. 61. PANIAGO AMM, AGUIAR JIA, AGUIAR ES, CUNHA RV, PEREIRA GROL, LONDERO AT, et al. Paracoccidioidomycosis - A clinical and epidemiological study of 422 cases observed in Mato Grosso do Sul. Rev Soc Bras Med Trop. 2003;36(4):455-9. 62. PANIAGO, A M M M., epidemiológico de casos Paracoccidioidomicose: estudo clínico e atendidos no Hospital Universitário da Universidade federal do Mato Grosso do Sul (HU-UFMS). Dissertação (MESTRADO) apresentada ao Instituto Oswaldo Cruz para obtenção de 57 grau de Mestre. 2000. 63. PARANÁ, SECRETARIA DE SAÚDE. Protocolo de Paracoccidioidomicose / Protocol of Paracoccidioidomicose. s.d. 21 p. 37. 64. REDE Intergencial de Informações pa a Saúde . Indicadores Basicos de Saúde no Brasil: Conceitos e Aplicações/ Rede Interagencial de Informações para a Saúde- RIPSA- Brasilia: Organização PanAmericana da Saúde , 2002. 65. RICCI, G., SILVA, IDDCG.,MOTA F T,. WAKAMATSU, A., FRANCO, M F,. Canine Paracoccidioidomycosis: report on the first case of the literature. ARBS. An Rev. Bio Sciences. Special Issue 2002. 66. SANTOS J.W, SEVERO L.C, PORTO N.S. Fine needle aspiration in the diagnosis of pulmonary diagnosis. Mycopathologia 1998; 143(2):65-9. 67. SANTO A. H. Tendência da mortalidade relacionada à paracoccidioidomicose, Estado de São Paulo, Brasil, 1985 a 2005: estudo usando causas múltiplas de morte. Rev Panam Salud Publica. 2008;23(5):313–24. 68. SEDAM-RO, Secretaria Estadual de Desenvolvimento Ambiental; boletim nº 7., 2009. 69. SCULLY, C., ALMEIDA, P. Or facial manifestations of the systemic mycoses. Journal of oral Pathology and medicine, Copenhagen, v. 1, n. 7-10, p. 289-294, 1992. 70. SILVA, W. S., Paracoccidioidomicose: estudo clínico-demográfico a partir de pacientes portadores de lesões bucais. Dissertação apresentada à Faculdade de Odontologia da Universidade Federal de Uberlândia para 58 obtenção do Título de Mestre em Odontologia. Uberlândia, MG – 2007. 71. SPOSTO M.R, SCULLY C, ALMEIDA OP, JORGE Jr.J, GRANER E, BOZZO L. Oral Paracoccidioidomycosis: a study of 36 South American patients. Oral Surgery Oral Medicine Oral Pathology 75: 461-465 1993. 72. TELLES FILHO, F.Q. Terapêutica da Paracoccidioidomicose. In Veronesi, R. & Focaccia, R. Tratado de Infectologia, Ed. Atheneu, São Paulo, 1996.11041111. 73. VALLE, A.C.F, WANKE B, WANK NCF, LIMA NS, PEREZ M. Treatment of Paracoccidioidomycosis: Retrospective study of 500 cases. Evaluation of therapeutic results with sulfonamides, anphotericin b, sulfamethoxazol plus trimethoprin, ketoconazole and miconazole. 1993; 68 (1): 65–70. 74. VALLE, A.C.F. DO; COIMBRA JR.C.E. A; BORNAY I. LINHARES, F. I; MONTEIRO, P.C. F. & GUIMARÃES, M. R. C. – Paracoccidioidomicose entre grupo indígena Suruí de Rondônia, Amazônia (Brasil). Registro de Caso. Rev. Inst. Méd. Trop. S. Paulo, 33 (5): 407.411,1991. 75. VERGARA, S.M.L; MARTINEZ R, CAMARGO ZP, MALTA MH, MAFFEI, CML, CHADU JB. Isolation of Paracoccidioides brasiliensis from armadillos (Dasypus novemcinctus) in an area where the fungus was recently isolated from soil. Méd. Mycol 2000; 38:193-9. 76. VERGARA S., M.L, MARTINEZ R, CHADU A, MADEIRA M, FREITASSILVA G, MAFFEI, CML. Isolation of a Paracoccidioides brasiliensis strain from the soil of a coffee plantation in Ibiá, State of Minas Gerais, Brazil. Méd. Mycol. 36:37-42 1998. 77. VERGARA S. Contribuição ao Estudo Epidemiológico da Paracoccidioidomicose: Estudo em Área de Cultivo de Café. Rev. Soc. bras. Med. Trop., v. 1, p. 83-6, Jan./fev., 1997. 59 78. VERLI, F. D.; MARINHO, S. A.; SOUZA, S. C. et al., Perfil Clínico epidemiológico dos Pacientes Portadores de Paracoccidioidomicose no Serviço de Estomatologia do Hospital São Lucas da Pontifícia Universidade Católica do Rio Grande do Sul, Brasil. Rev. Soc. bras. Med. Trop., v. 3, p. 234-7, mai/jun., 2005. 79. VIEIRA, S., Introdução a Bioestatistica, 4ª edição., ed. Elsevier., Rio de Janeiro : Campus, 2008. 80. WANKE, B; LONDERO, AT. – Epidemiology ad paracoccidomycosis infection. In: Eds. FRANCO, M., LACAZ. C. S. RESTREPO - MORENO, A. & DEL NEGRO, G. – Paracoccidioidomycosis. Boca Raton, Florida, U.S. A.; C. R. C Press, 1994. Cap. 7, p. 109-20. 81. YASUDA, M.A.S., Pharmacological management of Paracoccidioidomycosis. Expert Opinion Pharmacotherapy 6:385-397, 2005. 82. YASUDA, M. A. S.; TELLES, F. Q.; MENDES, R. P. et al., Consenso em Paracocidioidomicose, Rev. Soc. Bras. Med. Trop., v. 3, p. 297-10, mai.,/jun.,2006. OBRAS CONSULTADAS RIGO, A. A., DUEÑAS, G. G. Como elaborar e apresentar teses e trabalhos de pesquisa – Porto Alegre/RS: Artmed, 2006. 60 ANEXOS
Download