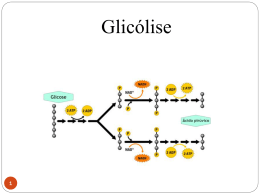
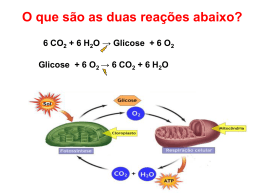
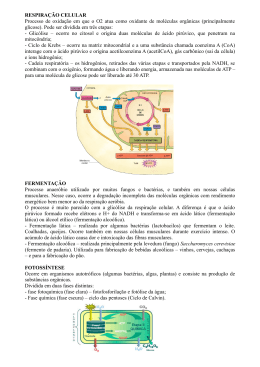
Moléculas envolvidas no metabolismo • • • • • • Carboidratos Lipídeos Proteínas Sais minerais Vitaminas Água Polissacarídeos Aminoácidos Aromáticos Hexoses Catecolaminas Pentoses Purinas Fotossíntese Pirimidinas Biosíntese de Lípídeos Degradação de Lipídeos d Fosfolipídeos Isoprenóides Esteróides Porfirinas Aminoácidos ALGUNS CONCEITOS INICIAIS Anabolismo • A fase do metabolismo (requerente de energia) que concerne a biossíntese dos componentes celulares a partir de precursores pequenos. Catabolismo • A fase do metabolismo que envolve a produção de energia por meio da degradação das moléculas dos nutrientes. A alimentação e o jejum alternam o metabolismo entre os estados Anabólico e Catabólico Complexa rede de interações entre as vias bioquímicas Metabólitos originados de uma via de degradação podem ser utilizados para a síntese de compostos Reversibilidade parcial das principais vias do metabolismo de carboidratos e lipídeos – o catabolismo é substituído pelo anabolismo em resposta à ingestão do alimento No estado alimentado: vias ativas são a glicólise, síntese de glicogênio, lipogênese e síntese de proteínas No estado de jejum (poucas horas após a alimentação): glicogênio e lipídeos armazenados são degradados, a proteína é convertida em glicólise (gliconeogênese), outros processos biossintéticos se tornam lentos. Visão Geral dos Processos Catabólicos FERMENTAÇÃO A fermentação é um movimento intestino de partículas ou principio de cada corpo, tendendo para a perfeição ou para a transformação em outro. Particulas elementares postas em movimento, devido a sua própria natureza ocasionalmente vibrando maravilhosamente, são aprisionadas e transforma-se em outras: as sutis e mais ativas esforçam-se na tentativa de escapar suavemente, mas estando entrelaçadas com outras mais espessas são impedidas também de fazê-lo. Também as mais expessas são mantidas unidas pelo intento. A expanção das mais sutis são enfraquecidas até que cada uma alcance sua própria grandeza e exaltação. Elas fixam em si a devida perfeição ou completam as alterações e mutações designadas pela natureza (Willis, 1684) • Na antiguidade sabia-se que a comida exposta ao ar apodrecia (liberava bolhas). Deram o nome de fermentação por analogia com a fervura – que também liberava bolhas • Séc XIX – Napoleão – Mr. Appert • Adicionar grandes quantidades de açúcar às frutas e ferver os alimentos, que deveriam ser imediatamente tampados e selados com parafina • Livro: “A arte de preservar os alimentos de origem vegetal e animal” – 10 Livro de Bioquimica Gay – Lussac vai pesquisar a fermentação ... Para isso testa “os experimentos” de Mr. Appert. O ar era necessário para a fermentação Interação entre O2 e nitrogênio dos alimentos liberava “as bolhas” (CO2 e N2) – Ligação desistabilizante – Reação Química “As substâncias em contato com o ar, adquirem prontamente uma tendência para a putrefação ou fermentação mas quando submetidas a temperatura de água fervida em vasos bem fechados, o oxigênio absorvido produz uma nova combinação que não é mais capaz de exitar fermentação ou putrefação, ou se torna coagulada pelo calor da mesma maneira que a albumina” • Por volta de 1850 os vinhos da França estavam muito ruins. Na quela época já se sabia que a qualidade do vinho dependia essencialmente da qualidade da uva e do repique • • • • • • Uma fábrica vinícula contrata Louis Pasteur Estudava a capacidade dos ácidos orgânicos de desviar o plano de luz Centrifugação – Amostra concentrada – Microscópio Teoria Vitalista Fermentação pode ser utilizada pelos seres vivos ... “Eu acredito que não há fermentação alcoólica sem que, ao mesmo tempo haja organização, desenvolvimento e multiplicação dos glóbulos” Louis Pasteur •A fermentação não é um processo metabólico dos glóbulos. É um processo meramente químico entre substâncias nitrogenadas, açúcar do meio na presença de ar. Pasteur ... •Derruba a Teoria da ligação desistabilizante •Para fermentar precisa-se de vida organizada ... •Seres vivos podem viver sem oxigênio Hans e Edward Buchner •Derrubam a Teoria Vitalista •Cunham o termo Zimases •Nasce a Bioquímica .... Glicólise Por que iniciar o estudo do metabolismo dos compostos combustíveis pela glicólise? Via metabólica universal (passos idênticos nas nossas células cerebrais e nas bactérias anaeróbicas) para metabolizar a glicose e produzir energia. Permite introduzir os mecanismos de regulação das vias metabólicas por pequenos efetores alostéricos, por modificações químicas reversíveis de enzimas e pelo controle da expressão gênica. Glicose Principal carboidrato combustível; forma de carboidrato circulante no sangue Finamente regulado: manutenção de uma concentração normal de 5 mmol/L é essencial para sobrevivência < 2,5 mmol/L → coma hipoglicêmico > 7 mmol/L → diabetes e riscos de doenças renais, vasculares e oculares. Oxidação completa a CO2 e água ocorre com uma variação de energia livre padrão de -2.840 kJ/mol!!! Nos vegetais superiores e nos animais tem 3 destinos principais: Corrente sanguínea Glicólise Primeira via metabólica a ser elucidada e, provavelmente, a melhor compreendida. Ocorre no citoplasma Primeiro estágio do catabolismo de carboidratos Açúcares simples são metabolisados a piruvato Processo anaeróbico – não necessita de oxigênio Fase preparatória Fase de produção de energia (fase de pagamento) Fase preparatória da Glicólise de Glicose a Gliceraldeído-3- P Aumenta o conteúdo de energia livre dos intermediários Requer o investimento de duas moléculas de ATP e resulta na clivagem da cadeia de hexose em duas trioses fosfato. Ocorrem duas reações de fosforilação. Isto é importante para que a célula não perca nenhum intermediário do ciclo após já ter investido energia na glicose, pois os compostos fosforilados (como o são todos os intermediários da glicólise) não atravessam as membranas livremente. Fase de produção de energia de Gliceraldeído-3-P a Piruvato Produção de 4 moléculas de ATP (ganho líquido de 2 ATP) Recuperação do “investimento” tem mais de 60% de eficiência Ocorrem duas reações de fosforilação em nível de substrato, assim denominadas porque a reação transfere não só energia livre ao ADP, mas também o próprio fosfato necessário à síntese de 1ATP. É importante notar que apenas 5,2% da energia de oxidação da glicose foram liberados ao fim da glicólise, permanecendo todo o restante na forma de piruvato São formados dois NADH Reações da Glicólise Balanço Saldo de energia = 02 ATPs 1. Fosforilação da Glicose ATP Glicose ADP hexoquinase glicoquinase Glicose-6-P Enzimas que Fosforilam a Glicose • Hexoquinase I Cérebro e Rins • Hexoquinase II Músculo esquelético • Hexoquinase I e II Fígado Diversos Tecidos • Hexoquinase III Fígado e • Hexoquinase IV células β-pâncreas ou Glicoquinase ∆G0’= - 16,7 kJ/mol = - 4,0 kcal/mol Glicólise – FASE PREPARATÓRIA 2. Conversão G6P a F6P 3. Fosforilação da F6P Inibida por ATP Ativada por ADP e Pi 3. Fosforilação da F6P Reação altamente exergônica e irreversível. ∆G0’= -13,8 kJ/mol = Reação que torna o açúcar comprometido com a glicólise. Glicólise – FASE PREPARATÓRIA 4. Quebra da F1,6P 5. Interconversão DHAP e G3P Glicólise – FASE PAYOFF 6. Oxidação do G3P a 1,3BPG 7. Transferência de PO32- para ADP Glicólise – FASE PAYOFF 8. Conversão 3-PG para 2-PG 9. Desidratação do 2-PG para PEP Glicólise – FASE PAYOFF 10. Transferência de PO4 para ADP Destinos do Piruvato O destino do piruvato pode variar significativamente Em nossas células, sob condições aeróbias, o piruvato é convertido a acetil-CoA nas mitocôndrias Destinos do Piruvato Fermentação – termo geral que denota a degradação anaeróbica da glicose ou de outros nutrientes orgânicos em vários produtos Em nosso organismo é usada para produzir NAD+ quando não há oxigênio suficiente NAD+ deve ser regenerado a NADH, caso contrário a glicólise é interrompida Vejamos rapidamente 02 tipos de fermentação Lactato Etanol Fermentação a Lactato Células animais sob condições anaeróbicas utilizam o Piruvato como aceptor final de elétrons para fazer a regeneração de NAD+, formando Lactato O fígado pode converter o lactato a uma “nova glicose” e reenviá-la para outro ciclo da glicólise no músculo, chamada gliconeogênese. Pode também ser sintetizada a partir do piruvato combinado com moléculas do ciclo do ácido cítrico. A gliconeogênese é importante para suprir o cérebro, que possui poucas reservas. Destinos do Piruvato Fermentação Alcoólica Compostos que alimentam a Glicólise Classificação dos monossacarídeos – Baseada no número de carbonos de suas moléculas: TRIOSES são os monossacarídeios mais simples, TETROSES, PENTOSES, HEXOSES, HEPTOSES, etc. – Destes, os mais importantes são as Pentoses e as Hexoses. – As pentoses mais importantes são: • Ribose • Arabinose • Xilose – As hexoses mais importantes são: • • • • Glicose Galactose Manose Frutose Compostos que alimentam a Glicólise Fígado Regulação Regulação Introdução quantidade de enzima como pela atividade Regulação gênica Regulação alostérica Enzimas do Metabolismo de Carboidratos que são Reguladas -Fosforilase -Hexoquinase -Fosfofrutoquinase 1 -Piruvato quinase Enzimas Alostéricas Ex: inibição por feedback A B Enzima possui um sítio alostérico ao qual se liga o produto final da via C D E Regulação Fosfofrutoquinase-1 Sítio Alosteria Sítio Ativo Regulação Fosfofrutoquinase-1 Frutose-2,6-bifosfato Frutose-2,6-bifosfato ↑Glucagon ↓Frutose-2,6-bifosfato Gliconeogênese favorecida Regulação Hexoquinase Isoenzimas: são enzimas diferentes que catalisam a mesma reação. Esta estratégia ajuda na regulação do metabolismo. músculo fígado Tecido que vai utilizar a glicose na via glicolítica Produzir glicose na gliconeogênese HEXOQUINASE GLICOQUINASE Inibida por glicose-6-fosfato Inibida por frutose-6-fosfato A hexoquinase muscular normalmente atua em velocidade máxima, contudo quando a concentração de glicose está acima de seu nível normal a enzima é temporariamente inibida levando a taxa de formação de G6P a se igualar a taxa de consumo de G6P. A glicoquinase normalmente abaixo de sua velocidade máxima, quando a concentração de glicose no sangue aumenta a sua velocidade aumenta levando a formação de G6P. Regulação Piruvato quinase A piruvato quinase é inibida alostericamente por ATP diminuindo a afinidade da enzima por PEP quando [ATP] ↑ ↓atividade enzima ↓glicólise quando [Acetil-CoA] e [ác. grax. longos] ↑ ↓atividade enzima ↓glicólise Control of the Catalytic Activity of Pyruvate Kinase. Pyruvate kinase is regulated by allosteric effectors and covalent modification. Aspectos clínicos - glicólise 1) Isquemia (Infarto do miocárdio): 2) Células tumorais: Otto Warburg – 1920 Células tumores Ascites convertem glicose equivalente a 30% do peso seco em lactato/h. (Músculo esquelético humano = 6% do peso seco em lactato/h)
Baixar