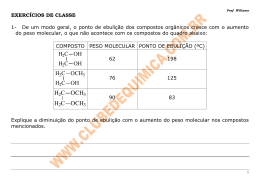
Prof. Willame EXERCÍCIOS DE CLASSE 1- De um modo geral, o ponto de ebulição dos compostos orgânicos cresce com o aumento do peso molecular, o que não acontece com os compostos do quadro abaixo: COMPOSTO PESO MOLECULAR PONTO DE EBULIÇÃO (ºC) H2C OH 62 198 76 125 90 83 H2C OH H2C OCH3 H2C OH H2C OCH3 H2C OCH3 Explique a diminuição do ponto de ebulição com o aumento do peso molecular nos compostos mencionados. 1 Prof. Willame 2- Observe a fórmula estrutural de algumas vitaminas abaixo: O O OH H3C CH3 CH3 CH3 OH OH HO OH I O CH3 CH3 II CH3 CH3 CH3 CH3 III CH3 O CH3 O HO N CH3 COOH H OH IV Uma das propriedades que determina a maior ou menor concentração de uma vitamina na urina é sua solubilidade em água. Qual dessas vitaminas é mais facilmente eliminada na urina? Justifique. 2 Prof. Willame 3- Em um laboratório, três frascos com líquidos incolores estão sem os devidos rótulos. Ao lado deles, estão os três rótulos com as seguintes identificações: ácido etanóico, pentano e 1 – butanol. Para poder rotular corretamente os frascos, determinam-se, para esses líquidos, o ponto de ebulição (P. E.) sob 1 atm e a solubilidade em água (S) a 25 º C. Líquido P. E. / ºC S/ (g/100 mL) X 36 0,035 Y 117 7,3 Z 118 infinita Com base nessas propriedades, conclui-se que os líquidos X, Y e Z são, respectivamente: a)1- butanol,ácido etanóico b) 1- butanol, pentano e c) ácido etanóico, pentano e d) pentano, 1- butanol e e)pentano, ácido etanóico e pentano. ácido etanóico. 1- butanol. ácido etanóico. e 1- butanol. 3 Prof. Willame 4- Com base nesta tabela: Alcanos Ponto de ebulição (ºC) CH3 CH3 C CH3 9,3 CH3 CH3 CH CH2 CH3 CH3 CH3 C C C CH3 H2 H2 H2 28,0 36,2 Conclui-se que os pontos de ebulição dos alcanos apresentados aumentam com: a)O b) A c) O d) A e)O aumento de suas massas moleculares. diminuição do número de ramificações. aumento do número de agrupamentos metila. diminuição da cadeia principal. aumento das interações por pontes de hidrogênio. 4 Prof. Willame 5- Sobre as ligações intermoleculares podemos afirmar: a) As ligações dipolo-dipolo são estabelecidas entre moléculas apolares. b) As forças de Van der Waals são ligações mais fortes do que as ligações covalentes c) As pontes de hidrogênio ocorrem quando se tem átomo de hidrogênio ligado a átomos pequenos e fortemente eletronegativos (F, O e N). d) As pontes de hidrogênio são ligações mais fracas do que as ligações dipolo-dipolo. e) As ligações intermoleculares são responsáveis pelas propriedades químicas das substâncias 5 Prof. Willame 6- Observe tabela a seguir. Substância Tipo de Força Intermolecular Ponto de Ebulição (º C) Butano I 0,6 II 8,0 III 97 (Hidrocarboneto) Metóxi – etano (Éter) Propanol (Álcool) Com base no dados da tabela, assinale a opção em que os tipos de interação entre moléculas semelhantes substituem I, II e III, respectivamente: a) b) c) d) e) dipolo induzido – pontes de hidrogênio – dipolo permanente dipolo permanente - dipolo induzido - pontes de hidrogênio pontes de hidrogênio - dipolo induzido - dipolo permanente dipolo induzido - dipolo permanente - pontes de hidrogênio pontes de hidrogênio - dipolo permanente - dipolo induzido 6 Prof. Willame 7- Na reação de substituição a espécie química destacada (A) é um(a) a) base de Lewis. b) eletrófilo. c) nucleófilo. d) carbânion. e) radical livre. 7 Prof. Willame 8- A reação que permite a produção do H3C - Cl, segundo a equação abaixo, é de: a) polimerização. b) eliminação. c) combustão. d) substituição. e) adição. 8 Prof. Willame 9- Os produtos (A), (B), (C) e (D) das reações mostradas a seguir têm as mais variadas aplicações. O etileno (A) é utilizado na obtenção de plásticos, o nitrobenzeno (B) é usado na preparação da anilina, o cloreto de etila (C) é largamente utilizado como solvente e anestésico tópico, e o álcool isopropílico (D) é usado na composição de anticongelantes. a) Classifique as reações dadas, considerando as categorias: adição, substituição ou eliminação. I) II) III) IV) b) Dê os nomes dos reagentes orgânicos, presentes nas reações citadas, que originaram os produtos (A), (B), (C) e (D). I) II) III) IV) 9 Prof. Willame 10- A seguinte reação: corresponde a: a) redução do propanal b) oxidação do ácido propanóico c) oxidação do propanal d) redução da propanona 11- As equações adiante respectivamente, reações de: representam, a) adição, substituição, eliminação. b) eliminação, substituição, polimerização. c) eliminação, adição, polimerização. d) substituição, adição, polimerização. e) substituição, eliminação, oxidação. 10 Prof. Willame 12- A partir do etanol, podemos obter muitos compostos orgânicos, como, por exemplo, o eteno, o acetato de etila, o etanal e o etano. No esquema a seguir, os processos indicados por I, II, III e IV são, respectivamente, reações de: a) oxidação, desidratação, redução e esterificação. b) oxidação, desidratação, oxidação e hidrólise. c) redução, hidratação, desidrogenação e esterificação. d) redução, oxidação, hidrogenação e hidrólise. e) desidrogenação, redução, oxidação e esterificação. 11 Prof. Willame 13- Considere a reação de substituição: CH3 + I CH3 AC3 + HI Se na reação o iodeto de metila for substituído por iodeto de etila, obter-se-á: a) tolueno b) naftaleno c) etilbenzeno d) orto etiltolueno e) para etiltolueno 12 Prof. Willame 14- Assinale, entre as alternativas abaixo, um produto formado pela reação: FeCl3 + Cl2 Cl a) Cl b) d) e) Cl Cl Cl Cl c) 13 Prof. Willame 15- A vanilina, cuja estrutura está representada a seguir, é uma substância responsável pelo odor característico da baunilha, sendo empregada como flavorizante na indústria de alimentos. Analisando a estrutura dessa substância, pode-se dizer que: OH O CH3 C O a) b) c) d) e) H há um grupo ativante e dois desativantes os grupos –OH, – OCH3, –CHO não exercem nenhum efeito sobre o anel aromático. há três grupos ativantes há três grupos desativantes há um grupo desativante e dois ativantes . 14 Prof. Willame 16- Se, pela síntese de Friedel-Crafts, se deseja obter etil-fenil-cetona, deve-se reagir benzeno com cloreto de: a) propanoíla. b) Fenila. c) Propila. d) Benzoíla. e) Etanoíla. 17- Observe as reações de adição dadas aos seguintes alcenos: Assinale a opção que contém APENAS a(s) reação(ões) que obedece(m) à Regra de Markovnikov: a) II. b) V. c) I e III. d) II e IV. e) IV e V. 15 Prof. Willame 18- A hidrogenação catalítica do propeno produz: a) 2 - propanol. b) propino. c) propano. d) ciclopropano. e) ciclopropeno. 19- O produto da hidrogenação do cicloexeno está apresentado na alternativa: 16 Prof. Willame 20- No sistema de equações a seguir, as substâncias A e B são, respectivamente: a) metano e bromo-metano. b) etano e bromo-etano. c) eteno e bromo-etano. d) propeno e 2-bromo-propeno. e) eteno e etino. 17
Baixar